INTRODUCCIÓN
La enfermedad meningocócica invasiva (EMI) es una infección grave y potencialmente mortal causada por la bacteria Neisseria meningitidis, asociada con una alta mortalidad y morbilidad, incluidas secuelas a largo plazo1. Aproximadamente 1,2 millones de casos de EMI ocurren cada año, lo que resulta en unas 335 000 muertes en todo el mundo, constituyendo un grave problema de salud pública que afecta principalmente a niños y adultos jóvenes2. En América latina, la mayoría de los casos son esporádicos, con variaciones estacionales y brotes que ocurren en intervalos irregulares3.
La mayor incidencia de la EMI se registra en África, en el cinturón de la meningitis con hasta 20 casos por 100.000 habitantes. Le siguen algunos países de Europa, Estados Unidos, Australia con 3 casos por 100.000 habitantes. En países como Paraguay y México la EMI tiene una incidencia de 0,1 casos por 100.000 habitantes y en Brasil de 2 casos por 100.000 habitantes4,5.
Neisseria meningitidis es parte de la microbiota comensal que reside en la nasofaringe de humanos. Bajo ciertas condiciones, la colonización asintomática puede progresar a EMI, que resulta en meningitis, septicemia fulminante o ambos6.
Se clasifica en 12 serogrupos, según la composición antigénica de los polisacáridos capsulares: A, B, C, H, I, K, L, W, X, Y, Z y 29E. Los serogrupos A, B, C, W135 e Y, y recientemente el serogrupo X, representan la mayoría de las enfermedades en todo el mundo. La distribución de los serogrupos que causan la enfermedad varía según el grupo de edad y la ubicación geográfica7. En América latina, los serogrupos B y C han sido responsables de la mayoría de los casos reportados en las últimas dos décadas, observándose una tendencia decreciente del serogrupo B en los últimos años (5).
En Paraguay, desde el inicio de la vigilancia en 1996 hasta el año 2015, el serogrupo prevalente fue el B, con un ligero aumento en los serogrupos C y W en los últimos años8. El número máximo de casos confirmados por laboratorio se registró en el año 2008 observándose 16 casos8.
La penicilina G y las cefalosporinas de tercera generación se utilizan generalmente para el tratamiento de enfermedades invasivas y rifampicina y ciprofloxacina para quimioprofilaxis de los contactos cercanos del caso9. En los últimos años, se ha observado un aumento de los aislamientos con sensibilidad disminuida a la penicilina G y se ha reportado también disminución de la sensibilidad a las cefalosporinas de tercera generación10.
Actualmente, existen diferentes vacunas disponibles para los serogrupos A, B, C, W e Y4. Las vacunas son serogrupo específicas por lo que los datos de vigilancia son fundamentales para monitorear la tendencia de la enfermedad y definir estrategias de prevención y control de la enfermedad meningocócica. referencia
El objetivo de este estudio es describir los serogrupos y resistencia antimicrobiana de N. meningitidis aisladas de enfermedad invasiva en Paraguay durante el periodo 2010-2020 en pacientes de todas las edades.
MATERIALES Y MÉTODOS
Estudio observacional descriptivo de corte transversal. Se incluyeron en este estudio todas las muestras de líquido cefalorraquídeo y sangre con aislamientos o detección de ADN de Neisseria meningitidis provenientes de pacientes con enfermedad invasiva de todas las edades, que fueron remitidas al Laboratorio Central de Salud Pública durante el periodo 2010-2020 dentro del marco de la vigilancia epidemiológica de meningitis (n=163) en Paraguay.
Métodos de laboratorio
Se estudiaron por técnicas microbiológicas convencionales y por reacción en cadena de la polimerasa (PCR) 95 aislamientos de N. meningitidis y 68 muestras de LCR o sangre con detección de presencia de ADN de N. meningitidis.
Las muestras de LCR y de sangre se sembraron en placas de agar sangre de carnero al 5% y en agar chocolate, se incubaron a 35 °C en una atmósfera enriquecida con CO2 al 5% y se examinó el crecimiento típico de N. meningitidis a intervalos de 24, 48 y 72 horas. Las placas que no exhibían crecimiento típico se descartaron después de 72 h. La identificación se efectuó por métodos microbiológicos de rutina con los procedimientos estándar del laboratorio11, con coloración de Gram (Britania, Argentina), producción de citocromo-oxidasa (dihidrocloruro de N, N, N ‘, N ‘-tetrametil-p-fenilendiamina, 1%, Becton Dickinson Microbiology Systems), catalasa y utilizando carbohidratos (glucosa, maltosa, lactosa, sacarosa, fructosa). El serogrupo se determinó mediante aglutinación en portaobjetos con antisueros comerciales contra polisacáridos capsulares meningocócicos (DIFCO, Beckton Dickinson, USA) y PCR para todos los aislamientos.
Todos los aislamientos fueron confirmados fenotípicamente y sometidos a análisis de susceptibilidad in vitro para penicilina G, ceftriaxona, rifampicina y ciprofloxacina. Se determinó la concentración inhibitoria mínima (CIM) mediante el método de epsilometría (bioMerieux) según los estándares del Clinical and Laboratory Standards Institute (CLSI) vigentes12. La identificación por PCR de N. meningitidis se basó en la amplificación del gen crgA utilizando partidores específicos y empleando secuencias ya descritas13. Para caracterizar el serogrupo, se realizó una PCR múltiple con oligonucleótidos en el gen siaD (serogrupos B, C, Y y W) y en el gen orf-2 requerido para la biosíntesis de la cápsula del serogrupo A13.
Para las muestras sin aislamiento la identificación y la determinación de los serogrupos se realizó por PCR en tiempo real utilizando partidores específicos y protocolo ya descripto14.
Análisis estadísticos
Los datos fueron recopilados en el marco de la Vigilancia de las meningitis y neumonías bacterianas en el Paraguay, se utilizaron cálculos de proporciones de frecuencias absolutas y de porcentajes con intervalos de confianza del 95%.
Se construyeron cuadros de contingencia con el fin de describir y encontrar posibles asociaciones entre los grupos de edades, diagnóstico de la infección y los distintos serogrupos de N. meningitidis.
Se describieron las características sociodemográficas y la frecuencia de los aislamientos por año. También se describe la susceptibilidad antimicrobiana a la penicilina G, ceftriaxona, rifampicina y ciprofloxacina. Además, se describe el perfil de susceptibilidad de la penicilina G por año y por serogrupos.
Consideraciones éticas
El estudio se llevó a cabo de acuerdo con los lineamientos éticos señalados en la Declaración de Helsinki. Este estudio fue aprobado por el Comité de Ética en Investigación del Laboratorio Central de Salud Pública (CEI) con el dictamen CEI-LCSP N°: 234/100921. La confidencialidad de los datos que consignan a la persona se respetaron en todo momento y únicamente los investigadores pudieron acceder a los datos referidos.
RESULTADOS
Se estudiaron 95 aislamientos y 68 muestras de LCR y/o sangre con identificación de N. meningitidis. Se procesaron 104 muestras provenientes de LCR, 42 de sangre (hemocultivo) y 17 muestras detectadas simultáneamente de LCR y sangre (hemocultivo).
La mayor frecuencia de aislamientos de N. meningitidis fue el grupo de edad de < 1 año (n=39), seguido del grupo de 1-5 años (n=23) y 11-15 años (n=21). Fue prevalente en el sexo masculino, así como, en Asunción (n=65) y en el departamento Central (n=64). Tabla 1.
Tabla 1. Características sociodemográficas de los aislamientos de N. meningitidis por grupo de edad en Paraguay (2010-2020) (n=163)
| Edad (en años) | N | Sexo n (%) | Procedencia n (%) | ||||
|---|---|---|---|---|---|---|---|
| Masculino | Femenino | Alto Paraná | Central | Asunción | Otros | ||
| < 1 | 39 | 21 (53,8) | 18 (46,1) | 8 (20,5) | 18 (46,1) | 12 (30,7) | 1 (2,5) |
| 1 a 5 | 23 | 15 (65,2) | 8 (34,7) | 5 (21,7) | 10 (43,4) | 8 (34,7) | 0 |
| 6 a 10 | 11 | 8 (72,7) | 3 (27,2) | 1 (18,1) | 6 (54,5) | 3 (27,2) | 0 |
| 11 a 15 | 21 | 11 (52,3) | 10 (47,6) | 2 (9,5) | 9 (42,8) | 9 (42,8) | 1 (4,7) |
| 16 a 20 | 20 | 14 (70,0) | 6 (30,0) | 2 (10,0) | 6 (30,0) | 10 (50,0) | 2 (10,0) |
| 21 a 25 | 12 | 7 (58,3) | 5 (41,6) | 3 (25,0) | 4 (33,3) | 5 (41,6) | 0 |
| 26 a 30 | 7 | 5 (71,4) | 2 (28,5) | 0 | 1 (14,2) | 5 (71,4) | 1 (14,2) |
| 31 a 35 | 2 | 2 (100,0) | 0 | 0 | 1 (50,0) | 0 | 1 (50,0) |
| 36 a 40 | 5 | 3 (60,0) | 2 (40,0) | 0 | 1 (20,0) | 4 (80,0) | 0 |
| > 41 | 23 | 11 (47,8) | 12 (52,1) | 3 (13,0) | 8 (34,7) | 9 (39,1) | 3 (13,0) |
| Total | 163 | 97 (59,5) | 66 (40,4) | 25 (15,3) | 64 (39,2) | 65 (39,8) | 9 (5,5) |
Otros: Concepción (3), Itapúa (2), Ñeembucú (2), Boquerón (2) y Amambay (1).
Se identificaron 42 casos correspondientes al serogrupo B (25.7%, IC95% 18,98-32,55), 85 al serogrupo C (52,1%, IC95% 44,39-59,89), 30 al serogrupo W (18,4%, IC95% 12,39-24,42) y 6 al serogrupo Y (3.6%, IC95% 0,75-6,60).
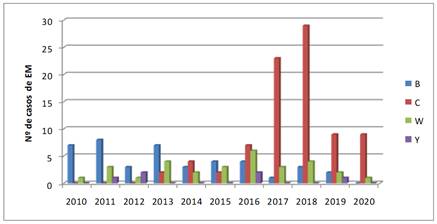
Durante el periodo de estudio el serogrupo C fue identificado con mayor frecuencia (n=85) observándose la mayor cantidad de número de casos entre los años 2017 (n=23) y 2018 (n=29). Se evidenció una disminución del serogrupo B y un aumento del C. Los serogrupos W e Y se mantuvieron relativamente estables, siendo que, en el año 2016, el W registró la mayor frecuencia de casos (n=6) Figura 1.
EM: Enfermedad meningocócica
Figura 1. Distribución de serogrupos de N. meningitidis por año (2010-2020) (N=163).
En los casos de meningitis, se encontró 28,4% de serogrupo B, 47,4% de C, 21,5% de W y 2,5% de Y. En sepsis 19,3% de B, 58,0% de C y 12,9% de W. En MBA/sepsis 18,7% de B, 75,0% de C, 6,2% de W.
En todos grupos de edad prevaleció el serogrupo C. Los casos de meningitis se hallaron con mayor frecuencia. La comparación de la distribución de los diferentes serogrupos de N. meningitidis según grupos de edad, plantea una diferencia estadísticamente significativa, no así la distribución del diagnóstico clínico con los grupos de edades. Tabla 2.
Tabla 2. Distribución de la enfermedad meningocócica según edad, diagnóstico y serogrupo (N=163)

*p<0.05, estadísticamente significativa
Se estudió el perfil de susceptibilidad de un total de 95 aislamientos, donde se determinó una sensibilidad intermedia o sensibilidad disminuida general a la penicilina G del 56,84% (54/95). En el año 2010 la sensibilidad disminuida fue del 12.5%, en 2011 (18,2%), 2012 todos los aislamientos fueron sensibles, 2013 (37,5%), 2014 (100,0%), 2015 (40,0%), 2016 (92,3%), 2017 (69,2%), 2018 (70,6%), 2019 (71,4%) y 2020 (80.0%). Figura 2.
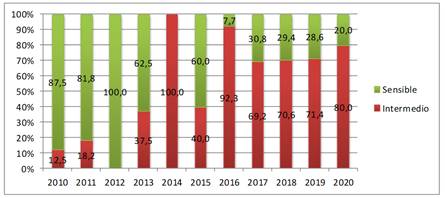
Figura 2. Perfil de susceptibilidad a la penicilina G de aislamientos de N. meningitidis (2010-2020) (n=95).
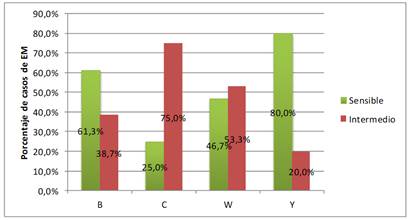
La sensibilidad disminuida a la Penicilina G distribuida por serogrupo presenta en B 12/31 (38,7%), en C 33/44 (75,0%), en W 8/15 (53,3%) y en Y 1/5 (20,0%). Figura 3. Todos los aislamientos fueron sensibles a ceftriaxona, rifampicina y ciprofloxacina.
DISCUSIÓN
La carga real de la EMI en América Latina se encuentra probablemente subestimada debido al subregistro de casos, consecuencia de factores como dificultades en la definición de casos e ingreso de datos, retraso en el aislamiento e identificación de los serogrupos por falta de la tecnología apropiada, así como también de personal capacitado, entre otros15. En Paraguay, la enfermedad meningocócica es relativamente infrecuente, sin embargo, al igual que en varias regiones del mundo, la epidemiologia de esta enfermedad ha cambiado en forma significativa. Durante el periodo de estudio (2010-2020), la mayoría de los casos de EMI fue en menores de 1 año y de sexo masculino, siendo la meningitis la forma más común de EMI.
En cuanto a los serogrupos, el C fue predominante, seguido del serogrupo B, similar a lo observado en estudios realizados en Brasil16, Colombia17, México18, mientras que en Argentina, los serogrupos más comunes fueron el B y W (15, 19) y en Chile se observó un aumento de casos del serogrupo W15. Países de otras regiones como Corea del Sur y Marruecos presentaron una prevalencia del serogrupo B6,20.
Entre los años 2015-2020, el serogrupo C fue dominante. Según un estudio realizado entre los años 1995 a 2015 se observó predominio del serogrupo B y un ligero aumento de casos de EMI por C y W8. Un estudio realizado entre 2002-2017 en Brasil, mostró un cambio en la prevalencia de serogrupos en 2006, cuando el serogrupo C se convierte en el más prevalente (65,5%), superando al B (21,9%)16. En Colombia, se observó que en años anteriores al periodo de estudio (2013-2016), el serogrupo B era prevalente para luego predominar en el periodo mencionado el C(17, 21). Existen algunas variables que podrían explicar los cambios en la prevalencia de los serogrupos, entre ellas, cambios periódicos que ocurren naturalmente y otra el impacto de los programas de inmunización, en donde si bien producen una disminución significativa de casos provocados por ciertos serogrupos, esto podría provocar aumento de otros serogrupos y aparición de nuevos serogrupos6,22. Durante los años 2006-2015 en Estados Unidos, se notificaron 7924 casos de enfermedad meningocócica, 2290 (35,8%) correspondieron al serogrupo B, 1827 (28,5%) a Y, 1457 (22,8%) a C, 436 (6,8%) eran W y 392 (6,1%) eran otros serogrupos23.
Se ha observado una disminución de la susceptibilidad a la penicilina G, a nivel mundial, pero clínicamente no es significativo. La gran mayoría de las cepas continúan demostrando sensibilidad in vitro a los antibióticos comúnmente utilizados en el tratamiento empírico de la meningitis bacteriana. La sensibilidad disminuida a penicilina en el presente estudio fue del 56,8% de todos los aislamientos (54/95). En Colombia, 43% de los aislamientos del año 2014 presentaron sensibilidad disminuida a la penicilina, mientras que en el año 2016 una cepa del serogrupo Y fue resistente (CIM=0,5ug/mL)18. En Argentina, se detectó sensibilidad disminuida a penicilina (CIM= 0.12 - 0,25ug/mL) en 35,4% de 130 aislamientos obtenidos de casos de EMI durante el año 2010, todos los aislamientos resultaron negativos para la producción de betalactamasa24. En Brasil, todos los aislamientos (n=3548) fueron sensibles a ceftriaxona, mientras que se encontró una sensibilidad intermedia del 33,0% a penicilina G, 45,3% a ampicilina y 0,07% a rifampicina. Además, se encontró resistencia del 0,1% a rifampicina, 0,07% a ciprofloxacina y 0,03% a cloranfenicol25. De 183 aislamientos obtenidos durante el periodo 2010 - 2019 en Marruecos, el 24% presentó susceptibilidad reducida a penicilina pero no se ha observado resistencia20. En Italia, 45 % de 866 cepas de Neisseria meningitidis aisladas durante el periodo 2006-2010 resultaron con sensibilidad disminuida a penicilina y 6 cepas resistentes a dicho antibiótico, con CIM entre 0,38-0.5 ug/mL9.
En el presente estudio, la sensibilidad disminuida encontrada fue para el serogrupo C = 75%, B = 38,7%, W=53,3% Y=20%. En Argentina, se detectó sensibilidad disminuida a penicilina del 68,5% en B, 33,3% en C, 25,0% en Y y 10,1% en W24, como así también en Marruecos, en donde 84,09% correspondieron al serogrupo B, 9,09% a W, 4,54% a C y 2,27% a Y20. A diferencia de este estudio, en Argentina y Brasil el mayor porcentaje de sensibilidad disminuida a penicilina se observó en el serogrupo B20,24. Esta disminución en la sensibilidad podría deberse a la presencia de mutaciones en el gen penA que codifica la proteína de unión a la penicilina (PBP2), principal mecanismo de la no susceptibilidad a la penicilina en Neisseria meningitidis, como así también a otros factores y a otras mutaciones aun no identificados en el gen penA17,24.
Todos los aislamientos fueron sensibles a ceftriaxona, rifampicina y ciprofloxacina, similar a lo observado en Colombia17 y Argentina, con la excepción de que en este último país, dos cepas fueron resistentes a ciprofloxacina con CIM=0,12ug/mL y halos de inhibición de 6 y 18 mm frente al disco de ácido nalidixico24, mientras que en Marruecos, todas las cepas fueron susceptibles a cefalosporinas de tercera generación y ciprofloxacina pero 18,03% de las cepas presentaron sensibilidad reducida a rifampicina20. En Italia, 2 cepas fueron resistentes a ciprofloxacina y 6 a rifampicina y todos fueron sensibles a cefalosporinas de tercera generación9.
En resumen, la carga de enfermedad causada por N. meningitidis es relativamente baja en Paraguay, sin embargo el cambio de serogrupos y la creciente disminución de la sensibilidad a la penicilina son motivos de preocupación. El fortalecimiento de los programas nacionales de vigilancia, mejoras en la notificación, junto con herramientas de diagnóstico avanzadas proporcionarán información relevante que permitirán implementar estrategias precisas para el control y prevención de la EMI.