INTRODUCCIÓN
El desarrollo de terapias biológicas ha transformado el manejo de las enfermedades reumáticas inflamatorias crónicas, permitiendo que un mayor número de pacientes alcance la remisión o mantenga una baja actividad de la enfermedad(1,2). Aunque los ensayos clínicos han demostrado la eficacia y seguridad de los FAME-b, estos estudios incluyen poblaciones altamente seleccionadas, con un seguimiento riguroso que no siempre refleja la práctica clínica real. Por ello, los registros de vida real son fundamentales para evaluar el perfil de seguridad de estas terapias en poblaciones más heterogéneas y en contextos específicos(3).
En América Latina, los datos sobre la seguridad de los FAME-b siguen siendo limitados, especialmente en países con características genéticas, demográficas y socioeconómicas particulares. Factores como el acceso al tratamiento, las diferencias en la farmacogenética y la carga de enfermedades infecciosas podrían influir en la incidencia y el tipo de efectos adversos asociados a estas terapias. En respuesta a esta necesidad, la Sociedad Paraguaya de Reumatología (SPR) y la Sociedad Uruguaya de Reumatología impulsaron la creación del registro Biobadaguay, un esfuerzo conjunto para documentar y analizar la seguridad de los FAME-b en la región.
El presente estudio tiene como objetivo evaluar la seguridad de las terapias biológicas en la cohorte paraguaya del registro Biobadaguay, proporcionando datos relevantes sobre los eventos adversos en esta población y contribuyendo al conocimiento global sobre el uso de estos tratamientos en entornos latinoamericanos.
MATERIAL Y MÉTODOS
Biobadaguay es un estudio prospectivo observacional de la seguridad en pacientes con enfermedades reumáticas inflamatorias crónicas. Este registro, que abarca a dos países de Latinoamérica, se inició en el año 2016 y su metodología ha sido descrita en artículos previos. Si bien el registro incluye a pacientes de Paraguay y Uruguay en la misma plataforma, cada país participa de manera independiente, con un coordinador común para ambos países(4). Más información sobre la metodología está disponible en la página web del registro (https://biobadaguay.ser.es).
Población y variables del estudio
Se incluyó en el análisis a todos los pacientes (tanto adultos como pediátricos) incluidos en el registro desde julio de 2016 a octubre de 2022. Se analizaron variables clínicas, epidemiológicas y tratamiento recibido (FAME-b, y FAME-sc). Para el análisis de los AA, se registró el tipo de AA, el desenlace y su gravedad. Se consideró grave aquel evento que produjera la muerte, ponga en peligro la vida, requiera hospitalización o la prolongue, produzca discapacidad persistente o importante o malformaciones congénitas. Se utilizó la nomenclatura MedDRA (Medical Dictionary for Drug Regulatory Activities) para clasificar cada uno de los AA (www.meddra.org).
Análisis estadístico
Se analizaron las variables epidemiológicas, clínicas y terapias recibidas. Las variables continuas se evaluaron en las medias con su correspondiente desviación estándar (DS) y las categóricas en frecuencia y porcentaje. Para el análisis de incidencia de AA se calculó la tasa de incidencia (IR) por 1000 pacientes-año, (IC) 95% y la razón de tasa de incidencia (IRR) mediante regresión de Poisson.
RESULTADOS
En el presente estudio se analizaron los datos de 11 centros en Paraguay.
Características clínicas de los pacientes y tratamiento
Se registraron 696 pacientes con FAME-b, 809 (71,3 %) fueron mujeres, con una edad media al inicio del primer tratamiento de 39,8 ±17,7 años y una duración media de la enfermedad al inicio del primer tratamiento de 7,5± 8,2 años. El diagnóstico más frecuente fue la artritis reumatoide (AR) 399 (57,3%). Las principales características de la población incluida en el registro se presentan en la Tabla 1. Se administraron un total de 847 tratamientos. Los fármacos más utilizados como primera línea de tratamiento (primer FAME-b utilizado) fueron adalimumab original (52,4%) y etanercept original (18,1%). En segunda línea y posteriores de tratamiento los fármacos más frecuentemente registrados fueron adalimumab original (29,8%), etanercept original (8,3%) y tocilizumab original (15,8%). El metotrexato fue el tratamiento concomitante más comúnmente utilizado tanto en la primera línea de tratamiento (73,3%) como en la segunda y posteriores líneas de tratamiento (63,6%). Los glucocorticoides fueron utilizados en un 61,9 % del total de tratamientos. Se registraron 325 suspensiones de tratamiento, la ineficacia y/o pérdida de eficacia (27,4%) fueron las principales causas de retirada de tratamiento. En la Tabla 2 se muestra la descripción de las líneas de tratamiento y los motivos de suspensión.
Tabla 1 Características de los pacientes al inicio.
| Pacientes, n | 696 |
| Edad media, n ± DE | 39,8 ±17,7 |
| Duración de la enfermedad, n ± DE | 7,5 ± 8,2 |
| Mujeres, n (%) | 496 (71,7) |
| Diagnóstico | |
| Artritis reumatoide, n (%) | 399 (57,3) |
| Artritis idiopática juvenil, n (%) | 89 (12,8) |
| Espondilitis anquilosante, n (%) | 74 (10,6) |
| Otros, n (%) | 134 (19,25) |
| Comorbilidades | |
| Hipertensión arterial, n (%) | 132 (19,3) |
| Dislipidemia, n (%) | 29 (4,2) |
| Diabetes, n (%) | 29 (4,2) |
| Osteoporosis, n (%) | 23 (3,9) |
| Fumadores, n (%) | 14 (2,1) |
| Cardiopatía isquémica, n (%) | 6 (0,8) |
| Insuficiencia renal, n (%) | 5 (0,7) |
| EPOC, n (%) | 4 (0,6) |
| Cáncer, n (%) | 4 (0,6) |
DE: desviación estándar (años), EPOC: enfermedad pulmonar obstructiva crónica. Otros: diagnósticos con valores < 5% del total.
Tabla 2 Descriptivo de terapias y motivos de suspensión
| Fármaco | 1º línea de tratamiento n (%) | 2ª y posteriores líneas de tratamiento n (%) | Todos n (%) |
|---|---|---|---|
| Anti-TNF original | |||
| Adalimumab | 365 (52,4) | 45 (29,8) | 410 (48,4) |
| Etanercept | 126 (18,1) | 29 (19,2) | 155 (18,3) |
| Golimumab | 1 (0,1) | 0 (0,0) | 1 (0,1) |
| Anti- TNF biosimilar | |||
| Infliximab | 43 (6,2) | 4 (2,6) | 47 (5,5) |
| Adalimumab | 13 (1,9) | 1 (0,7) | 14 (1,7) |
| Inhibidores de IL-6 | |||
| Tocilizumab original | 74 (10,6) | 60 (39,7) | 134 (15,8) |
| Anti CD20 | |||
| Rituximab original | 73 (10,5) | 11 (7,3) | 84 (9,9) |
| Anti-TNF | 547 (78,6) | 79 (52,3) | 626 (73,9) |
| No anti-TNF | 149 (21,4) | 72 (47,7) | 221 (23,1) |
| Todos ciclos | 696 (100) | 151 (100) | 847 (100) |
| Motivos de Suspensión | n (%) | n (%) | n (%) |
| Ineficacia | 66 (25,6) | 23 (34,3) | 89 (27,4) |
| Acontecimiento adverso | 45 (17,4) | 16 (23,9) | 61 (18,8) |
| Pérdida paciente | 37 (14,3) | 11 (16,4) | 48 (14,8) |
| Remisión | 27 (14,3) | 2 (3,0) | 39 (12,0) |
| Embarazo o DG | 13 (5,0) | 4 (6,0) | 17(5,2) |
| Razones no médicas | 13 (5,0) | 3 (4,5) | 16 (4,9) |
| Desconocido | 7 (2,7) | 3 (4,5) | 19 83,19 |
| Otros | 7 (2,7) | 3 (4,59 | 10 (3,1) |
| Total suspensiones | 258 (100) | 67 (100) | 325 (100) |
Anti- TNF: inhibidores del factor de necrosis tumoral. DG: deseo gestacional. Otros: pérdida de seguro médico 39 (57,4%), cambio de centro de atención 12 (17,6%), decisión del paciente 8 (11,8%) e intervención quirúrgica 8 (13.2%).
Seguridad de las terapias biológicas
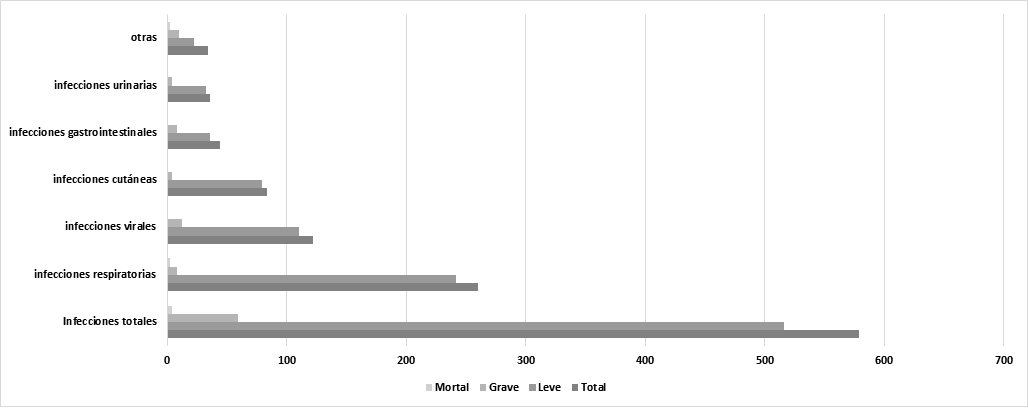
Se registraron 1047 acontecimientos adversos, 928 (88,6%) fueron leves, 110 (10,5%) graves y 9 (0,8%) mortales. En la Tabla 3 se muestran las frecuencias y porcentajes de los AA. Los AA globales más frecuentes fueron los procesos infecciosos: 579 (55,3%), de ellos 516 (89,1%) fueron leves, 59 (10,2%) graves y 4 (0,7%) mortales. La infección respiratoria fue la más frecuente del total de infecciones 267 (43,3%), de estas 242 (93,1%) fueron leves y 16 (6,1%) fueron graves y 2 (0,7%) mortales. En el Gráfico 1 se muestran la distribución de infecciones por tipo y gravedad. Entre los AA infecciosos graves se registraron 8 casos de tuberculosis, de los cuales 5 fueron graves y todos se recuperaron sin secuelas. Se observaron 6 neoplasias malignas, el más frecuente fue el cáncer de mama en un 66,7%. Se registraron 10 defunciones (dos sepsis, una neumonía, dos fibrosis pulmonares, una leucemia linfocítica aguda, dos accidentes cerebrovasculares, una peritonitis y una cirugía cardiaca).
Tabla 3 Descripción de acontecimientos adversos con terapias biológicas
| Tipo de acontecimiento adverso | Total n (%) | Leves n (%) | Graves n (%) | Mortales n (%) |
|---|---|---|---|---|
| Infecciones | 579 (55,3) | 516 855,6) | 59 (53,6) | 4 (44,4) |
| Procedimientos médicos y quirúrgicos | 54 (5,2) | 43 (4,6) | 10 (9,1) | 1 (11,1) |
| Trastornos de la piel y del tejido subcutáneo | 46 (4,4) | 44 (4,7) | 2 (1,8) | 0 (0,0) |
| Trastornos gastrointestinales | 45 (4,3) | 41 (4,4) | 3 (2,7) | 1 (11,1) |
| Trastornos sistema nervioso | 41 (3,9) | 37 (4,0) | 2 (1,8) | 2 (22,2) |
| Trastornos vasculares | 30 (2,9) | 22 82,4) | 8 (7,3) | 0, (0,0) |
| Trastornos hematológicos | 29 (2,8) | 28 (3,0) | 1 (0,9) | 0 (0,0) |
| Traumatismos/intoxicaciones/complicaciones de procedimientos terapéuticos | 27 (2,6) | 24 (2,6) | 3 (2,7) | 0 (0,0) |
| Trastornos metabolismo y nutrición | 27 (2,6) | 25 (2,7) | 2 (1,8) | 0 (0,0) |
| Exploraciones complementarias | 23 (2,5) | 23 (2,2) | 0 (0,0) | 0 (0,0) |
| Trastornos hepatobiliares | 21(2,0) | 20 82,2) | 1 (0,9) | 0 (0,0) |
| Trastornos de sistema inmune | 20 (1,9) | 13 (1,4) | 7 (6,4) | 0 (0,0) |
| Trastornos musculoesqueléticos y tejido conjuntivo | 19 (1,89 | 17 (1,8) | 2 (1,8) | 0 (0,0) |
| Neoplasias | 13 (1,2) | 7 (0,7) | 5 (4,5) | 1 (11,1) |
| Trastornos aparato reproductor y de la mama | 12 (1,1) | 11 (1,2) | 1 (0,9) | 0 (0,0) |
| Trastornos oculares | 12 (1,1) | 11 (1,2) | 1 (0,9) | 0 (0,0) |
| Trastornos respiratorios /torácicos / mediastínicos | 10 (0,9) | 9 (1,0) | 1 (0,9) | 0 (0,0) |
| Trastornos renales /urinarios | 8 (0,8) | 8 (0,9) | 0 (0,0) | 0 (0,0) |
| Trastornos psiquiátricos | 8 (0,8) | 8 (0,9) | 0 (0,0) | 0 (0,0) |
| Trastornos cardiacos | 8 (0,8) | 6 (0,6) | 2 (1,8) | 0 (0,0) |
| Trastornos generales y del lugar de aplicación | 6 (0,6) | 6 (0,6) | 2 (1,8) | 0 (0,0) |
| Trastornos endocrinos | 4 (0,4) | 4 (0,4) | 0 (0,0) | 0 (0,0) |
| Embarazo/puerperio/enfermedades perinatales | 3 (0,3) | 3 (0,3) | 0 (0,0) | 0 (0,0) |
| Trastorno oído /laberinto | 2 (0,2) | 2 (0,2) | 0 (0,0) | 0 (0,0) |
| Total de Acontecimientos adversos | 1047 (100) | 928 (100) | 110 (100) | 9 (100) |
La tasa de incidencia (IR) global de AA por 1000 pacientes año (IC 95%) fue de 323,8 (304,5-265,5), al estratificar en función de la gravedad, la IR de AA leves fue 219,7 (IC 95%, 207,4-344,0) y de 34,0 (IC 95%, 28,0-41,0) para graves y 2,8 (1,3-5,3) para mortales. Se analizó la incidencia de tipos de AA en función de la línea de tratamiento. La IR de AA globales de la primera línea fue 286,2 (266,5- 306,9) y como segunda opción o posteriores 534,5 (471,7-603,2). Se observó que segunda línea y posteriores de tratamiento se asociaron de modo significativo a una mayor tasa de AA globales (IRR=1,9 [IC 95% (1,4-2,5)], p=0,00001). Se analizó la incidencia de AA según tipo de AA y tratamiento (antiTNF o no-antiTNF). La IR de AA globales con terapia antiTNF fue de 284,9 (264,6- 306,4) y con terapia no-antiTNF fue 468,4 (418,5-522,5), se observó que la terapia antiTNF se asociaba de modo significativo a una menor tasa de incidencia de AA globales (IRR=0,6 [IC 95% (0,5-0,8)], p=0,0004). Se analizó la incidencia de AA en función de la gravedad y línea de tratamiento. Se observó que segundas líneas y posteriores de tratamiento se asociaban a una mayor IR de AA globales. Del mismo modo al analizar la IR en función de la gravedad y tipo de tratamiento, la terapia anti-TNF se asoció a una menor tasa de AA globales que el tratamiento no-antiTNF (ver Tabla 4, Figura 1 y Figura 2).
Tabla 4 Tasa de incidencia de acontecimientos adversos en función de la gravedad según línea de tratamiento y tipo de tratamiento.
| AA | Primera línea | Líneas posteriores | IRR test | |||
|---|---|---|---|---|---|---|
| Eventos | IR (IC 95%) | Eventos | IR (IC 95%) | IR (IC 95%) | P | |
| Global | 785 | 286,2 (266,5-306,9) | 262 | 534,5 (471,7-603,2) | 1,9 (1,4-2,5) | 0,00001 |
| Leve | 690 | 251,5 (233,1-271,0) | 238 | 485,5 (425,7-551,2) | 1,9 (1,4-2,6) | 0,00001 |
| Grave | 90 | 32,8 (26,4-40,3) | 20 | 40,8(17,9-40,1) | 1,24 (0,7-2,3) | 0,4733 |
| Mortal | 8 | 1,8 (0,8-3,5) | 5 | 5,3 (1,7-12,3) | 4,5 (1,2-16,8) | 0,0206 |
| AA | No-antiTNF | AntiTNF | IRR test | |||
| Eventos | IR (IC 95%) | Eventos | IR (IC 95%) | IRR (IC 95%) | P | |
| Global | 321 | 468 (418,5-522,05) | 726 | 284.69(264,6-306,4) | 0,6 (0,5-0,8) | 0,0003 |
| Leve | 275 | 401,3 (355,2-451,6) | 653 | 256.3 (236,9-276,7) | 0,6 (0,5-0,9) | 0,0030 |
| Grave | 40 | 58,4 (41,7-79,5) | 70 | 27.5 (21,4-34,7) | 0,5 (0,3-0,7) | 0,0015 |
| Mortal | 6 | 8,8 (3,2-19,1) | 3 | 1,8 (0,2-3,4) | 0,1 (0,0-0,5) | 0,0046 |
AA: acontecimiento adverso, IC: intervalo de confianza, IR; tasa de incidencia, IRR: razón de tasa de incidencia, antiTNF: anti-factor de necrosis tumoral.
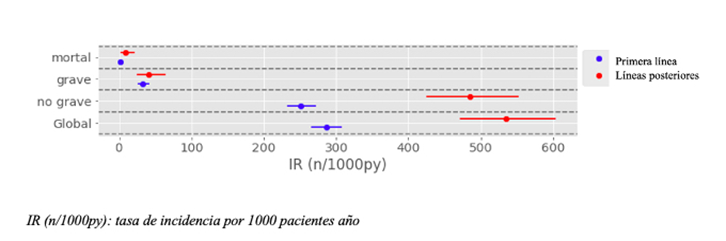
Figura 1 Incidencia de acontecimientos adversos en función de la gravedad según línea de tratamiento.
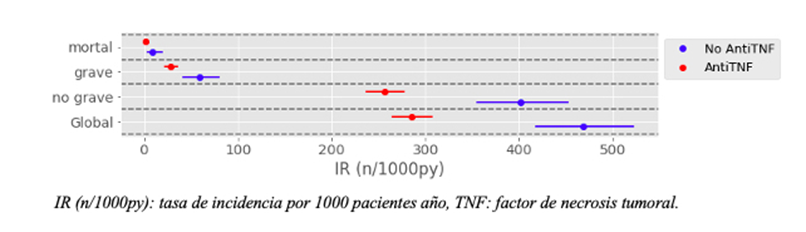
Figura 2 Incidencia de acontecimientos adversos en función de la gravedad y terapia antiNTF vs no-antiTNF.
La IR global de AA infecciosos fue de 179,1(168,8-194,3), para infecciones leves 159,6 (146,1-174,0) y para graves y mortales 19,5 (14,0-25,0). Se analizó la IR global de infección en función de la línea de tratamiento (1º línea con 2ª y posteriores), se observó que segundas líneas de tratamiento se asociaban a una mayor IR de AA infecciosos (IRR=1,6 [IC 95% (1,2-2,2)], p=0,003). No se encontraron diferencias significativas al analizar la IR infección en función de terapia antiTNF y no- TNF (IRR =0.8 [IC 95% (0,6-1,1),] p= 0,09).
Al analizar la IR en función del diagnóstico y gravedad se observó que la AR mostró una mayor IR de AA global, leves y graves-mortales que otros diagnósticos (IRR= 1,4 [IC 95%, (1,1-1,8)], p=0,01), (IRR=1,3 [IC 95% (1,0-1,7)], p=0,04) y (IRR= 2,1 [IC 95%, (1,3-3,3)], p=0,004) respectivamente. La artritis psoriásica (APSo) mostró una menor tasa de AA globales y leves que otros diagnósticos, (IRR = 0,6 [IC 95% (0,3-1,0)], p=0,03) y (IRR = 0,6 [IC 95% (0,3-1,0)], p=0,05) respectivamente.
En el análisis multivariante de AA globales (usando de referencia la primera línea de tratamiento), las líneas posteriores de tratamiento estaban asociadas a un mayor riesgo de AA (IRR=1,5 [IC 95% (1,3-1,7)], p <0.0001). Al analizar en función del diagnóstico (usando de referencia la AR) la APSo y la espondilitis anquilosante (EA) mostraron una menor tasa de AA globales (IRR=0,6 [IC 95% (0.5-0.9)] p =0.009) y (IRR=0,7 [IC 95% (0.6-1,0)] p =0.02) respectivamente. En análisis multivariante de AA globales en función de la terapia recibida (usando de referencia el adalimumab original); el tocilizumab original y el etanercept original presentaron un mayor riesgo de AA globales (IRR=1,6 [IC 95% (1,4-1,9], p<0.0001) y (IRR=1,2 [IC 95% (1,0-1,4)], p=0,02) respectivamente; en cambio el rituximab original mostró menor riesgo (IRR=0,4 [IC 95% (0,2-0,6)], p <0.0005). No hubo diferencias en el uso concomitante de corticoides o FAME convencionales. El análisis multivariante de AA graves y mortales, las mujeres presentaron un menor riesgo de AA graves y mortales (IRR=0,5 [IC 95% (0,4-0,9)], p=0,02). Al analizar en función del diagnóstico (usando de referencia la AR), la artritis idiopática juvenil (AIJ) y la EA se asoció con un menor riesgo (IRR=0.4 [IC 95% (0,2-0,9)], p=0.02) y (IRR=0.4 [IC 95% (0,2-1,0)], p=0.02) respectivamente. Al analizar en función de la terapia recibida (usando de referencia adalimumab original), el tocilizumab original está asociado a un mayor riesgo (IRR=1,9 [IC 95% (1,3-3,1)], p= 0.006). No hubo diferencias en el uso concomitante de corticoides o FAME convencionales ni líneas de tratamiento.
DISCUSIÓN
Este estudio proporciona datos de importancia sobre la seguridad de terapias biológicas en pacientes paraguayos con enfermedades reumáticas inflamatorias, utilizando datos del registro BIOBADAGUAY. Los resultados muestran la presencia de AA de predominio leve, siendo más frecuentes los procesos infecciosos. Por estas razones se requiere una vigilancia continua y especifica de los pacientes en este aspecto.
En esta cohorte predomina el sexo femenino y el diagnóstico más frecuente es la artritis reumatoide, datos similares a lo observado en otros registros sudamericanos como Biobadasar, Biobadamex, BiobadaBrasil(5,6,7). El tratamiento con mayor número de registros fue el Adalimumab original, quizás porqué fue el primer y único fármaco comercializado durante varios años. En diferentes registros como Biobadasar, Biobadamex y Biobadabrasil(5,6,7) encontramos una exposición variable de las distintas terapias, probablemente esté en relación con la comercialización y aprobación de cada agente para su uso en un determinado país.
La principal causa de suspensión de tratamiento fue la ineficacia o pérdida de eficacia. Datos similares a los observados en Biobadasar, Biobadamex y Biobadaser(5,6,8). Así mismo, en un estudio de colaboración de registros de 17 países, Kim Lauper et al. observaron las mismas causas de discontinuación(9).
La incidencia de AA globales fue menor que la observada en Biobadaser(10). El AA más frecuentemente observado fue la infección similar a lo comunicado en otros registros (11,12). Siendo las infecciones del tracto respiratorio las más frecuentes. Quizás esto pudiera tener una causa multifactorial; por lo cual se requerirían análisis más específicos sobre este punto para valorar las causas.
Las neoplasias malignas son otros de los AA de interés, entre los cuales el cáncer de mama fue el más frecuentemente reportado. Estos datos están en concordancia con lo publicado en los registros Biobadasar y Biobadaser(5,13). En este sentido, esta frecuencia está dentro de los valores descritos para la población de la región(14) y lo que nos insta a intensificar los estudios de detección precoz.
El análisis de incidencia de AA según línea de tratamiento mostró mayor incidencia de AA en segundas o posteriores líneas de tratamiento. Estos resultados están en consonancia con publicaciones previas en las cuales se constató que líneas posteriores de tratamiento se han asociado a un mayor riesgo de AA(13,15). En este sentido se ha postulado que este hallazgo se podría relacionar con pacientes con una enfermedad más grave, por el uso de mayor número de inmunosupresores, quizás mayor dosis acumulativa de corticoides o la suma de dichos factores.
La AR se asoció a una mayor incidencia de AA globales. Estos datos podrían estar en relación con múltiples factores como el mayor número de pacientes con AR en el registro Biobadaguay, así como las diferencias de edad y múltiples tratamientos concomitantes de los pacientes(16).
Nuestro estudio tiene puntos fuertes y limitaciones. Este estudio representa datos de la práctica clínica real de una cohorte de pacientes bajo tratamiento con terapias biológicas, lo cual aporta datos de nuestra realidad y colabora al seguimiento de nuestros pacientes; así mismo constata la necesidad de continuar con una constante vigilancia de seguridad a través del registro.
Con relación a las limitaciones se puede mencionar el hecho que los distintos agentes biológicos han tenido una diferencia temporal de comercialización y disponibilidad, el número de registros es superior para los que fueron primeramente introducidos, lo que puede ocasionar sesgos en el análisis de los datos. Otra limitación importante es el posible sesgo en la información de los AA no cumplimentados por el investigador. Por estos motivos se seguirá trabajando para obtener una mejor notificación, y obtener datos de mayor calidad.
Este proyecto es resultado de la colaboración de reumatólogos paraguayos y uruguayos con el apoyo de las Sociedades de Reumatología de ambos países. Es importante la continuidad de este tipo de registros para mejorar la información sobre el uso de estas terapias que podrá ser utilizada en la mejor atención de nuestros pacientes.