1. INTRODUCCIÓN
La contaminación del agua por metales pesados ocasionada por actividades industriales, agrícolas, mineras, actividad volcánica, y alojamiento de aguas residuales negras está afectando drásticamente la seguridad alimentaria. Incluso bajas concentraciones de metales pueden amenazar la salud de organismos acuáticos y terrestres, incluido el hombre1. Es importante considerar que los seres vivos al ingerir estos metales pesados sufren efectos tóxicos y nocivos debido a que alteran varias funciones biológicas2. Sin embargo la excesiva concentración de estos metales pesados pueden alterar procesos bioquímicos y/o fisiológicos en el organismo del ser humano, lo que hace tóxico a los metales es su concentración elevada por encima de lo permitido en las normas que rigen y controlan3. No sólo por sus características químicas y más importante aún, el tipo de compuesto o metabolito que forman, porque interaccionan con otros compuestos, lo que provoca la aparición de enfermedades4).
Se puede decir que el ser humano al exponerse a concentraciones altas de arsénico (As), puede presentar problemas en su fertilidad atacando órganos vitales del sistema reproductivo5).
La Organización Mundial de la Salud (OMS) y algunos organismos ambientales de control, han establecido niveles de riesgo en función de la concentración de metales, con respecto a aguas de consumo humano y alimentos; como es el caso para el arsénico, según estadísticas establecidas, la población en riesgo de exposición supera los 150 millones. Esto ve obligado a fortalecer los programas de saneamiento apoyados en tecnologías emergentes de control como la bio y nanotecnología, para el desarrollo de procesos y estrategias experimentales en tareas de detección, cuantificación y remediación6.
Debido a su alta concentración en los sedimentos marinos, el arsénico puede causar toxicidad aguda y crónica a los organismos que allí habitan6. Se dice que en las especies comestibles que son de gran demanda en países de medio oriente como Japón, el (As) se puede almacenar en su interior de una forma no controlable y por lo tanto es muy nociva7.
Se ha reportado que el arsénico se asocia a las vitaminas, minerales y carbohidratos por lo que, la exposición crónica al arsénico puede producir cáncer de vejiga, pulmones, piel y próstata, así como, enfermedad del corazón(8, 9). A corto plazo puede causar problemas gastrointestinales, calambres musculares y lesiones en manos y pies. El riesgo de envenenamiento por arsénico es mayor para personas que comen arroz varias veces al día10).
Esta situación ha generado la aparición de desórdenes en el ser humano, ocasionados por la toxicidad alta que tienen algunos metales pesados11. La contaminación por metales pesados ocasiona graves daños en el organismo, ya que incluso a niveles de ultrazas, como es el caso del arsénico (As), generan alteraciones de diferente índole, incluyendo cambios metabólicos, neurológicos, mentales y genéticos12. De allí, la necesidad de realizar controles de la concentración de estos compuestos y desarrollar metodologías para su determinación en muestras biológicas, ambientales y alimenticias13. Las diferentes técnicas espectroscópicas, han jugado un papel destacado en la determinación de ultrazas de metales, alcanzándose en una amplia variedad de muestras, con bajos límites de detección, amplios rangos lineales y determinaciones multielementales rápidas.
La exactitud y la reproducibilidad de los resultados obtenidos mediante estas técnicas pueden verse afectadas por la matriz en la que se encuentra el analito, ya que normalmente la concentración analítica de interés es muy baja o la matriz de la muestra es muy compleja14. Por ello, usualmente es vital implementar metodologías de preconcentración y/o de introducción de muestras en el espectrofotómetro, implicando la separación del analito de la matriz y así logrando óptimos resultados ]. En este sentido, la generación electroquímica de hidruros como técnica de introducción de muestra, constituye un procedimiento ideal para el transporte de muestras en fase gaseosa y su posterior determinación por Espectroscopia de Absorción Atómica, presentando ventajas significativas; que se traducen en mejoras de sensibilidad y capacidad de detección15. El presente trabajo evalúa la generación electroquímica de arsina (AsH3), un compuesto de arsénico, utilizando diferentes materiales catódicos para su determinación y se comparan los parámetros analíticos del método (exactitud, precisión) con los reportados por otros autores, estableciendo comparaciones; La eficacia de la metodología se ha demostrado mediante la determinación de este metal por espectroscopia de absorción atómica en materiales de referencia estándar16.
2. METODOLOGÍA
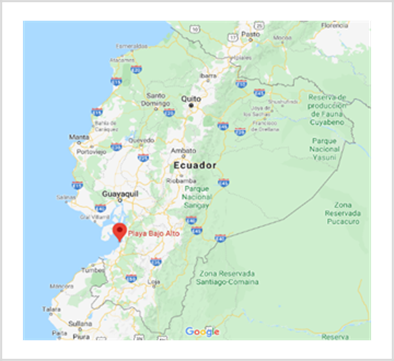
El lugar de estudio correspondió a la Comuna de Bajoalto, ubicada en la Provincia El Oro, Ecuador, zona fronteriza con Perú, tal como se puede observar en la Figura 1. La generación electroquímica de arsina (AsH3), fue realizada acorde a lo reportado por Caiminagua et al. (16. Para lo cual,
en la superficie del cátodo se induce la reducción del As3+ al estado elemental, y posteriormente su hidrogenación por átomos de hidrógeno producidos y adsorbidos en el mismo cátodo para formar el hidruro volátil, que fue transportado por gas argón (Ar) a través de una celda de cuarzo, para su posterior cuantificación en el espectrofotómetro de absorción atómica (Figura 2)16.

Figura 2 Sistema de una celda electroquímica acoplada al Espectrofotómetro de Absorción Atómica Shimadzu modelo AA-6300.
En la Figura 3 se puede observar que dentro de la celda de generación electroquímica se encuentra el cátodo amalgamado de Au o Ag (área 3 cm2) y un ánodo de platino en espiral que lo rodea completamente para la separación del analito de su matriz con la minimización inherente de interferencias.

Figura 3 Celda electroquímica desarrollada en este estudio para introducir la muestra en el espectrofotómetro de absorción atómica y su respectiva generación de hidruros.
Por su parte, la Tabla 1 presenta los parámetros operacionales para el funcionamiento en la celda electroquímica utilizada en este estudio.
Tabla 1 Parámetros operacionales para el funcionamiento en la celda electroquímica.
| Parámetros | |
| Materiales catódicos | Au, Au/Hg, Ag, CV, Pb ó Pt |
| Superficie de cátodo (cm2) | 3.0 |
| Material del Ánodo | Platino (Alambre en forma de espiral) |
| Corriente Electroquímica (A) | 0.6 - 0.8 |
| Electrolito (M) y Flujo de Argón (mL min-1) | H2SO4/HCl 0.5M y 50 mL/min |
La digestión ácida se realizó es un digestor microonda tratando 0,4634 g de material de referencia con 3 mL de mezcla ácida (HNO3: HF: HClO4 (3: 3: 1). La curva de calibración se obtuvo utilizando la metodología propuesta por Caiminagua et al. (16.
3. RESULTADOS Y DISCUSIÓN
Los resultados que se analizan en este trabajo fueron obtenidos de la absorbancia en función del incremento de corriente debido a las variaciones en las concentraciones del hidruro generado (AsH3), acorde a lo reportado por Caiminagua et al.16.
De acuerdo a la curva de calibración, sobre el cátodo de Au/Hg se determinaron los siguientes parámetros analíticos de validación del método: Límite de detección; 0,027 µg Kg-1; calculado a partir de tres veces la desviación estándar de 10 medidas de la solución del blanco entre la pendiente de la curva de calibración. Se obtuvo una reproducibilidad (RSD) de 2,4% y una exactitud de 95,04%. Debido a que el resultado del análisis de material de referencia de sedimento marino PACS-2 (Consejo Nacional de Investigación de Canadá), tiene un certificado de concentración de As de 26,2 ± 1,5 mg / kg, el resultado promedio obtenido fue de 24,9 ± 1,1 mg / kg, error de 2,4 %16.
El análisis de muestras de sedimento marino en una muestra real como es de la comuna de Bajo Alto, arrojó como resultados preliminares, un contenido de As del 0.05 mg/Kg, siendo el límite permitido por la Organización Mundial de la Salud de 5 mg/Kg.
Dentro de este estudio los valores de precisión obtenidos no exceden del 2,4%. En este sentido17, han reportado límites de detección de 0,09 mg .kg-1(90 µg/kg) mayor que el de 0,000027 mg.kg-1 (0,027 µg/kg) reportado en este estudio para As, Estos autores reportaron una repetibilidad 0,6% y precisión inferior al 3%. Para valores inferiores a 7,2 mg kg-1 de concentración no existe riesgo potencialmente tóxico para la biota según la NOAA13. En la literatura se han encontrado concentraciones de arsénico total de sedimentos arenosos con una variación de 0,3 mg/Kg a 13 mg/Kg en arenas, de 4 mg/Kg a 23 mg/Kg en lodos y de 15 mg/Kg a 23 mg/Kg en aleurita18. Estos valores superan los 0.05 mg/Kg reportados en este estudio.
Por otro lado, los valores de límites de detección presentados en este trabajo de investigación (0,027 µg/kg) son más bajos a lo reportado por Sankararamakrishnan & Mishra19, donde se obtuvieron límites de detección de As(III) 0,6 (µg/kg) y As(V) 0,5 (µg/kg).
Adicionalmente, en la literatura existen varios artículos relacionados al acoplamiento de técnicas para mejorar la sensibilidad y demás parámetros analíticos para la validación de métodos analíticos de determinación de arsénico. Tal es el caso de la determinación de arsenito As (III) y arsenato As (V) en algunos sedimentos y muestras de agua utilizando espectrometría de absorción atómica con generación química de hidruros (HG-AAS). La precisión para nueve réplicas de muestra fue de 3.1% para todas las especies de arsénico. Esto fue determinado mediante el análisis de un material de referencia de sedimento lacustre (IAEA-SL-1)20.
4. CONCLUSIÓN
Utilizando el sistema de generación electroquímica de hidruros propuesto, fue posible generar especies volátiles de As, los cuales se detectaron por Espectroscopia de Absorción Atómica.
Se determinaron los siguientes parámetros analíticos de validación del método estudiado: límite de detección; 0,027 µg L-1; reproducibilidad (RSD) de 2.4% y una exactitud de 95,04%. Debido a que, el resultado del análisis de material de referencia de sedimento marino PACS-2 (Consejo Nacional de Investigación de Canadá), tiene un certificado de concentración de As de 26,2 ± 1,5 mg / kg, el resultado promedio obtenido fue de 24,9 ± 1,1 mg / kg, error de 2,4 %. El análisis de muestras de sedimento marino en una muestra real como es de la comuna de Bajo Alto, arrojó como resultados preliminares, un contenido de As del 0.05 µg/g, siendo el límite permitido por la Organización Mundial de la Salud de 5 mg/Kg.












 uBio
uBio