Introducción
El riesgo del ser humano de padecer un aneurisma intracraneal se calcula entre 1-2 %1, en el 80 % de los casos su forma de presentación es una hemorragia subaracnoidea (HSAa), cuya incidencia varía considerablemente de un área geográfica a otra, se estiman 2 casos/100 000 habitantes en China y 22,5/100 000 en Finlandia2. En los Estados Unidos de Norteamérica se informaron 14,5/100 000 hospitalizaciones por esta causa en el año 20033. El objetivo fundamental del tratamiento de un aneurisma intracraneal es su exclusión de la circulación, este puede obtenerse por dos formas, el tratamiento microquirúrgico o a través de la obliteración endovascular.
Durante varias décadas la microcirugía ha sido el método más usado, pero en los inicios de la década de los noventa, la mejoría en la técnica del tratamiento endovascular informada por Guglielmi y posteriormente el mejoramiento de los materiales usados para la obliteración, representó una nueva etapa en el tratamiento de estos pacientes y una controversia por la búsqueda del método ideal que se mantiene hasta la actualidad4.
En el año 2017 Bender et al4, publicaron un artículo en el que revisan una base de datos que incluye información de pacientes admitidos por una HSAa entre los años 1991 y 2016, con una disponibilidad de 1 306 pacientes de 1 562 que padecieron la enfermedad, en el que se encuentra que el 72 % de los casos fueron tratados con microcirugía, contra 22 % de tratamiento endovascular y el 5,7 % no fueron tratados, también se demuestra un incremento exponencial por quinquenios de este último procedimiento que alcanza entre los años 2012-2016 el 41,9 %, lo que evidencia la preferencia de muchos neurocirujanos por esta modalidad, sin embargo un ensayo publicado recientemente, en el que se estudian 104 pacientes con diagnóstico de aneurismas no rotos, 48 tratados con microcirugía y 56 con endovascular concluyó que no existían diferencias significativas en lo concerniente a morbilidad y mortalidad al comparar ambos procedimientos5. El presente informe tiene como objetivo divulgar la experiencia acumulada durante más de 20 años por el servicio de neurocirugía del Hospital Provincial “Roberto Rodríguez”, con el uso de la obliteración microquirúrgica de aneurismas intracraneales.
Metodología
El inicio del servicio de neurocirugía vascular en el Hospital General Docente “Roberto Rodríguez Fernández”, en Morón, provincia de Ciego de Ávila, Cuba, estuvo precedido por un entrenamiento del autor principal de este artículo bajo el principio pedagógico de educación continuada en el trabajo, que incluyó los cuatro años de la residencia y luego seis meses en los que se intervinieron los primeros 10 pacientes, que fueron trasladados hacia el servicio de neurocirugía del hospital “Manuel Ascunce Domenech” de Camagüey, Cuba, cuyo proceso docente asistencial estuvo bajo la supervisión del Profesor Sergio Vega Basulto, formador de varias generaciones de neurocirujanos de la región central de Cuba.
El presente es un estudio descriptivo que incluye a todos los pacientes que presentaron un diagnóstico de aneurisma intracraneal y que fueran intervenidos con técnica de microcirugía para su exclusión de la circulación, en el periodo comprendido entre enero de 1997 y diciembre del 2020.
Todos los enfermos fueron atendidos a su llegada al departamento de emergencias de acuerdo con los algoritmos diseñados para el tratamiento de la enfermedad cerebrovascular hemorrágica en el hospital y fueron admitidos en las unidades de atención al grave (cuidados intermedios y cuidados intensivos), en dependencia de su estado neurológico al momento del ingreso, evaluado por la clasificación de la escala mundial de neurocirujanos (WFNS)6) y el Intracerebral Haemorrhage Score (ICH score) en caso que se acompañara de una hemorragia intraparenquimatosa7.
A todos se les realizó un estudio de opacificación vascular a través de angiografía cerebral de los cuatro vasos, Angio-tomografía axial computarizada (Angio-TAC) multicortes o Angio-resonancia magnética; que fue evaluado por un equipo multidisciplinario constituido por dos especialistas en neurocirugía y un especialista en neurorradiología. Se consideró la presencia de al menos un aneurisma intracraneal como condición imprescindible para decidir el tratamiento quirúrgico. El momento de la cirugía dependió totalmente de esta condición. La información fue obtenida del cuestionario y de los expedientes clínicos y vertida en una base de datos creada por el autor con el sistema SPSS versión 21 para Windows.
Las variables consideradas en la serie fueron: Edad: que fue dividida en grupos: de 18-30 años, de 31-40, de 41-50, de 51-60 y más de 60. Sexo: masculino o femenino. Color de la piel: blanca, negra, mestiza y amarilla. Procedencia: se distribuyeron los casos en nueve categorías dependiendo del municipio de la provincia del cual procedían. Estado clínico al ingreso: fue evaluado por la clasificación de la WFNS6. Los resultados de los estudios de neuroimagen al ingreso y secuenciales: En la TAC simple al ingreso y en los estudios secuenciales se evaluó la presencia de sangre intracraneal de acuerdo con la clasificación de Columbia (Fisher modificada)8. Estudios de opacificación vascular: se clasificaron los sacos aneurismáticos en micro aneurismas, pequeños, medianos, grandes y gigantes, además fueron divididos de acuerdo a su número en únicos y múltiples, también se distribuyeron de acuerdo a su localización en el segmento anterior o posterior del círculo de Willis. Corredores quirúrgicos: Los corredores quirúrgicos fueron seleccionados en dependencia de la localización, disposición espacial del saco en el circulo de Willis y el espacio subaracnoideo, tamaño y morfología. Estrategias adyuvantes: Se utilizaron estrategias adyuvantes al procedimiento convencional para facilitar el acto del presillamiento aneurismático como lo fueron el drenaje espinal continuo, la ventriculostomìa al exterior para drenaje de LCR y monitorización continua de la PIC y de la presión de retracción cerebral, cierre temporal de la arteria madre, clinoidectomía y sección del ligamento falciforme para los aneurismas del segmento oftálmico y succión retrograda descompresión en los aneurismas gigantes. La comprobación de la exclusión de la circulación del saco aneurismático se obtuvo por dos vías, a través del ponchado trans operatorio del saco una vez presillado y a través de la angiografía transoperatoria. Las complicaciones: se dividieron en pre operatorias, trans operatorias y post operatorias. Los resultados: fueron evaluados de acuerdo con la escala de Rankin modificada para resultados8. Se correlacionan algunas de las variables para llegar a conclusiones más precisas.
Se utiliza la prueba no paramétrica de bondad de ajuste de Chi cuadrado para evaluar hipótesis acerca de las relaciones entre dos variables. Se consideran significativos los valores de p≤0,05. Los resultados son expuestos en figuras para su mejor análisis y comprensión.
Resultados
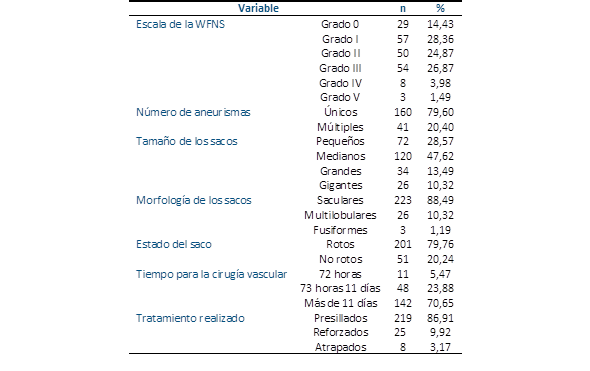
Se estudiaron 201 pacientes, de los cuales 198 (98,51 %), mostraban aneurismas de la circulación anterior y solo 3 (1,49 %), de la circulación posterior. En total fueron abordados 252 sacos, de los cuales 201 (79,76 %) estaban rotos y 51 (20,24 %) no rotos, formando parte de un estado de multiplicidad aneurismática. Las características generales de la muestra se encuentran en la Tabla 1.
En cuanto a los datos clínicos, los hallazgos más frecuentes fueron malformación arteriovenosa cerebral, angiografía normal y aneurisma. Los presentan los motivos de consulta más frecuentes fueron cefalea con 61,95 %, déficit neurológico con 7,08 %, alteración del sensorio 7,08 %, convulsión 2,65 %, accidente transitorio isquémico 2,65 %, control 2,65 % y parkinsonismo en el 1,77 %.
Para el diagnóstico imagenológico se emplearon la panangiografía cerebral en 106 casos (52,74 %), la angio TAC multicortes en 91 (45,27 %) y la angio RMN en 4 pacientes (1,99 %). La distribución topográfica de los sacos por grupos arteriales fue la siguiente: Segmento de la arteria oftálmica 22 (8,73 %), segmento de la arteria comunicante posterior 118 (46,82 %), segmento de la arteria coroidea anterior 25 (9,92 %), arteria cerebral media 55 (21,82 %), complejo arteria cerebral anterior-comunicante anterior 28 (11,11 %), tope de la arteria basilar 1 (0,40 %), arteria cerebelosa superior 1 (0,40 %), arteria cerebelosa postero-inferior 1 (0,40 %) y rama distal de la arteria cerebral anterior 1(0,40 %).
El mayor número de enfermos en el momento de la cirugía se encontraban entre los grados I y III de la clasificación de la WFNS, 161 (80,09 %), de acuerdo a su número predominaron los aneurismas únicos 160 (79,60 %) y 41 (20,40 %) tuvieron aneurismas múltiples. Los 41 casos con aneurismas múltiples, además de tener un saco roto tuvieron sacos no rotos distribuidos de la siguiente manera hasta completar los 252 sacos tratados en la serie. 32 pacientes mostraron dos aneurismas (1 roto y 1 no roto), 8 casos presentaron 3 sacos (1 roto y dos no rotos y 1 enfermo evidenció 4 sacos, 1 roto y 3 no rotos. Los aneurismas de mediano tamaño y los de morfología sacular. Todos los pacientes tuvieron al menos un saco aneurismático roto y la mayoría de los enfermos, 190 (94,53 %) fueron operados en la fase intermedia o tardía de su evolución. La mayoría de los sacos, rotos y no rotos fueron presillados y excluidos de la circulación en un mismo tiempo quirúrgico.
Las lesiones asociadas a la HSAa fueron: Hemorragia intraventricular en 12 pacientes (5,97 %), infarto cerebral en 9 (4,48 %), hemorragia intraparenquimatosa en 6 (2,99 %), hidrocefalia 7 (3,48 %), concomitó la presencia de una malformación arteriovenosa en 3 casos (1,49 %), hematoma subdural crónico 1(0,50 %), para un total de 38 casos con lesiones asociadas, lo que representó un 18,91 % de la serie.
Los corredores quirúrgicos utilizados estuvieron en relación con la localización de los sacos, con un predominio del keyhole supra orbitario, 154 (61,11 %) y los aneurismas situados en el segmento de la comunicante posterior de la arteria carótida supraclinoidea (Figura 1). Los procedimientos adyuvantes para facilitar la disección subaracnoidea, de la arteria madre y del cuello aneurismático son expuestos en la Figura 2.
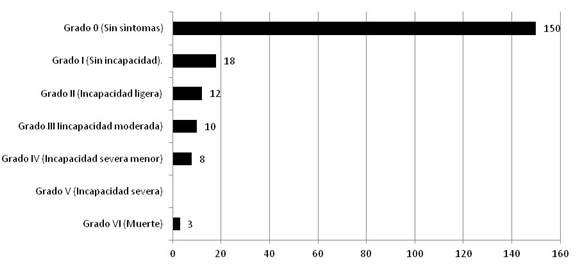
Las complicaciones fueron divididas en pre operatorias, trans operatorias y post operatorias. Entre las pre operatorias se presentaron con mayor frecuencia el vasospasmo sin infarto 14 (6,97 %) y el infarto cerebral 13 (6,47 %). Además, la hidrocefalia estuvo presente en 7 (3,48 %), la hemorragia intraparenquimatosa en 7 (3,48 %), así como 3 resangrado (1,49 %) y 1 hematoma subdural crónico (0,50 %). Las complicaciones trans operatorias fueron edema cerebral en 12 (5,97 %) y sangrado en 6 (2,99 %). Entre las post operatorias se encontraron 7 hidrocefalias (3,48 %), 5 vasospasmos post quirúrgicos (2,48 %), 5 disturbios hidroelectrolíticos (2,48 %), 2 disturbios acido-base (0,99 %), 2 infecciones de heridas quirúrgicas (0,99 %), 1 edema agudo de pulmón (0,50 %), 1 infarto agudo de miocardio (0,50 %), 1 hematoma epidural en el área de la craneotomía (0,50 %) y 1 infección de la herida quirúrgica (0,50 %). Los resultados son expuestos en la Figura 3, donde se aprecia el predominio de los Grados 0 o pacientes sin síntomas, también se expone una mortalidad para la serie de 1,49 %.
Discusión
La exclusión de la circulación a través de procedimientos microquirúrgicos, ha representado la única forma de tratamiento definitivo de los aneurismas intracraneales rotos y no rotos durante más de 20 años en el hospital general docente “Roberto Rodríguez Fernández” de Morón, en la provincia de Ciego de Ávila, Cuba.
La necesidad de re intervención para exclusión de la circulación de los sacos en pacientes ya tratados y la mortalidad, son dos variables a considerar cuando se evalúa la utilidad de un procedimiento. En esta serie de 201 enfermos con 252 sacos aneurismáticos abordados, solo dos casos (0,99 %), necesitaron un nuevo procedimiento después de intervenidos quirúrgicamente, uno de ellos requirió de un procedimiento endovascular después de un intento fallido de presillamiento de un saco en el segmento de la arteria oftálmica izquierda, que no pudo realizarse por la presencia de un sangrado antes de acceder al área, este paciente mostraba además otros dos micro aneurismas de la circulación anterior, que fueron manejados conservadoramente. El otro caso mostró crecimiento de un remanente del saco, en un aneurisma de la arteria comunicante anterior después de dos años de la cirugía inicial practicada en otra institución de nuestro país. La incidencia de remanentes aneurismáticos o aneurismas de novo en nuestra serie se comportó por debajo de lo informado por Burkhardt JK et al9, quienes tuvieron una incidencia del 4,6 %.
El predominio de los aneurismas con tamaño superior a los 7mm y de la localización en el segmento de la arteria comunicante posterior probablemente haya incidido en la alta frecuencia de ruptura de los aneurismas. Desde la publicación del estudio internacional para aneurismas no rotos (ISUIA)10, se conoce que el riesgo de ruptura para 5 años es de 0 % para aquellos sacos con diámetro inferior a los 7mm, de 2,6 % para los que tienen entre 7-12mm, 14,5 % para los que tienen entre 13-24 mm y 40 % para los que tienen 25mm o más11, esto explica la alta incidencia de ruptura en esta serie. En el ISUIA, los aneurismas de la arteria comunicante posterior fueron agrupados con los de la circulación posterior en lo que respecta al riesgo de ruptura, al considerar que los aneurismas del mismo tamaño en estas localizaciones mostraban un riesgo de ruptura superior al resto de las topografías10.
La selección del corredor quirúrgico utilizado en relación con la topografía y la proyección del saco, es importante para lograr de forma exitosa la posterior disección subaracnoidea y el presillamiento del cuello. En esta serie se muestra la experiencia adquirida por el autor con la utilización del Keyhole supra orbitario; con incisión transciliar, para abordar los aneurismas localizados en el segmento anterior del círculo de Willis. Esta experiencia está fundamentada en estudios de comparación entre varias craneotomías, en el análisis espacial de la cavidad intracraneal y la aplicación de principios de óptica, que han garantizado utilizar de forma eficiente el corredor y obtener los objetivos quirúrgicos trazados en cada paciente12. El empleo del endoscopio como instrumento auxiliar en este tipo de corredor (usado en esta serie) y la utilización de angiografía endoscópica fluorescente intraoperatoria con verde de indocyanina, tecnología con la que no contamos en nuestro centro, han facilitado el desarrollo del procedimiento en las últimas cuatro décadas12-15.
Ante la presencia de aneurismas gigantes o en aquellos con alto riesgo de ruptura transoperatoria, incluida la cirugía en fase aguda, la utilización de corredores con mayor exposición y versatilidad respecto a la disponibilidad de diferentes ángulos de visualización del campo quirúrgico, como el corredor fronto-temporo-orbito-cigomàtico y sus variantes16, fue de gran utilidad.
La utilización de medidas adyuvantes para facilitar la retracción cerebral, la disección subaracnoidea, la disección de las estructuras vasculares y sus relaciones neurales y óseas en la base del cráneo hasta acceder al saco, fue una práctica usual durante las cirugías en la serie y sirvió para permitir la adecuada disección y posterior presillamiento del cuello aneurismático.
La apertura y drenaje de LCR en la cisterna opto carotidea se realizó en todos los casos, combinado con el uso de manitol, conducta que facilitó la relajación necesaria en el parénquima cerebral, para permitir la retracción y exposición de las estructuras neurovasculares en la base. Estas maniobras fueron reforzadas con el drenaje intermitente de LCR a través de una ventriculostomía funcional al exterior, por medio de un catéter colocado en el ventrículo lateral o a través de un catéter para drenaje continuo de LCR colocado en el espacio subaracnoideo espinal de la columna lumbar, este último procedimiento fue menos utilizado. La ventriculostomía fue usada, además, para monitorizar la presión intracraneal y la presión de retracción cerebral, intentando mantenerla alrededor de 20 mmHg, también se realizó retracción intermitente, ambas maniobras tuvieron como objetivo evitar lesiones isquémicas sobre la corteza cerebral provocadas con frecuencia por la retracción desmedida.
El cierre temporal de la arteria madre constituye una práctica frecuente por la mayoría de los neurocirujanos vasculares, en la fase final de disección del cuello antes del presillamiento definitivo. En esta serie se utilizó como medida de protección cerebral un coctel (“Coctel de Morón”), constituido por: 100 ml de manitol al 20 %, 500 mg de metilprednisolona y 600mg de ácido ascórbico, administrado 20 minutos antes del cierre temporal, esta medida fue acompañada por la indicación de hipotensión controlada obtenida con el empleo de nitroglicerina o nitroprusiato de sodio. El cierre se mantuvo durante un mínimo de cinco minutos y un máximo de 20.
En más de la mitad de los pacientes con aneurismas gigantes, que fueron aquellos localizados en el segmento paraclinoideo, utilizamos la técnica de succión retrograda-descompresión, para lograr “desinflar” el saco y permitir la disección del cuello y su presillamiento.
Una vez logrados los objetivos propuestos para la cirugía se usó una solución de suero fisiológico al 0,9 % con metilprednisolona (bulbos de 500 mg), a razón de 1mg/ml, para irrigar las cisternas involucradas en el procedimiento quirúrgico, con el propósito de prevenir la ocurrencia de vasospasmo mecánico tras la manipulación de las paredes arteriales a través del efecto anti inflamatorio de los esteroides17,18.
Los resultados obtenidos en este estudio, evaluados a través de la escala de Rankin modificada, evidencian la alta eficacia del tratamiento microquirúrgico para los aneurismas intracraneales en nuestro medio, en el que un elevado número de pacientes fueron egresados sin ningún tipo de secuelas (74,62 %) y la mortalidad fue de 1,49%. La controversia internacional sobre cuál sería el tratamiento ideal para un aneurisma intracraneal roto o no roto, la microcirugía o el endovascular, aún continua en la actualidad, mientras el presillamiento microquirúrgico mejorado con el empleo de nuevas técnicas diagnósticas y de ópticas, continúa representando un arma eficaz para el tratamiento de este tipo de enfermedad(19, 20).
De esta forma podemos concluir que el tratamiento microquirúrgico representa la principal forma de tratamiento para excluir de la circulación los aneurismas intracraneales en nuestro hospital, hasta tanto se implementen y estén disponibles de forma regular otras alternativas de tratamiento4,5,21-24, como opción primaria o con la que se puedan realizar tratamientos híbridos o combinados. Los procedimientos adyuvantes son estrategias elegidas por el cirujano para garantizar la relajación del parénquima y del saco aneurismático y de esta forma facilitar el presillamiento del cuello.