Introducción
El glaucoma se define como una neuropatía óptica progresiva multifactorial1. A nivel mundial el glaucoma es la principal causa de ceguera irreversible2,3. Uno de los principales factores de riesgo para su desarrollo y progresión es la presión intraocular (PIO) elevada4. Los medicamentos tópicos para el glaucoma disminuyen la PIO al reducir la producción de humor acuoso o mejorar el flujo de salida5.
Las prostaglandinas tópicas (PGs), con su potente efecto hipotensor ocular son una importante opción de tratamiento para el glaucoma6. El Latanoprost fue el primer análogo de PG del que se desarrollaron genéricos7. Latanoprostene Bunod (LBN) es una nueva prostaglandina F2 donante de óxido nítrico. El compuesto se metaboliza rápidamente en ácido latanoprost, un análogo de prostaglandina, y mononitrato de butanodiol, una fracción que dona óxido nítrico (NO), luego de la exposición a esterasas en el ambiente ocular8. Los datos indican que los efectos de LBN sobre la PIO es una sumatoria de acciones en las vías de flujo de salida del humor acuoso tanto convencionales como no convencionales. Mientras que el latanoprost reduce la PIO solo por la vía no convencional9,10,11.
Se sabe que los donantes de NO inducen la relajación de la red trabecular y el canal de Schlemm, lo que aumenta el flujo de salida del humor acuoso a través de la vía convencional12,13. El Latanoprost, está indicado para la reducción de la PIO elevada en pacientes con glaucoma de ángulo abierto (GAA) e hipertensión ocular (HTO)14. En este estudio comparamos el efecto reductor de la PIO de Latanoprostene bunod (LBN) al 0,024 % con Latanoprost al 0,005 % así como evaluar los efectos secundarios asociados a ambas medicaciones.
Metodología
Se realizó un ensayo observacional, de cohorte prospectivo, donde se comparó la eficacia del tratamiento médico hipotensor entre dos grupos uno tratado con Latanoprostene bunod (LBN) al 0,024 % y otro grupo tratado con Latanoprost al 0,005 %. Se reclutaron pacientes del servicio de oftalmología del Hospital de Clínicas con diagnóstico de Glaucoma de ángulo abierto y/o Hipertensión ocular cuya consulta fue entre los meses de abril a agosto del año 2022.
El muestreo fue aleatorio simple y se incluyeron pacientes con diagnóstico de glaucoma de ángulo abierto (glaucoma primario de ángulo abierto, glaucoma pseudoexfoliativo y glaucoma pigmentario) o hipertensión ocular, quienes tuviesen disponibilidad y colaboración para la realización de las pruebas del protocolo exploratorio, sin ningún tratamiento hipotensor previo y que hayan aceptado y firmado el consentimiento informado. Los pacientes fueron divididos en 2 grupos paralelos: un grupo tratado con Latanoprostene bunod (LBN) al 0,024 % y otro grupo tratado con Latanoprost al 0,005 %, las variables cualitativas medidas fueron sexo, tipo de glaucoma, procedencia, sensación de visión borrosa, sensación de ojo seco, lagrimeo, quratopatía punteada superficial, congestion conjuntival, efectos esteticos locales; las variables cuantitativas medidas fueron edad, agudeza visual (sistema decimal), tiempo de ruptura del film lagrimal, presion intraocular (medida en mmHg con el tonómetro de Goldman), la relación copa-disco. Para el cálculo del tamaño de la muestra se consideró una magnitud del efecto de 5 mmHg con un DE de 2 y una magnitud de efecto estandarizado de 0,5, para un alfa unilateral de 0,05 y una potencia de 80 %.
Se utilizó el programa Gpower 3.1 para el cálculo del tamaño muestral. Con estos parámetros el cálculo de la muestra es de 26 ojos por grupo. Los datos fueron consignados en una planilla electrónica Excel 2022 con las variables incluidas en la investigación y posteriormente fueron analizadas con el programa SPSS Versión 22, los resultados se expresaron en frecuencias, porcentajes, medias y desvíos estándar. Para los análisis comparativos de variables dicotómicas se utilizó el Test exacto de Fischer y para los análisis comparativos de variables continuas la prueba de t de student y ANOVA.
Se consideró una p<0,05 como estadísticamente significativa. Se informó a los participantes sobre el propósito del estudio; una explicación completa acerca de la participación voluntaria, sin compensación, donde la atención médica no sería comprometida si se negaran a participar del estudio, los mismos firmaron un consentimiento informado por escrito de acuerdo a los estándares éticos de la revisión 2000 de la Declaración de Helsinki para formar parte del trabajo de investigación.
Los sujetos con diagnóstico nuevo de glaucoma de ángulo abierto (específicamente glaucoma primario de ángulo abierto, glaucoma psedoexfoliativo y glaucoma pigmentario) o hipertensión ocular en los meses de abril a agosto del año 2022 fueron aleatorizados 1:1 a grupo Latanoprost o grupo LBN con una instilación del fármaco correspondiente de una gota una vez por día (a las 21:00 horas) durante un mes.
Al grupo LBN se le dio VYZULTA® de Bausch+Lomb (latanoprostene bunod ophthalmic solution 0,024 %) y al grupo Latanoprost se le dió LATOF® de Saval (latanoprost ophthalmic solution 0,005 %). Se realizó la medición de la PIO en dos cortes: en el día 0 (antes de empezar el tratamiento), y luego de 1 mes de iniciado el tratamiento. En estas dos oportunidades la PIO se tomó de la siguiente manera: tres mediciones, hechas por el mismo operador utilizando el mismo tonómetro de Goldman, separadas por 10 minutos y se utilizó el promedio de estas tres mediciones. La primera medición se hizo a las 9:00 h de la mañana.
Con respecto a los asuntos éticos, la investigación tuvo como base los fundamentos de las normas de Declaración de Helsinki. No se realizó distinción de sexo, raza, creencias o ideologías. Se respetó el anonimato de cada individuo ya que a cada uno de ellos le fue asignado un código, conociendo su identidad únicamente el investigador principal. Todas las demás personas que colaboraron en el proyecto tuvieron conocimiento del código asignado a cada paciente, no así a su identidad real. Cada paciente firmó un consentimiento informado para participar del estudio.
Resultados
El estudio fue realizado en 28 pacientes (56 ojos) quienes fueron aleatorizados en 2 grupos paralelos (28 ojos por grupo), el grupo latanoprost y el grupo latanoprostene bunod (LBN). Con respecto a las variables demográficas, la distribución por sexo fue igual en ambos grupos (8 hombres y 6 mujeres). En el grupo LBN la media de la edad fue de 60,9 ± 9 años y en el grupo latanoprost la media de edad fue de 64,2 ± 6 años.
La agudeza visual promedio de los pacientes, medida en el sistema decimal, en el grupo LBN fue de 0,6 décimas mientras que en el grupo latanoprost fue de 0,5 décimas. La relación copa-disco en ambos grupos fue de 0,7. Los diagnósticos encontrados en ambos grupos se detallan en la tabla 1, donde se puede observar que en los dos grupos el diagnóstico con más prevalencia fue el de glaucoma primario de ángulo abierto (GPAA) con 12 casos en el grupo LBN (42,8 %) y 16 casos en el grupo latanoprost (57,1 %) (Tabla 1).
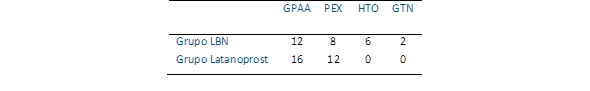
Tabla 1 Diagnósticos encontrados por grupo (GPAA: glaucoma primario de ángulo abierto, PEX: glaucoma pseudoexfoliativo, HTO: hipertensión ocular, GTN: glaucoma de tensión normal) (n=56).
Con respecto a la eficacia del tratamiento; tomando a todos los pacientes del estudio (tanto del grupo LBN como del grupo latanoprost), y comparando las presiones intraoculares antes del tratamiento y al mes de inicio del tratamiento, se pudo objetivar en ambos gupos una diferencia significativa en la reducción de la presión intraocular (significancia para dos colas bilateral de p<0,001) como se puede observar en la Tabla 2. Al individualizar cada grupo; en el grupo LBN la media de la presión intraocular antes del tratamiento fue de 25,3 ± 6,6 mmHg y la media de la presión intraocular luego de 1 mes de tratamiento fue de 16,5 ± 4,9 mmHg. La reducción de la presión intraocular fue significativa (p=0,01) según la prueba de T de student. En el grupo Latanoprost la media de la presión intraocular antes del tratamiento fue de 23,6 ± 3,6 mmHg y la media de la presión intraocular luego de 1 mes de tratamiento con Latanoprost al 0,005% fue de 15,3 ± 2,4 mmHg. La reducción de la presión intraocular también fue significativa (p=0,01) según la prueba de T de student (Tabla 3).
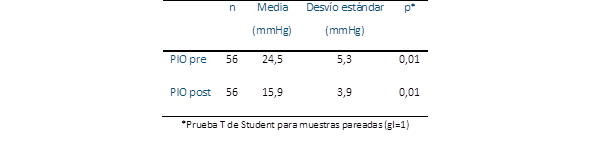
Tabla 2 Media presiones intraoculares antes y después del tratamiento de todos los pacientes del estudio (pio pre: presión intraocular antes del tratamiento, pio post: presión intraocular después del tratamiento) (n=56).

Tabla 3 Media de presiones intraoculares antes y después de 1 mes de tratamiento (pio pre: pio pre tratamiento, pio post: pio post tratamiento) (n=56).
La reducción de la presión intraocular para los pacientes del grupo LBN fue de 34,7 % y la reducción de la presión intraocular para los pacientes del grupo Latanoprost fue de 35,1 %. Finalmente, al comparar las presiones intraoculares posteriores al tratamiento de 1 mes con Latanoprostene bunod 0,024 % y Latanoprost 0,005 % se objetiva, a través de ANOVA, que la diferencia en reducción de la presión intraocular entre estos dos fármacos no es significativa (p= 0,238). Teniendo en cuenta los posibles efectos adversos; con respecto a síntomas de visión borrosa, este síntoma fue negado por todos los pacientes luego de 1 mes de uso del principio activo de su grupo.
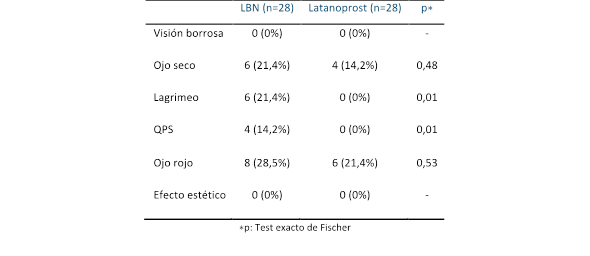
Con respecto a la sensación de ojo seco; este signo fue objetivado en la lámpara de hendidura con un tiempo de ruptura del film lagrimal menor a 10 segundos. Se encontró en 6 ojos sometidos a LBN 0,024 % y en 4 ojos sometidos a Latanoprost 0,005 % luego de 1 mes de uso del principio activo. Si se tiene en cuenta la sensación de lagrimeo; este signo fue objetivado en 6 ojos que utilizaron LBN 0,024 % por 1 mes. En el grupo Latanoprost 0,005 % no fue objetivado en ningún ojo luego de 1 mes de uso. La queratopatía punteada superficial pudo ser objetivada en 4 ojos sometidos a LBN 0,024 %, pero en ninguno del grupo Latanoprost 0,005 % luego de 1 mes de uso del principio activo.
Si tenemos en cuenta el enrojecimiento ocular; este signo fue constatado en 8 ojos sometidos a LBN 0,024 % y en 6 ojos sometidos a Latanoprost. 0,005% luego de 1 mes de uso. En todos estos pacientes existió un enrojecimiento ocular de características leves. Con respecto a los efectos estéticos locales, estos síntomas fueron negados por todos los pacientes del estudio; y al examen no se constató ninguno de estos efectos adversos estéticos locales.
En la Tabla 4 se resumen los hallazgos correspondientes a los efectos adversos encontrados en los pacientes del grupo LBN y del grupo Latanoprost. En el grupo LBN se encontró más efectos adversos oculares relacionados con el fármaco luego de 1 mes de uso (estos fueron ojo seco, lagrimeo, queratopatía punteada superficial y ojo rojo), pero la diferencia fue significativa solo con la queratopatía punteada superficial y el lagrimeo (p< 0,05).
Discusión
Siendo el glaucoma, la principal causa de ceguera irreversible en todo el mundo y con el creciente número y proporción de personas mayores en la población, se prevé que 111,8 millones de personas tendrán glaucoma en 204015. Realidades socioeconómicas y culturales pueden explicar la variabilidad en los procesos de toma de decisiones entre expertos en glaucoma que residen en diferentes partes del mundo y América Latina16. La reducción de la PIO es el único medio comprobado de detener o retardar la progresión del glaucoma17. Incluso los pacientes con Glaucoma primario de ángulo abierto en los que la PIO inicial es inferior o igual a 21 mmHg se benefician del tratamiento para disminuir aún más la PIO18.
Los tratamientos disponibles actualmente no pueden revertir el daño glaucomatoso al sistema visual; sin embargo, el diagnóstico precoz y el tratamiento eficaz pueden prevenir la progresión de la enfermedad. La absorción sistémica de medicamentos oftálmicos administrados tópicamente ocurre a través del sistema de drenaje nasolagrimal, condición que puede conducir a eventos adversos serios, particularmente asociado con el uso de bloqueadores beta tópicos y agonistas alfa2-adrenérgicos19. En la mayoría de los casos, el glaucoma es una condición crónica que requiere manejo de por vida. Al analizar las variables demográficas de los pacientes que participaron del estudio nos encontramos con que en ambos grupos hubo mayor cantidad de hombres (57,1 %) que de mujeres, tanto en el grupo latanoprostene bunod como en el grupo latanoprost. Con respecto a la edad, en el grupo LBN la media fue de 60,9 ± 9 años y en el grupo latanoprost la media de edad fue de 64,2 ± 6 años.
En el estudio Voyager, la edad media de los individuos fue muy similar (61 años), sin embargo tuvo un mayor porcentaje de sujetos femeninos. Los sujetos eran predominantemente no hispanos / no latinos y caucásicos20. Si tenemos en cuenta el estudio Lunar, los sujetos tenían en promedio 64,7 años de edad (rango, 23-88 años) y eran predominantemente mujeres (58,2 %), blancos (70,8 %) y no hispanos / no latinos. Los sujetos negros / afroamericanos constituían el 27,8 % de la población total21,22.
Los sujetos del estudio Apollo tenían una edad media de 64,2 años, eran de ascendencia predominantemente europea o africana y eran de etnia no hispana/no latina22. Los grandes estudios clínicos sobre latanoprostene bunod analizados no mencionan la agudeza visual de sus pacientes ni la valoración clínica del nervio óptico. En este estudio se consideró importante conocer la agudeza visual de los pacientes a pesar de que el tratamiento no mejoraría este aspecto ya que el daño glaucomatoso no puede ser revertido con los tratamientos actuales. También se consideró importante conocer el estado clínico del nervio óptico al momento de examen, a pesar de que el daño a la capa de fibras nerviosas en el glaucoma no es reversible. La agudeza visual promedio de los pacientes en este estudio, medida en el sistema decimal, en el grupo LBN fue de 0,6 mientras que en el grupo latanoprost fue de 0,5 y con respecto a la valoración clínica del nervio óptico con la lámpara de hendidura, el promedio de excavación en ambos grupos fue de 0,7. Esto nos da una pauta de que con los pacientes en el Hospital de Clínicas de Paraguay se llega tarde al diagnóstico de glaucoma , cuando ya hay un daño anatómico y funcional en la mayoría de los casos. El campo visual no fue una variable incluida en este estudio, pero en el seguimiento de estos pacientes (tanto en el grupo latanoprost como en el grupo latanoprostene bunod) se pudo constatar que varios sujetos ya tenían alteraciones en su primer campo visual.
Con respecto a los diagnósticos encontrados; en los dos grupos el diagnóstico con más prevalencia fue el de glaucoma primario de ángulo abierto (GPAA) con 12 casos en el grupo LBN y 16 casos en el grupo latanoprost. En segundo lugar, en ambos grupos, quedó el glaucoma pseudoexfoliativo. Esto coincide con la literatura en el cual el glaucoma primario de ángulo abierto (GPAA), con mucho, es la forma más común de glaucoma. Según datos estadísticos afecta actualmente a más de 2 millones de estadounidenses, más de la mitad de los cuales probablemente no saben que lo tienen. Es asintomático en las primeras etapas, reduce gradual y progresivamente el campo visual y conduce a la ceguera si no se trata23.
Si se analiza los TEAE (efectos adversos emergentes del tratamiento); El porcentaje de sujetos que experimentaron al menos 1 TEAE ocular fue mayor en el grupo de LBN 0,024 % (35,7 %) que en el grupo Latanoprost 0,005 % (28,5 %). El TEAE ocular notificado con más frecuencia fue el enrojecimiento ocular tanto en el grupo de LBN como en el grupo Latanoprost. Este signo fue constatado en 8 ojos sometidos a LBN 0,024 % y en 6 ojos sometidos a Latanoprost. 0,005 % luego de 1 mes de uso. En todos estos pacientes existió un enrojecimiento ocular de características leves. En segundo lugar quedó la sensación de ojo seco. Este signo fue objetivado en la lámpara de hendidura con un tiempo de ruptura del film lagrimal menor a 10 segundos. Se encontró en 6 ojos sometidos a LBN 0,024 % y en 4 ojos sometidos a Latanoprost 0,005 % luego de 1 mes de uso del principio activo.
Con respecto a la sensación de visión borrosa y los efectos estéticos locales, estos síntomas fueron negados por todos los pacientes del estudio luego de 1 mes de uso de LBN o Latanoprost. Otros TEAE oculares notificados como la queratopatía punteada superficial y el lagrimeo tuvieron una menor prevalencia, pero siempre un ligero predominio en el grupo de LBN 0,024 %.
Resumiendo, los TEAE oculares, en el grupo LBN se encontró más efectos adversos oculares relacionados con el fármaco luego de 1 mes de uso (estos fueron ojo seco, lagrimeo, queratopatía punteada superficial y ojo rojo), pero la diferencia fue significativa solo con la queratopatía punteada superficial y el lagrimeo (p< 0,05). En este estudio no se consideró como variables los TEAE no oculares.
En el estudio Voyager, que comparó diferentes concentraciones de LBN (0,006 %, 0,012 %, 0,024 %, 0,040 %) con latanoprost 0,005 %, se encontró que para el ojo del estudio, hubo una incidencia numéricamente mayor de al menos un TEAE ocular informado en cada uno de los grupos LBN en comparación con el grupo de Latanoprost. El TEAE ocular notificado con mayor frecuencia fue el dolor en el lugar de la instilación (es decir, el dolor de la instilación de la gota) notificado por el 14,6 %, 16,7 %, 12,0 % y 17,3 % de los sujetos en los grupos LBN 0,006 %, 0,012 %, 0,024 % y 0.040 %, respectivamente, frente al 6,1 % de los sujetos del grupo de latanoprost. El TEAE ocular notificado con mayor frecuencia en el grupo de latanoprost fue la hiperemia ocular, notificada en el 8,5 % de los sujetos frente al 1,2 %, 6,0 %, 2,4 % y 4,9 % de los sujetos en los grupos LBN 0,006 %, 0,012 %, 0,024 % y 0,040 %, respectivamente. Todos los TEAE oculares notificados fueron leves y de fácil manejo. Los TEAE no oculares se informaron con menos frecuencia y la mayoría se consideró no relacionados con el fármaco del estudio20.
Si analizamos otro gran ensayo clínico como el Lunar, que comparó la eficacia en la disminución de la PIO de LBN 0,024 % y timolol al 0,5 %, nos encontramos con resultados similares. El porcentaje de sujetos que experimentaron al menos 1 TEAE ocular en el ojo del estudio fue mayor en el grupo de LBN 0,024 % que en el grupo de timolol 0,5 %. En el grupo LBN 0,024 % se objetivó 66 casos de al menos 1 TEAE (24,8 %) y en el grupo timolol 0,5 % se objetivó 18 casos (13,4 %). Los TEAE oculares notificados con más frecuencia en los ojos del estudio tratados con LBN fueron hiperemia conjuntival, irritación ocular y dolor ocular. Solo 2 sujetos en el grupo de LBN 0,024 % experimentaron TEAE oculares que se consideraron no relacionados con el fármaco del estudio; todos los demás TEAE se consideraron relacionados con el tratamiento. Con la excepción de 1 incidente de hiperemia conjuntival grave en el grupo de LBN 0,024 % que se consideró posiblemente relacionado con el fármaco del estudio, todos los TEAE oculares del estudio fueron de gravedad leve o moderada21.
El estudio Apollo, que comparó la eficacia en la disminución de la PIO de LBN 0,024 % y timolol al 0,5 % encontró resultados similares a los estudios anteriormente citados en cuanto a los TEAE. El porcentaje de sujetos que experimentaron al menos 1 TEAE ocular en el ojo del estudio fue mayor en el grupo de LBN 0,024 % que en el grupo de timolol 0,5 %. En el grupo LBN 0,024 % se objetivó 38 casos de al menos 1 TEAE ocular (13,4 %) y en el grupo timolol 0,5 % se objetivó 16 casos (11,9 %). Los TEAE mencionados en el estudio fueron irritación ocular, hiperemia conjuntival, dolor ocular, ojo seco y dolor en el lugar de la instilación. La mayoría de los TEAE oculares se consideraron relacionados con el fármaco del estudio y de gravedad leve o moderada, con algunas excepciones22.
Con respecto a la eficacia del tratamiento; la reducción general de la presión intraocular, tomando a todos los pacientes del estudio (tanto del grupo LBN como del grupo latanoprost), fue significativa. En otras palabras, utilizar Latanoprostene Bunod 0,024 % o Latanoprost 0,005 % indistintamente disminuirá la presión intraocular de forma significativa. Esto es similar a lo encontrado en el estudio Voyager en la reducción general de la presión intraocular.
El estudio Voyager, que comparó diferentes concentraciones de LBN (0,006 %, 0,012 %, 0,024 %, 0,040 %) con latanoprost 0,005 %, encontró primeramente que todos los tratamientos condujeron a reducciones significativas en la PIO diurna desde el inicio (p<0,0001 prueba t pareada)20. En nuestro trabajo, en el grupo LBN la media de la presión intraocular antes del tratamiento fue de 25,3 ± 6,6 mmHg y la media de la presión intraocular luego de 1 mes de tratamiento fue de 16,5 ± 4,9 mmHg. La reducción de la presión intraocular fue significativa (p=0,01) según la prueba de T de student. Por otro lado, en el grupo Latanoprost la media de la presión intraocular antes del tratamiento fue de 23,6 ± 3,6 mmHg y la media de la presión intraocular luego de 1 mes de tratamiento con Latanoprost al 0,005 % fue de 15,3 ± 2,4 mmHg. La reducción de la presión intraocular también fue significativa (p=0,01) según la prueba de T de student. La reducción de la presión intraocular para los pacientes del grupo LBN fue de 34,7 % y la reducción de la presión intraocular para los pacientes del grupo Latanoprost fue de 35,1 %.
En el estudio Voyager, entre los diferentes grupos LBN, las reducciones de la PIO fueron dependientes de la dosis y pareció estabilizarse con la dosis de 0,024 % - 0,040 %20. Los grupos de tratamiento con LBN al 0,024 % y al 0,040 % demostraron una reducción significativamente mayor desde el inicio en la PIO diurna en comparación con el grupo de latanoprost (p=0,005 y p=0,009, respectivamente) en el día 28. Aunque los grupos LBN 0,006 % y 0,012 % también mostraron reducciones numéricamente mayores en la PIO en comparación con el grupo de latanoprost, estas diferencias no fueron significativas20.
Contrastando con lo que se encontró en el estudio Voyager, en nuestro estudio al comparar las presiones intraoculares posteriores al tratamiento de 1 mes con Latanoprostene bunod 0,024 % y Latanoprost 0,005 % pudimos objetivar que la diferencia en reducción de la presión intraocular entre estos dos fármacos no fue significativa (p= 0,238)
Otros hallazgos encontrados en el estudio Voyager fueron que las evaluaciones secundarias de eficacia demostraron reducciones significativamente mayores en la PIO diurna media en comparación con latanoprost en el día 7 para los grupos LBN 0,024 % y 0,040 % (p=0,033 y p=0,009, respectivamente), y en el día 14 para el grupo LBN 0,024 % (p=0,015)20.
Estas mediciones en puntos específicos, en diferentes días y en diferentes horarios, permitió al estudio Voyager tener comparaciones más refinadas entre las diferentes concentraciones de LBN y el grupo Latanoprost. En el estudio de nuestro trabajo solo se utilizaron 2 días de mediciones (antes de empezar el estudio y luego de 1 mes de uso del fármaco asignado).
Al revisar y comparar la eficacia del tratamiento con otros grandes estudios, encontramos que el estudio Lunar, que comparó la eficacia en la disminución de la PIO de LBN 0,024 % y timolol al 0,5 %, encontró que la presión intraocular media fue significativamente menor en el grupo LBN 0,024 % que en el grupo de timolol 0,5 % en la mayoría de los puntos de tiempo medidos. En la semana 2 a las 12 pm y 4 pm ; y en la semana 6 y el tercer mes a las 8 am, 12 pm y 4 pm21. LBN 0,024 % cumplió con los criterios de superioridad estadística sobre timolol al 0,5 % en todos los puntos excepto a las 8 am de la semana 2 (se excedió el límite superior del IC del 95 % en este único punto de evaluación)21.
Por su parte, el estudio Apollo encontró que la presión intraocular media fue significativamente menor en el grupo LBN 0,024 % (rango de 17,8 a 18,7 mmHg) que en el grupo de timolol al 0,5 % (rango de 19,1 a 19,8 mmHg) en los 9 puntos temporales de eficacia evaluados22. Los resultados de ANCOVA demostraron la superioridad de LBN 0,024 % sobre timolol 0,5 % en la población porque el límite superior del IC del 95 % para la diferencia entre los tratamientos fue < 0 mmHg en los 9 puntos temporales22.
De esta forma se puede observar que los grandes estudios que incluyeron al Latanoprostene Bunod 0,024 % en sus mediciones encontraron disminuciones significativas en la presión intraocular. Nuestro estudio también encontró que el LBN 0,024 % reduce la presión intraocular de manera significativa; pero no hubo tal diferencia significativa en la reducción de la presión intraocular al compararlo con los pacientes que utilizaron Latanoprost 0,005 %.
En conclusión, enfatizar que el glaucoma es la principal causa de ceguera irreversible. Y uno de los principales factores de riesgo para su desarrollo y progresión es la presión intraocular elevada. Uno de los tratamientos de primera línea es por lo general un medicamento tópico para reducir la presión intraocular. Las prostaglandinas tópicas, con su potente efecto hipotensor ocular (resultado del aumento del flujo de salida uveoescleral), son una importante opción de tratamiento para el glaucoma. Tanto el Latanoprostene bunod (LBN) al 0,024 % como el Latanoprost al 0,005 % constituyen excelentes opciones de medicación tópica para reducir la PIO y controlar el glaucoma, aunque aparentemente no existirían diferencias en el efecto hipotensor entre ambas medicaciones.