INTRODUCCIÓN
La cetoacidosis diabética es una complicación aguda y grave de la diabetes, con una tasa de mortalidad global de hasta 5%. Los estudios han reportado que la mortalidad es más alta en los pacientes con diabetes tipo 2 que en los pacientes tipo 1 1. La incidencia depende de la edad, sexo, raza, y oscila entre 0,5 a 17 por cada 1.000 personas al año. Un estudio informó la incidencia de la cetoacidosis diabética en Suecia es 0,5 por 1000 pacientes al año, en Dinamarca es 1,34 por cada 1000 pacientes al año 1. En Estados Unidos la tasa promedio anual de cetoacidosis diabética es 6,3%, con una tasa de letalidad intrahospitalaria de 0,4% y más de 20% de los pacientes que ingresan a las emergencias por cetoacidosis diabética no conocen su enfermedad base 2.
La cetoacidosis diabética consiste en una tríada clínica: acidosis metabólica, hiperglucemia y aumento de cuerpos cetónicos séricos o en orina 3. Existe un subconjunto de pacientes en donde los niveles de glucosa sérica estarán dentro de los límites normales, condición denominada cetoacidosis diabética euglucémica. El fenómeno es descrito por primera vez por Munro et al. quienes determinaron que la triada está dada por acidosis metabólica con anión gap alto, cetonemia o cetonuria con niveles séricos de glucosa <250 mg/dL 4. Su presentación clínica no permite dar un diagnóstico certero, no está asociada a manifestaciones típicas de la cetoacidosis como es la deshidratación provocada por una hiperglucemia marcada. A menudo los pacientes con cetoacidosis diabética euglucémica tratados con inhibidores del cotransportador de sodio-glucosa 2 (SGLT2i) pueden presentar menos poliuria y polidipsia por el grado leve de hiperglucemia, aparecen otras manifestaciones tales como malestar general, anorexia, taquicardia, taquipnea, con o sin fiebre. En bioquímica, su característica más importante es la acidosis metabólica que suele ser persistente y severa y, por ende, se convierte en una condición que amenaza la vida del paciente 5.
En la cetoacidosis diabética euglucémica el déficit de insulina y la resistencia a la insulina son menos agresivos. Esto provoca que la sobreproducción de glucosa y subutilización de la misma sean menores que en la cetoacidosis diabética, Lo que claramente sí está evidenciado es que el aclaramiento renal de glucosa es el doble que en la cetoacidosis diabética 5. Las condiciones que pueden dar cetoacidosis diabética euglucémica son: el ayuno prolongado, el exceso de consumo de alcohol, sobredosis de salicilato, acidosis láctica, sobredosis de antidepresivos tricíclicos, acidosis tubular renal, inanición y tratamiento con SGLT2i 5.
Los SGLT2i son recomendados por la Asociación Americana de Diabetes (ADA) en el tratamiento de diabetes mellitus tipo 2 como una de las seis opciones de terapia de segunda línea después de la terapia inicial con metformina o se los puede utilizar como monoterapia en aquellos pacientes que no toleran la metformina 6. Los SGLT2i disminuyen la glucosa sérica mediante un mecanismo independiente de la insulina, por medio de la supresión de la reabsorción renal de glucosa y el incremento de la excreción urinaria de glucosa que lleva a niveles bajos de glucosa en plasma 1. Esto reduce la secreción de insulina de las células β pancreáticas, que lleva a la disminución de los niveles circulantes de insulina, lo que provocará disminución de la actividad anti-lipolítica de la insulina resultando en la estimulación en la producción de ácidos grasos libres, que se convertirán en cuerpos cetónicos en el hígado por β-oxidación. Esto da lugar a la cetosis y posteriormente a la aparición de signos y síntomas de la enfermedad con glicemias dentro de rangos normales o ligeramente elevados 6.
En los 4 principales estudios correspondiente a los SGLT2i (EMPAREG, CANVAS, DECLARE-TIMI 58 y DAPA HF), en lo que corresponde a estudios de seguridad y efectos adversos, ninguno de ellos arrojó resultados significativos con respecto a la presencia de cetoacidosis diabética 7. Se ha informado que la incidencia de cetoacidosis diabética en pacientes que tomaron canagliflozina es 0,522 y 0,763 por 1000 pacientes, y se observó que existían factores precipitantes en estos pacientes, tales como diabetes mellitus tipo 1 o diabetes autoinmune latente de la edad adulta (LADA). La evidencia señala bajo riesgo de cetoacidosis diabética con SGLT2i y sus beneficios de uso son mayores que el riesgo 6.
En el siguiente caso a presentar es uno de los tantos pacientes que en la práctica clínica podemos obviar, subestimar o demorar su diagnóstico lo que podría acarrear complicaciones si no instauramos o iniciamos el tratamiento adecuado de manera oportuna.
CASO CLÍNICO
Paciente de sexo femenino de 48 años de edad, residente de la ciudad de Guayaquil (Ecuador), de ocupación parvularia, ingresa al Servicio de emergencia del Hospital Luis Vernaza por cuadro clínico de aproximadamente 8 horas de evolución caracterizado por dolor abdominal tipo cólico, de intensidad moderada 6/7, de irradiación difusa, que no cede con analgésicos, que se acompaña de náuseas que llegan al vómito de características alimentarias en 6 ocasiones. Tiene historial médico de diabetes mellitus 2 con mal control glucémico (HbA1C 12,4%) en tratamiento los últimos 3 meses con un SGLT2i (empagliflozina). Paciente refiere que hace una semana presentó cuadro de disuria, polaquiuria y tenesmo por lo cual su médico particular le administró antibioticoterapia por vía oral y 48 horas antes de su ingreso le suspende hipoglucemiante oral. Antecedente quirúrgico de colecistectomía laparoscópica hace 5 años. A su ingreso está deshidratada, taquicárdica, taquipneica, con dificultad respiratoria de moderados esfuerzos que se acompaña de dolor torácico tipo opresivo en región precordial sin irradiación.
Tiene presión arterial 130/85 mmHg, frecuencia cardiaca 112 lpm, frecuencia respiratoria 24 rpm, temperatura 36,5 °C, saturación de O2 90% con aire ambiente y 95% con cánula de O2 a 3 litros, glicemia capilar 129 mg/dL, IMC 26 kg/m2. Al examen físico se constata palidez generalizada, facie álgica, mucosas orales secas, campos pulmonares bien ventilados, abdomen blando, depresible, doloroso a palpación profunda en epigastrio y mesogastrio, protrusión umbilical.
En el hemograma muestra leucocitos 8.09x103/ul (4.40-10.00), hemoglobina 12,8 g/dL (12,6-16,4), hematocrito 38% (38-48), plaquetas 191.000 x103/ul (150-400), sodio 140 mEq/L (133-145), potasio 4,3 mEq/L (3,5-5,4), cloro 104 mEq/L (95-105), calcio 8,8 mg/dL (8,4-10,2), magnesio 1,74 mg/dL (1,58-2,55), fósforo 4,3 mg/dL (2,7-4,5), creatinina 0,64 mg/dL (0,50-1,30), urea 28 mg/dL (16-48), amilasa 43 U/L (28-100), lipasa 31 U/L (1-60), TGO 18 U/L (0-32), TGP 20 U/L (0-33), GGT 17 U/L (7-32), bilirrubina total 0,43 mg/dL (0-1,20).
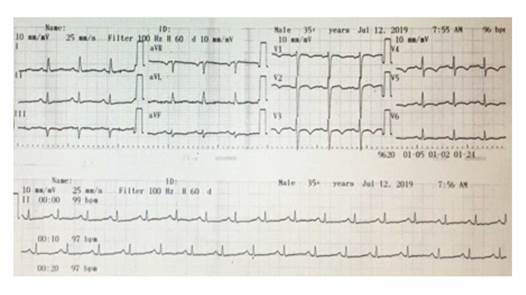
Por presencia de dolor precordial y ondas T negativa en derivaciones precordiales V2, V3, V4 y V5 (figura 1) se solicita enzimas cardiacas: troponina 13 ng/L (1-14 ng/L), CPK 96 U/L (1-167), CK-MB 18 U/L (1-25), péptido natriurético 57,52 pg/mL. Por dificultad respiratoria se solicita gasometría encontrando acidosis metabólica leve compensada: pH 7,34 (7,35-7,45), PCO2 32 mmHg (35-45), PO2 99 mmHg (80-95), SO2 96% (94-98), BE -8 mmol/l (-2 a +3), HCO3 16 mEq/L (22-26), con anión gap de 20.
A pesar de hidratación con cristaloides, la paciente evoluciona desfavorablemente y se realiza un control de gasometría con acidosis metabólica moderada descompensada con pH 7,29, PCO2 26 mmHg, PO2 124 mmHg, BE -12 mmol/l, HCO3 12,10 mEq/L, SO2 96%, anión gap 23. Por esto se solicita glicemia central 128 mg/dL y HbA1c 12,4% y se pide análisis de orina que revela glucosuria 1000 y cetonuria 150.
Ante la sospecha de cetoacidosis euglucémica se inicia insulinoterapia y fluidoterapia en Y, siendo necesaria la insulinización por 96 horas hasta la normalización del bicarbonato (HCO3 20 mEq/L) y disminución de cuerpos cetónicos en uroanálisis (cetonas 50). La glicemia se mantuvo dentro de valores ligeramente elevados, pero dentro de rango para hospitalización. Posteriormente se rota a insulina intermedia y a los 10 días se da el alta médica en buen estado.
DISCUSIÓN
La cetoacidosis diabética euglucémica fue descrita en 1973 por Munro y colaboradores, mediante la evaluación de 211 episodios de cetoacidosis diabética, de los cuales 37 tenían un nivel de glicemia menor de 300 mg/dL y bicarbonato menor a 10, todos eran jóvenes con diabetes mellitus tipo 1. Esta cetoacidosis se caracteriza por un grado leve de hiperglucemia no mayor a 200 mg/dL lo que da lugar al retraso del diagnóstico y el tratamiento, lo que podría traer consecuencias metabólicas adversas 5,8. Las causas son diversas: embarazo, consumo de alcohol en exceso, ayuno prolongado, sobredosis de salicilatos, sobredosis de antidepresivos tricíclicos, acidosis tubular renal, acidosis láctica, tratamiento con SGLT2i, etc 5.
Se puede presentar en el embarazo durante el último trimestre, donde el feto incrementa dramáticamente el metabolismo basal de la glucosa y acentúa el proceso anabólico por el crecimiento. De por sí el embarazo es un estado propenso a la cetosis, y se producen niveles disminuidos de glucosa que es utilizada en grandes cantidades por el feto y la placenta, convirtiendo el metabolismo materno en un proceso catabólico. A esto se asocia a un déficit relativo de insulina que conduce a un aumento en la producción de ácidos grasos libres, que luego se convierten en cetonas en el hígado, dando origen a la cetosis 5. Fue el primer diagnóstico en descartar en nuestra paciente ya que no cursaba estado gestacional.
Normalmente cuando un paciente con diabetes disminuye su ingesta calórica, puede desarrollar cetoacidosis diabética y se puede agravar si presenta una enfermedad subyacente que la precipita, que es lo que ocurre cuando el paciente debe seguir tomando su medicación (hipoglucemiantes o insulina), la insulina puede mantener la euglucemia, pero es incapaz de detener la formación de cuerpos cetónicos, y así aparece la cetoacidosis euglucémica 8. Otra causa común es el ayuno prolongado, donde existe agotamiento casi total del glucagón, el cual contribuye a la normoglucemia, pero de todas formas se desarrollará la acidosis metabólica. En esta situación la lipólisis y la producción de ácidos grasos libres son acelerados, la insulina se vuelve menos eficaz para suprimir la lipólisis y la cetogénesis, lo que agrava el desarrollo de la acidosis 5. Nuestra paciente cursó una semana previa con enfermedad subyacente que precipitó este cuadro y fue tratada para ello, pero no disminuyó la ingesta calórica, hasta que se presentaron los síntomas agudos que fueron 8 horas previas a su ingreso.
Entre las causas raras está la enfermedad de Hers (enfermedad por almacenamiento del glucógeno tipo VI) en la que hay deficiencia de la enzima glucógeno fosforilasa hepática, enfermedad autosómica recesiva tipo I y tipo IV pero que tiene características propias: hepatomegalia, disfunción hepática, hipoglucemia en ayunas y cetosis euglucémica en jóvenes 5. Nuestra paciente no cumplía con esos criterios: su hígado era de tamaño normal, las enzimas hepáticas estaban dentro de normalidad y no era joven. Dentro de otras causas menos comunes están la pancreatitis aguda (la paciente tenía dolor abdominal pero sus enzimas pancreáticas normales), exceso de alcohol (que ella no había consumido) y la intoxicación por cocaína (que no tenía antecedentes en este caso).
Ciertas hipótesis biológicas han propuesto que SGLT2i pueden incrementar directa o indirectamente el riesgo de cetoacidosis diabética, sin embargo, ese riesgo en el mundo real no ha sido tal 9. Los ensayos clínicos aleatorios de momento no han demostrado un incremento estadísticamente significativo de cetoacidosis diabética por SGLT2i 7. En el análisis de 17.596 pacientes con diabetes mellitus tipo 2, de ensayos clínicos controlados con canagliflozina a dosis de 100 mg y 300 mg, la tasa de incidencia de cetoacidosis fue 0,56 por 1000 pacientes. En un ensayo clínico aleatorizado de empagliflozina frente a placebo entre 7.018 pacientes con diabetes tipo 2, la tasa de incidencia fue 1,41 por 1000 pacientes en el grupo empagliflozina frente a 0,84 por 1000 pacientes en el grupo placebo 1. La paciente venía tomando desde hace 3 meses un SGLT2i (empagliflozina), fue suspendido 48 horas previas por enfermedad subyacente precipitada, sus síntomas y la acidosis presente fueron asociadas a la presencia de cetoacidosis euglucémica por SGLT2i. Diversos estudios no han determinado el tiempo de toma de estos medicamentos para poder desarrollar dicha complicación, muchos casos presentados se han originado incluso con la ingesta del medicamento por primera vez.
La evidencia actual demuestra que la presencia de los SGLT2i conlleva a dos mecanismos. Uno es a nivel de las células pancreáticas especificamente en las células α-pancreáticas estimulando directamente la secreción de glucagón, y al mismo tiempo actúa sobre las células β-pancreáticas disminuyendo la producción de insulina exagerando la cetogénesis, gluconeogénesis y la glucogenólisis por una mayor reducción de la proporción de insulina a glucagón 10. El segundo mecanismo lo produce por glucosuria que conduce a la disminución de los niveles de glucosa en sangre, la gluconeogénesis y la glucogenólisis. De manera que la presentación hiperglucémica o euglucémica de la cetoacidosis en pacientes con diabetes mellitus tipo 2 que toman SGLT2i depende del equilibrio que exista entre la producción de glucosa endógena y el aclaramiento renal de glucosa 6.
Los factores de riesgo que inciden en la cetoacidosis diabética euglucémica por SGLT2i incluyen diabetes latente autoinmune de la edad adulta (LADA), dietas bajas en carbohidratos, insulina retirada o reducción de la dosis, cirugías y alguna enfermedad médica aguda 10. En un análisis de 46 informes de pacientes con cetoacidosis diabética asociada a la toma de SGLT2i determinaron que 24 de ellos tenían diabetes mellitus tipo 2, 15 diabetes mellitus tipo 1, 5 tenían diabetes autoinmune latente de la edad adulta (LADA), 2 tenían diabetes pancreática tipo 3c, de todos ellos 70% tenían cetoacidosis diabética euglucémica, 50% de los diabéticos tipo 2 usaban insulina o alguna sulfonilurea. Los precipitantes más frecuentes encontrados fueron la reducción inadecuada de insulina u omisión de la dosis, cirugía reciente de tipo bariátrica, ingesta excesiva de alcohol, el esfuerzo o ejercicio físico, y restricción de la dieta (baja en carbohidratos o la ingesta reducida). Como conclusión del análisis de este informe los autores determinaron que los SGLT2i son un contribuyente posible de la cetoacidosis diabética, pero al menos debía estar acompañada de un factor precipitante. Por ende, realizar la historia clínica completa y hacer una evaluación clínica correcta del paciente con cetoacidosis diabética euglucémica son elementales para una verdadera comprensión de todas las causas y los factores patogénicos que contribuyen este estado potencialmente mortal 1.
Algo llamativo en todos los pacientes con cetoacidosis, y como ocurrió en nuestro caso, es la presencia de dolor abdominal que ocurre habitualmente en las complicaciones agudas de la diabetes. El dolor abdominal está presente en la cetoacidosis diabética y no en el estado hiperosmolar hiperglucémico. En una revisión actualizada de 189 casos de cetoacidosis y 11 de estado hiperosmolar hiperglucémico, 46% de los pacientes con cetoacidosis diabética presentaban dolor abdominal, de ellos 86% se asociaban con un bicarbonato menor a 5 mEq/L y 13% con bicarbonato mayor a 15 mEq/L. Es decir, mientras más bajo se encuentre el bicarbonato (y mayor la cetosis) el paciente presentará más probablemente dolor abdominal 11.
Nos impresionó observar en el electrocardiograma de la paciente la presencia de ondas T negativas en las precordiales derechas (V1-V3) que suele ser un hallazgo común en jóvenes, pero en una paciente diabética puede tratarse de la presencia de una enfermedad cardiaca subyacente y en muchos pacientes jóvenes, sobre todo atletas, el inicio de presentación de una miocardiopatía arritmogénica del ventrículo derecho. La evaluación a profundidad de este hallazgo quedó pendiente. En un estudio finlandés se evaluaron electrocardiogramas realizados a 10.899 hombres y mujeres de 30 y 59 años, entre 1966 y 1972 (52% varones, edad media 44 ± 8,5 años), con un seguimiento medio de 30 ± 11 años. Los objetivos primarios fueron: mortalidad por cualquier causa, mortalidad por causa cardiaca y arritmia mortal. Se encontró la presencia de inversión de onda T en las derivaciones de V1 a V3 en apenas 0,5%. Concluyeron en que la presencia de ondas T invertidas en derivaciones V1 a V3 es rara y no se asoció con un incremento en la mortalidad global o de causa cardiaca 14.
El manejo de la cetoacidosis diabética euglucémica es similar a la cetoacidosis diabética. La base del tratamiento implica la rápida corrección de la deshidratación con cristaloides, de las alteraciones de electrolitos y luego el uso de insulina junto con dextrosa hasta que el bicarbonato se normalice con el anión gap. El tiempo medio para la resolución de acidosis metabólica en cetoacidosis diabética es de 35 horas tras una buena perfusión o manejo, con un estimado de 2 a 4 días, según un estudio en Corea del Sur que demostró que la cetoacidosis diabética euglucémica tarda 2 veces más de tiempo en resolverse 12. Tal fenómeno ocurrió en el caso que presentamos, ya que el tiempo de resolución total fue aproximadamente a las 96 horas de inicio del cuadro.
En conclusión, la cetoacidosis diabética es muy rara en pacientes con diabetes mellitus tipo 2 que toman SGLT2i, realmente muchos de los eventos que se han descrito han sido en pacientes con diabetes mellitus tipo 1 mal diagnosticados que normalmente son los conocidos tipo LADA o estaban utilizando el fármaco fuera de la indicación actual terapéutica 9. Entonces nos haremos 2 preguntas: ¿qué debemos hacer? y ¿qué precauciones debemos tomar? para evitar que aparezca cetoacidosis diabética en los pacientes que son tratados con SGLT2i.
Lo primero es estar seguro que se lo administramos a un paciente con diabetes mellitus tipo 2. Hay pacientes que nos dejan dudas, por ejemplo, un paciente de mediana edad, con sobrepeso, asintomático, con deterioro progresivo del control metabólico. En cambio, otros pacientes que no dejan esas dudas como puede ser un paciente delgado, más joven o con un inicio abrupto de la enfermedad, creemos que aquí estamos más seguros que es diabetes mellitus tipo 2 13. Como pueden surgir más dudas como en el caso de nuestra paciente, era correcto que una diabética en mal control metabólico (HbA1C 12,4%) solamente haya estado tomando un SGLT2i, si bien sabemos que con ese nivel de hemoglobina glicosilada lo más recomendable según las guías de diabetes es que esté recibiendo terapia inyectable combinada (insulina) o tratamiento triple como una opción, independiente de si la paciente tiene o no enfermedad cardiaca establecida que es una las principales indicaciones de los SGLT2i. Esto hubiese sido ideal en ese contexto, pero en combinación 10.
Otra manera de salir de la duda es la determinación de los niveles de péptido C en plasma por encima. Si es >1,8 ng/dL indica que hay reserva pancreática y genera tranquilidad, además de la ausencia característica de los anticuerpos de la diabetes mellitus tipo 1 que son los antiGAD 13. Otra precaución que se debe tomar es suspender el fármaco ante cualquier evento intercurrente, ya sea por enfermedad médica aguda, intervención quirúrgica, cualquier situación con riesgo de deshidratación o situación que se asocie a una baja ingesta de alimentos 9.