REPORTE DE CASO
Quimioembolización transarterial en carcinoma hepatocelular atípico
Transarterial chemoembolization in atypical hepatocellular carcinoma
Andrea Verónica García Pacheco1
Leonel Alberto Dajaro Castro1
Juan Carlos Bermeo Ortega2
Gonzalo Nicolás Benalcazar Decker3
1Universidad de Especialidades Espíritu Santo. Facultad de Medicina. Postgrado en Medicina Interna. Guayaquil, Ecuador.
2Universidad de Especialidades Espíritu Santo. Facultad de Medicina. Postgrado en Cirugía General. Guayaquil, Ecuador.
3Hospital Luis Vernaza. Servicio de Gastroenterología. Programa de trasplante hepático. Guayaquil, Ecuador.
RESUMEN
Una de las grandes controversias dentro del manejo médico integral del carcinoma hepatocelular es la estimación precisa de la efectividad de la terapia con quimioembolización transarterial. Las evidencias demuestran que la misma hace parte del núcleo de tratamiento para aquellos pacientes con tumores no resecables y, comparado con la resección hepática y ablación por radiofrecuencia, oferta supervivencia a largo plazo si cumplen las características de nódulo hasta 3 cm o menores sin invasión vascular. Presentamos un caso clínico de carcinoma hepatocelular atípico con manejo médico integral, mediante la quimioembolización transarterial, evidenciando por imágenes y macroscópicamente la efectividad de la misma hasta el trasplante hepático ortotópico.
Palabras clave: carcinoma hepatocelular; quimioembolización terapéutica; trasplante de hígado
ABSTRACT
One of the major controversies within the comprehensive medical management of hepatocellular carcinoma is the accurate estimation of the effectiveness of transarterial chemoembolization therapy. Evidence shows that it is part of the treatment nucleus for patients with unresectable tumors and, compared to hepatic resection and radiofrequency ablation, offers long-term survival if the characteristics of nodules up to 3 cm or less without vascular invasion are met. We present a clinical case of atypical hepatocellular carcinoma with integral medical management, through transarterial chemoembolization, evidencing its effectiveness by images and macroscopically until the orthotopic liver transplantation.
Keywords: hepatocellular carcinoma; therapeutic chemoembolization; liver transplantation
El carcinoma hepatocelular es considerado la tercera causa de muerte relacionada con el cáncer y el sexto más común en el mundo. Está comúnmente asociado a enfermedades crónicas hepáticas representando más del 85% de los tumores malignos primarios del hígado. Aparece principalmente sobre una enfermedad preexistente ya sea en el estadio de cirrosis debido a una infección crónica por el virus de la hepatitis B o C, consumo de alcohol o esteatohepatitis no alcohólica y por trastornos metabólicos como diabetes u obesidad
1-4).
El carcinoma hepatocelular se presenta con mayor prevalencia entre 60-70 años, con una distribución por género de 2 a 4 veces mayor en hombres que en mujeres. Su distribución a nivel mundial no es homogénea, produciéndose en países en vías de desarrollo en 85% de los casos
2,5,6).
El ultrasonido es comúnmente utilizado como prueba de imagen inicial para la detección y vigilancia en individuos de alto riesgo porque detecta lesiones pequeñas con un alto nivel de sensibilidad, sin embargo, los resultados varían entre operadores debido a que la cúpula del hígado es difícil de visualizar, la obesidad o esteatosis hepática crean artefactos y por último, la diferencia entre un nódulo de carcinoma pequeño y un nódulo de regeneración en el contexto de cirrosis pueden confundirse
7-9).
Las características radiológicas típicas mediante resonancia magnética o tomografía permiten establecer el diagnóstico de un nódulo mayor de 1 cm que presente hipervascularización en fase arterial seguido de lavado precoz en la fase venosa portal. Sin embargo, en algunos casos el hepatocarcinoma puede mostrar un comportamiento atípico con hipocaptación sin hipervascularización arterial, siendo importante la fase portal y tardía donde permanecen hipodensos/hipointensos. La biopsia de una lesión sugestiva ha quedado relegada para aquellos pacientes en quienes el estudio de imágenes no proporciona datos certeros para el diagnóstico
2,5,6,8).
El pronóstico del carcinoma hepatocelular se estima en una sobrevida de 5 años sin la instauración de tratamiento que equivale a menos del 5%. El tratamiento curativo se basa en la resección y trasplante hepático, por lo que un punto fundamental a considerar es el estado funcional elegible para determinar aquellos pacientes candidatos a una terapia curativa radical. De acuerdo a la disponibilidad de donante es necesario controlar la progresión de la enfermedad para mantener la elegibilidad, para lo cual la quimioembolización transarterial (TACE, por sus siglas en inglés) es el tratamiento estándar
10,11).
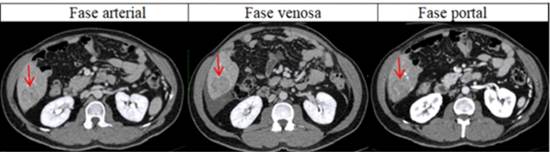
Varón de 55 años de edad, con antecedentes patológicos de diabetes mellitus tipo 2 controlado con insulina, cirrosis hepática diagnosticado en el año 2015, dentro de su evaluación médica integral pre trasplante, en abril del 2016 se realiza angiotomografía de abdomen la cual revela un nódulo atípico hipoatenuante en segmento VI del hígado que mide 3,1 cm en su diámetro mayor pero que en la fase portal y tardía permanecen hipodensos/hipointensos (
figura 1). El 21 de mayo del 2016 se realiza estudio tomográfico de control sin evidenciar cambios.
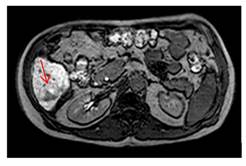
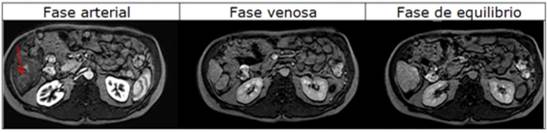
El 16 de noviembre del 2016 se realiza control tomográfico observándose cambios en la captación del nódulo por lo que se decide el 17 de enero de 2017 realizar resonancia magnética con gadoxetato de disodio que evidencia nódulo en segmento VI hepático, de 3 cm de diámetro que lava rápidamente en fase venosa, sugestivo de hepatocarcinoma (
figuras 2 y
3).
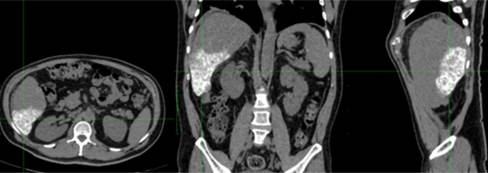
El 4 de abril del 2017 se realiza nueva tomografía trifásica donde se evidencia incremento en el tamaño del nódulo y se decide realizar TACE para detener la progresión de la enfermedad y evitar la salida de la lista de espera (
figura 4).
El 06 de abril del 2017 mediante cateterismo con acceso en arteria femoral derecha, se identifica tumor con realce parenquimatoso de aproximadamente 4 cm en el segmento VI hepático. Se procede a TACE convencional con lipiodol ultrafluido y doxorrubicina 50 mg y se completa embolización con plegs de
Spongostan, logrando desvascularización total de dicho segmento (
figura 5).
El 19 de abril del 2017 se realiza trasplante hepático ortotópico completo de donante cadavérico. El estudio macroscópico de pieza explantada revela: hígado de 28x15x10 cm de superficie externa nodular, de color pardo amarillento que alterna con áreas violáceas. Al corte presenta una zona irregular amarillenta, ubicada en el segmento VI del lóbulo derecho en contacto con la cápsula hepática, que mide 4 cm de diámetro mayor, de bordes mal delimitados, correspondiente al área de hepatocarcinoma previo. El resto de la superficie interna es nodular de color pardo amarillento (
figura 6). El estudio microscópico indica: área de necrosis rodeada de hepatocitos reactivos. Los estudios de inmunohistoquímica realizados fueron negativos para hepatocarcinoma (AFP alfafetoproteína, CEA antígeno carcinoembrionario, CK7 citoqueratina 7, CK20 citoqueratina 20, anticuerpo Ki-67), sin evidencia de residuos tumorales.
El caso presenta el seguimiento de un paciente diagnosticado con cirrosis hepática candidato para trasplante hepático. Durante la evaluación pretrasplante se identifica un nódulo hepático con comportamiento atípico en sus características radiológicas al mostrar hipocaptación en la fase arterial, distinto a las características de hipercaptación de contraste que suele presentarse en los hepatocarcinomas típicos, en estos casos es importante la fase portal y tardía donde permanecen hipodensos/hipointensos. La biopsia de una lesión sugestiva ha quedado relegada para aquellos pacientes en quienes el estudio de imágenes no proporciona datos certeros para el diagnóstico. La lesión fue catalogada como hepatocarcinoma atípico tras resonancia magnética con gadoxetato de disodio, que revela imagen nodular en segmento VI hepático con realce tenue en fase arterial y lavado en fase venosa y de equilibrio
. Se realizó TACE para prevenir la progresión y disminuir la recidiva de patología posterior al alotrasplante. En el estudio de patología del órgano explantado se identifica la zona que recibió quimioembolización como tejido de necrosis, mal diferenciado, sin evidencia microscópica de lesión. El trasplante de hígado representa la mejor opción de tratamiento para los pacientes con carcinoma hepatocelular en pacientes seleccionados, pero debido a que el tiempo de espera de un donante cadavérico es incierto, se han utilizado técnicas que permiten el control de la progresión del tumor mientras el paciente espera un injerto disponible y potencialmente reducir las tasas de recurrencia después del trasplante. Entre las técnicas descritas más comunes encontramos la TACE, técnicas de ablación por radiofrecuencia, ablación por microondas o inyección percutánea de etanol
12. En un estudio publicado en marzo 2017 por Sapisochin G y cols. se compara la radioterapia corporal estereotáctica vs. TACE o ablación por radiofrecuencia como puente hasta el trasplante en pacientes con carcinoma hepatocelular. Como información relevante no se demostraron diferencias estadísticamente significativas en cuanto a la remisión del cáncer ni deterioro de la función hepática, por lo que se concluye que cualquiera de las técnicas loco regionales pueden ser utilizadas con seguridad como terapia puente hasta el trasplante hepático
13. En general, la modalidad de tratamiento recomendado para la etapa B de la clasificación de Barcelona para el carcinoma hepatocelular es la TACE. Sin embargo, aquellos con clasificación A puede ser considerada la TACE como terapia puente pretrasplante y, en este caso en particular se tomó en cuenta los tiempos en lista de espera, que son prolongados en nuestro país para la obtención de alotrasplante hepático, decidiéndose realizar quimioembolización para evitar progresión de la enfermedad. Dos ensayos controlados aleatorios publicados por Galle PR y Cols demostraron un significativo beneficio terapéutico con esta opción terapéutica. En pacientes con un tumor amplio, propagación multinodular o deterioro de la función hepática se debe considerar otras opciones terapéuticas como el uso de terapias sistémicas (inhibidores multikinasas, por ejemplo sorafenib)
14. Se conocen dos tipos diferentes de TACE: convencional y con fármaco liberador de perlas. En TACE convencional, el agente quimioterapéutico (por lo general doxorrubicina, mitomicina C o cisplatino), típicamente incrustado en lipiodol, se infunde en la arteria del tumor seguida de una embolización con partículas de esponja de gelatina. En la segunda modalidad se implantan perlas de fármaco (doxorrubicina) en la vasculatura del tumor por lo que el fármaco se libera mayor tiempo dentro de la lesión. Esto trae consigo una mayor reducción del tumor y aumento de las concentraciones locales de fármaco, con mejor tolerancia del paciente y con mayores tasas de supervivencia a largo plazo
14. Sin embargo, en un estudio unicéntrico retrospectivo publicado por Wörns MA y cols se demostró que la técnica convencional produce mayores tasas de respuestas objetivas en menor tiempo, necesaria para que el paciente permanezca en la lista de espera apto para recibir el trasplante hepático lo que repercute en la progresión del carcinoma
14. Esto demuestra la utilidad de la terapia convencional como tratamiento puente, reservándose la segunda modalidad para el carcinoma no resecable. Se realizó el trasplante de hígado en el paciente con cirrosis hepática descompensada con nódulo de hepatocarcinoma atípico previa terapia de quimioembolización, como un coadyuvante antes de la obtención de donante, demostrando macroscópicamente y microscópicamente la efectividad de control tumoral y disminución de la progresión patológica mediante la TACE.
REFERENCIAS BIBLIOGRÁFICAS
1. Turnes J, Díaz R, Hernandez-Guerra M, Gómez M, Castells L, Bustamante J, et al. Decisiones terapéuticas en el tratamiento del carcinoma hepatocelular y patrones de uso de sorafenib. Resultados del estudio internacional observacional GIDEON en España. Gastroenterol Hepatol. 2015; 38(4):263-73.
[ Links ]
2. Zani C, Pasquale L, Bressanelli M, Puoti M, Paris B, Coccaglio R, et al. The epidemiological pattern of chronic liver diseases in a community undergoing voluntary screening for hepatitis B and C. Dig Liver Dis. 2011; 43(8):653-8.
[ Links ]
3. Visag-Castillo V. Mini-review. Liver transplantation for hepatocellular carcinoma. Rev Med Hosp Gen Mex. 2018. 81(2):97-101.
[ Links ]
4. Raoul J-L, Latournerie M, Guillygomarc'h A, Boudjema K, Audrain O, Boucher É. Carcinoma hepatocelular. EMC-Tratado de Medicina. 2011; 15(3):1-9.
[ Links ]
5. Martínez J, Lledó J, Aicart-Ramos M, Mateos B, Albillos A. Carcinoma hepatocelular. Medicine-Programa de Formación Médica Continuada Acreditado. 2016; 12(12):683-92.
[ Links ]
6. European Association for the Study of the Liver. EASL clinical practice guidelines: liver transplantation. J Hepat. 2016; 64(2):433-85.
[ Links ]
7. Mitchell DG, Bruix J, Sherman M, Sirlin CB. Li-RADS (Liver Imaging Reporting and Data System): Summary, discussion, and consensus of the LI-RADS Management Working Group and future directions. Hepatology. 2015; 61(3):1056-65
[ Links ]
8. Bruix J, Reig M, Sherman M. Evidence-based diagnosis, staging, and treatment of patients with hepatocellular carcinoma. Gastroenterology. 2016; 150(4):835-53.
[ Links ]
9. Forner A, Reig M, Varela M, Burrel M, Feliu J, Briceño J, et al. Diagnóstico y tratamiento del carcinoma hepatocelular. Actualización del documento de consenso de la AEEH, SEOM, SERAM, SERVEI y SETH. Med Clin (Barc). 2016; 146(11):511. e1-e22.
[ Links ]
10. Wáng YX, De Baere T, Idée JM, Ballet S. Transcatheter embolization therapy in liver cancer: an update of clinical evidences. Chin J Cancer Res. 2015; 27(2):96-121.
[ Links ]
11. Martinez-Mier G, Esquivel-Torres S, Medina Granados JP, Luna-Castillo M, Castillo-Chiquete R, Calzada-Grijalva JF, Gonzalez-Velazquez F. Presentación, clasificación y evolución de los pacientes con carcinoma hepatocelular en un centro de Veracruz, México. Rev gastroenterol méx. 2014;79(3):171-9.
[ Links ]
12. Bruix J, Sherman M. Management of hepatocellular carcinoma: an update. Hepatology. 2011;53(3):1020-2.
[ Links ]
13. Sapisochin G, Barry A, Doherty M, Fischer S, Goldaracena N, Rosales R, et al. Stereotactic body radiotherapy vs. TACE or RFA as a bridge to transplant in patients with hepatocellular carcinoma. An intention-to-treat analysis. J Hepatol. 2017;67(1):92-9.
[ Links ]
14. Galle PR, Tovoli F, Foerster F, Wörns MA, Cucchetti A, Bolondi L. The treatment of intermediate stage tumours beyond TACE: From surgery to systemic therapy. J Hepatol. 2017;67(1):173-83.
[ Links ]