Las polimixinas constituyen un grupo de antimicrobianos antiguos activos contra varias bacterias Gram negativas. Fueron descubiertas en 1947. Están disponibles para su uso terapéutico desde hace más de 50 años1. Constituyen un grupo de 5 sustancias íntimamente relacionadas que recibieron el nombre de polimixinas A, B, C, D y E. Sólo las polimixinas B y E han sido utilizadas clínicamente2-4. Es producido por el Bacillus polymyxa subspecies colistinus5,6.
Entre los gérmenes sensibles destacan los bacilos Gram negativos no fermentadores como: Pseudomonas aeruginosa, Acinetobacter baumannii y Klebsiella pneumonie, Stenotrophomonas maltophilia. Están caracterizados por su perfil de multirresistencia y a veces de panrresistencia antibiótica. No son activas contra bacterias Gram positivas y hongos7,8.
Las bacterias Gram negativas extensamente resistentes a los antibióticos son una importante preocupación de salud pública en todo el mundo y representan un reto para la terapia antimicrobiana actual. La mayor incidencia de dichas bacterias ha surgido como uno de los graves problemas a los que se enfrentan los médicos a nivel mundial9. La actividad bactericida de esta clase de antibióticos se mantuvo inalterada desde su introducción a pesar de haber sido observada alguna resistencia y existir relatos de asociación de antibióticos para potencializar su efecto bactericida10-12.
La utilización de la colistina se había suspendido en la década de 1980 debido a la elevada incidencia de nefrotoxicidad y neurotoxicidad durante aproximadamente 30 años13,14. A pesar de la preocupación por su toxicidad, la colistina se convirtió en un agente terapéutico importante en varios centros médicos y ha resurgido como agente de último recurso para tratar infecciones causadas por estos gérmenes, pero a pesar del tratamiento con estos fármacos, la mortalidad es generalmente alta15,16.
En un estudio prospectivo que incluyó a 200 pacientes con infección microbiológicamente documentada, la mortalidad del grupo tratado con colistina (39%) fue superior a la del grupo no tratado con colistina (28,8%)17. A pesar de ello, se considera que la utilidad de la colistina como terapia de rescate frente a microorganismos multirresistentes es incuestionable principalmente en pacientes críticos, inmunodeprimidos y trasplantados18. La literatura médica sobre la efectividad de la colistina como droga de elección para las infecciones causadas por dichos microorganismos es unánime19.
Un informe actualizado sobre el desarrollo de nuevos antimicrobianos realizado por la Sociedad de Enfermedades Infecciosas de América (IDSA) indicó que ningún nuevo antibiótico contra las bacterias Gram negativas multirresistentes ha alcanzado la etapa avanzada de desarrollo de fármacos en los últimos 10 años20. Existen dos presentaciones comerciales de colistina: sulfato de colistina para uso tópico y oral, y colistimetato sódico (CMS) para administración parenteral o inhalada21.
Los mecanismos de toxicidad renal inducida por colistina son desconocidos y siguen siendo un tema de debate. Algunos informes muestran un riesgo 4 veces mayor de nefrotoxicidad en pacientes que reciben colistina durante más de 14 días, lo que sugiere que la toxicidad está relacionada con la dosis total y la duración de la terapia. La nefrotoxicidad no parece estar relacionada con la dosis diaria (mg/kg/día), sino más bien con la dosis total acumulada22-24. La colistina se acumula en la región cortical del riñón especialmente en las células del túbulo proximal donde los transportadores tubulares reabsorben más de la droga25-27. El estrés oxidativo, la apoptosis y alteraciones en los niveles de óxido nítrico sintetasa también podrían jugar un rol importante en la nefrotoxicidad inducida por colistina28.
La injuria renal aguda representa un problema clínico importante, especialmente en los cuidados intensivos. Se ha demostrado en múltiples estudios como un factor de riesgo independiente para mortalidad, incluso después del ajuste por la demografía, la gravedad de la enfermedad y otros factores relevantes29.
Para evaluar la nefrotoxicidad se utilizan los criterios RIFLE. Las variables que la integran (del acrónimo Risk, Injury, Failure, Loss y End Stage Kidney Disease) son: riesgo, lesión, fracaso, pérdida y enfermedad renal terminal30.
Los criterios RIFLE se han desarrollado para estandarizar el diagnóstico de injuria renal aguda. Es un instrumento de clasificación que unifica los criterios clásicos de injuria renal aguda facilitando la estratificación de los enfermos. RIFLE utiliza dos criterios: cambios en la creatinina sérica o tasa de filtración glomerular (TFG) desde un valor basal, y las tasas de flujo de orina por peso corporal durante un período de tiempo especificado. Una de las características principales de la clasificación es que cuenta con tres niveles de gravedad de lesión renal aguda con respecto al nivel de creatinina, el gasto urinario o ambos 31:
• Risk (riesgo): Incremento en la creatinina sérica de 1.5 veces o una disminución en el índice de filtrado glomerular mayor de 25% con un gasto urinario menor a 5 mL/kg/h por 6 horas.
• Injury (lesión): Incremento de la creatinina sérica de 2 veces en valor basal o una disminución en el índice de filtración glomerular mayor de 50% con un gasto urinario menor de 5 mL/kg/h por 12 horas.
• Failure (falla): Incremento de 3 veces el valor basal de la creatinina sérica o una disminución de más de 75% en el índice de filtración glomerular o una creatinina sérica mayor a 4 mg/dL con un gasto urinario menor de 3 mL/kg/h sostenido por 24 h o anuria por 12 h. La definición de falla renal crónica agudizada cae en esta clasificación.
• Loss (pérdida): se considera falla renal aguda persistente por más de 4 semanas.
• End stage kidney disease (enfermedad renal terminal) es la falla renal sostenida por más de 3 meses.
El valor pronóstico de la clasificación RIFLE ha sido validado a través de grandes estudios de cohorte, de gran heterogeneidad, en donde se ha confirmado su correlación con la mortalidad de una manera estadísticamente significativa, mostrando ser una importante herramienta pronóstica32.
Los objetivos de este estudio fueron determinar la frecuencia de injuria renal aguda en pacientes adultos tratados con colistina del Hospital Nacional de Itauguá e identificar la presencia de afecciones comórbidas específicas asociadas a la injuria renal aguda.
Diseño metodológico: observacional, descriptivo, retrospectivo, de corte transverso
Población de estudio: pacientes mayores de 18 años, tratados con colistina, internados en el Departamento de Medicina Interna, Hospital Nacional (Itauguá, Paraguay) en 2016-2017.
Criterios de inclusión:
Pacientes que reciben colistina por vía intravenosa durante al menos 48 horas.
Contar con aislamiento bacteriano y sensibilidad antimicrobiana
Criterios de exclusión:
Pacientes con enfermedad renal en etapa terminal o terapia de reemplazo renal requerida antes del inicio de la colistina.
Pacientes con clearance de creatinina ≤ 10 mL/min.
Ausencia de evaluación de seguimiento de la creatinina sérica.
Muestreo: no probabilístico, de casos consecutivos.
Variables:
Demográficas: edad, sexo, peso
Clínicas: diabetes mellitus, hipertensión arterial, urea, creatinina, germen aislado, criterios de RIFLE.
Reclutamiento: se recurrió inicialmente a los registros de infecciones asentados en el libro de actas del Servicio de Bacteriología del Dpto. de Laboratorio del Hospital Nacional. Posteriormente se extrajeron los datos de los expedientes clínicos obrantes en archivo.
Gestión de datos: las variables fueron registradas en planilla electrónica y sometidas a estadística descriptiva con el programa informático Epi Info 7 TM . Las variables cualitativas se expresaron en frecuencias y porcentajes y las cuantitativas en medias ± desvío estándar.
Tamaño muestral: muestreo por conveniencia
Aspectos éticos: no existen conflictos de interés. Se respetó la confidencialidad de los datos personales. El protocolo fue evaluado por el Comité de Ética de la Facultad de Medicina de la Universidad Nacional de Itapúa.
Se estudiaron 80 pacientes, siendo 64% del sexo masculino. La edad media fue 50±17 años (rango 18-89 años)
La prevalencia de injuria renal aguda fue 70%. Según los criterios de RIFLE hubo lesión en 45%, riesgo de lesión en 25% y no riesgo/no lesión en 30%.
Entre las afecciones comórbidas predominó la hipertensión arterial (61%) seguida de la diabetes mellitus (31%).
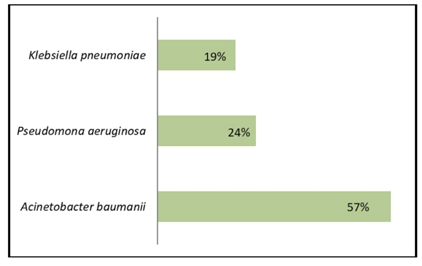
Entre los gérmenes sensibles destaca Acinetobacter baumannii (gráfico 1).
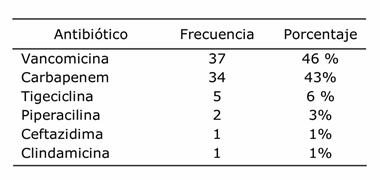
Entre los antibióticos más utilizados en forma combinada predominó la vancomicina (tabla 1).
El tratamiento con colistina debe suspenderse si aparecen signos de nefrotoxicidad y otras drogas potencialmente nefrotóxicas deben ser evitadas.
Datos experimentales y estudios clínicos de los efectos protectores de los agentes antioxidantes son controvertidos. Se demostró que el ácido ascórbico tiene un papel protector si se administra posteriormente al uso de altas dosis de colistina en un estudio observacional33.
Una de las pocas alternativas en el tratamiento de infecciones por bacilos Gram negativos multirresistentes es la colistina, a pesar de su uso clínico desde hace más de 50 años. No existen recomendaciones definitivas con respecto a la manera más eficaz y menos tóxica para su empleo. Varios autores investigaron sus efectos adversos, particularmente la nefrotoxicidad34.
En nuestro estudio hemos utilizado los criterios RIFLE para evaluar la nefrotoxicidad; encontramos riesgo en el 25% y lesión en el 45% de los pacientes estudiados; sin embargo, en otros estudios realizados se reportó riesgo en el 24% y lesión en el 15% de los pacientes incluidos en el estudio; es decir, un menor porcentaje de lesión comparado a nuestro estudio35.
La incidencia global de IRA asociado al uso de colistina informada en diferentes estudios es muy variable36. La observada en nuestro estudio está dentro de las más elevadas con una incidencia de 70% comparado con estudios de otros países como Italia en donde se observó una incidencia del 44,3%37. En un estudio realizado en Brasil se demostró una incidencia de 38,3%35. En Taiwán el 14% experimentaron nefrotoxicidad después del tratamiento con colistina38. En Estados Unidos hallaron una incidencia de 45%.39 En Corea del Sur descubrieron una incidencia de 31,9%40. Esto podría deberse a la escasa utilización de las recomendaciones de dosificación de CMS en pacientes críticos41. Estos hallazgos sugieren una evaluación adicional de la dosificación correcta del CMS, al igual que con dosis diarias de colistimetato aprobado para uso clínico, de igual manera más del 50% de los pacientes pueden experimentar daño renal agudo42,43.
Actualmente hay una preponderancia del sexo masculino en casos de IRA44. En nuestro estudio también predominó el sexo masculino.
Entre los factores que juegan un papel crucial en la afectación de la función renal tenemos la edad45. A mayor edad mayor riesgo de desarrollo de afectación renal. Entre las afecciones comórbidas, la diabetes mellitus y la hipertensión arterial son clasificados como grupo de riesgo para el desarrollo de IRA. En nuestro estudio la edad media fue 50,6±17,2 años (rango 18-89 años) comparado con otro estudio donde se observa una media de 57 años (rango 40 a 69 años)46. En otro estudio la edad promedio fue mayor 62,8±13,7 años35. En cuanto a las afecciones comórbidas estudiadas se encuentra a la hipertensión arterial. El 61% de la población estudiada presentaba dicha afectación. Respecto a la diabetes mellitus, se encontró que la mayoría de los pacientes incluidos en nuestro estudio no se conocían diabéticos, al igual que otro estudio realizado en Italia47.
El germen aislado con mayor frecuencia fue Acinetobacter baumanniien un 57% de los casos al igual que en otros estudios47. Dicha prevalencia se debe a que este microorganismo es un importante patógeno capaz de producir infecciones nosocomiales severas en pacientes hospitalizados en todo el mundo por lo que para prevenir o minimizar potenciales brotes es esencial el cumplimiento de las medidas de óptimo control de infecciones.
En nuestro estudio se encontró que entre los antibióticos más utilizados en forma combinada con la colistina predomina la vancomicina, a diferencia de otros estudios que han demostrado una actividad sinérgica de colistina con rifampicina, ceftazidima, y con carbapenémicos48.
En conclusión, la prevalencia de injuria renal aguda fue elevada. Según los criterios RIFLE predominó la lesión renal. Las afecciones comórbidas más frecuentes fueron la hipertensión arterial y la diabetes mellitus.