C. difficile es un bacilo Gram positivo, formador de esporas, que forma parte de la microbiota intestinal normal en 1 a 3% de los adultos sanos. El primer caso de colitis pseudomembranosa se reportó en 1893 y su relación con el uso prolongado de antibióticos fue descrito por primera vez en 1974 en asociación a clindamicina.
En las últimas 2 décadas ha habido un ascenso considerable en la incidencia y mortalidad de diarrea asociada a C. difficile, de pacientes hospitalizados y ambulatorios, debido a la diseminación de cepas hipervirulentas y al uso inapropiado de antibióticos, con brotes de colitis severa y recurrente (1,2.
Además de la terapia antimicrobiana, otros factores de riesgo conocidos son la edad avanzada, larga estancia intrahospitalaria, severidad de la enfermedad de base, cirugía o manipulación gastrointestinal, inmunocompromiso, ingesta de inhibidores de bomba de protones y la polifarmacia (3,4.
La infección se transmite principalmente por vía fecal oral. Se adquiere por la ingestión de esporas resistentes al medio ambiente y al pH ácido del estómago. Una vez en el intestino delgado las esporas germinan a su estado vegetativo. Cualquier factor que altere la flora bacteriana habitual del colon favorece la colonización por C. difficile, ya que no hay otras bacterias con las cuales competir por nutrientes, permitiendo así su crecimiento y multiplicación, y la producción de toxinas.
Las principales toxinas producidas por esta bacteria son la toxina A, una enterotoxina (tcd A), y la toxina B, una citotoxina (tcd B), ambas proinflamatorias y responsables en gran parte de la virulencia asociada al cuadro de colitis pseudomembranosa. Algunas cepas pueden producir ambas toxinas. Ciertas cepas producen también una toxina binaria, la cual se piensa contribuye en algunos casos a la virulencia (5,6.
El espectro clínico de afectación por C. difficile puede ir desde una colonización asintomática en el estado de portador a diarrea episódica llegando hasta una colitis pseudomembranosa severa (7.
Un estudio en realizarse para detectar cepas enterotoxigénicas de C. difficile es el ensayo de detección de actividad de las citotoxinas en cultivo celular, con 95% de sensibilidad y 98% de especificidad en pacientes con colitis pseudomembranosa. Es considerado el estudio de elección, con la desventaja de ser sumamente costoso y que toma de 24 a 72 horas en informarse. Sin embargo, continúa siendo la pauta a partir de la cual se desarrollaron las pruebas más modernas. El inmunoensayo de enzimas (EIA por sus siglas en inglés) es ahora uno de los métodos más utilizados para detección de toxinas A y/o B. Se prefiere la prueba que detecta ambas toxinas, ya que solo 1-2% de las infecciones por C. difficile son causadas únicamente por la toxina B. En vista de la limitante en cuanto a falsos negativos con el EIA, es importante recordar la correlación clínica al momento de indicar el estudio (8,9. Finalmente, el coprocultivo es el estudio más sensible y esencial para procesos epidemiológicos y de investigación, sin embargo, en la clínica no resulta práctico por el tiempo que tarda en crecer (10.
Mujer de 22 años, estudiante, procedente de San Bernardino, consulta por dolor abdominal. Refiere cuadro de 2 semanas de evolución de dolor abdominal que inicia en epigastrio y posteriormente se generaliza, intenso, tipo cólico, que cede parcialmente con antiespasmódicos. Acompaña al cuadro náuseas sin vómitos, deposiciones líquidas 5-6 veces por día, que cambia de características con el transcurso de los días pues en ocasiones es flemoso y con estrías de sangre. Refiere tenesmo rectal. Dos días antes del ingreso se agrega fiebre graduada de 38 °C, en dos oportunidades, que cede con antipiréticos comunes.
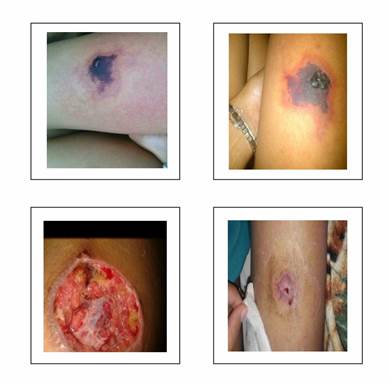
Antecedentes remotos de la enfermedad actual: refiere picadura de araña hace aproximadamente 2 meses en la región del muslo lado derecho. Consultó en el Servicio de Dermatología donde se hace el diagnóstico de celulitis y recibe antibióticos: amoxicilina/sulbactam 1,5 g vía oral durante 14 días. Ante la no mejoría de la lesión se rota a ciprofloxacina más clindamicina vía parenteral durante 5 días y luego ciprofloxacina más metronidazol vía parenteral durante 5 días más, todos de forma ambulatoria. Se realiza además desbridamiento de la lesión.
Antecedentes patológicos: no se conoce portadora de comorbilidades.
Ingresa con presión arterial 100/80 mm Hg, pulso 105/min, respiración 22/min, temperatura 37,5 °C. Examen físico: conjuntivas normocoloreadas, labios y mucosa oral secos. Área cardiovascular: taquicardia, no soplos ni galope. Aparato respiratorio: murmullo vesicular conservado. Abdomen: plano, simétrico, blando, depresible, doloroso a la palpación profunda en flanco y fosa iliaca izquierdas, sin defensa ni irritación peritoneal. Ruidos hidroaéreos aumentados. Sistema nervioso: lúcida, sin déficit motor ni sensitivo. Miembros inferiores: cicatriz eritematosa redondeada localizada en región antero interna de muslo derecho (figura 1)
Ingresa con los diagnósticos de sepsis a punto de partida gastrointestinal, diarrea aguda de etiología a determinar, deshidratación moderada, celulitis en muslo derecho.
Entre los datos laboratoriales destacan: hemograma con leucocitosis de 14.000/mm3, neutrófilos 80%, hemoglobina 12 g/dL, hematocrito 37%, eritrosedimentación 15 mm/1° hora, PCR 1,1 mg/dL, calcio sérico 9 mg/dL, albúmina 4,2 mg/dL. Electrolitos, perfil renal y hepático en rango. Amilasa y lipasa normales. Complementos, ANA, anti-DNA y anticuerpos IgA antitransglutaminasa: negativos.
El frotis de mucus fecal informa: examen macroscópico de color marrón, aspecto semilíquido. Examen microscópico: leucocitos 13-15 por campo, hematíes 3-5 por campo, células 2-3 por campo, filamentos mucosos abundantes, gotas de grasa ausentes.
Coproparasitológico: no se observan vermes ni protozoarios. Coloración de Gram: se observa microbiota mixta. Cultivo: microbiota entérica normal. No se aísla Salmonella sp., Shigella sp., E. coli enteroinvasiva ni Campylobacter sp. En heces frescas se detecta presencia de ADN de C. difficile. Se detecta el ADN del gen de la toxina A (tcdA) y la presencia de ADN del gen de la toxina B (tcdB).
En ecografía abdominal se constata líquido libre interasas en hipogastrio en aproximadamente 20 cc, 4 cc en fondo de saco de Douglas y laminar en espacio de Morrison. Asas de paredes engrosadas a nivel de fosa iliaca izquierda con aumento de la ecogenicidad de la grasa peritoneal, sugerente de proceso inflamatorio en cavidad abdominal.
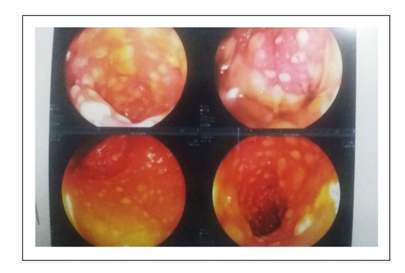
Se realiza rectosigmoidoscopía que informa mucosa rectal con placas blancoamarillentas, de 3 a 5 mm, con restos de fibrina. Las mismas lesiones tapizan toda la mucosa colónica hasta la unión rectosigmoidea. También existe pérdida del patrón vascular. Se realizan biopsias aleatorias. Se hace el diagnóstico de colitis pseudomembranosa.
Se inicia tratamiento con metronidazol 500 mg cada 8 horas por vía oral y ante la persistencia del cuadro diarreico a las 72 horas se agrega vancomicina 125 mg cada 6 horas vía oral, con buena respuesta a las 48 horas. Fue notable el cambio de las deposiciones, que fueron disminuyendo en cantidad y así como la eliminación de pseudomembranas amarillentas. (figura 2)
Este caso se presenta por ser un diagnóstico inusual en el Servicio de Clínica Médica del Hospital Nacional. La infección por C. difficile (CDI) en la actualidad continúa siendo una complicación importante de la terapia antimicrobiana. Corresponde a un 20% de las infecciones nosocomiales y se le atribuye una mortalidad de 6-15% en pacientes hospitalizados y tratados con antibióticos para infecciones severas 7.
La infección ocurre cuando un huésped susceptible ingiere esporas de C. difficile que colonizan el intestino donde liberan exotoxinas que causan colitis. Las personas inmunocompetentes están protegidas de esta colonización por la flora bacteriana normal. Por lo tanto, cualquier situación que altere la microflora natural del intestino deja al huésped propenso a ser colonizado (11,12.
El espectro clínico de esta enfermedad se encuentra influenciado por 2 factores: la virulencia de la cepa infectante y la respuesta inmune del huésped. Existen varios factores de riesgo identificados para el desarrollo de colitis pseudomembranosa, pero el más importante sigue siendo el uso de antibióticos. La mayoría de los antibióticos pueden causar la infección por C. difficile, sin embargo los más frecuentemente asociados han sido ampicilina, cefalosporinas, clindamicina y fluoroquinolonas.
El espectro clínico de presentación es variable, según el contexto en el que se den, sea una infección comunitaria o nosocomial. También deben tenerse en cuenta todos los diagnósticos diferenciales, entre ellos los más comunes el síndrome de colon irritable, enfermedad celiaca, enfermedad inflamatoria del colon y otras infecciones abdominales, como ser por Klebsiella oxytoca, Clostridium perfringes y Staphylococcus aureus13.
En el caso que presentamos, la paciente estaba siendo tratada de forma ambulatoria por un cuadro infeccioso de celulitis por lo que recibe varios esquemas de terapia antimicrobiana, incluyendo quinolonas y clindamicina. Desarrolló posteriormente cuadro de fiebre elevada, dolor abdominal y episodios de diarrea. La habilidad de realizar el diagnóstico de forma rápida y certera ayuda a reducir la morbilidad y mortalidad asociada.
El tratamiento de la infección causada por C. difficile requiere de la restauración completa de la microbiota normal del intestino que resulta de la eliminación del germen. Los pacientes asintomáticos en riesgo pueden ser tratados en ocasiones de forma conservadora únicamente al omitir el antibiótico asociado al brote, manejo de sostén e hidratación, con seguimiento cercano del caso. Aunque diferentes opciones se encuentran en estudio, entre ellas el uso de probióticos, de resinas ligadoras de toxinas o de inmunoglobulinas intravenosas, la única terapia de efectividad confirmada es la cobertura antibiótica.
De primera elección en pacientes con episodios leves a moderados está recomendado el metronidazol 500 mg vía oral tres veces al día, por 10 a 14 días, con una tasa de respuesta inicial mayor del 90% y resolución de los síntomas en la primera semana en la mayoría de los casos. Hasta 15% de los pacientes pueden presentar colitis con criterios de severidad y en ellos se recomienda la administración de vancomicina 125 mg vía oral (aunque su presentación sea intravenosa) cuatro veces al día, ya sea sola o acompañada de metronidazol 14. En casos de colitis fulminante se aumenta la dosis a 500 mg cuatro veces al día. Si el cuadro se acompaña de íleo, también se puede administrar vancomicina por vía rectal diluyendo 500 mg en 100 mL de solución salina, como enemas de retención. En pacientes críticos, que no responden a antibióticos, con riesgo de perforación de colon, íleo severo o megacolon tóxico, está indicada la colectomía subtotal, preservando el recto.
Hasta 30% de los pacientes pueden presentar recurrencias a pesar de una respuesta inicial satisfactoria, y en este grupo de pacientes se recomienda tratar con el mismo esquema antibiótico utilizado la primera vez, según la severidad del cuadro.
Con la emergencia de nuevas cepas más virulentas, resistentes a vancomicina, asociadas a mayor capacidad de producción de toxinas y eficiencia elevada de esporulación, ha hecho necesario el estudio de otras opciones de tratamiento. Dentro de estas opciones se ha estudiado la fidaxomicina, un antibiótico macrocíclico de espectro estrecho, con absorción mínima en el tracto gastrointestinal, que alcanza concentraciones medias en heces por encima de la concentración inhibitoria mínima para C. difficile más de 5.000 veces, por lo que actúa como bactericida contra esta bacteria e inhibe la formación de esporas, sin alterar de manera significativa la microbiota habitual del intestino (15.
El trasplante fecal puede considerarse el "tema candente" en la terapia para esta enfermedad en el siglo XXI, aunque en realidad se describió por primera vez en 1958. Teniendo en cuenta que la mayoría de las infecciones por C. difficile se deben al agotamiento de la microflora intestinal sana después del uso de antibióticos, fue lógico intentar reemplazar estos "buenos insectos" perdidos con bacterias obtenidas de individuos sanos. En la bacterioterapia fecal, de hecho, las heces de personas sanas se transfirieron al intestino grueso de pacientes infectados con C. difficile a través de enemas, por lo que se llama trasplante fecal o terapia de microbioma fecal 16. Un artículo informó una tasa de éxito del 80% para el tratamiento de la colitis recurrente mediante infusión duodenal de heces de donantes en comparación con la terapia con vancomicina 17.
Este novedoso tratamiento puede ser llevado a través de las entradas proximales o distales del tracto gastrointestinal. La instilación puede realizarse con colonoscopía, enema o tubo rectal para su introducción en el tracto gastrointestinal inferior, y mediante sonda nasogástrica o endoscopía/gastroscopía para el pasaje del tracto gastrointestinal superior en el duodeno. La administración a través del tracto gastrointestinal superior mostró un mejor éxito del tratamiento (92%) en comparación con el enema (79%)18.
Finalmente, se recomienda promover programas de uso racional de antimicrobianos, especialmente restringir el uso de aquellos más fuertemente asociados al desarrollo de colitis pseudomembranosa, como fluoroquinolonas, clindamicina, cefalosporinas. Otras medidas incluyen evitar fármacos considerados de riesgo como los inhibidores de la bomba de protones, minimizar los tiempos de internación, educar sobre medidas generales de higiene y prevención de infecciones adquiridas por vía oral, dirigida a pacientes, acompañantes y personal de salud, especialmente respecto a los riesgos de la ingesta de alimentos en las áreas asistenciales.