INTRODUCCIÓN
En el sistema de siembra directa el agricultor depende en gran medida del herbicida glifosato para el control de las malas hierbas y la desecación de cultivos de cobertura (Salas y Sarubbi, 2013). Esto se confirma en los datos oficiales de la Dirección Nacional de Aduanas, según los cuales Paraguay importó 16,8x106 Kg de glifosato en el año 2021 y 14,3x106 Kg en 2022, en relación al total de herbicidas 51,7 y 45,9%, respectivamente (Dirección Nacional de Aduanas, 2022).
El glifosato es un herbicida de postemergencia de amplio espectro y de acción sistémica (Chikoye, Lum y Udensi, 2010; Schönbrunn et al., 2001). La forma de aplicación de este herbicida es foliar, a través de picos de pulverización hidráulica, un método inherentemente ineficiente, con pérdidas que ocurren desde reflejo de gotas, perdidas por escurrimiento, deriva y evaporación en vuelo (Leaper y Holloway, 2000). Sin embargo, el efecto de herbicidas, en especial el glifosato, puede ser mejorado mediante el uso de coadyuvantes (Sharma y Singh, 2000; Wang y Liu, 2007). Según el modelo de Bromilow, Chamberlain y Evans (1990) la molécula de glifosato posee excelentes características para la movilidad en floema, con consecuente comportamiento sistémico en la planta, luego de la absorción. Sin embargo, el paso por la cutícula puede ser complicado por la naturaleza lipídica de la misma, y las características hidrofílicas de la molécula del glifosato (Santier y Chamel, 1992). Según Hao et al. (2019) la medida de la penetración del glifosato en la cutícula es una buena medida de la eficacia de un coadyuvante. Los mismos autores encontraron aumentos de penetración al reducir la tensión superficial y consecuentemente el ángulo de contacto entre gota y superficie foliar con la adición de un coadyuvante.
Los coadyuvantes más utilizados en aplicaciones agroquímicas (Travlos, Cheimona y Bilalis, 2017) y también los más eficientes en aumentar el efecto de los agroquímicos son los surfactantes, materiales que reducen la tensión superficial del caldo de aplicación y con ello el ángulo de contacto de la gota sobre la superficie de la hoja, lo cual aumenta el efecto humectante y el contacto entre gota y superficie foliar (Wang y Liu, 2007).
El tipo de surfactante que resulta en la mayor absorción foliar de herbicidas varía en función a la especie de planta y al tipo de herbicida (Travlos et al., 2017, Wang y Liu, 2007). Por lo tanto, la actividad foliar del glifosato puede optimizarse utilizando distintos tipos de adyuvantes. Según Sharma y Singh (2000) el uso del coadyuvante organosiliconado L-77 en Bidens frondosa, aumenta significativamente la absorción y translocación de glifosato y logra un mayor control de la planta en comparación con otros coadyuvantes. Sin embargo, en el caso de Panicum maximum, el uso de L-77 no revela ninguna mejora en la absorción de glifosato e incluso ejerce un efecto antagonista, mientras el aceite de semillas metilado muestra una mayor absorción y eficacia del glifosato. También Durigan (1992) reportó importante aumento en el control de P. máximum con glifosato al usar aceite vegetal como coadyuvante. Por lo tanto, la elección del adyuvante debe ser específica para cada especie a fin de optimizar la actividad foliar del glifosato en estas dos especies de plantas.
Por otro lado, el efecto del pH del medio portador del glifosato ha sido enfatizado por técnicos en aplicación, empresas formuladoras y vendedoras de coadyuvantes y herbicidas, y solicitudes de patentes (Green y Beestman, 2007). Pocos son los estudios que experimentaron en condiciones de campo su efecto sobre la eficacia del glifosato, el cual no está completamente elucidado y los resultados reportados en la literatura son inconsistentes. Por un lado, los resultados de Gómez Vargas, Pitty y Miselem (2006) no muestran variación en la eficacia de glifosato al variar el pH inicial del agua portador (tratamientos de pH 4,5, 6,5 y 8,5), aparentemente por el poder acidificante de la formulación de glifosato que redujo el pH del caldo resultante a valores cercanos a 4. Sin embargo, Shilling y Haller (1989) usando valores de pH del agua portador similares, pero tamponados, obtuvieron mayor control de Panicum repens con pH cercano a 4.
El estado de ionización de la molécula del glifosato en solución está en función del pH del medio portador (Bromilow y Chamberlain, 2000; Fliss, Essalah, & Ben Fredj, 2021), con cuatro grupos ionizables y valores de pKa de 0.8, 2.2, 5.5 y 10.2 (Fiorilli et al., 2017; Pereira et al., 2021). A mitad de camino entre los puntos de pKa adyacentes la carga neta de la molécula es 0, -1 y -2, respectivamente (Gougler & Geiger, 1981). Según la teoría de los ácidos débiles, este estado de ionización tiene efecto sobre la absorción foliar con un aumento de absorción con valores de pH menores, estados menos ionizados (Green & Beestman, 2007; Wang y Liu, 2007). Resultados recientes de Devkota y Johnson (2019,2020) demostraron el efecto del pH sobre la eficacia del glifosato experimentalmente, obteniendo mejor control con pH 4 comparado con pH 6.5 y 9 para varias especies de malezas dicotiledóneas. Estos autores resaltan que la especie de la maleza podría jugar un rol importante en el efecto del pH sobre la eficacia del glifosato.
Recientemente, pesticidas botánicos, ecológicamente amigables han sido promovidos ampliamente, aunque hasta el día cuestiones como su estabilidad y eficacia mantienen baja su aceptación y uso sostenido (Iqbal, Hazra, Purkait, Agrawal, y Kumar, 2022). Estos autores exitosamente formularon nanoemulsiones de aceite de neem, considerado un insecticida botánico, con bioadjuvantes incluyendo Cymbopogon citratus y Prosopis juliflora. Los resultados indicaron la estabilidad de la Azadirachtina en la formulación y una reducida tensión superficial y ángulo de contacto resultando en mejor adhesión y efecto humectante de la formulación.
Coadyuvantes de origen biológico también han recibido atención últimamente (Iqbal et al., 2022; Marcinkowska et al., 2018). Localmente, el Ácido Piroleñoso (AP) obtenido a partir de la condensación de los productos volátiles de la producción de carbón vegetal, ha recibido especial atención y hay reportes anecdóticos de reducciones hasta 50% en la dosis de glifosato necesaria para un control eficaz en combinación con este producto (Pankratz, 2022).
Actualmente existe una falta de información acerca de la coadyuvancia de productos basados en compuestos naturales utilizados por agricultores en Paraguay, en la desecación de malezas con glifosato. Por ello, se investigó el efecto de dos coadyuvantes basados en compuestos naturales sobre la eficacia biológica del glifosato en la desecación de Brachiaria ruziziensis.
MATERIALES Y MÉTODOS
El estudio fue realizado en dos etapas, primero un experimento de desecación de B. ruziziensis a campo y, segundo, un experimento en laboratorio para determinar el efecto acidificante de los productos utilizados en el experimento a campo.
Experimento de desecación de B. ruziziensis a campo
El experimento fue realizado el 14 de noviembre del 2022 en una parcela de pastura B. ruziziensis perteneciente a la Estación Experimental Isla Po’í, ubicada en el distrito Loma Plata del departamento Boquerón, Paraguay. El cultivo antecesor durante la campaña 2021/22 fue Maíz (Zea mays) en asociación con la pastura B. ruziziensis, la cual permaneció en la parcela luego de la cosecha del maíz. El suelo de la parcela fue de textura arenosa y de baja fertilidad. Los principales parámetros meteorológicos fueron medidos durante la aplicación con un Higro Termo-Anemómetro portátil AKSO modelo AK821. La dirección del viento fue del norte, con temperatura de 31,5°C ±3°C, velocidad del viento entre 10 y 15 km h-1 y una humedad relativa de 35% ±3%.
El glifosato utilizado tenía una concentración de 66,2 % sal potásica (54% p/v de equivalente ácido de glifosato). Las dosis de glifosato se expresaron como la cantidad de i.a. ha-1 (sal potásica del glifosato). Se comparó dos coadyuvantes de origen natural y un coadyuvante sintético.
El primer coadyuvante de origen natural fue el Ácido piroleñoso (AP) obtenido de un vendedor local. El AP es un líquido con alta concentración de ácido acético, además de ácido fórmico y otros de bajo peso molecular obtenido a través de la pirolisis lenta de biomasa vegetal y la condensación de los productos volátiles (Manals Cutiño, Penedo Medina, Giralt Ortega, Beltrán Guilarte, y Sánchez del Campo, 2009).
El segundo coadyuvante de origen natural fue una solución producto de fermentación de hierbas (FB) obtenido de la empresa Microvita S.A. La FB es descrito como un probiótico con alta concentración de bacterias ácido-lácticas e hierbas fermentadas promovido localmente como apto de acompañar a todo tipo de aplicaciones de fitosanitarios vía pulverización.
El coadyuvante sintético (AT) fue incluido como producto de referencia en la comparación por su amplia aceptación entre los productores locales, siendo uno de los coadyuvantes más vendidos en la región según los datos de comercialización de la Cooperativa Chortitzer Ltda. (G. Coppens, comunicación personal, seis de octubre, 2023). Las funciones de este producto mencionadas en la etiqueta son dispersante, anti-espumante, secuestrante, reductor de pH, emulsionante, antivolatilizante, anti deriva y estimulante.
Además, el caldo de pulverización para cada tratamiento contenía un por ciento de aceite vegetal desgomado, y 200 ml ha-1 de un humectante siliconado (EMP) con el objetivo de generar condiciones similares de tensión superficial y adherencia para todos los tratamientos considerando que la hipótesis fue que el efecto acidificante de los coadyuvantes influye la eficacia del glifosato. Para todos los coadyuvantes las dosis recomendadas por los fabricantes fueron respetadas.
Se diseñó un experimento con seis tratamientos (Tabla 1). Estos fueron diseñados para representar la dosis de glifosato recomendada en la etiqueta del producto, además una subdosis (50% de la recomendada) para determinar mejor la coadyuvancia del AP (Leaper y Holloway, 2000). Para facilitar la aplicación de los productos con una pulverizadora montada al enganche de tres puntos de un tractor, se utilizó un diseño experimental en franjas de manera que cada franja representaba un tratamiento. Cada franja medía 18 m de ancho y mínimamente 250 m de largo. Dentro de cada franja se tomó seis muestras, las cuales consistían en la parte aérea de la pastura que caía dentro de un m2 y las mismas fueron tomadas como repeticiones. Los puntos de muestreo fueron distribuidos sobre la franja y tomadas con cierto control local a criterio del investigador con el objetivo de representar el estado de la pastura observado a campo.
Tabla 1 Tratamientos del experimento a campo con sus respectivas dosis y el pH del caldo de aplicación resultante. AT (coadyuvante sintético), AP (Ácido Piroleñoso), FB (solución producto de fermentación de hierbas).
| Tratamiento | Descripción | pH del caldo resultante | |||
| Glifosato (i.a. kg ha-1) | Coadyuvante (dosis) | ||||
| 1 | 0,83 | AT (0,056 L ha-1) | 4,2 | ||
| 2 | 0,83 | AP (4 L ha-1) | 4,5 | ||
| 3 | 1,66 | AP (4 L ha-1) | 4,3 | ||
| 4 | 1,66 | AT (0,056 L ha-1) | 4,3 | ||
| 5 | 1,66 | AP (4 L ha-1) + FB (4 L ha-1) | 4,2 | ||
| 6 | 1,66 | FB (4 L ha-1) | 4,3 | ||
La cantidad de caldo aplicado fue de 80 L ha-1. Para la preparación de este, se utilizó agua de lluvia almacenada en un tajamar luego de ser tratada con Sulfato de Aluminio para lograr la floculación y sedimentación del material en suspensión que produce turbidez (Zand y Hoveidi, 2015), un procedimiento adoptado comúnmente por productores locales. Esta agua acondicionada tenía una conductividad eléctrica de 1,44 µS cm-1 y un pH de 7,8 antes de la preparación del caldo.
El contenido de agua (CA, la masa seca en relación con la masa fresca) de la B. ruziziensis fue utilizada como parámetro indicador de mortandad de la misma (Hunsche, Scherhag, Schmitz-Eiberger, y Noga, 2007). La evaluación del efecto de los tratamientos sobre la mortandad de la B. ruziziensis fue realizada 21 días posterior a la aplicación mediante seis muestras por tratamiento. Luego de determinar su peso las muestras fueron secadas en estufa a 65°C hasta masa constante (Shuaibu, Fasae, Adeleye, Wheto, y Oluwatosin, 2018). El CA de cada muestra fue determinado por la pérdida de peso durante el secado en relación con el peso inicial (Tabla 1A y Tabla 2A).
El segundo experimento fue realizado entre noviembre y diciembre del 2022 en el laboratorio Lab-DEPROVE, en la ciudad de Loma Plata, para determinar el efecto acidificante de los coadyuvantes y productos utilizados en el experimento de desecación a campo.
El experimento fue diseñado para determinar el efecto acidificante de los coadyuvantes y productos utilizados en el experimento de desecación a campo. Para ello, seis tratamientos (Tabla 2) fueron analizados en tres repeticiones. Las concentraciones de cada producto fueron las mismas utilizadas en el experimento a campo y también se utilizó agua de la misma calidad. Los coadyuvantes fueron añadidos al agua en agitación midiendo el pH de la solución resultante.
Tabla 2 Tratamientos del experimento de determinación del efecto acidificante de los productos utilizados. AP (Ácido Piroleñoso), FB (solución producto de fermentación de hierbas), AT (coadyuvante sintético), EMP (humectante siliconado).
| Tratamiento | Producto | Dosis (ml L-1) | Función indicada | |
| 1 | AP | 50 | No indicada | |
| 2 | FB | 50 | Probiótico | |
| 3 | AT | 0,7 | Reductor de pH / antiespumante | |
| 4 | EMP | 2,5 | Humectante siliconado | |
| 5 | Glifosato | 31,3 | Herbicida | |
| 6 | Glifosato | 15,6 | Herbicida |
Para ambos experimentos se realizó el análisis de la varianza con el software InfoStat. Para determinar los tratamientos diferentes estadísticamente se utilizó la comparación de medias de Tukey a un nivel de significancia del cinco por ciento.
RESULTADOS
Experimento de desecación de B. ruzisiensis a campo
Los resultados de desecación de la B. ruziziensis fueron medidos a través del CA de la parte aérea de la pastura y mostraron diferencias significativas entre tratamientos (Figura 1). Los datos crudos se presentan en Tabla 1A. La mejor desecación de la pastura se obtuvo con la dosis mayor de glifosato en combinación con el coadyuvante AT alcanzando un CA de 0.1. La combinación de la misma dosis de glifosato con AP y AP más FB no difirió significativamente con el tratamiento AT, pero se observó una tendencia de menor eficacia (mayor CA). Sin embargo, utilizando únicamente FB como coadyuvante con la misma dosis de glifosato, la eficacia en la desecación fue significativamente menor a todos los demás tratamientos, incluso a los dos tratamientos con la menor dosis de glifosato.
Para los dos coadyuvantes que se aplicó en dos dosis de glifosato, la relación dosis-CA se presenta en la Figura 2. Para ambas dosis, la diferencia entre tratamientos de coadyuvantes no es significativa. La pendiente de esta correlación negativa indica un aumento en eficacia de desecación de la pastura con el aumento en dosis de glifosato.
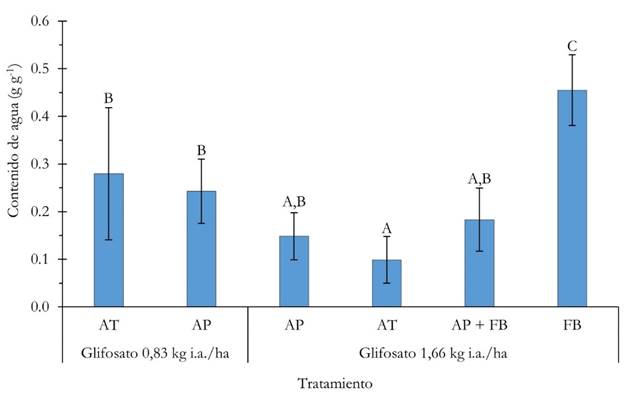
Figura 1 Contenido de agua de la parte aérea de la pastura B. ruziziensis luego de tres semanas de la aplicación de los tratamientos, AT (coadyuvante sintético), AP (Ácido Piroleñoso), FB (solución producto de fermentación de hierbas). Tratamientos con letras iguales no difieren significativamente (p>0,05). Barras de error ± 1 DE.
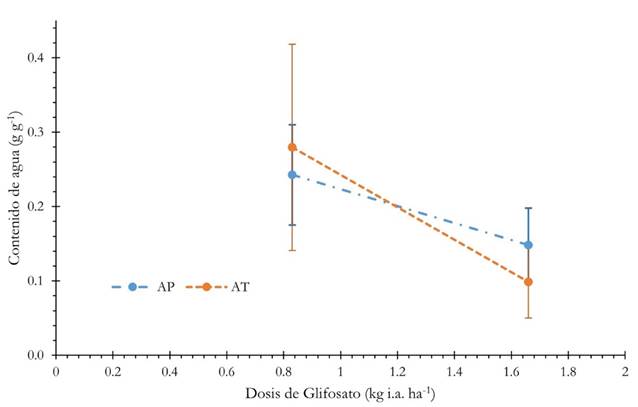
Figura 2 Contenido de agua de la pastura B. ruziziensis en función de la dosis de glifosato y coadyuvante empleado luego de tres semanas de la aplicación de los tratamientos. AP (Ácido Piroleñoso) y AT (coadyuvante sintético). Barras de error ± 1 DE.
Tabla 1A Datos crudos de las muestras (repeticiones) tomadas en las franjas de aplicación de los tratamientos.
| 1. Tratamiento | 2. Repetición | 3. Tara (g) | 4. Peso humedo + tara (g) | 5. Peso humedo (g) | 6. Peso seco + tara (g) | 7. Peso seco (g) | 8. Agua (g) | 9. CA (g g-1) |
| 1 | 1 | 78,0 | 190,2 | 112,2 | 174,3 | 96,3 | 15,9 | 0,14 |
| 1 | 2 | 75,2 | 335,9 | 260,7 | 251,3 | 176,1 | 84,6 | 0,32 |
| 1 | 3 | 75,6 | 386,5 | 310,9 | 233,5 | 157,9 | 153,0 | 0,49 |
| 1 | 4 | 75,3 | 263,7 | 188,4 | 237,5 | 162,2 | 26,2 | 0,14 |
| 1 | 5 | 69,3 | 216,1 | 146,8 | 183,9 | 114,6 | 32,2 | 0,22 |
| 1 | 6 | 79,0 | 282,0 | 203,0 | 208,7 | 129,7 | 73,3 | 0,36 |
| 2 | 1 | 78,6 | 246,4 | 167,8 | 211,3 | 132,7 | 35,1 | 0,21 |
| 2 | 2 | 76,8 | 308,5 | 231,7 | 263,0 | 186,2 | 45,5 | 0,20 |
| 2 | 3 | 71,7 | 306,1 | 234,4 | 246,3 | 174,6 | 59,8 | 0,26 |
| 2 | 4 | 81,0 | 220,0 | 139,0 | 187,8 | 106,8 | 32,2 | 0,23 |
| 2 | 5 | 69,9 | 345,2 | 275,3 | 292,3 | 222,4 | 52,9 | 0,19 |
| 2 | 6 | 75,2 | 322,3 | 247,1 | 230,5 | 155,3 | 91,8 | 0,37 |
| 3 | 1 | 81,4 | 419,0 | 337,6 | 349,5 | 268,1 | 69,5 | 0,21 |
| 3 | 2 | 81,8 | 454,6 | 372,8 | 389,4 | 307,6 | 65,2 | 0,17 |
| 3 | 3 | 75,9 | 247,1 | 171,2 | 232,5 | 156,6 | 14,6 | 0,09 |
| 3 | 4 | 78,1 | 366,9 | 288,8 | 311,3 | 233,2 | 55,6 | 0,19 |
| 3 | 5 | 71,9 | 241,5 | 169,6 | 223,2 | 151,3 | 18,3 | 0,11 |
| 3 | 6 | 72,8 | 234,7 | 161,9 | 214,8 | 142,0 | 19,9 | 0,12 |
| 4 | 1 | 74,1 | 412,2 | 338,1 | 347,7 | 273,6 | 64,5 | 0,19 |
| 4 | 2 | 90,1 | 415,0 | 324,9 | 382,5 | 292,4 | 32,5 | 0,10 |
| 4 | 3 | 77,5 | 315,3 | 237,8 | 300,3 | 222,8 | 15,0 | 0,06 |
| 4 | 4 | 67,8 | 177,9 | 110,1 | 168,6 | 100,8 | 9,3 | 0,08 |
| 4 | 5 | 75,2 | 487,1 | 411,9 | 446,0 | 370,8 | 41,1 | 0,10 |
| 4 | 6 | 76,8 | 392,5 | 315,7 | 375,3 | 298,5 | 17,2 | 0,05 |
| 5 | 1 | 68,3 | 505,0 | 436,7 | 387,3 | 319,0 | 117,7 | 0,27 |
| 5 | 2 | 72,8 | 327,5 | 254,7 | 294,5 | 221,7 | 33,0 | 0,13 |
| 5 | 3 | 74,3 | 297,6 | 223,3 | 241,6 | 167,3 | 56,0 | 0,25 |
| 5 | 4 | 71,5 | 247,3 | 175,8 | 228,0 | 156,5 | 19,3 | 0,11 |
| 5 | 5 | 72,4 | 273,4 | 201,0 | 234,1 | 161,7 | 39,3 | 0,20 |
| 5 | 6 | 75,2 | 303,9 | 228,7 | 270,9 | 195,7 | 33,0 | 0,14 |
| 6 | 1 | 73,0 | 492,9 | 419,9 | 264,4 | 191,4 | 228,5 | 0,54 |
| 6 | 2 | 74,7 | 425,7 | 351,0 | 264,0 | 189,3 | 161,7 | 0,46 |
| 6 | 3 | 83,9 | 421,3 | 337,4 | 270,2 | 186,3 | 151,1 | 0,45 |
| 6 | 4 | 78,8 | 301,4 | 222,6 | 227,3 | 148,5 | 74,1 | 0,33 |
| 6 | 5 | 74,0 | 568,6 | 494,6 | 357,6 | 283,6 | 211,0 | 0,43 |
| 6 | 6 | 69,0 | 390,5 | 321,5 | 224,0 | 155,0 | 166,5 | 0,52 |
Para obtener el CA de la muestra se realizó los siguientes cálculos para cada repetición (los números representan las columnas de la Tabla 1A):
5 = 4 - 3
7 = 6 - 3
8 = 5 - 7
9 = 8 / 5
Efecto acidificante de coadyuvantes y glifosato
Los productos utilizados como coadyuvantes y el glifosato, todos en su formulación comercial, con la misma dosis y en solución con agua de la misma calidad que la utilizada en el experimento a campo, mostraron diferencias en el pH resultante (Figura 3, Tabla 2A). Los valores de pH más bajos fueron obtenidos con los coadyuvantes FB y AP (4,14 y 4,22, respectivamente). Las soluciones con los coadyuvantes AT y EMP resultaron en valores de pH levemente ácidos (5,91 y 6,0, respectivamente). Además, se comprobó que el glifosato redujo el pH del agua a valores de 4,64 y 4,78 con las concentraciones de 31,3 y 15,6 ml L-1, respectivamente. Esto también confirma las mediciones del pH de los caldos aplicados como tratamientos, los cuales estaban dentro de un rango de 4,2 a 4,5 sin importar el coadyuvante utilizado.
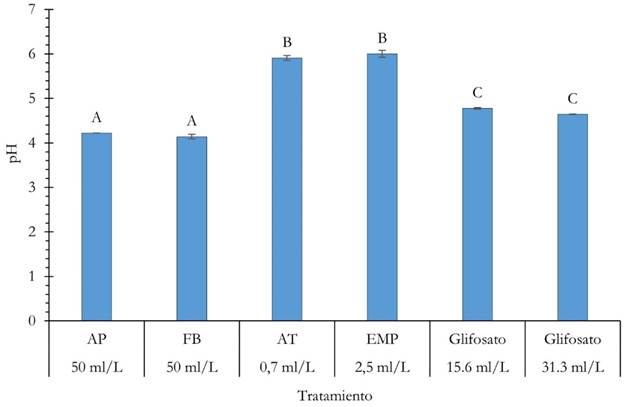
Figura 3 Efecto acidificante de los coadyuvantes y productos utilizados en solución con agua de la misma calidad como empleada en el experimento a campo, AP (Ácido Piroleñoso), FB (solución producto de fermentación de hierbas), AT (coadyuvante sintético), EMP (humectante siliconado). Tratamientos con letras iguales no difieren significativamente (p>0,05). Barras de error ± 1 DE.
En la Tabla 2A se presentan los datos crudos del experimento de determinación del efecto acidificante de los productos utilizados en el experimento de desecación a campo.
Tabla 2A Datos crudos y medias de pH, con la desviación estándar (DE) y coeficiente de variación (CV) para cada tratamiento. Además, se indica la concentración y el producto utilizado para cada tratamiento.
| Tratamiento | Producto | Dosis | Repetición | Media | DE | CV | ||
| 1 | 2 | 3 | ||||||
| 1 | AP | 50 ml l-1 | 4,22 | 4,22 | 4,22 | 4,22 | 0,00 | 0,00 |
| 2 | FB | 50 ml l-1 | 4,20 | 4,11 | 4,11 | 4,14 | 0,05 | 1,26 |
| 3 | AT | 0,7 ml l-1 | 5,96 | 5,91 | 5,85 | 5,91 | 0,06 | 0,93 |
| 4 | EMP | 2,5 ml l-1 | 5,91 | 6,03 | 6,06 | 6,00 | 0,08 | 1,32 |
| 5 | Glifosato | 15,6 ml l-1 | 4,76 | 4,77 | 4,80 | 4,78 | 0,02 | 0,44 |
| 6 | Glifosato | 31,3 ml l-1 | 4,65 | 4,64 | 4,64 | 4,64 | 0,01 | 0,12 |
DISCUSIÓN
El CA de todos los tratamientos muestra efecto del glifosato cuando se lo compara con el CA de B. ruziziensis en estado vivo entre 0,58 y 0,64 (Shuaibu et al., 2018).Enoh et al. (2005) reportaron un CA de 0,11 para heno de B. ruziziensis específicamente, por lo cual es razonable asumir la mortandad de la pastura con CA cercanos a los valores del heno.
Los valores de pH de los caldos resultantes de todos los tratamientos aparentemente no diferían significativamente (Tabla 1). Esto indica que la formulación comercial de glifosato utilizada tiene poder tampón y enmascara el efecto acidificante del coadyuvante. Por lo tanto, la hipótesis que el efecto acidificante de los coadyuvantes influye en la eficacia biológica del glifosato no puede ser resuelta con los datos obtenidos en este estudio. Las diferencias entre tratamientos parecen deberse a otros factores.
Entre los tratamientos con la dosis mayor de glifosato no se observó diferencias significativas con excepción del tratamiento FB, el cual resultó en la menor eficacia de desecación (Figura 1). La grande diferencia entre este tratamiento y los demás indica un efecto antagonista a la actividad biológica del glifosato. De hecho, la adsorción de glifosato a sustancias orgánicas ha sido reportado por varios autores, específicamente la adsorción a ácidos húmicos (Albers, Banta, Erik, y Jacobsen, 2009; Piccolo, Celano, & Conte, 1996) pero también a ácidos fúlvicos (Mazzei y Piccolo, 2012). Shehata, Kühnert, Haufe y Krüger (2014) determinaron la inhibición del efecto antimicrobiano del glifosato por una concentración de ácidos húmicos de 1 mg L-1, lo cual indica la reducción o inhibición de la actividad biológica del glifosato por los ácidos húmicos. Los resultados de Mazzei y Piccolo (2012) indican una reacción no covalente entre glifosato y sustancias orgánicas disueltas a pH levemente ácido, dándole a ambas moléculas sitios adicionales para la formación de puentes de hidrógeno a través de la protonación de los sitios funcionales y disminuyendo la repulsión electronegativa que ocurriría entre dos moléculas con carga negativa.
Los valores de pH medidos en este estudio con los coadyuvantes, pero sin agregar el glifosato (Figura 3), y también del caldo preparado (Tabla 1), están dentro de un rango de 4,1 a 6,0, por lo cual se darían condiciones de protonación de los grupos funcionales de la materia orgánica disuelta y se facilitaría así la formación de puentes de hidrógeno con el glifosato. De hecho, el glifosato mismo mostró efecto acidificante. Esto se observa comparando los valores de pH de las soluciones con los coadyuvantes solo y a la misma concentración (Figura 3) como en el experimento a campo, donde los valores de pH no variaban significativamente entre tratamientos (Tabla 1). Resultados similares fueron obtenidos por Gómez Vargas et al. (2006) al usar agua portador de diferentes valores de pH inicial (8,5, 6,5 y 4,5) que al añadir el glifosato (Roundup Max® 680 SG) se establecieron entre pH 4,03 y 4,13. Mencionados autores no pudieron determinar un efecto del pH inicial del agua portador sobre la eficacia del glifosato.
El orden de adsorción del glifosato a los compuestos orgánicos no sigue un orden de acidez sino de alifaticidad y de tamaño de molécula, con mayor adsorción a moléculas más alifáticas y de mayor tamaño (Piccolo, Celano y Conte, 1996). FB es descrito en su etiqueta comercial como un probiótico conteniendo alta concentración de bacterias acido lácticas e hierbas fermentadas. Considerando que el ácido láctico producido por estas bacterias tiene características alifáticas (Vranova, Rejsek, y Formanek, 2013), además de la posible presencia de materia orgánica disuelta no degradada por el proceso de fermentación, reacciones entre la FB y la molécula del glifosato podrían ser responsables del antagonismo observado en este estudio.
Con la dosis de glifosato de 0,84 kg i.a. ha-1 la desecación fue menos eficaz resultando en mayor CA de la pastura, aunque sin diferencia estadística entre coadyuvantes usados. Esto demuestra que la coadyuvancia del AP no fue suficiente como para reducir la dosis del glifosato como manifestado por Pankratz (2022).
Este estudio tiene tres limitaciones principales. Primero, la falta de un tratamiento sin coadyuvante para la determinación de la eficacia biológica de glifosato solo. Como testigo se utilizó glifosato con un coadyuvante de referencia ya que esto representa la combinación utilizada en la agricultura local. Por siguiente, la utilización de una formulación de glifosato con poder tampón dificulta resolver la hipótesis de la investigación, ya que los caldos de los tratamientos del experimento a campo no diferían significativamente en su pH. Por último, el diseño en franjas con control local en la toma de muestras dentro de las franjas no provee una completa aleatorización.
CONCLUSIÓN
Para las condiciones de los experimentos de este estudio se concluye que la mejor desecación de la B. ruziziensis se obtiene con los coadyuvantes del AT y AP.
El probiótico FB es antagónico al efecto de desecación del glifosato y resulta en la menor eficacia del herbicida. Basándose en resultados de este estudio, su uso como coadyuvante del glifosato para la desecación de B. ruziziensis no es recomendado.
Ninguno de los coadyuvantes utilizados permite la reducción de la dosis de glifosato manteniendo la misma eficacia.
Considerando las limitaciones del estudio, los datos obtenidos en este estudio no permiten inferir algún efecto de la diferencia en reducción de pH de los coadyuvantes utilizados sobre la eficacia biológica del glifosato.
Para futuros estudios se recomienda utilizar una formulación de glifosato sin poder tampón para evaluar el efecto acidificante del coadyuvante sobre la eficacia del glifosato. Además, la inclusión de un tratamiento sin coadyuvantes es deseable.















