Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Investigación Agraria
versión On-line ISSN 2305-0683
Investig. Agrar. vol.16 no.2 San Lorenzo dic. 2014
ARTÍCULO CIENTÍFICO
Efecto del riego sobre la abundancia de Raoiella indica en plantas de Cocos nucifera L.
Effect of irrigation on abundance of Raoiella indica on Cocos nucifera trees
Reinaldo Villasmil1, Neicy Valera1 y Carlos Vásquez1*
1 Universidad Centroccidental Lisandro Alvarado. Decanato de Agronomía. Departamento de Ciencias Biológicas. Cabudare, estado de Lara, Venezuela.
* Autor para correspondencia (carlosvasquez@ucla.edu.ve)
Recibido: 08/09/2014; Aceptado: 11/11/2014.
RESUMEN
El ácaro rojo de las palmeras, Raoiella indica Hirst es una plaga en plantaciones de coco en el Caribe. Hasta el presente no existe información disponible sobre el efecto de las prácticas culturales sobre las poblaciones de este ácaro. En este estudio se evaluó el efecto del riego sobre la abundancia de R. indica en plantas de Cocos nucifera en condiciones de umbráculo en el Decanato de Agronomía de la Universidad Centroccidental Lisandro Alvarado, Venezuela. Plantas de coco var. Enano Amarillo Malayo de 1-2 años de edad fueron infestadas artificialmente con 20 hembras adultas. Posteriormente, las plantas fueron divididas en tres grupos (T0= 100%, T1= 50% y T2= 25% del requerimiento de agua de riego). Cada siete días se contó el número de huevos y formas móviles por folíolo en cada uno de los tratamientos. Durante todo el ensayo, el número de huevos y formas móviles fue significativamente mayor en plantas regadas con el 100% de su requerimiento hídrico. Los resultados obtenidos sirven de base para futuros estudios por lo que se sugiere evaluar los posibles cambios bioquímicos en la hoja por efecto de la supresión del riego de modo a entender mejor cuales cambios bioquímicos ocurren y su posible relación con la dinámica poblacional de R. indica.
Palabras clave: Ácaro rojo de las palmeras, coco, manejo cultural.
ABSTRACT
The red palm mite, Raoiella indica Hirst is a pest on coconut plantations in the Caribbean. To date there is no available information on the effect of cultural strategies on this mite population. In this study the effect of irrigation on R. indica abundance on Cocos nucifera plants was evaluated under greenhouse conditions at the Faculty of Agronomy, Universidad Centroccidental Lisandro Alvarado, Venezuela. Coconut plants var. Malayan Yellow Dwarf of 1-2 years-old were artificially infested with 20 adult females. Subsequently, the plants were divided into three groups (T0= 100%, T1= 50% and T2= 25% of water requirement). Every seven days the number of eggs and motile forms per leaflet was counted in each treatment. Throughout the test, the number of eggs and motile forms was significantly higher on plants irrigated with 100% of its water requirement. The results provide the basis for future studies, thus it is suggested to evaluate the possible biochemical changes in leaves due to the suppression of irrigation, to better understand biochemical changes and their possible relation with R. indica population dynamics.
Key words: Red palm mite, coconut, cultural management.
INTRODUCCIÓN
El ácaro rojo de las palmeras, Raoiella indica Hirst ha sido considerado por décadas como una plaga importante en plantaciones de coco (Cocos nucifera L.) y palma areca (Areca catechu L.) en la India (Daniel 1981, Chandra y Channaβasanna 1984) y en palma dátil (Phoenix dactyliphera) en Egipto (Zaher 1969). Al inicio del presente siglo, esta plaga también fue reportada en el Cercano y Medio oriente incluyendo Mauritius, Islas Reunión, Rusia y el norte de África y más recientemente en las Américas (Etienne y Flechtmann 2006), incluyendo islas del Caribe (Rodrigues et al. 2007), Venezuela (Vásquez et al. 2008), Colombia (Carrillo et al. 2011) y Brasil (Návia et al. 2011).
Desde su reporte en la región del Caribe, el ácaro rojo de las palmeras ha sido considerado una seria amenaza para las especies de palmeras, incluyendo no sólo cocoteros sino también otros taxa botánicos tales como Musaceae, Strelitziaceae, Zingiberaceae (Flechtmann y Etienne 2004, Vásquez y Moraes 2013). En esta región, el ácaro rojo de las palmeras ha sido registrado principalmente en 73 especies de Arecaceae, sin embargo también ha sido colectada en seis especies de Musaceae, cinco de Heliconiaceae, cuatro de Zingiberaceae y dos de Pandaceae y Strelitziaceae (Carrillo et al. 2012a).
El acaro rojo de las palmeras puede causar daños severos en especies de Arecaceae, especialmente en plantas de coco, en las cuales puede provocar muerte de plantas jóvenes y en plantas adultas el daño se evidencia por fuerte amarillamiento de las hojas maduras (Peña et al. 2006). Desde la detección de R. indica en América, se ha estimado una reducción en la producción de frutos de 70-75% en plantas de coco en Trinidad y Tobago y Venezuela (Návia 2008).
Los estudios sobre la biología y ecología de R. indica han indicado que esta plaga se reproduce en aproximadamente 21,5 días sobre hojas de cocotero (Vásquez et al. 2015) hasta 31 días sobre palma areca (Flores-Galano et al. 2010), pudiendo mantener altas poblaciones durante todo el año, características que unidas a la rápida dispersión de la plaga en el cultivo dificultan la escogencia y aplicación de los adecuados métodos de control.
Debido a los altos niveles de daño que puede llegar a ocasionar este ácaro, principalmente en plantaciones de coco, esta plaga ha recibido especial atención, siendo señalada con el estatus de plaga de importancia económica. En tal sentido, dentro de los programas de manejo de este ácaro se han probado varias herramientas de control, destacando principalmente la estrategia química, con el uso de productos selectivos a los enemigos naturales (Rodrigues y Peña 2012). Sin embargo, debido a los daños al ambiente y lo costoso de la aplicación de productos químicos, el control natural con depredadores se ha convertido en una excelente alternativa. Al respecto, 28 especies de depredadores han sido señaladas como enemigos naturales potenciales de R. indica (Carrillo et al.2012b), destacando con los mayores atributos para el control, el fitoseído Amblyseius largoensis (Carrillo et al. 2010).
En Venezuela, R. indica fue registrada inicialmente en el estado de Sucre a finales del 2007 (Vásquez et al. 2008). No obstante, al inicio de 2008 fueron observadas altas poblaciones del ácaro en el estado Falcón, el principal productor de coco del país, lo que indica la rápida dispersión de la plaga a lo largo del litoral venezolano. Es por ello, que se requiere realizar evaluaciones de campo y laboratorio para medir la eficiencia de técnicas ecológicas propuestas que permitan mantener controladas las poblaciones del ácaro rojo de las palmeras. En tal sentido, el presente trabajo pretende evaluar el efecto de diferentes requerimientos de agua de plantas de coco sobre las densidades poblacionales de R. indica
MATERIALES Y MÉTODOS
Obtención y adecuación de las plantas
El ensayo fue realizado en las instalaciones del Decanato de Agronomía, Universidad Centroccidental Lisandro Alvarado (UCLA). Se usaron 60 plantas de coco variedad ‘Enano Amarillo Malayo’ de 1-2 años de edad, las cuales fueron plantadas en bolsas plásticas (40 cm x 50 cm) con substrato conformado por tierra negra y cascarilla de arroz (1:1). Posteriormente fueron tratadas con Phytosoap (sal de potasio rica en ácidos grasos al 61%) a dosis de 2 cc/L de agua. Una vez establecidas, las plantas fueron artificialmente infestadas con 20 hembras adultas de R. indica colectadas en plantas de coco en Agua Viva, estado de Lara y transferidas mediante un pincel 000. Posteriormente, las plantas fueron divididas en tres grupos experimentales, cada uno constituyó un tratamiento.
Cálculo de la lámina del riego:
ETo=Kp*Evap (1)
Donde
ETo = Evaporación Potencial
Kp = coeficiente de tina (tabla) = 0,79
Evap calculada= 4 mm/día
ETo = 0,79 x 4 mm/día = 3,16 mm/día
ETc=Eto*k (2)
Donde:
ETc= Evaporación del cultivo
Kc = coeficiente del cultivo = 0,9
ETc = 3,16 mm/día x 0,9 = 2,844 mm/día = 2,844L/m2
Considerando el área de la bolsa (0,4 m x 0,5 m) se tiene que la necesidad de agua por bolsa es 0,6 L.
Los tratamientos fueron establecidos de acuerdo a diferentes volúmenes de agua, como sigue:
T0= plantas regadas con el 100% del agua requerida calculada con base en la evapotranspiración del cultivo (0,6 L/día).
T1= plantas regadas con 50% del agua requerida (0,3 L/día).
T2= plantas regadas con 25% del agua requerida (0,15 L/día).
En cada tratamiento fueron seleccionadas 15 plantas en las cuales se tomó una hoja completamente desarrollada y de ésta 5 folíolos en los cuales se contó el número de huevos y formas móviles por folíolo en cada uno de los tratamientos cada semana durante 6 semanas.
El ensayo fue conducido en un diseño completamente al azar.
Análisis de los Datos
El número de huevos y ácaros/cm2 fue transformado por 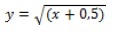
RESULTADOS Y DISCUSIÓN
Efecto del riego sobre la abundancia y oviposición de R. indica en plantas de coco variedad enano amarillo malayo
Se encontró efecto de los diferentes volúmenes de agua aplicados como riego sobre las densidades poblacionales de R. indica en plantas de coco variedad amarillo malayo (Tabla 1).
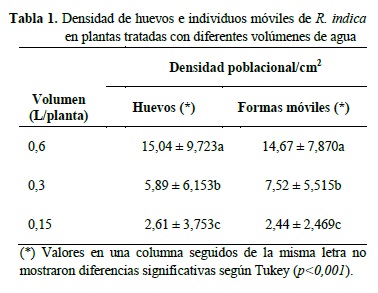
Con relación al número de huevos, la mayor densidad fue observada sobre plantas que recibieron el 100% del requerimiento de riego donde se encontró un promedio de 15,04 huevos/cm2. Adicionalmente, las plantas de coco regadas con el 50 y 25% del requerimiento mostraron diferencias entre ellas, encontrándose valores de 5,89 y 2,61 huevos/cm2, respectivamente.
Similarmente, cuando fue considerado el número de individuos móviles (larvas, ninfas y adultos), la mayor densidad fue observada en plantas tratadas con el 100% de su requerimiento hídrico, cuyo promedio alcanzó 14,67 individuos/cm2, mientras que en el resto de los tratamientos se observó 48,8 y 83,4 % menos población.
Con relación a la variación de la densidad poblacional de R. indica a lo largo de los muestreos, se encontró en plantas tratadas con 100% del requerimiento, las densidades tanto de individuos móviles como de huevos fueron consistentemente superiores al resto de los tratamientos, con valores promedios que variaron entre 10,67 y 18,92 ácaros/cm2 (Figura 1). En plantas regadas con el 50% del requerimiento se obtuvieron densidades entre 6,73 y 9,36 ácaros/cm2. Por último, en las plantas con el menor volumen de agua aplicada se encontraron las menores densidades, oscilando entre 0,95 y 4,31 ácaros/4cm2, con una tendencia a disminuir a medida que avanzaron los muestreos.
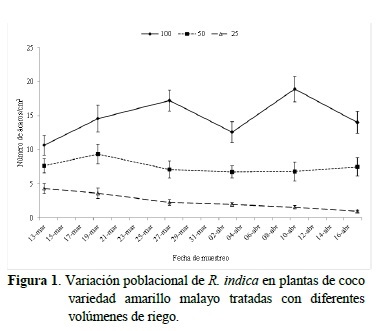
El estrés hídrico provoca cambios en la morfología, la fisiología y la bioquímica de la planta (Chaves et al. 2003). Sin embargo, las respuestas en la constitución química de la planta son muy variables y dependen de factores, tales como especie de planta, adaptación a la sequía de los genotipos y de la intensidad y frecuencia del estrés hídrico (Mody et al. 2009). Estos cambios provocados por el estrés hídrico han sido asociados con cambios en las densidades poblacionales de los artrópodos fitófagos (Mattson y Haack 1987), pudiendo llegar a variar de positivo a negativo, dependiendo de la intensidad del estrés (English-Loeb 1990, Daane y Williams 2003, Huberty y Denno 2004) y las especies de artrópodos y de planta (Waring y Cobb, 1992).
En general, es aceptado que plantas sometidas a estrés moderado muestran un incremento del valor nutricional de algunos contenidos celulares y reducción de la concentración de sustancias relacionadas con la defensa de la planta, resultando en incremento de poblaciones de fitófagos e intensificación del nivel producido en la planta (Showler 2013). Varios estudios señalan el incremento poblacional de la plaga en plantas sometidas a condiciones de estrés hídrico. Así, las poblaciones del ácaro de dos manchas, Tetranychus urticae Koch, aumentaron durante la época de sequía en el cultivo de soya (Klubertanz et al. 1990). De igual manera, poblaciones de los áfidos Diuraphis noxia (Morvilko) y Schizaphis graminum (Rondani) en trigo de secano (Dorschner et al. 1986) y de Brevicoryne brassicae L., sobre Brassica napus L. (Popov et al. 2006) fueron mayores en plantas sometidas a estrés hídrico cuando fueron comparadas con las plantas irrigadas. En general, el crecimiento poblacional de especies fitófagas se traduce en mayor daño a los cultivos debido a la susceptibilidad producida por la tensión del déficit hídrico (Showler 2013).
Contrariamente, Gillman et al. (1999) no observaron diferencias en el número de huevos, ninfas y adultos de T. urticae en plantas de Buddleia davidii ‘Pink Delight’ estresadas o no estresadas. Por su parte, Gutbrodt et al. (2011) demostraron que el estrés hídrico podía provocar patrones opuestos en las preferencias de alimentación (palatabilidad de la planta) entre las especies herbívoras, puesto que Pieris brassicae mostró preferencia para consumir plantas con riego, mientras que Spodoptera littoralis prefirió plantas severamente afectadas por la sequía, aunque también se observó retraso en el desarrollo. Estos autores sostienen que el estrés hídrico puede causar disminución de la producción de compuestos secundarios relacionados con la defensa, lo cual puede provocar respuestas de alimentación contrastantes, posiblemente originadas por la especificidad de alimentación del herbívoro.
Por otra parte, plantas sometidas a condiciones de estrés acentuado pueden ser más susceptibles al ataque de plagas, incluso con niveles poblacionales relativamente bajos. Sin embargo, bajo estas condiciones los artrópodos no pueden alimentarse de este tipo de plantas debido a la poca disponibilidad de agua para la plaga (Mattson y Haack 1987, Showler 2012). Considerando que R. indica se alimenta a través de las aberturas estomáticas (Beard et al. 2012), probablemente, la aplicación del bajos volúmenes de agua (50 y 25% del requerimiento de la planta) pudo haber inducido un estrés suficientemente grande para provocar el cierre de estomas que consecuentemente imposibilitaron la alimentación del ácaro, lo cual debería ser abordado en estudios futuros. Sin embargo, debido a que en el efecto del déficit hídrico sobre las poblaciones de artrópodos herbívoros existen relaciones más complejas que pueden involucrar factores físicos, bioquímicos y ecológicos éste no puede ser considerado desde una óptica unifactorial (Showler 2013), por lo que los estudios deberían ser concebidos desde una óptica multifactorial de manera de encontrar explicación a este fenómemo.
CONCLUSIÓN
La disminución del volumen de agua mostró tener un efecto negativo sobre la oviposición y la densidad poblacional de R. indica en plantas de coco del cultivar Enano Amarillo Malayo. Sin embargo, es recomendable evaluar los cambios bioquímicos en la hoja de plantas de coco por efecto de la supresión del riego de modo de entender mejor cómo estos podría influir en la dinámica poblacional de R. indica.
REFERENCIAS BIBLIOGRÁFICAS
Beard, JJ; Ochoa, R; Bauchan, GR; Welbourn, WC; Pooley, C; Dowling, APG. 2012. External mouthpart morphology in the Tenuipalpidae (Tetranychoidea): Raoiella a case study. Exp Appl Acarol 57:227-255. [ Links ]
Carrillo, D; Amalin, D; Hosein, F; Roda, A; Duncan, RE; Peña, JE. 2012a. Host plant range of Raoiella indica (Acari: Tenuipalpidae) in areas of invasion of the New World. Exp Appl Acarol 57: 271-289. [ Links ]
Carrillo, D; Frank, JH; Rodrigues, JCV; Peña, JE. 2012b. A review of the natural enemies of the red palm mite, Raoiella indica (Acari: Tenuipalpidae). Exp Appl Acarol 57(3-4): 347-360. [ Links ]
Carrillo, D; Navia, D; Ferragut, F; Peña, JE. 2011. First report of Raoiella indica (Acari: Tenuipalpidae) in Colombia, Fl. Entomol 94(2): 370-371. [ Links ]
Carrillo, D; Peña, JE; Hoy, MA; Frank, JH. 2010. Development and reproduction of Amblyseius largoensis (Acari: Phytoseiidae) feeding on pollen, Raoiella indica (Acari: Tenuipalpidae), and other microarthropods inhabiting coconuts in Florida, USA. Exp Appl Acarol 52(2): 119-29. [ Links ]
Chandra, B; Channabasanna, G. 1984. Development and ecology of Raoiella indica Hirst (Acari: Tenuipalpidae) on coconut. In; Griffiths, DA; Bowman, CE, Editors. Acarology VI . Chicester, UK, Ellis Horwood Publishers, v 2. p. 7850-790. [ Links ]
Chaves, MM; Maroco, JP; Pereira, JS. 2003. Understanding plant responses to drought: from genes to the whole plant. Funct Plant Biol 30: 239-264. [ Links ]
Daane, KM; Williams, LE. 2003. Manipulating vineyard irrigation amounts to reduce insect pest damage. Ecol Appl 13: 1650-1666. [ Links ]
Daniel, M. 1981. Bionomics of the predaceous mite Amblyseius channabasavanni (Acari: Phytoseiidae), predaceous on the palm mite. Proceedings of the Ist Indian Symposium in Acarology 1981: 167-173. [ Links ]
Dorschner, KW; Johnson, RC; Eikenbary, RD; Ryan, JD. 1986. Insect-plant interactions: greenbug (Homoptera: Aphididae) disrupt acclimation of winter wheat to drought stress. Environ Entomol 15: 118-121. [ Links ]
English-Loeb, GM 1990. Plant drought stress and outbreaks of spider mites: a field test. Ecology 71: 1401-1411. [ Links ]
Etienne, J; Flechtmann, C. 2006. First record of Raoiella indica (Hirst, 1924) (Acari: Tenuipalpidae) in Guadalupe and Saint Martin, West Indies. Int J Acarol 32: 331-332. [ Links ]
Flechtmann, C; Etienne, J. 2004. The red palm mite, Raoiella indica Hirst, a threat to palms in the Americas (Acari: Prostigmata: Tenuipalpidae). Syst Appl Acarol 9: 109-110. [ Links ]
Flores-Galano, G; Montoya, A; Rodríguez, H. 2010. Biología de Raoiella indica Hirst (Acari: Tenuipalpidae) sobre Areca catechu L.Rev Protección Veg 25 (1): 11-16. [ Links ]
Gillman, JH; Rieger, MW; Dirr, MA; Braman, SK. 1999. Drought stress increases densities but not populations of two-spotted spider Mite on Buddleia davidii Pink Delight. Hortscience 34(2): 280-282. [ Links ]
Gutbrodt, B; Mody, K; Dorn, S. 2011. Drought changes plant chemistry and causes contrasting responses in lepidopteran herbivores. Oikos 120(11): 1732-1740. [ Links ]
Huberty, AF; Denno, RF. 2004. Plant water stress and its consequences for herbivorous insects: a new synthesis. Ecology 85: 1383-1398. [ Links ]
Klubertanz, TH; Pedigo, LP; Carlson, RE. 1990. Effects of plant moisture stress and rainfall on population dynamics of the twospotted spider mite (Acari: Tetranychidae). Environ Entomol 19: 1773-1779. [ Links ]
Mattson, WJ; Haack, RA. 1987. The role of drought in outbreaks of plant-eating insects. Bioscience 37: 110-118. [ Links ]
Mody, K; Eichenberger, D; Dorn S. 2009. Stress magnitude matters: different intensities of pulsed water stress produce non-monotonic resistance responses of host plants to insect herbivores. Ecol Entomol 34: 133-143. [ Links ]
Návia, D. 2008. Riesgo del ácaro rojo de la palma, Raoiella indica Hirst, para Brasil. In Acta del VI Seminario Científico Internacional de Sanidad Vegetal. La Habana, Cuba. 22-26 sep. [ Links ]
Návia, D; Marsaro Junior, AL; Silva da, FR; Gondim Jr, MGC; Moraes de, GJ. 2011. First report of the red palm mite, Raoiella indica Hirst (Acari: Tenuipalpidae), in Brazil. Neotrop Entomol 40(3): 409-411. [ Links ]
Peña, J; Mannion, C; Howard, F; Hoy, M. 2006. Raoiella indica (Prostigmata: Tenuipalpidae): the red palm mite a potential invasive pest of palms and bananas and other tropical crops in Florida. University of Florida IFAS Extension, ENY-837. [ Links ]
Popov, C; Trotus, E; Vasilescu, S; Barbulescu, A; Rasnoveanu, L. 2006. Drought effect on pest attack in field crops. Rom Agric Res 23: 43-52. [ Links ]
Rodrigues, J; Ochoa, R; Kane, E. 2007. First report of Raoiella indica Hirst (Acari: Tenuipalpidae) and its damage to coconut palms in Puerto Rico and Culebra Island. Int J Acarol 33(1): 3-5. [ Links ]
Rodrigues, JVC; Peña, JE. 2012. Chemical control of the red palm mite, Raoiella indica (Acari: Tenuipalpidae) in banana and coconut. Exp Appl Acarol 57(3-4): 317-29. [ Links ]
Showler, AT. 2012. Drought and arthropod pests of crops. In Neves, DF; Sanz, JD. eds. Drought: new eesearch, nova science. Hauppauge, New York, USA. p. 131-154. [ Links ]
Showler, AT. 2013. Water deficit stress-host plant nutrient accumulations and associations with phytophagous arthropods. In Vahdati, K; Leslie C. eds. Abiotic stress - plant responses and applications in agriculture. Intech Publisher. p. 387-410. [ Links ]
Vásquez, C; Colmenárez, Y; Moraes, GJ. 2015. Life cycle of Raoiella indica Hirst (Acari: Tenuipalpidae) on ornamental plants, mostly Arecaceae. Exp Appl Acarol 65(2): 227-235. Epub 2014 Oct 24. doi: 10.1007/s10493-014-9858-z. [ Links ]
Vásquez, C; Moraes de, GJ. 2013. Geographic distribution and host plants of Raoiella indica and associated mite species in northern Venezuela. Exp Appl Acarol 60 (1): 73-82. [ Links ]
Vásquez, C; Quirós, M; Aponte, O; Sandoval, M. 2008. First report of Raoiella indica Hirst (Acari: Tenuipalpidae) in South America. Neotrop. Entomol 37(6): 739-740. [ Links ]
Waring, GL; Cobb, NS. 1992. The impact of plant stress on herbivore population dynamics In Bernays, E, ed. Insect-plant interactions. CRC, Boca Raton, Florida. p. 167-226. [ Links ]
Zaher, M. 1969. Biological studies on Raoiella indica Hirst and Phyllotetranychus aegyptiacus Sayed infesting date palm trees in the UAR (Acarina: Tenuipalpidae). Z. Angew. Entomol 63(3): 406-411. [ Links ]













