INTRODUCCIÓN
Los parásitos de las aves siempre han sido de interés veterinario tanto sanitario como productivo, en principio en la producción de aves de corral y actualmente en las denominadas aves de compañía o de la clínica no convencional o silvestre12, donde los psitaciformes adquieren notoriedad, debido a que sus especies son apetecidas como mascota 5.
Los psitácidos son una familia de aves psitaciformes llamadas comúnmente loros o papagayos, que incluye a los guacamayos, las cotorras y formas afines distribuidos principalmente en América y muchas de ellas en grave peligro de extinción 5,7. Dicha familia se encuentra integrada por diversos géneros donde el Ara, Aratinga o Psittacara, Forpus y Amazona8 y sus híbridos 10,11,14,22, suelen ser los más habituales en los centros de fauna debido a que son animales usuales en el tráfico ilegal de fauna silvestre 21.
El hábito gregario de la mayoría de los psitácidos sumado a condiciones particulares de cautividad como la convivencia con otras especies, ambiente reducido, estrés, contaminación del alimento y el agua con materia fecal, inadecuadas medidas de desinfección, pisos de tierra, contacto con aves silvestres libres y mala calidad del agua, son condiciones ideales para la multiplicación y propagación parasitaria, fundamentalmente de ciclos de vida monoxenos 1,2,3,6. Considerando también, las de carácter zoonótico, ya se estima que el 75% de las enfermedades humanas emergentes tendrían conexión con animales silvestres 4.
En Argentina las investigaciones sobre parásitos en loros, son esporádicas y sujetas a eventuales hallazgos 12, reportando registros parciales de parásitos gastrointestinales, según aportes de diferentes aviarios del país. 15,17,19,21.
Por todo lo antes dicho, el objetivo del presente trabajo fue determinar la presencia de parásitos gastrointestinales en los género Amazona sp., Ara sp., Aratinga sp., Forpus sp., e híbridos de guacamayos en cautiverio originados del tráfico ilegal de fauna albergados en la Estación Biológica La Esmeralda, Santa Fe, Argentina.
MATERIALES Y MÉTODOS
El origen de los animales de nuestro estudio fue el tráfico ilegal de fauna. Los muestreos se realizaron en la Estación Biológica "La Esmeralda" de la Ciudad de Santa Fe y el procesamiento en el laboratorio de la Cátedra de Zoología, Diversidad y Ambiente de la Facultad de Ciencias Veterinarias de Esperanza de la Universidad Nacional del Litoral ambas Instituciones de Argentina, en el mes de agosto de 2019.
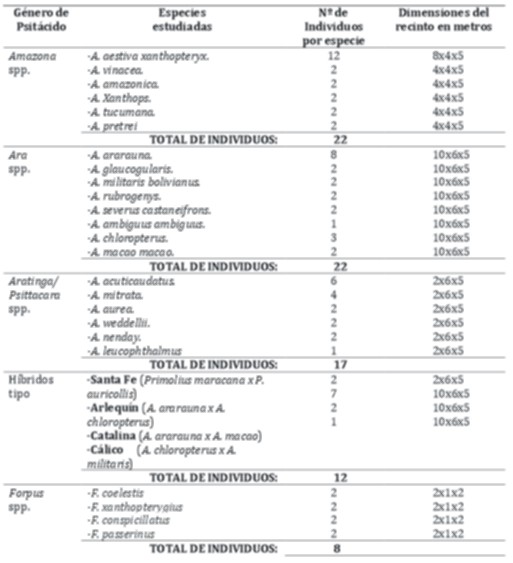
Se tomaron muestras de materia fecal de 81 individuos de 28 especies de psitácidos (Tabla 1).
Tabla 1. Representación de los géneros, especies/tipo, número de individuos de psitácidos por especie y dimensiones de los recintos/habitáculos que los albergaron durante el estudio.
Las muestras fueron recolectadas mediante lonas de polietileno colocadas en el piso y en las plataformas de alimentación de cada habitáculo (28 recintos en total), las cuales fueron retirados al cabo de 6 horas. Repitiéndose la toma de muestras 3 veces con un intervalo de una semana entre cada una. Se identificaron debidamente y se transportaron refrigeradas en bolsas de polietileno. Fueron procesadas empleándose la técnica combinada de flotación y sedimentación de Teuscher (sedimentación- flotación con SO4Zn) y observadas al microscopio óptico (para la identificación, conteo y medición); la esporulación de los ooquistes encontrados se realizó con flotación Willis y posteriormente se evidenciaron al microscopio, según Martínez Tovar et al. 13,16.
Las medidas obtenidas para cada género parasitario observado al microscopio, se promediaron con el fin de obtener valores como rango y prevalencia de cada género en este muestreo.
RESULTADOS Y DISCUSIÓN
Los resultados obtenidos para cada grupo taxonómico fueron los siguientes:
Amazona sp.:
Todas las muestras estaban parasitadas, se encontró: Capillaria sp. en las 6 especies, (promedio de medidas de 54,518 µ de largo por 28,346 µ de ancho), constituyeron el 18,99% de las muestras; Trichostrongylus sp. (largo de 65,352 µ por 33,626 µ de ancho) en el 11,39% de la muestra y Strongyloides sp. (largo de 55,995µ y un ancho de 32,891µ, en un 32,92% de la muestra. Los ooquistes de coccidios no esporulados, mediante previa incubación en estufa a 27° y a la técnica de flotación de Willis, pertenecieron a Isospora sp. (tamaño de 21,65 µ de largo y 19,96µ de ancho). Se detectó la presencia de Ascaridia sp. en Amazona tucumana, representando el 4,16% del total de las muestras (tamaño de 62,65µ de longitud y un ancho de 43,25µ) (Figura 1).
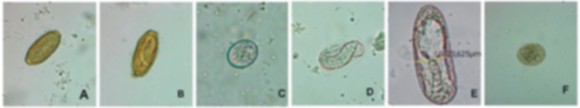
Figura 1. Huevos hallados en Amazona sp., donde: A. Capillaria sp., B. Capillaria sp. larvado, C. Ooquiste, D. Strongyloides sp., E. Trichostrongylus sp., F. Isospora sp.
En nuestro estudio, la presencia de huevos de Capillaria sp. (18,99%), mostró una prevalencia menor en comparación con el 29,2% y 87% reportado por Freytas et al (2002) 7 en Pernambuco, Brasil y los 58% resultante de las investigaciones de Santa Cruz Burbano et al. 1818 en Colombia. Con respecto a los coccidios, nuestro estudio arrojó un valor de 36,70% indicando un aumento en la prevalencia con respecto a la de 3,1% en Pernambuco7 y 6% en Colombia18; pero nuestra prevalencia fue menor a lo hallado por al en Venezuela cuya prevalencia fue del 93%. Para los casos de Strongyloides sp. y Trichostrongylus sp. (23,6% de presencia en las muestras analizadas en nuestro estudio) los mismos no fueron reportados por otros autores para psitácidos de éste grupo taxonómico.
Ara sp.:
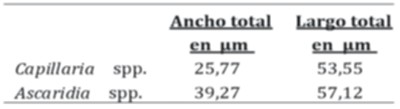
El 100% de la población estaba parasitada, siendo Capillaria sp. la de mayor prevalencia (89,01%), seguido por Ascaridia sp. (10,99%). A partir de la segunda muestra analizada de éste grupo de aves, se detectó solo Capillaria sp. El promedio de medidas, tomadas en 400 aumentos totales, fueron expresadas en micras (µm) y expuestas en la Tabla 2.
Tabla 2. Medidas promedio expresadas en micras (µm) a 400 aumentos totales para Capillaria spp. y Ascaridia spp. halladas en muestras de materia fecal de Ara sp.
Para mejor visualización del número de huevos de Ascaridia spp. y Capillaria spp. hallados en cada especie de Ara sp. muestreada, se confeccionó la Figura 2.
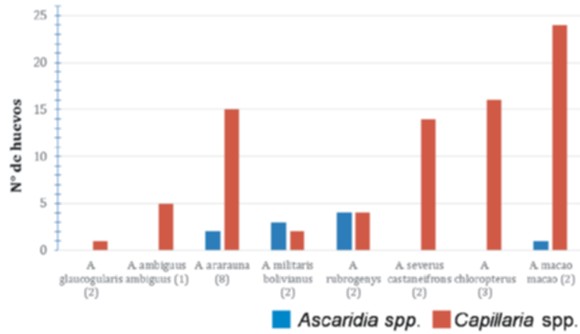
Figura 2. Número de huevos de Ascaridia spp. y Capillaria spp. encontrados en cada especie de Ara sp.
El elevado porcentaje de Capillaria sp. hallado en nuestro estudio (89,01%) tuvo una prevalencias mayor a la reportada por Sciabarrasi y Gervasoni en 200919 (22%) para la misma locación ("La Esmeralda") de Argentina; siendo de prevalencia mayor a la reportada por Freytas et al. (2002) 7 en Brasil (29,2% y 87%) y el 58% obtenido por estudios de similar metodología en el Zoológica de Cali, Colombia 3. A su vez la prevalencia de Ascaridia sp. (10,99%) fue menor a la reportada por la Fundación Zoológica de Cali (13%) 18.
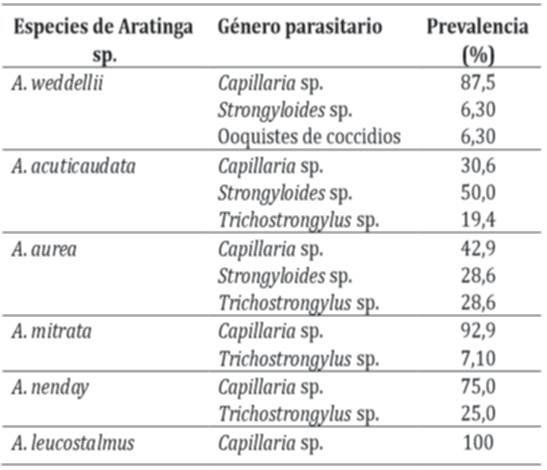
Aratinga/Psittacara sp.:
Las especies de loros de éste género dieron resultados positivos a la presencia de nematodos. Capillaria sp. fue encontrado en todas las muestras (medidas promedio de 55,44 µm de longitud por 27.98 µm de ancho), represento un 66,4% del total de parásitos encontrados. En A. weddellii, A. acuticaudatus y A. aurea se encontró Strongyloides sp (medidas promedio: 59,64 µm por 36,32 µm), representando el 20 % de los hallazgos. Trichostrongylus sp. fue el menos encontrado (medidas promedio de 64,33 µm por 33,25 µm) con una ocurrencia del 12,8% solo para las especies A. acuticaudatus, A. aurea, A. mitrata y A. nenday. Un ooquiste fue encontrado (largo 8,92 µm y un ancho de 6,78µm) solo en A. weddellii, significando el 0.8% del total. La totalidad de géneros parasitarios encontrados por grupo de aves así como la proporción que representa cada uno en el total se pueden observar en la Tabla 3.
El análisis individual de los géneros parasitarios hallados en las especies de Aratinga spp reportadas en nuestro estudio manifiestan que la prevalencia más elevada corresponde a Capillaria sp. Estudios parasitológicos realizados en loros describen a Capillaria como el parásito más comunes de los psitácidos 18. Una prevalencia de Capillaria sp. del 22% fue hallada en un estudio similar, realizado en la misma estación experimental, pero en este caso, no reportada para el género Aratinga sp19,20, nuestro trabajo reporta la presencia y predominancia de dicho género representada por un 66,4% sobre el total de géneros parasitarios encontrados. Solo se halló un ooquiste no esporulado en el total de las muestras, sin poder determinar el género al que pertenece este protozoario, a diferencia de lo encontrado por Sciabarrasi y Gervasoni 19 que pudieron evidenciar la presencia de coccidios del género Isospora sp. Quizá esto requiere de estudios posteriores donde la aparición de este parásito sea mayor.
Guacamayos Híbridos:
Todas las muestras analizadas en éste grupo, resultaron parasitadas (Figura 3), en las cuales se encontraron: Capillaria sp. (68,4% de las muestras) en tres de los cuatro tipos de híbridos; en los Santa Fe (largo entre 49,98 y 60 µ, por un ancho de 24,99 a 30 µ), Catalina (largo de 52,5 a 82,11µ y un ancho de 21,42 a 30 µ) y en Arlequín (medidas de longitud de 42,89 a 57,12 µ y de un ancho de 21,42 a 26,77 µ). Otros nematodos, representaron el 23,6% de las muestras, de los cuales se destacan Trichostrongylus sp. (largo de 53,55 a 82,11 µ y un ancho de 28,56 a 32,3 µ) y Strongyloides sp. (largo de 42,84 a 53,55 µ y un ancho de 39,27 µ) en el híbrido Cálico; también se detectaron en el fenotipo Arlequín la presencia de Trichostrongylus sp. (tamaño de 76,75 a 78,54 µde largo por un ancho de 35,7 a 42,84µ) y Strongyloides sp. (tamaño de 49,98 µ de largo por 32,13 µ de ancho. Se hallaron ooquistes del género Isospora (tamaño 20,17 a 22,97 µ de largo y 18,25 a 21,83 µ de ancho), solamente en Catalina (2,6% de las muestras). Se detectó la presencia de Ascaridia sp. en los análisis del híbrido Cálico, representando un total del 5,4% de las muestras, (tamaño de 64,26 µ de longitud y un ancho de 35,7 a 48,84 µ)(Figura 3).
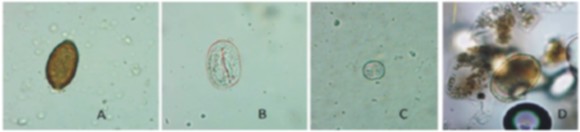
Figura 3. Huevos de parásitos hallados en los híbrido de guacamayos estudiados, donde A. Capillaria sp., B. Strongyloides, sp. C. Isospora sp., D. Ascaridia sp.
Los datos obtenidos del laboratorio permitieron comprobar la existencia de diferentes tipos de parásitos en todos los individuos de híbridos. En nuestros estudios la presencia de Capillaria fue elevada (68,4%) en comparación a lo reportado por Sciabarrasi y Gervasoni (22,2%) (19) en igual sitio de muestreo y por Figueiroa et al.7 en un estudio (29,2%) en Pernambuco para otros guacamayos no híbridos. La prevalencia de Ascaridia spp (5,4%) fue menor comparadas con un 13% obtenidos en los estudios en Colombia de Santa Cruz Burbano etal. 18 y los 66% encontrados por Martínez Tovar 16 en un híbrido Catalina (A. ararauna x A .macao) en El Salvador. Siendo también baja la presencia de coccidios (2,6 %), en Pernambuco 3,1 %7 y 6 % en Colombia18. Figueiroa et al.7 no reporta casos de Strongyloides sp. ni Trichostrongylus sp. en psitácidos, mientras que en nuestro estudio y para el género Aratinga sp. dichos parásitos se encontraron en un 23,6% de las muestras analizadas.
Forpus sp.:
Las cuatro especies de Forpus se encontraron parasitadas. En Forpus coelestis se hallaron 17 huevos de cestodes (tamaño promedio: 50,912 por 49,33 µ) compatibles con Raelletina sp.; 4 Ooquistes Eimeria sp. (tamaño promedio: 25,48 por 23,32 µ); 4 ooquistes de Isospora sp. (tamaño promedio: 24,41 µ por 25,55 µ) y 26 ooquistes sin esporular (medida promedio: 24,44 µ por 23,37 µ.
Para el caso de Forpus conspicillatus los parásitos encontrados fueron Railletina sp. (1 huevo de tamaño promedio: 51,01 por 50,25 µ); 26 ooquistes Isospora sp. (medición promedio: 24,06 x 25,71 µ); 56 ooquistes sin esporular (medición promedio: 23,85 por 23,57 µ); Strongyloides sp. (1 huevo) y Trichostrongylus sp. (1 huevo)
Los resultados para Forpus xanthopterygius fueron 387 ooquistes Isospora sp. (medición promedio: 22,18 por 22,20 µ); 830 ooquistes sin esporular (tamaño promedio: 25,055 por 25,31 µ); de Trichostrongylus sp. (4 huevos) y de Strongyloides sp. (1 huevo).
En Forpus passerinus los parásitos hallados fueron solamente coccidios: 62 ooquistes de Isospora sp. (medición promedio: 22,8 por 21,94 µ ) y 110 ooquistes sin esporular (tamaño promedio de 22,07 x 21,02 µ).
Globokar et al. (2017) 9 reportó en un estudio en Berlín sobre Forpus spp. una prevalencia del 80,6% para Capillaria sp., nematodo no hallado en nuestros estudios para éste género de psitácido. Sin embargo para el caso de los cestodos, Sciabarrasi et al. 19 en F. xanthopterygius obtuvieron huevos de cestodes (de 53,9 a 57,7 por 42 μ) aislados o en cápsulas ovígeras sin llegar a identificar el género de los mismos.
En nuestro estudio los cestodos hallados fueron compatibles con Raelletina sp, resaltando el primer reporte de Trichostrongylus sp. y Strongyloides sp. para éstas especies de Forpus sp. estudiadas.
En líneas generales y luego de todos los resultados expuestos, concordamos con Costa et al. 6 en que los elevados porcentajes obtenidos de muestras positivas a parasitosis son frecuentes en psitaciformes en cautiverio que se mantienen en ambientes contaminados.
CONCLUSIONES
Con los resultados obtenidos podemos concluir que:
·Existe una alta frecuencia parasitaria en los psitácidos rescatados del tráfico ilegal y que en éste caso, son albergados en la Estación de Fauna La Esmeralda.
·Al reportarse parásitos de ciclos de vida monoxenos como Ascaridia spp, Capillaria spp e Isospora spp, podemos inferir que, las condiciones habitacionales y el manejo de las aves de este estudio no eran las adecuadas.
·La prevalencia de protozoos y nematodos se consideran altas, siendo este un problema de importancia médica y económica que debe ser objeto de mayor atención para su prevención y control.
·Se observó la presencia de Raillietina spp, parásito potencialmente zoonótico, lo que conlleva a que las personas que estén en permanente contacto con las aves están en riesgo de infección por dicha entidad parasitaria.
·Dicho trabajo representa el primer reporte en Argentina de parásitos en guacamayos híbridos, Forpus coelestis, F. conspicillatus y F. passerinus.
·El análisis parasitológico en estas especies constituye una herramienta importante para la evaluación de las condiciones sanitarias del ambiente. A pesar de la limitación de las investigaciones en este campo por la dificultad para acceder a los hospedadores, el conocimiento sobre las enfermedades y sus implicaciones es de fundamental importancia para los programa de manejo y conservación de la biodiversidad.
AGRADECIMIENTOS:
Agradecemos al personal de Estación Biológica La Esmeralda (Santa Fe, Argentina) y a la Cátedra de Parasitología de la Facultad de Ciencias Veterinarias de la Universidad Nacional del Litoral (FCV-UNL, Argentina) por la orientación y asistencia durante los estudios.
Declaración de divulgación:
Los autores no informaron ningún conflicto de interés potencial.