INTRODUCCIÓN
La tuberculosis es una enfermedad trasmisible de distribución mundial, con elevada morbimortalidad constituyendo una de las 10 principales causas de muerte. Más del 95% de las muertes se producen en países con ingresos bajos y medianos como en India, Indonesia, China, Filipinas, el Pakistán, Nigeria y Sudáfrica, con el 64% de la mortalidad total. Se considera que un tercio de la población mundial está infectada con nuevos casos preferentemente en niños y adolescentes1. La Organización Mundial de la Salud, en el 2016 reportó 10,4 millones de personas enfermas de tuberculosis, un millón en niños y de los 1,7 millones de muertes, 250.000 fueron niños y 40% en personas VIH-positivas. La tuberculosis multirresistente constituye una crisis de salud pública porque amenaza la seguridad sanitaria con 600.000 nuevos casos de resistencia a la rifampicina, que es la medicación de elección.
Esta enfermedad transmisible causada por organismos del complejo Mycobacterium tuberculosis es adquirida por gotitas de pacientes con infección activa que constituyen solo 10%. En el 90 a 95% de los casos persiste la infección latente (LTBI), que es asintomática no transmisible pero puede desarrollar tuberculosis en meses o años en el 10% de la población general y en 15-43% de los niños2. En éstos es una causa importante de morbilidad y mortalidad, así como en pacientes inmunosuprimidos. LTBI es el síndrome clínico causado por la exposición al M. tuberculosis seguida de infección, evidenciada por la presencia de prueba cutánea positiva de tuberculina (PPD) en ausencia de signos y síntomas clínicos y radiológicos de la enfermedad activa 3,4. El diagnóstico de la LTBI requiere por ende los datos epidemiológicos, la historia personal o familiar, el examen físico y los estudios de laboratorio, ya que se estima que una cuarta parte de la población mundial tiene tuberculosis latente.
La prueba de la tuberculina ha sido utilizada durante mucho tiempo como apoyo en el diagnóstico de tuberculosis latente o activa, pero su limitada en sensibilidad dirigio las investigaciones hacia métodos más sensibles, planteandosis el diagnostico de tuberculosis latente mediante la detección in vitro de liberación de interferón gamma (IGRA) o Quantiferon TB Gold®In tube en sangre, con 70 a 80% de sensibilidad y 79 a 96% de especificidad3. Esta prueba mide producción de IFN ɤ producido por linfocitos T, en contacto con antígenos peptídicos que simulan ser proteínas bacterianas: ESAT-6, CFP10, TB7.7. Estos antígenos están ausentes en la BCG y micobacterias no tuberculosas, por lo que en pruebas positivas se debe considerar el M. kansaii, M. szulgai y M. marinu, a fin de diferenciar entre infección por M. tuberculosis con PPD positivo por inmunización o por las otras micobacterias5. Diagnosticar la LTBI permite instaurar el tratamiento preventivo para tuberculosis además sirve como complemento en enfermedades reumatológicas, inmunocomprometidos, en regímenes de trasplante de órgano sólido, contactos familiares y personal de salud con pacientes bacilíferos.
En el Paraguay, el Programa Nacional de Tuberculosis notificó en el 2015 un total de 2.069 casos nuevos de infección activa y 389 retratados, en población general, con una incidencia de 30.5/100.000 hab. De entre ellos, 253 (10,3%) fueron casos de tuberculosis todas las formas en niños/as, 357 (14,5%) en población indígena, 280 (11,4%) en personas privadas de libertad y 181 (7,4%) fueron por co-infección tuberculosis/VIH, similar a lo observado en varios países de la región aunque sin datos de la proporción de la infección latente (6,7. En los Departamentos Central, Alto Paraná y Asunción se concentra el 60% de la carga de enfermedad del país por lo que se intensifica la detección de casos así como en Presidente Hayes en comunidades indígenas8.
El presente trabajo se realizó con el objetivo de determinar la prevalencia de tuberculosis latente n la utilización del IGRA en pacientes con factores de riesgo o exposición.
MATERIALES Y MÉTODOS
Diseño: estudio retrospectivo de corte transversal realizado del 2014 al 2017.
Población: pacientes con sospecha de tuberculosis latente, de cualquier edad o sexo, incluidos en forma consecutiva. Las muestras sanguíneas y fichas epidemiologicas provinieron de hospitales de referencia del área urbana.
Metodología: luego del llenado de datos clínicos y demográficos en los centros de referencia, las muestras de sangre de los mismos se remitieron a un laboratorio especializado en la técnica laboratorial. Para la determinación del IGRA se tomaron muestras de sangre con heparina de litio a los pacientes. El estudio se realizó mediante el reactivo comercial, Quantiferon TB Gold® In Tube (Cellestis, Australia), de acuerdo las instrucciones del fabricante: con 3 tubos heparinizados especiales conteniendo el mitógeno o control positivo, antígenos peptídicos de tuberculosis (ESAT-6, CFP-10, TB 7,7) y un control negativo o NIL. Estos tubos con la sangre heparinizada se agitaron e inmediatamente incubaron por 24 horas a 37 °C, posteriormente previa centrifugación se recolecto el plasma y conservó a -20 °C hasta su procesamiento. La determinación de la concentración del Interferón gamma se realizó por el método de ELISA, la lectura e interpretación de las absorbancias obtenidas por medio del software QFT v2.62. Los resultados se informaron como positivos, negativos e indeterminados y expresados en UI/mL.
Para el análisis de estos datos se utilizó la estadística descriptiva. Para la interpretación de las variables, se transcribieron a una planilla electrónica en el formato Microsoft Excel 2010, analizados mediante el programa estadístico Epi Info.7®, se expresaron en tablas a manera de frecuencias absolutas y relativas.
Consideraciones éticas: se tuvieron en cuenta las consideraciones éticas dispuestas para los estudios a partir de muestras clínicas que se analizan con fines diagnósticos, donde se respetó la confidencialidad de los datos de los pacientes. Además, se respetaron los principios de beneficencia y justicia, puesto que no se realizó ninguna intervención y tampoco implico ningún riesgo para los pacientes.
RESULTADOS
Se analizaron los resultados del IGRA de 261 muestras de sangre de pacientes de entre 3 a 86 años, con una media de 47 años, mediana 49 años y moda 54 años. Los hombres fueron 126 y las mujeres 105. La mayoría eran procedentes de los servicios privados y tenían antecedentes de enfermedad pulmonar.
De este total de 261 muestras resultaron positivas para tuberculosis latente 38 (15%) y 10(4%) fueron indeterminados. Al excluir los registros sin datos sobre condiciones de la indicación, quedaron 147 con datos válidos, 37,4% (55) con antecedentes clínicos o sospecha de enfermedad tuberculosa como presencia de fiebre y/o tos, o un nódulo o linfoadenopatía. Hubo predominio de varones y sujetos del riesgo etario de 51 - 60 años. (Tabla 1).
Tabla 1 Características generales de la muestra sometida a detección in vitro de liberación de interferón gamma para M. tuberculosis
| Edad | Menores a 10 10 a 20 21 a 30 31 a 40 41 a 50 51 a 60 61 a 70 71 a 80 81 a 90 Sin datos | 13 (4,9%) 15 (5,7%) 33 (12,6%) 32 (12,2%) 34 (13%) 47 (18%) 30 (11,4%) 30 (11,4%) 8 (3%) 19 (7,3%) |
| Sexo | Femenino Masculino Sin datos | 105 (40,2%) 126 (48,3%) 30 (11,4%) |
| Procedencia | Instituto Previsión Social Salud Pública Servicios privados | 56 (21,5%) 35 (13,4%) 170 (65%) |
| Cuadro clínico | Pulmonar Trasplante Mieloproliferativo Autoinmune HIV Contacto con tuberculosis Inmunosupresión Infeccioso Sin datos | 75 (28,7%) 32 (12,3%) 20 (7,6%) 15 (5,7%) 11 (4,2%) 5 (1,9%) 4 (1,5%) 3 (1,1%) 96 (36,7%) |
De entre las 38 muestras positivas por el IGRA, el 18% (19/105) correspondió a mujeres y el 11% (14/126) a hombres. En cuanto al grupo etario con más casos positivos fue el de 81 a 90 años (37%) (Gráfico 1).
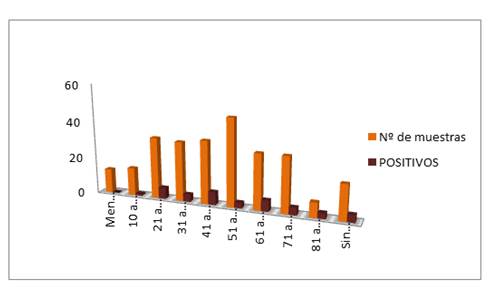
Gráfico 1 Distribución etaria de tuberculosis latente obtenida por detección in vitro de liberación de interferón gamma (n 261)
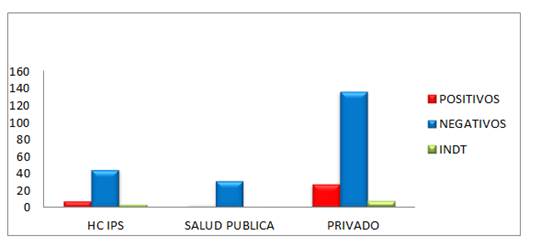
La procedencia mostró que el 16% fue de Servicios privados, 14% de Instituto Previsión Social y 9% del Ministerio de salud (Gráfico 2).
En cuanto a las presentaciones más frecuentes, el cuadro pulmonar fue el principal con un 24%, seguido de enfermedades autoinmunes del 20% así como en contacto con pacientes baciliferos (Tabla 2).
Tabla 2 Presentación clínica de pacientes con tuberculosis latente (n 147)
| Afectación clínica | Total (n 147) | Positivo (n 27) | Indeterminado (n 8) |
|---|---|---|---|
| Pulmonar | 68 | 18 (26%) | 4 (6%) |
| Mieloproliferativo | 13 | 3 (23%) | 0 |
| HIV | 11 | 0 | 1 (9%) |
| Trasplante | 32 | 2 (6%) | 1 (3%) |
| Autoinmune | 15 | 3 (20%) | 1 (7%) |
| Infeccioso | 2 | 0 | 1 (50%) |
| Inmunosupresión | 1 | 0 | 0 |
| Contacto con tuberculosis | 5 | 1 (20%) | 0 |
DISCUSIÓN
Se confirmaron los primeros 38 casos (15%) de LTBI en el país mediante el IGRA, que en su mayoría fueron adultos de 81 a 90 años y en 18% de mujeres. El 37,4% de estos casos fueron compatibles con infección activa por M. tuberculosis en base a los antecedentes clínicos recopilados, ya que ante un resultado del IGRA positivo o negativo (Quantiferon®TB) debe combinarse con la epidemiologia, clínica y otros datos a fin de confirmar o excluir la enfermedad tuberculosa12. Así, 26% presentó un cuadro pulmonar y 20% contacto con pacientes bacilíferos, por lo que podemos considerar que hubo sobre-indicación del IGRA, ya que, con la baciloscopía, el cultivo o biología molecular se podría haber logrado la confirmación necesaria.
El porcentaje de tuberculosis latente fue aumentado con las edades, de un 20% entre personas de 61 a 70 años y 37% entre 81 a 90 años, similar a la casuística de Chile en personal de salud con un 83% entre 60 a 69 años6.
El IGRA que confirma el diagnóstico de infección latente, tiene una sensibilidad de 84% y 93% de especificidad con respecto a la PPD en inmunocompetentes y en niños >5 años3,12, lo que explicaría ningún caso positivo en nuestro reducido número de niños. Además, detectó un 23% en pacientes con procesos mieloproliferativos.
Esta casuística que mostró 20% de LTBI en personas con contacto familiar con pacientes bacilíferos, fue superior al 8,35% de Alemania en trabajadores de la Salud, donde el mayor número de casos fue entre el personal de Enfermería, Medicina Interna, Radiología y Laboratorio de Microbiología y Patología11,17,18.
En Chile de los 26,3% casos de LTBI en trabajadores de la salud, la mayoría fue en personal del Programa de tuberculosis, 40% de los encargados de la baciloscopía y los cultivos, 42% en enfermeros que ayudan en el esputo inducido6.
En nuestro estudio ninguno de los 11 pacientes portadores de HIV resultó con LTBI, probablemente por los recuentos menores a 200 de CD4, diferente al observado en 6% de Brasil13,14,15) pero menor al 52% de Irán en personas en situación de calle19, con mejores resultados que con la prueba cutánea a tuberculina.
En los trasplantados del estudio, el IGRA resulto positivo en 6% mucho menor al 32,5% entre los trasplantados de riñón en China, donde solamente uno desarrolló la enfermedad, aunque su porcentaje global de LTBI fue del 46%9,17.
El 16% detectado en pacientes provenientes de los servicios privados sugieren mayor vigilancia en esta población a fin de cortar la transmisión, mediante el tratamiento e identificación la fuente de contagio, porque es imposible correlacionar la concentración del IFN ɤ con el grado de infección y progresión a enfermedad activa11,16. En Polonia, el mejor factor predictivo de progresión a tuberculosis activa en el 36,7% de personas sin hogar y 27,2% de contacto cercano fue la detección simultánea de un IGRA positiva junto con una prueba cutánea a la tuberculina positiva10.
Entre las limitaciones del IGRA en otras casuísticas se han mencionado resultados falsos negativos en casos de anergia en los estados avanzados, desnutrición, recuento bajo de los linfocitos CD4 o en el laboratorio por demoras en los procesos, temperatura, volúmenes inadecuados o un periodo corto entre exposición al bacilo y la realización de la prueba. En cambio, los falsos positivos se observaron por el efecto booster de los antígenos ESAT-6 y CFP-10. En nuestra casuística fue la detección de 8 (5%) de resultados indeterminados2,19) que se hubieran definido con una segunda determinación, para confirmar conversión o variación del resultado obtenido. Este dato podría relacionarse a lo observado en Perú donde se sugiere una activación inmune en curso en LTBI, aumentando también la posibilidad de detección21.
Los IGRAs se relacionan mejor que PPD con el grado de exposición al bacilo, por lo que serían más indicativos de existencia de TB latente que la prueba cutánea, sin embargo no son marcadores del pronóstico de la enfermedad.
CONCLUSIÓN
Con esta metodología (IGRA) se pudo detectar casos de tuberculosis latente, en los principales grupos de riesgo pero en un solo caso se observó discordancia entre el IGRA y la PPD, en su mayoría hubo correlación20 por lo que convendría seguir ampliando este estudio, a fin de definir su aplicación y limitación, porque con el tratamiento oportuno de los casos detectados se podría disminuir la elevada prevalencia de tuberculosis en nuestro país.