INTRODUCCIÓN
Las reacciones adversas a medicamentos figuran entre las diez causas principales de morbilidad y mortalidad en todo el mundo. Los niños constituyen una población especialmente susceptible, debido a las diferencias farmacocinéticas que se observan en las distintas etapas del crecimiento y desarrollo, los niveles plasmáticos del fármaco alcanzados en diferentes patologías y la inmadurez fisiológica, especialmente en los neonatos1.
Desde 1957 es utilizada la anfotericina B como droga antifúngica y hasta hoy día continúa jugando un papel importante en el tratamiento de las infecciones fúngicas sistémicas. Es un antibiótico natural del grupo polieno, aislado en 1955 de una cepa de actinomiceto Streptomyces nodosus. Tanto la eficacia farmacológica como los efectos secundarios tóxicos dependen de la organización molecular del fármaco 2-4.
La membrana plasmática desempeña una importante función en la división celular y el metabolismo. Las partículas lipídicas llamadas esteroles constituyen aproximadamente 25% de la membrana celular fúngica. En las células de los mamíferos predomina el colesterol y en las células fúngicas el ergosterol. Los polienos inhiben la síntesis del ergosterol, o se fijan al mismo modificando la permeabilidad de la membrana plasmática,ocasionando la pérdida de moléculas intracelulares, esto impide la viabilidad del hongo. También ejerce efectos sobre la oxidación celular que incrementan su actividad antifúngica (5,6.
La anfotericina B in vitro es fungicida; no obstante, su actividad in vivo semeja más un efecto fungistático. Su larga vida media permite la dosificación cada 24 horas. Varios estudios han mostrado que al administrarla en forma continua aumentan su eficacia y seguridad 7. En cuanto a su espectro de acción, es especialmente activa frente Aspergillus spp., Candida spp., entre muchos otros 5,8.
La absorción oral es mínima o casi nula (5%), por lo que la vía de administración de elección es la vía intravenosa. Se unen ampliamente a lipoproteínas del plasma (90-95%). Alcanza altas concentraciones en hígado, bazo, pulmón y riñones. En líquido pleural, peritoneal, sinovial y humor acuoso las concentraciones alcanzadas del fármaco son 50-60% de la concentración plasmática mínima. Penetra mal en líquido cefalorraquídeo (2-4%) aumentando en casos de inflamación meníngea. Atraviesa bien la placenta. No se disponen de ensayos clínicos que determinen la eliminación por leche humana ni la seguridad de su utilización en embarazadas 9.
Los polienos tienen pocas interacciones con otros fármacos, pero son poco seguros, ya que pueden dar lugar a nefrotoxicidad irreversible, hipokalemia grave y otros eventos clínicos adversos de gravedad moderada a elevada que tienden a relacionarse directamente con la velocidad de la infusión 7.
La administración de anfotericina B desoxicolato se puede asociar a efectos adversos inmediatos, tales como fiebre, escalofríos, vómitos, cefalea, choque anafiláctico, arritmias y falla hepática. Pero existen también reacciones adversas que se presentan después de administraciones repetidas, incluyendo entre estas últimas la hipokalemia, la hipomagnesemia y la toxicidad medular. Sin embargo, la toxicidad más preocupante y en la cual se han centrado la mayoría de los estudios es la nefrotoxicidad 10-12.La nefrotoxicidad es el principal inconveniente de la anfotericina B y se atribuye a la utilización de desoxicolato sódico y fosfato sódico como excipientes.
En el desarrollo de la toxicidad renal la filtración glomerular decae en aproximadamente 40% en las primeras dos semanas de tratamiento y luego se estabiliza a 20 a 60% del valor normal hasta el fin del tratamiento, constituyendo un cambio reversible en la mayor parte de los pacientes 13.
Dos estrategias se han delineado para controlar los efectos adversos asociados al uso de anfotericina B desoxicolato. Por una parte, modificaciones en la forma de administración de la misma, lo que incluye precargas salinas (ya que el aporte de cloruro de sodio ha sido descripto como protector de la función renal en prematuros 14) y administración del medicamento en 24 horas en lugar de las 4 horas convencionales, disminuyen en gran medida la aparición de efectos adversos. La otra alternativa es el reemplazo por formulaciones asociadas a lípidos (8, 15).
Las formulaciones de anfotericina B asociadas a lípidos han intentado mejorar la solubilidad de las moléculas apolares de anfotericina B convencional, originalmente dispersas en desoxicolato, por moléculas lipídicas con cabezas polares. Diferentes estudios demuestran que las formulaciones asociadas a lípidos presentan una eficacia clínica similar a anfotericina B desoxicolato y se demostró que este último se asocia significativamente a una mayor frecuencia de efectos adversos en comparación a la presentación liposomal 15.
Entre las reacciones adversas más conocidas se encuentran la presencia de fiebre, náuseas, vómitos, tromboflebitis, mialgias, manifestaciones de nefrotoxicidad con presencia de proteinuria, cilindruria, acidosis tubular renal e hipokalemia. Asimismo, después de periodos prolongados de administración puede aparecer anemia, depresión de la serie blanca y megacariocítica 17. También es posible la aparición de efectos neurotóxicos.
Entre los puntos a considerar para la aparición de reacciones adversas medicamentosas por anfotericina B se encuentran, en primer lugar, la posología empleada. Es común observar que en algunas instituciones aún se emplea la anfotericina B a dosis estándar de 1 mg/Kg/día sin tomar en cuenta factores como tipo de micosis, epidemiología hospitalaria, tipificación del agente causal, sensibilidad antimicótica, edad del paciente, forma clínica, tiempo de evolución y estado general del paciente. El empleo de una posología estándar de anfotericina B, cuando es posible emplearla a dosis terapéuticas más bajas, posibilita una dosis total acumulada elevada de manera temprana y, por consiguiente, la aparición temprana de reacciones adversas 16.
La aparición de reacciones adversas también se pueden observar en los casos que se decide prolongar el tratamiento o incrementar la dosis de anfotericina B debido a la mala respuesta en pacientes con cepas previamente tipificadas como sensibles y el posterior aislamiento de una cepa resistente a anfotericina B.
Se ha descripto que la farmacocinética en Pediatría difiere de la de los adultos y a algunos de estos aspectos se le han atribuido las diferencias en la nefrotoxicidad observadas entre ambos grupos 18. En la edad pediátrica se han descripto vidas medias que oscilan entre 10-18 h, habiéndose observado vidas medias más largas en pacientes prematuros extremos 19. Pareciera ser que en los prematuros extremos, la anfotericina tiene una vida media más larga y menor depuración, comparado con los lactantes y niños mayores. Esto podría deberse al grado de maduración de los órganos encargados del metabolismo del fármaco, por lo que los pacientes prematuros extremos podrían necesitar intervalos más largos entre dosis, y los recién nacidos de termino necesitan recibir con más frecuencia anfotericina B al igual que los lactantes 20.
La nefrotoxicidad es el efecto adverso más relevante, por estar asociada con mayor morbimortalidad, requerimiento de hemodiálisis, prolongación de la estadía hospitalaria y mayores costos 21.Algunos autores han descripto que el medicamento en los pacientes pediátricos tiene menor toxicidad renal que en los adultos, diferenciándose en cuanto a la gravedad y la incidencia, como el de Starke que describió que la nefrotoxicidad fue leve, transitoria y sin significación clínica 22. Baley observó variaciones significativas en la función renal, pero las describió como leves, y que mejoraron al concluir el tratamiento 21. Koren encontró diferencia estadísticamente significativa en las creatininemias pre tratamiento y durante el tratamiento 23. Sandler informó nefrotoxicidad en 52% 24 en tanto que Lee observó nefrotoxicidad en 16% de neonatos que se resolvió en el 99% de los casos 25.
Según Safdar, la creatininemia puede subestimar el filtrado glomerular y que no hay estudios a largo plazo sobre la evolución del compromiso renal. La nefrotoxicidad ha sido definida como un aumento de la creatininemia de 0,4 mg/dL durante el tratamiento con la anfotericina B; o si la misma se duplica y es mayor a 1,2 mg/dL, o sufre un aumento de más del 20% la depuración de creatinina 26).
El compromiso renal es glomerular y tubular. La afectación glomerular se evidencia por aumento de la concentración plasmática de urea y creatinina, y el compromiso tubular por acidosis tubular distal, hipokalemia, hipomagnesemia y menor concentración de la orina. Debido a la tubulopatía, existe pérdida urinaria de Potasio, Magnesio y bicarbonato. Asimismo, hay menor producción de eritropoyetina 18.Se verifica disminución del flujo plasmático renal, que produciría isquemia renal y reducción del filtrado glomerular por aumento de la resistencia arteriolar. Finalmente, podría producir apoptosis de las células tubulares y de las células intersticiales de la médula renal 27.
Existen factores que aumentan la morbilidad renal de la anfotericina, como la presencia de hipoflujo renal, hiponatremia y el uso de otros fármacos nefrotóxicos 27.
El esquema posológico en neonatología más utilizado es comenzar con 0,5 mg/kg el primer día y si es tolerado, aumentar la dosis diaria hasta 1 mg/kg para el segundo o tercer día de tratamiento 8. Se recomienda iniciar tratamiento con la dosis que requiere el paciente y no administrar dosis mayores de 1 mg/kg/día. La dosis máxima no debe exceder 50 mg como dosis total diaria 28.Re sugiere iniciar el tratamiento con 0,25 mg/kg I.V. a lo largo de 6 h, con monitorización de signos vitales durante las primeras horas de infusión. Si no produce ninguna reacción, administrar la dosis completa. La dosis de mantenimiento más utilizada es de 0,5 mg/kg/día (rango 0,25-1 mg/kg/día) 29.
Bes, tras una revisión bibliográfica realizado en la Argentina, exponen que en la población neonatal, la anfotericina B desoxicolato es el antifúngico de elección. Si bien fuera del período neonatal, las últimas recomendaciones sugieren usar anfotericinas asociadas a lípidos, sus precios son una limitante importante para su empleo. La anfotericina B es adecuada para comenzar el tratamiento antimicótico en el paciente neutropénico febril y para la mayoría de los pacientes con candidiasis sistémicas, criptococosis y micosis endémicas. En pacientes pediátricos que requieran tratamientos antifúngicos prolongados o que tengan factores de riesgo aumentados para el compromiso renal, las anfotericinas asociadas a lípidos son una alternativa que debe considerarse 19.
Domaniczky, tras el estudio realizado en nuestro país en el Hospital Central de IPS entre 2010-2011, sobre prevalencia de pacientes que presentaron efectos colaterales durante la administración de anfotericina B, manifiestan que las reacciones adversas asociadas a la infusión de anfotericina B desoxicolato son fenómenos frecuentes pero la nefrotoxicidad es ocasional y de baja magnitud 30.
Por su parte Rosanova explica que el uso de los antifúngicos convencionales, tales como anfotericina B desoxicolato, no ha permitido reducir la mortalidad en las infecciones fúngicas invasivas y ha generado, además, efectos adversos potenciales no despreciables, como la nefrotoxicidad 31. A su vez Moreno expone que el uso de anfotericina B desoxicolato ha quedado prácticamente proscrito por su perfil de efectos adversos, aunque es un medicamento muy económico y de mayor uso que otros antimicóticos 32.
Entonces, ¿cuál podría ser el escenario de uso en la práctica en nuestra región? Probablemente sea posible iniciar anfotericina B desoxicolato en los pacientes con indicación para su uso, maximizando las estrategias de prevención de la toxicidad aguda y la nefrotoxicidad.
El objetivo del estudio fue determinar los efectos adversos asociados al empleo de anfotericina desoxicolato en neonatos del Servicio de Neonatología del Hospital Nacional de Itauguá, y las características de la población afectada, durante el periodo 2013-2015.
MATERIAL Y METODOS
Estudio observacional, descriptivo, transversal, retrospectivo realizado en recién nacidos del Servicio de Neonatología del Hospital Nacional de Itauguá durante el periodo de agosto 2013 hasta noviembre de 2015, que hayan recibido tratamiento con anfotericina B.
Criterios de inclusión:
Recién nacidos que hayan recibido tratamiento con anfotericina B desoxicolato por un periodo mínimo de una semana.
Recién nacidos que cuenten con determinaciones de urea, creatinina, hepatograma, electrolitos al iniciar el tratamiento, durante el mismo, y/o al final del mismo.
Muestreo no probabilístico, de conveniencia.
Variables:
Edad gestacional: según Capurro o Ballard
Vía de parto: vaginal o cesárea
Sexo
Peso al nacer: medido en gramos
Apgar: determinado al minuto y a los 5 minutos de nacer
Diagnósticos previos al de sepsis fúngica
Tratamiento con anfotericina B: total de días, dosis de prueba (uso o no de dosis de prueba de 0,1 mg/kp/día), aumento progresivo de dosis hasta llegar a la dosis/día máxima (de 0,5 mg/kp/día a 1 mg/kp/día), dosis diaria, tipo de dilución: adecuada (dilución en 1 ml de dextrosa al 5% por cada 0,125 mg de anfotericina B) o no adecuada, tiempo de infusión (2, 4 o 6 horas)
Medicaciones asociadas: aminoglucósido, furosemida, indometacina, ibuprofeno, corticoides.
Cambios en la función renal y hepática al iniciar, durante y hasta la finalización del tratamiento:se consideró anormal todo aumento de 0,5 mg/dL y 20 UI a partir de nivel basal de la creatinina y enzimas hepáticas, respectivamente.
Perfil hematológico alterado: todo descenso de leucocitos de 2000 o más, leucopenia menor a 5.000, descenso de hemoglobina de 1,5 gr/dL, plaquetas: aumento o descenso de 100.000/m3 con respecto al basal.
Electrolitos en sangre: determinación cada 72 hs. de Na, K, P, Mg, Ca.
Análisis de orina: pH en orina durante la utilización de anfotericina B
Presencia de cilindros y proteínas en las 2 semanas posteriores al inicio de la anfotericina B
Manifestaciones clínicas durante infusión: rash, tromboflebitis, hipotensión, hipertensión, taquicardia, arritmias, convulsión y fiebre.
Día de tratamiento en que comienzan los efectos adversos
Dosis acumulativa al iniciar efectos adversos
Conducta frente a efecto adverso: administración de clorfeniramina, corticoides, antipirético, suspensión del medicamento, espaciamiento de dosis, disminución de dosis o prolongación del tiempo de administración.
Respuesta al tratamiento del efecto adverso: revierte hipokalemia, hiponatremia, fiebre, anemia revierte parcialmente, se mantiene sin variación, empeora a pesar del tratamiento.
Estado clínico a la semana de suspender tratamiento con anfotericina B.
Estado clínico al alta: vivo (con o sin secuelas secundarias al uso de anfotericina B), óbito (y causa del fallecimiento)
Otras variables: días de vida al momento de inicio de tratamiento con anfotericina B, diagnósticos y tratamientos previos a la utilización de anfotericina B, tiempo que lleva la normalización de efectos adversos.
Método de recolección de datos:
Para identificar a los recién nacidos que recibieron tratamiento con anfotericina B se recurrió a la base de datos del Servicio. Luego se recurrió a la revisión de las historias clínicas de los pacientes, previa autorización del Jefe del Servicio. Las variables fueron registrados en fichas técnicas y descriptas con el programa estadístico Epi Info 7©.
Aspectos éticos:
Se respetó el derecho de confidencialidad de los datos, ya que para identificarlos se emplearon códigos numéricos. Este trabajo no requirió consentimiento informado pues se trabajó con expedientes médicos y el estudio es retrospectivo. Se solicitó al Comité de Bioética del Departamento de Pediatría del Hospital Nacional de Itauguá la revisión de este protocolo.
RESULTADOS
Se incluyeron 28 recién nacidos (RN) durante el periodo de estudio, en quienes se empleó anfotericina B como tratamiento por riesgo o sospecha de sepsis fúngica. Se observó una mayor prevalencia en el sexo masculino n= 18 (64%).
Respecto a la edad, 21 (75%) fueron de pretérmino, con un promedio de edad gestacional y peso de nacimiento de 34±3 semanas y de 1.910 gramos, respectivamente. En el grupo de RN de término, que constituyeron 7 (25%), el promedio de peso fue 3150 gramos, con edad gestacional media 38,7 semanas.
Agrupando la muestra por categorías de peso, se notó preponderancia de RN del grupo pequeños para edad gestacional 15 (53,57%), siguiéndole los neonatos con peso adecuado para edad gestacional: 12 (42,85%) y grande para edad gestacional: 1 (3,57%). Cabe mencionar que en 7 casos (25%) se presentó restricción del crecimiento intrauterino.
La edad media de los RN al inicio de tratamiento con anfotericina B fue aproximadamente de 19 días. Los pacientes recibieron anfotericina B por un promedio de 12 días.
El promedio de dosis acumulativa en los pacientes analizados fue 12±4 mg/kg (rango 5,5-29,5 gr.) En 19 (67,8%) de los pacientes se utilizó un aumento progresivo de la dosis, desde 0,5 mg/kg/día hasta 1 mg/kg/día, en un lapso de tiempo de 24 horas.
El tiempo de infusión de anfotericina B fue en casi todos (96,4%) fue de 4 horas; utilizándose la administración en 6 horas solo en 1 caso.
En 13 (46,42%) se emplearon junto a anfotericina B otros antibióticos: ampicilina 2 (15,38%), gentamicina 1 (7,69%), cefotaxima 2 (15,38%), meropenem 4 (30,76%), vancomicina 4 (30,76%). En sólo 4 casos (14,28%) se utilizó diurético asociado al tratamiento con anfotericina B.
Los efectos secundarios detectados fueron: anemia en 22 pacientes (78,57%), de los cuales unos 12 (54,54%) presentaban anemia antes del inicio del tratamiento con anfotericina, en 3 de los 28 pacientes (10,71%) se observó en la semana de tratamiento y en 7 (25%) después de la primera semana. Por esto 35,7% de anemia se asume como efecto adverso.
Con respecto a la anemia que se presentó en la segunda semana de tratamiento, se observó que en 3 (42,85%) de los casos persistía después de concluir tratamiento. Mientras que en los 4 pacientes (57,14%) restantes hubo mejoría de la anemia tras 1 semana de haber terminado el tratamiento sin recibir transfusión de glóbulos rojos concentrados. Es importante mencionar que el grupo que recuperó la anemia a la semana de suspender el tratamiento correspondió al grupo que inició anemia luego de una semana de haber comenzado la medicación.
Se halló que 10 pacientes (35,7%) presentaron anemia durante el curso del tratamiento, en 3 de ellos se presentaron al final de la primera semana y en 4 durante la segunda semana de tratamiento.
En cuanto al análisis de los glóbulos blancos, al inicio del tratamiento se observó que en 22 (78,57%) RN se encontraban normales, presentando leucocitosis (mayor a 10.000 y/o aumento de 2.000 leucocitos respecto al nivel basal) en 4 (14,29%) y leucopenia (menor a 5.000) en 2 (7,14%). Tanto los pacientes con leucopenia como aquellos que presentaron leucocitosis recuperaron los valores normales entre el sexto y séptimo día de tratamiento continuando con el tratamiento con anfotericina B en la mayoría de los casos. En todos los casos se observó normalidad de leucocitos en sangre al culminar el tratamiento.
En cuanto a las plaquetas, al iniciar tratamiento, en 15 casos (53,57%) se encontraban alteradas (plaquetopenia inferior a 100.000/mm3), normalizándose al realizar control tras 72 horas de haber iniciado tratamiento. De los 13 casos restantes que presentaban niveles normales inicialmente, se observó plaquetopenia en 3 pacientes (23,07%) a las 48 horas de haber iniciado anfotericina B, normalizándose en un paciente a las 72 horas (no fue posible analizar si fue o no error de laboratorio) y en los otros dos últimos se observaron valores persistentemente bajos durante la primera y segunda semana de tratamiento. No se pudo definir con el análisis de la historia clínica si los cambios observados fueron debidos a la infección o como efecto adverso de la medicación.
A pesar de las alteraciones hematológicas observadas en los pacientes no se efectuaron cambios en el tratamiento administrado, así como en la forma de administración.
Con respecto al perfil renal, la creatinina aumentó en las primeras 48 hs en 2 pacientes (7,14%), observándose entre 0,5 a 0,7 mg/dL por encima del valor basal, manteniéndose dicho aumento a la semana de tratamiento y retornando a nivel basal al terminar el tratamiento.
Teniendo en cuenta que la urea es fácilmente alterada por diversos factores como aporte de líquidos, en este trabajo no se incluye el análisis de la misma.
En 96,43% de los casos no se observó alteración del perfil hepático. La enzima afectada fue GOT en un paciente, pero teniendo en cuenta de que es la menos específica del hígado, en este trabajo no se cataloga como efecto adverso.
En cuanto al ionograma, el principal electrolito alterado fue el Potasio, produciéndose hipokalemia con valores de 2,4 a 3 mEq/L, en 7 pacientes (25%) en las primeras 48 hs, seguido del Sodio, hallándose hiponatremia con valores de sodio menor a 130 mEq/L en 4 (14,28%) en las primeras 48 horas y en 8 (28,57%) en la segunda semana de tratamiento (Gráfico 1).

Gráfico 1. Alteración de Potasio y Sodio en las 48 a 72 hs y en la primera semana de tratamiento con anfotericina B (n 28).
Se observó descenso de los valores de Magnesio, Calcio y Fósforo (Gráfico 2) en todos los casos, requiriendo corrección de calcio en un paciente y magnesio en dos pacientes. Los hallazgos fueron por control laboratorial, sin clínica evidente de hipocalcemia ni de hipomagnesemia.
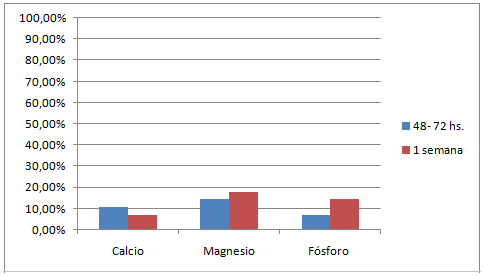
Gráfico 2. Distribución de alteraciones de electrolitos durante tratamiento con anfotericina B (n 28)
En cuanto a los efectos secundarios atribuidos a la infusión de anfotericina B presentados por los pacientes se destacan la taquicardia e hipotensión arterial, que se observaron en 8 (28,5%) y 7 (25%) respectivamente (Gráfico 3).
Solo en uno (3,57%) de los pacientes se suspendió anfotericina B ante la aparición de síntomas y efectos adversos (convulsión) y en uno (3,57%) se espació la anfotericina B cada 48 horas debido a insuficiencia renal.
En pacientes que presentaron efectos secundarios con el uso de anfotericina B, la mayoría de los casos lograron la corrección de la función renal luego de finalizar tratamiento, el tiempo promedio de normalización de las alteraciones fue de 7 días posterior a la suspensión del tratamiento.
Las características de la población que presentó mayor número de efectos adversos fueron los prematuros, de bajo peso, con drogas asociadas, ya sean diuréticos y/o antibióticos nefrotóxicos. Los que presentaron alteraciones renales también tienen en común la prematurez en su mayoría y 13 (46,42%) se asoció a antibióticos, con mayor frecuencia meropenem y vancomicina (30,46% y 30,76% respectivamente)
La anfotericina B fue administrada en 28 casos (96,5%) en infusión de 4 horas y en solo un caso la duración de la administración fue de 6 horas. Se recibió a intervalos de 24 horas entre una y otra dosis, la dosis en el 100% de los casos fue de 1 mg/kg/día.
DISCUSIÓN
Considerando el aumento de frecuencia de sepsis fúngica en la población neonatal, secundaria a la mayor sobrevida de este grupo susceptible, y siendo la medicación de elección en esas circunstancias la anfotericina B, se decició describir las características de la población que presenta esta patología, así como los efectos secundarios de la medicación administrada. Durante el periodo de estudio 28 RN fueron tratados con anfotericina B por sospecha de sepsis fúngica; resaltando la prevalencia del sexo masculino en la población: 18 (64.28%); con respecto a la edad gestacional, 75% fueron prematuros, con un promedio de edad gestacional y peso al nacimiento de 34±3 semanas y de 1.910 gramos respectivamente.
El estudio realizado por Moreno sobre aislamiento de Candida en el Hospital Miguel Hidalgo, Departamento de Pediatría, obtuvo 72 aislamientos de Cándida, con predominio en el sexo masculino, con una media de edad 19,2 meses, resultado que coincide en cuanto al predominio según sexo, sin embargo en la media de edad esta investigación arrojó cifra superior al obtenido por Moreno (34±3 semanas) 32.
El estudio realizado por Carrasco Sanchez a 15 RN ingresados en la unidad de neonatología arrojó que la edad gestacional media es 33 ± 6 semanas, con un total de 7 niños de menos de 29 semanas y 6 de más de 37 semanas. El peso medio al nacimiento fue de 1.877 g. En cuanto a la distribución por sexo fue semejante en dicho estudio (8/7) 33.
El reporte de Carrasco obtuvo resultados muy similares al de este estudio en cuanto a la edad gestacional y peso con una mínima diferencia, sin embargo no coincide en el sexo ya que esta investigación mostró predominio en el sexo masculino.
La edad media al iniciar tratamiento con anfotericina B y en el momento de sospechar la sepsis fúngica fue 13,4 días. Trece presentaban sepsis; de los cuales en tan solo 4 pacientes se certificó el diagnóstico de infección fúngica, la mayoría por Candida sp. Recibieron tratamiento con anfotericina B desoxicolato comenzando con dosis de 0,5 mg/kg/día, como dosis de inicio y llegando en 24 horas a dosis de 1 mg/kp/día.
Los efectos secundarios más llamativos encontrados durante el tratamiento con anfotericina B fueron la anemia, alteraciones de Sodio y Potasio.
Weitkamp y cols., de Alemania, comunicaron su experiencia con anfotericina B liposomal en 21 lactantes con bajo peso al nacer que tenían candidiasis sistémica. La edad mediana al inicio del tratamiento fue de 13 días. La dosis del fármaco fue de 1 a 5 mg/kg/día y se administró en niños de 11 a 79 días. Todos los lactantes tratados se recuperaron y no se observó toxicidad relacionada con el fármaco (8.
Carrasco, por su parte, obtuvo que todos los pacientes estudiados recibieron antibioterapia intravenosa, 6 niños recibieron más de 4 tipos de antibióticos, con una media de 10 días, entre ellos se utilizó ampicilina, tobramicina, cefotaxima, amikacina, cloxacilina, vancomicina y clindamicina. Las alteraciones analíticas al realizar el diagnóstico de sepsis fúngica fueron anemia y trombopenia en 7 casos, leucocitosis en 6, leucopenia en 3 y neutrofília absoluta o relativa en 7, 11 presentaban sepsis (1 Candida sp., 9 C. albicans, 1 C. parapsilosis), 2 infección del tracto urinario (C. albicans) y 2 candidemias (C. parapsilosis). Recibieron tratamiento con anfotericina B liposomal comenzando con dosis de 0,5-1 mg/kg/día, hasta un máximo de 4 mg/kg/día 32.
Fraga menciona que el tratamiento de las candidemias sistémicas se basa en el empleo de anfotericina B, la dosis diaria óptima no está bien establecida y lo más habitual es comenzar por 0,25 mg/kg/día por vía intravenosa en un tiempo de infusión superior a 6 horas, aumentando la dosis en los días siguientes hasta alcanzar una dosis máxima de 2 mg/kg/día. La dosis acumulativa de anfotericina B necesaria para el tratamiento adecuado de las candidiasis sistémicas no está bien definida, aunque se estima como suficiente una dosis total de 20-30 mg/kg. La vida media y las concentraciones séricas de esta droga son muy variables en el periodo neonatal y parece ser mejor tolerada en niños que en adultos 34.
Diversos autores han descrito efectos secundarios durante la perfusión intravenosa del fármaco (fiebre, taquicardia, hipotensión arterial, temblores y rash cutáneo), toxicidad renal (creatinina > 1,5 mg/dL), alteraciones electrolíticas (Na <130 mmol/L, K <3 mmol/L), toxicidad hepática (aumento de TGO y TGP) y depresión medular (Hb < 10 gr/dL y plaquetopenia) 30,33. Por estos motivos la anfotericina B está contraindicada en situaciones de insuficiencia renal, anemia y plaquetopenia y se debe utilizar con precaución en el RN prematuro con inmadurez renal o con transaminasas elevadas 34.
En esta investigación las alteraciones hematológicas detectó anemia en los pacientes durante el empleo de anfotericina B (13,63%) en la semana de inicio de tratamiento y en 7 pacientes (31,81%) después de la primera semana de haberse iniciado anfotericina B. Sin embargo, la presencia de leucocitosis y leucopenia se presentó frecuentemente al inicio del tratamiento, desapareciendo en el curso del mismo, lo cual hace pensar que estos cambios podrían ser debidos al proceso infeccioso en sí y no como consecuencia del tratamiento administrado.
En cuanto a la plaquetopenia vista en 3 pacientes durante el tratamiento administrado no pudo evaluarse adecuadamente a qué pudo deberse, ya que en uno de ellos la alteración se notó solo en un resultado laboratorial y fue revertido en 72hs, lo que hace presumir un error laboratorial; en tanto que los otros 2 casos persistieron durante el curso del tratamiento con plaquetopenia; el cual no persistió al suspender la medicación, lo que hace deducir que otras situaciones pudieron serla causa de las mismas en los pacientes, como una infección mixta por otro agente no susceptible a anfotericina B.
Con respecto a 7,14% de los pacientes con alteración de creatinina, el valor aumentado se mantuvo durante todo el tratamiento, retornando a nivel basal al concluir la medicación, el aumento fue leve y no se tomó conducta alguna. En más de la mitad de los neonatos se utilizó un aumento progresivo de la dosis, que fue de 0,5 mg/kg/día en 24 horas, con intervalo de 24 horas entre una y otra dosis.
En cuanto a las características de la muestra que presentó efectos adversos, sobresale que fueron prematuros, de bajo peso, con drogas asociadas, ya sean diuréticos y/o antibióticos nefróticos. Los que presentaron alteraciones renales también fueron prematuros en su mayoría y en 13 (46,42%) se asoció antibiótico con mayor frecuencia meropenem (30,46%) y vancomicina (30,76%).
El estudio realizado por Domaniczky, Samudio y Carreras sobre Efectos colaterales durante la infusión de anfotericina B en la terapia intensiva de marzo 2010 a setiembre del 2011 en el Hospital Central del IPS, incluyó a 32 pacientes en quienes la duración promedio del tratamiento fue de 12 días, con una dosis acumulada promedio de 40 mg totales. El 100% de los tratados recibió infusiones de 4 a 6 horas. El 40% de los tratamientos se acompañó de reacciones adversas asociadas a la infusión, predominando la hipokalemia (35%) 30.
Comparando con el estudio de Domaniczky, Samudio y Carreras 30, en este también se asoció efectos adversos como hipokalemia (35%), la nefrotoxicidad fue baja, en un 3%, pero al igual que en nuestro trabajo ninguno requirió ingreso a diálisis.
En cuanto a las debilidades del estudio, nos encontramos con el bajo número de pacientes y teniendo en cuenta de que se trata de un análisis retrospectivo, nos encontramos con fichas incompletas, limitándonos el acceso a la información.
En base a los resultados obtenidos se arribó a las siguientes conclusiones: del total de 28 RN tratados con anfotericina B por sospecha de sepsis fúngica hubo prevalencia del sexo masculino (64,28%), con respecto a la edad gestacional, 75% fueron prematuros en ese grupo, el promedio de edad gestacional y peso al nacimiento fue de 32 ±4 semanas y de 1.910 g respectivamente. Presentaron bajo peso al nacer el 32,14%.
La edad media de inicio de anfotericina fue 19±9 días. Los días totales de anfotericina que recibieron los pacientes fueron en promedio de 12±4 días con un rango de 6-30 días. El promedio de dosis acumulativa en los pacientes analizados fue 12±4 mg con un rango 1,5-29,5 gr. En más de la mitad de los neonatos se utilizó un aumento progresivo de la dosis, que fue de 0,5 mg/kg/día a 1 mg/kg/día, en 24 horas, con intervalo de 24 horas entre una y otra dosis.
El tiempo de infusión de anfotericina B fue en su mayoría (96,4%) de 4 horas, utilizándose 6 horas solo en 1 caso analizado en el que se presentó rash cutáneo, mejorando con la infusión más lenta. En 13 (46,5%) neonatos se emplearon junto a anfotericina B otros antibióticos. En tan solo 14,28% se utilizó diurético asociado.
Se comprobó anemia en 10 pacientes (35,71%) y 4 de ellos presentaron mejoría de la anemia tras una semana de haber concluido el tratamiento, sin recibir transfusión de glóbulos rojos concentrados.
En cuanto a las plaquetas, se observó plaquetopenia en 3 pacientes a las 48 horas de haber iniciado anfotericina B.
Los electrolitos alterados fueron por descenso del Potasio (25%), Magnesio (14,28%), Sodio (14,28%), los cuales aparecieron en la segunda semana de tratamiento.
En cuanto al perfil renal, la creatinina en las primeras 48 hs se alteró en 2 pacientes (7,14%), observándose un aumento de entre 0,5 y 0,7 mg/dL, por encima del valor basal, manteniéndose en la semana de tratamiento con el mismo porcentaje.
En cuanto a los síntomas presentados por los pacientes durante la infusión de anfotericina B, se destacan la taquicardia e hipotensión arterial, que se observaron en 28,5 y 25% respectivamente.
Solo en 3,57% de los pacientes se suspende anfotericina B ante la aparición de síntomas y/o efectos adversos (convulsión) y en 3,57% se espacia anfotericina B cada 48 horas por insuficiencia renal.
En pacientes que tuvieron alteraciones, la mayoría de los casos lograron su corrección luego de finalizar tratamiento con anfotericina B, el tiempo promedio de normalización de las alteraciones fue de 7 días.















