Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista del Nacional (Itauguá)
versión impresa ISSN 2072-8174
Rev. Nac. (Itauguá) vol.7 no.1 Itauguá jun. 2015
https://doi.org/10.18004/rdn2015.0007.01.008-016
ARTÍCULO ORIGINAL
Manifestaciones del dengue a nivel renal
Manifestations of dengue in the kidney
Daiana María Correa Recalde1, Raúl Real2
RESUMEN
Introducción: el dengue es una infección con afectación multisistémica, autolimitada, con espectro clínico que varía de formas asintomáticas a graves y fatales. Hay descripciones de casos de afectación renal en todo el mundo. Objetivo: describir las manifestaciones renales por el dengue. Metodología: estudio observacional, descriptivo, prospectivo realizado en pacientes adultos con dengue grave internados en el Dpto. de Medicina Interna del Hospital Nacional (Itauguá, Paraguay) durante la epidemia del verano 2013-2013. Fueron evaluados parámetros clínicos y laboratoriales con énfasis en la función renal. Resultados: se reclutaron 135 pacientes, 69 varones y 66 mujeres, con edad media 42,7±18 años. En 37% de los casos había alguna comorbilidad. Se midió proteinuria de 24 hs en 34 sujetos, encontrándose en rango nefrótico en 8,8% y en rango elevado ( = 160 mg/día) en 67,6%. Otros hallazgos llamativos fueron la hematuria (38%) e hipertensión arterial transitoria (39%). Un solo paciente presentó alteración de urea y creatinina al alta. Conclusiones: las manifestaciones renales por el dengue grave son frecuentes, predominando la proteinuria, hematuria e hipertensión arterial, aunque son transitorias en la mayoría.
Palabras claves: Dengue, Factores de riesgo, Riñón, Hipertensión, Adultos, Paraguay.
ABSTRACT
Introduction: dengue fever is an infection with multisystem involvement, self-limiting, clinical spectrum ranging from asymptomatic to severe and fatal forms. There are descriptions of cases of renal disease worldwide. Objective: to describe renal manifestations of dengue. Methodology: observational, descriptive, prospective study in adult patients with severe dengue admitted to the Department of Internal Medicine, National Hospital (Itauguá, Paraguay) during summer 2013 to 2013 epidemic. We evaluated clinical and laboratory parameters with emphasis on renal function. Results: 135 patients, 69 men and 66 women were recruited, mean age 42.7 ± 18 years. In 37% of cases there was any comorbidity. 24 h proteinuria were measured in 34 subjects, being in nephrotic range at 8.8% and high range (= 160 mg / day) in 67.6%. Other striking findings were hematuria (38%) and transient hypertension (39%). Only one patient presented alterations in urea and creatinine at discharge. Conclusions: renal manifestations of severe dengue are common, predominantly proteinuria, hematuria and hypertension, although they are transient in most.
Keywords: Dengue, Risk factors, Kidney, Hypertensión, Adults, Paraguay.
INTRODUCCION
El dengue es una enfermedad viral febril aguda, infecciosa, sistémica, transmitida por mosquitos del género Aedes, caracterizándose por diferentes presentaciones clínicas y con evolución clínica impredecible1. Se la describe como la principal enfermedad viral transmitida por artrópodos en áreas tropicales y subtropicales2. Su incidencia ha aumentado en las últimas décadas, por lo que es considerada hoy en día como una enfermedad infecciosa emergente, se ha convertido en uno de los problemas más serios de salud pública acompañado con el incremento de la morbilidad3,4.
Es extensamente aceptado como una enfermedad inmunopatogénica. Desde esta perspectiva, la patogénesis del dengue puede explicarse por varias hipótesis implicadas en los factores inmunitarios, incluyendo: 1- aumento de la infección viral mediante anticuerpos de reacción cruzada, 2- activación de la memoria de células T de reacción cruzada, 3- acción de citocinas y 4- activación del complemento5.
Se considera que la población mundial en riesgo de contraer dengue supera los 2.000 millones de personas y es la décima causa de muerte debida a enfermedades infecciosas6. En el 2005, el dengue fue la enfermedad vírica atribuida a un mosquito que más afectó a los seres humanos, su distribución global es comparable con la distribución del paludismo. Se calcula que 2,5 mil millones de personas viven en áreas expuestas al riesgo de transmisión epidémica. Todos los años se registran decenas de millones de casos de dengue y, dependiendo del año, hasta cientos de miles de casos de dengue hemorrágico. La tasa de mortalidad del dengue hemorrágico en la mayoría de los países es 5%, pero este porcentaje puede reducirse a menos del 1% con el tratamiento adecuado. La mayoría de los casos mortales se dan entre niños y adultos jóvenes7.
El aumento de casos de dengue con manifestaciones atípicas, como miocarditis, encefalitis, hepatitis o afectación renal, sugiere cambios en el perfil de la enfermedad que podrían deberse a cambios del tropismo del virus; esto último muestra la necesidad de conocer más sobre el virus y los posibles mecanismos que está utilizando para infectar diferentes tipos celulares o tejidos2.
Fisiopatología
Una vez establecida la infección en el huésped, las células expresan como primera línea de defensa el interferón (IFN) de tipo I (a y ß), que busca inhibir la replicación viral. Por otro lado, se inicia el proceso de presentación de antígenos mediante el complejo mayor de histocompatibilidad (CMH) de tipo I y II, lo que conlleva a que células como las NK (natural killer) ataquen a las células infectadas y liberen, junto a los linfocitos T, el IFN de tipo II (?). Esta actividad es el fenómeno responsable del control de la infección, ya que se establece un estado antiviral mediado por IFN que evita la replicación del virus en las células infectadas o la infección de nuevas células8.
Por otro lado, los linfocitos T desempeñan un papel preponderante en el establecimiento y control de la respuesta inmunitaria frente al virus. Tanto los linfocitos CD4+ como los CD8+ estimulados por diferentes citocinas, como el IFN (tipo I y II) y el factor de necrosis tumoral alfa (TNFa), se activan y secretan citocinas que pueden tener un carácter proinflamatorio o antiinflamatorio9-12.
Entonces la infección viral induce apoptosis de linfocitos T en los primeros días de la infección que, de acuerdo a su intensidad, puede influir favorablemente en la desaparición del virus o puede provocar la lisis de grandes cantidades de esas células y disminuir transitoriamente la competencia inmunológica del paciente, así como provocar daños en otras células y tejidos del huésped, tales como los endotelios, hepatocitos, miocardiocitos, neuronas, células tubulares renales, y otras, lo cual podría explicar la afectación de muchos órganos durante esta infección13-16.
La trombocitopenia se produce por destrucción de plaquetas en sangre periférica por un mecanismo inmunomediado. Los sangrados durante el dengue no están en relación directa con la intensidad de la trombocitopenia pues se producen por un conjunto de factores. Las causas de los sangrados en el dengue son múltiples, incluidos los vasculares y algunas alteraciones de la coagulación por acción cruzada de algunos anticuerpos antivirales contra el plasminógeno y otras proteínas, así como un disbalance entre los mecanismos de la coagulación y los de la fibrinolisis16.
En resumen, esta respuesta inmunitaria es la que normalmente se presenta en los pacientes infectados por primera vez que logran resolver la infección; sin embargo, en los pacientes que sufren una nueva infección con un serotipo diferente al que causó la primera (frecuente en zonas endémicas donde circula más de un serotipo), ocurre un fenómeno que estimula y exacerba la respuesta inmunitaria del paciente, lo que aumenta las probabilidades de que desarrolle dengue grave, con manifestaciones hemorrágicas o sin ellas16.
Afectación de órganos.
El dengue es un virus que puede presentar afectación multisistémica13. El daño hepático se manifiesta con incremento significativo de la alanino aminotransferasa (GPT o ALT) y la aspartato aminotransferasa (GOT o AST). En el examen físico se constata dolor abdominal, ictericia y hepatomegalia, similar a lo encontrado en otras hepatitis causadas por virus hepatotropos clásicos. En la hepatitis por virus del dengue los niveles de GOT son superiores que los de GPT, mientras que otros tipos de hepatitis virales elevan más la GPT que GOT13.
Estudios de dengue produjeron resultados controversiales con respecto a la afectación pulmonar debido a que este es un síntoma inusual en esta patología. El virus aparece infectando potencialmente macrófagos y células tanto epiteliales como endoteliales del pulmón17,18. Esto demuestra que el antígeno viral es posiblemente secuestrado por pinocitosis por numerosas células parenquimatosas, que no pertenecen al sistema reticuloendotelial13. Post-mortem, en las piezas se describen en el estudio histopatológico edema intersticial, congestión alveolar difusa y hemorragia pulmonar18.
Las manifestaciones cardiacas varían desde arritmias autolimitadas, desórdenes en la conducción aurículo-ventricular hasta severo daño miocárdico con edema agudo de pulmón o choque cardiogénico debido a daño celular miocárdico con falla del ventrículo izquierdo. Es común que la miocarditis se confunda con infarto agudo de miocardio o que enmascare a éste13,19,20.
La prevalencia de afectación neurológica varía entre 0,5-6%13. El virus del dengue es capaz de producir lesiones en el cerebro, médula espinal, raíces nerviosas, nervios periféricos y músculos. Las manifestaciones neurológicas del dengue comprenden las mononeuropatías, polineuropatías, encefalitis, el síndrome de Guillain Barre y la rabdomiólisis18.
Afectación del músculo esquelético: las mialgias son muy frecuentes en el dengue. La afectación muscular en el dengue ha sido estudiada por investigadores sobre todo en India y Brasil, donde la enfermedad es endémica. Actualmente se sabe que el virus del dengue afecta las fibras musculares, produciendo un cuadro inflamatorio, detectable por histopatología, demostrada por biopsia muscular en pacientes con cuadro clínico de miositis por dengue, caracterizada por infiltración mononuclear y acumulación de lípidos en las fibras musculares. En cuanto a la fisiopatología de la miositis en el dengue, hay consenso sobre el papel que juegan las citotoxinas liberadas en las fibras musculares. Entre las miotoxinas involucradas el factor de necrosis tumoral tendría un papel muy importante21-24.
Dengue y afectación renal
La afección renal en el dengue está demostrada en varios trabajos de investigación, la forma de presentación está dada por la proteinuria, cuya fisiopatología aún no está clara25,26. La hipoalbuminemia y proteinuria son bien reconocidos en la infección por dengue. Esto se cree se debe a la alteración de la filtración alterada por alteración del glicocálix, como el virus del dengue y NS1 son conocidos por unirse a sulfato de heparán, que es parte de la glicocálix27-28.
La infección por dengue ha sido asociada con una variedad de desórdenes renales: injuria renal aguda, proteinuria, hematuria y glomerulonefritis han sido reportadas durante o poco tiempo después de la infección29. La infección severa complicada con falla renal aguda se ha visto en 2-5% de los casos ocasionando una gran mortalidad. La proteinuria ha sido detectada hasta en 74% de pacientes con dengue grave. Hematuria ha sido detectada hasta en 12,5% de pacientes. Varios tipos de glomerulonefritis han sido reportados durante o poco tiempo después de infección por dengue en humanos y modelos de ratones infectados con el virus29. La proliferación mesangial y depósito de complejos autoinmunes son las alteraciones histológicas dominantes en el dengue asociado a glomerulonefritis. Se ha informado en una ocasión la infección por dengue asociado a una enfermedad sistémica con afectación renal29.
Permeabilidad capilar
El estudio de proteínas y albúmina se puede utilizar como criterio clínico-laboratorial para el diagnóstico de dengue hemorrágico. Las manifestaciones de la alteración de la permeabilidad vascular, que es lo que caracteriza a esta entidad, se reflejan en los valores de plaquetas, hemoconcentración, proteína y albúmina sérica, por lo que el estudio de éstas podría ser fundamental6.
Falla renal aguda
La infección severa, particularmente el dengue hemorrágico y choque por dengue, pueden ocasionar disfunción multiorgánica. La falla renal aguda es una complicación potencial de estos tipos de dengue y es típicamente asociado a hipotensión, rabdomiolisis o hemólisis29-31. La falla renal aguda en el dengue hemorrágico es debida principalmente a una necrosis isquémica tubular aguda con edema e infiltración de células mononucleares13.
La prevalencia de falla renal aguda fue de 1,6% entre 617 niños con dengue hemorrágico en Colombia, 3,3 % en adultos hospitalizados, 4,9 % en 81 pacientes chinos con dengue hemorrágico/choque por dengue y 5% en pacientes con dengue hemorrágico en Qatar29.
El desarrollo de falla renal aguda en pacientes con dengue está asociado a aumento de la mortalidad. En Tailandia la prevalencia de falla renal aguda en casos fatales de dengue hemorrágico fue 33,3%, en comparación con 0,3% en todos los casos de dengue hemorrágico. En una serie retrospectiva, 60% de los pacientes hospitalizados con dengue hemorrágico con falla renal aguda era hombres adultos mayores y tuvieron otras comorbilidades. Un análisis multivariado mostró que el choque por dengue fue un factor de riesgo independiente para el desarrollo de falla renal aguda29. En Brasil se describió un caso de injuria renal aguda asociado a rabdomiólisis por necrosis tubular aguda confirmada por biopsia que requirió tratamiento sustitutivo renal durante su internación con posterior remisión de la misma31. Por lo que la rabdomiólisis en estos pacientes constituye un factor de riesgo de injuria renal aguda.
La injuria renal aguda ha sido reportada también en el dengue clásico, dengue hemorrágico y choque por dengue sin rabdomiólisis. Como se mencionó, la inestabilidad hemodinámica, hemólisis, injuria glomerular y la acción directa de partículas virales en el tejido renal han sido considerados como probables mecanismos29-31.
Proteinuria
Algunos autores han descrito casos de proteinuria, aún en ausencia de alteración de la función renal, en 12% de niños con dengue y no asociado al descenso de plaquetas ni la hemoconcentración del hematocrito. Otros autores hallaron valores altos de proteinuria en 22% y otros investigadores han encontrado clara asociación entre proteinuria y formas graves de dengue13.
La proteinuria ha sido detectada en proporciones tan elevadas como 74% en pacientes con dengue hemorrágico. En una cohorte un paciente tuvo 10,8 g/día de proteinuria y fue diagnosticado como síndrome nefrótico. La excreción diaria fue de 8,1 g/día y 9,0 g/día basada en un rango de proteinuria/ creatininuria. Estos pacientes no tuvieron hematuria o concentración de creatinina sérica elevada29.
García et al. estudiaron retrospectivamente 74 pacientes con dengue hemorrágico que tuvieron un recuento de plaquetas menor a 125.000/mm3. La prevalencia de proteinuria en esta cohorte fue 30%29.
Hutspardol et al. reportaron un caso de un niño de 9 años, sin historia médica significativa, quien presentó 4 días de fiebre, cefalea, diarrea, hepatomegalia y azoemia. El diagnóstico de dengue fue sugerido por una prueba del lazo positiva y confirmada con detección de anticuerpos por IgM. La excreción diaria de proteína fue de 3,4 g/día basada en la relación proteinuria/creatininuria. La biopsia renal no fue realizada. Un mes después al alta hospitalaria la excreción urinaria de proteína era normal29.
Afortunadamente, no se vio que la proteinuria se relacione con deterioro severo de la función renal ni tampoco con la persistencia en un tiempo superior a 28 días. La resolución de proteinurias severas se debería a la autolimitación de la infección, al escaso aumento de los inmunocomplejos circulantes y/o a la eliminación renal de los mismos13. Es importante descartar otras causas de proteinuria como las postinfecciosas (hepatitis B, hepatitis C) y midiendo títulos de estreptococo antiestreptolisina O (ASTO), marcadores inmunológicos y niveles de C3 y C432.
El grado del índice creatininuria/proteinuria podría indicar la severidad de la infección por el dengue, manifestando una patogénesis por mecanismo autoinmune que el virus desencadena en el sistema linforeticular resultando en la fuga de proteínas en el glomérulo debido a glomerulonefritis asociada33.
En un estudio actual de los pacientes adultos con dengue se observó que el pico UPCR (índice proteinuria/creatininuria) podía distinguir a los pacientes susceptibles de desarrollar dengue hemorrágico de los que no lo hicieron y ese pico UPCR ocurrió en el día 7 de la enfermedad. Un aumento significativo de la proteinuria se observó un día antes de desaparición de la fiebre que corresponde a un día antes del desarrollo de dengue hemorrágico. Los pacientes con dengue leve tuvieron proteinuria significativamente más bajos que los pacientes con dengue hemorrágico inminente y choque por dengue. El seguimiento diario en este estudio prospectivo permitió determinar el valor discriminatorio de proteinuria, que no fue evidente en el período febril temprano pero sí entre los días 4 y 7, justo antes de desaparición de la fiebre y coincidente con la fuga plasmática27.
Se llegaría así a la conclusión de que la aparición y el pico de proteinuria mediante una prueba UPCR basada en el laboratorio se asocia significativamente con el desarrollo posterior de dengue hemorrágico, ya sea en ambulatorios u hospitalizados. El dosaje diario de UPCR puede ser una herramienta de pronóstico útil, sensible y específico en relación con otros parámetros clínicos para ayudar en el triaje de aquellos que requieren atención hospitalaria27. Cabe destacar que, utilizando UPCR ajustada por edad y día de enfermedad, tuvo una sensibilidad de 76% y especificidad de 77% para predecir el dengue hemorrágico, mientras que la combinación con recuento de glóbulos blancos, hematocrito sérico, recuento de plaquetas, proteínas séricas y sangrado tuvo una sensibilidad de 92% y especificidad de 80%. Esto se compara favorablemente con otros biomarcadores en investigación así como algoritmos predictivos. Comercialmente, las tiras reactivas de orina disponibles no eran útiles como herramienta de pronóstico en este estudio. No obstante, tal vez otras tiras reactivas podrían desarrollarse para diferenciar los valores UPCR basado en un valor de corte discriminatorio de 29 mg / mmoL 27.
Vasanwala et al., en un estudio similar en Singapur, encontraron asociación estadísticamente significativa del decremento de la trombocitopenia con proteinuria correspondiendo esto con la aparición de dengue hemorrágico33.
En un estudio en 54 adultos, portadores de dengue, internados en el Hospital Nacional entre diciembre 2012 y mayo 2013, se constató que el nivel de proteinuria de 24 hs en toda la muestra tuvo una media de 926 ± 1105 mg/día, rango 13 a 5.000 mg/día. La proteinuria se hallaba en rango nefrótico (media 3184±916 mg/24 hs) en 8 casos (14,8%) y dentro de valores elevados (media 669±494 mg/24 hs) en 35 casos (64,8%)34.
Un reporte en Singapur de dos casos en pacientes previamente sanos con proteinuria en rango nefrótico con diagnóstico de dengue hemorrágico, fueron atribuidos al virus tras descartar otras causas y presentar los mismos evidencia de fuga capilar en otros órganos32. Horvath et al reportaron que 74% de pacientes hospitalizados con dengue en Queensland, Australia, tuvieron proteinuria. Sin embargo, solo uno tenía características clínicas de síndrome nefrótico y la proteína en orina fue cuantificada en 10,8 g/24 hs35.
Glomerulonefritis
La glomerulonefritis secundaria inducida por dengue está demostrada por varios autores. La biopsia renal en pacientes con dengue hemorrágico incluso mostró presencia de nefropatía por depósitos, la cual fue transitoria, sugiriendo la posibilidad de una enfermedad por inmunocomplejos con depósitos en el tejido glomerular. La identificación del complejo soluble en suero reafirma este tema. La presencia de anticuerpos contra el virus asociado en dengue hemorrágico es conocida en estudios anteriores como en 1969. In vitro, estudios con linfocitos B humanos demostró la presencia de inmunocomplejos contra antígeno dengue preformado. Esto indica que el complejo inmune podría depositarse en el tejido vascular y glomerular ocasionando vasculitis y glomerulonefritis con presencia de proteinuria35.
Así la nefritis o nefropatía puede ser causa de fallo renal agudo o puede afectar selectivamente a la función de reabsorción propia del túbulo renal distal y de esa manera contribuir al aumento de líquido del espacio extravascular16.
En un estudio de 36 pacientes que habían fallecido con diagnóstico probable de dengue en el Hospital Nacional de Niños Benjamín Bloom de San Salvador, El Salvador, durante el período de octubre de 1999 y todo 2000, los riñones presentaron lesiones hemorrágicas y signos de glomerulonefritis, tubulitis y necrosis tubular aguda de alguna intensidad en todos los casos con autopsia realizada. En 3 casos pudo apreciarse apoptosis en las células epiteliales del túbulo proximal36.
Varios tipos de glomerulonefritis han sido reportados durante y poco tiempo después en humanos y modelos de ratones infectados con el virus del dengue29. Barreto et al, así como Boonpucknavig et al. examinaron muestras de tejido de pacientes con infección por el serotipo 2 del dengue. Para la tercera semana de infección, depósitos de complejos inmunes y lesiones proliferativas eran evidentes en el glomérulo. Ellos observaron depósitos de IgG, IgM y C3 en 10 de 20 pacientes (50%) con dengue hemorrágico y enfermedad renal. El examen ultraestructural demostró depósito de complejos inmunes asociado con hipertrofia de células mesangiales. En adición, partículas esféricas de 40-50 diámetros fue encontrado en 12 casos (60%)29. Hematuria fue reportada en 12,5% de los pacientes con dengue hemorrágico por Futrakul et al29.
En pacientes con enfermedad renal e inmunoreactantes la biopsia fue realizada durante la segunda semana luego del final de la fiebre. Para localizar el antígeno viral, Jessie et al. examinaron tejidos obtenidos de pacientes en quienes se confirmó la infección serológica o viralmente. Antígenos del dengue fue detectados en células del epitelio tubular renal en 3 de 8 casos (37,5%)29.
Un reciente caso describe alteración de la función renal y hematuria en un niño de 3 años con dengue. El paciente también presentó fiebre, vómitos, hipertensión y oliguria. Sin embargo el no tuvo choque, sepsis, hemólisis o rabdomiólisis. El examen de orina demostró hematíes y cilindros granulares. Los niveles de C3 del complemento se encontraban disminuidos. Se concluyó que el paciente padecía glomerulonefritis. No se realizó la biopsia renal. El mismo se recuperó con tratamiento de mantenimiento29.
Una mujer de 66 años de Honduras fue diagnosticada con infección por dengue por la clínica y confirmada por serología IgM y glomerulonefritis rápidamente progresiva. La biopsia renal reveló glomerulonefritis creciente severa. El examen con inmunofluorescencia demostró un fuerte patrón IgG lineal de depósitos alrededor de las paredes capilares. Estudios serológicos demostraron anticuerpos contra ANCA con MPO específico. A pesar de gran inmunosupresión y plasmaféresis, IgG contra el virus del dengue continuó ascendiendo confirmando el diagnóstico de infección aguda29.
OBJETIVOS
Describir las alteraciones renales en pacientes con dengue
Determinar la presencia de signos de fuga capilar y alteración de la presión arterial de los pacientes con dengue.
MATERIAL Y METODOS
Diseño: observacional, descriptivo, prospectivo, de corte transversal.
Población de estudio: varones y mujeres, mayores de edad, portadores de dengue, internados en el Dpto. de Medicina Interna (Hospital Nacional, Itauguá) entre diciembre 2012 y mayo 2013.
Criterios de inclusión: dengue grave con signos de alarma, confirmado por antígeno NS1 y/o IgM positivo, en período crítico o postfebril.
Criterios de exclusión: portadores de afecciones renales conocidas.
Muestreo: no probabilístico de casos consecutivos
Variables: datos demográficos, hemograma, proteinuria de 24 hs, orina simple, albuminemia. proteinemia, enzimas hepáticas y cardiacas, hallazgos ecográficos, presión arterial.
Reclutamiento: los sujetos que ingresaban con sospecha de dengue y luego confirmados fueron sometidos a los estudios diagnósticos de afectación renal. El método utilizado para la confirmación de la infección fue la prueba rápida SD BIOLINE Dengue Duo, un ensayo in vitro inmunocromatográfico de un paso diseñado para detectar el antígeno NS1 del virus del dengue en suero, plasma o sangre total humano. El otro método laboratorial confirmatorio fue el SD Dengue IgM Capture ELISA el cual utiliza una enzima inmunoabsorbente para la detección cualitativa de anticuerpos IgM específicos contra el virus del dengue en suero humano. Ambos reactivos son de ESTÁNDAR DIAGNOSTICS, INC, Korea.
Todos los pacientes fueron tratados según el protocolo de tratamiento sugerido en la Guía de Manejo Clínico 2012 del MSP y BS/OPS2.
Gestión de datos: las variables fueron registradas en fichas técnicas y trascriptas a planilla electrónica por los autores. Los cálculos estadísticos se realizaron con el programa estadístico Epi Info©. Las variables nominales se expresaron en porcentajes y las cuantitativas en medias ± DE.
Aspectos éticos: se respetaron los Principios de la Bioética. Se mantuvo la confidencialidad de los sujetos. No se requirió consentimiento informado por tratarse de un estudio observacional.
RESULTADOS
Ingresaron al estudio 135 pacientes de los cuales 69 eran varones y 66 eran mujeres. La edad media de los mismos era 42,7 ± 18 años (16 - 92 años).
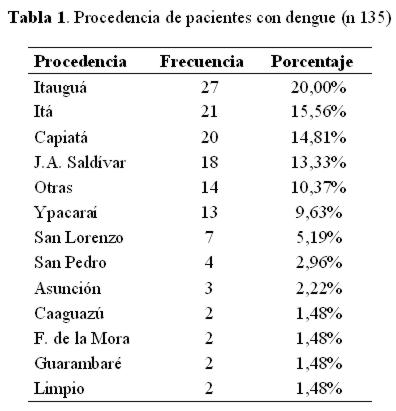
La mayoría de los pacientes procedían de poblaciones próximas al Hospital Nacional, centro de referencia de la región (tabla 1).
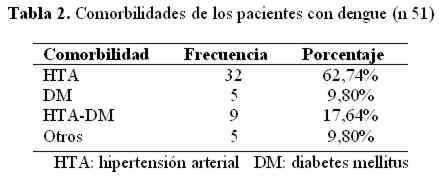
De los 135 pacientes estudiados, 84 no eran conocidos portadores de patología alguna, mientras que 51 tenían comorbilidades, sobre todo hipertensión arterial (tabla 2)
La albuminemia media de toda la muestra fue 2,9 ± 0,48 mg/dL, rango 1,9 a 4,3 mg/dL. La proteinemia media fue 5,9 ± 0,8 mg/dL, rango 3,6 a 5,9 mg/dL.
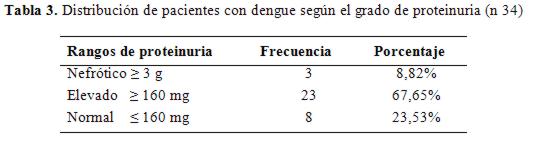
Se midió la proteinuria 24 hs en 34 sujetos y el nivel medio fue 768 ± 1057 mg/día, rango 13 a 5000 mg/día. Categorizando la proteinuria 24 hs en rangos, el nivel elevado fue el hallazgo más habitual (tabla 3).
En cuanto al estudio físico de la orina simple (n 135) se obtuvieron los siguientes hallazgos: pH promedio de 5,8 ± 0,6; rango 5 a 8; densidad media 1016 ± 9,06; rango 1000 a 1045. El aspecto ligeramente turbio fue el predominante en los sujetos estudiados (tabla 4).
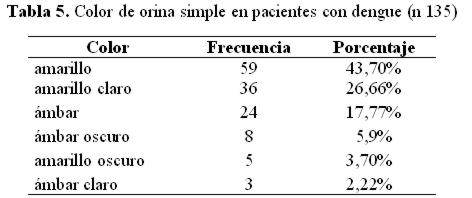
En cuanto al color de la orina simple, el amarillo fue el más frecuente (tabla 5).
Entre los hallazgos físico-químicos alterados sobresale la proteinuria seguido de la hematuria (tablas 6 y 7).
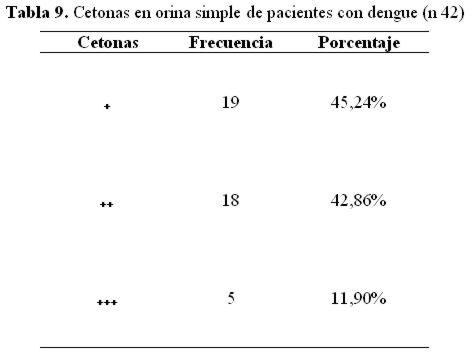
En menor proporción fueron hallados otros parámetros de orina simple alterados como el urobilinógeno (n 42), cetonas (n 42), bilirrubina (n 15) y glucosa (n 11). (Tablas 8, 9, 10 y 11 respectivamente).
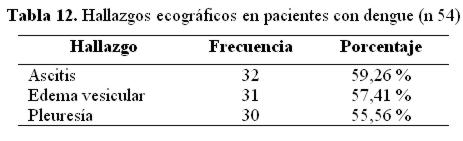
Entre los hallazgos microscópicos, la hematuria (hematíes = 3/campo) se encontró en 56 muestras (41,4%) y la leucocituria (leucocitos = 3/campo) en 37 pacientes (27,4%).Se realizó ecografía abdominal en 54 pacientes buscando signos de fuga plasmática, constatándose la presencia de éstos en más de la mitad de los pacientes (tabla 12).
Otro hallazgo fue que 53 pacientes (39,26%) sin antecedentes de hipertensión arterial presentaron cifras elevadas presión arterial sistólica.
Los parámetros de dengue grave fueron la plaquetopenia severa (= 20000/uL) encontrada en 29 pacientes (21,64%), hepatitis (enzimas hepáticas 10 veces sobre el valor normal) en 15 pacientes (11,90%), hemoconcentración del hematocrito (aumento = 20% del hematocrito basal) en 48 pacientes (35,82%) y hemoconcentración de la hemoglobina (aumento = 20% de la hemoglobina basal) en 44 pacientes (32,84%).
Un solo paciente presentó alteración de urea y creatinina al alta. Dicho paciente no volvió para control.
DISCUSION
El dengue, la principal arbovirosis de regiones tropicales y subtropicales, reemergente y conocido típicamente como hepatotropo, es actualmente distinguido por su inmunopatogénesis y afectación multisistémica6,10,17.
Nuestro país, al igual que otros países sudamericanos, no estuvo exento en este siglo de epidemias de dengue catalogadas como más drásticas17. Tuvo gran aumento de casos graves, registrándose en el 2013 (año de este estudio) 1870 casos en comparación con 29, 100 y 119 pacientes graves en los años 2010, 2011 y 2012 respectivamente. Nuestro hospital, centro de referencia de la región, se abocó a la atención, seguimiento e investigación de esta afección que se presentó en forma de epidemia8.
El endotelio vascular, a través de los glucosaminoglicanos, involucrado como principal órgano blanco, es caracterizado por la fuga capilar y alteraciones en la homeostasis con implicancias desde leves a severas en el organismo humano8,17,31. La identificación de predictores tempranos de severidad es la mejor estrategia para disminuir la tasa de morbimortalidad del dengue, motivo por lo cual se han buscado y discutido signos clínicos y laboratoriales para poder actuar oportunamente31.
La alteración proteica sérica podría ser la clave en evaluar la severidad de la fuga capilar ya que es reconocida la correlación entre hipoalbuminemia y derrames en cavidades serosas producidas en enfermedades crónicas, como ser desnutrición, nefropatías, hepatopatías, cardiopatías, etc.
El estudio de la funcionalidad renal en el dengue, además de informarnos de la gravedad del dengue, similar a la afectación de otros órganos (hepatitis, miocarditis, etc), podría ayudarnos a predecir pacientes con riesgo de dengue grave. La hipoalbuminemia y la proteinuria fue observada por otros autores en muchos casos de dengue, aún sin evidencia de afectación renal. La presencia y severidad de la microalbuminuria ha sido postulada como factor de riesgo potencial de un dengue severo, aunque hay poca información de la magnitud, tiempo de inicio y evolución de este fenómeno durante la infección8,18,31-33.
Pocos estudios a gran escala estudian la incidencia de las alteraciones renales en los pacientes con dengue. La mayoría se tratan de reportes de casos aislados, dificultando la comparación de este estudio con otros similares.
La mayoría de nuestros pacientes eran varones, a pesar de que se describen más casos de dengue en mujeres, por los hábitos domiciliarios del vector8. Este trofismo por el riñón debería ser confirmado por otras investigaciones. Se ha descrito infección de dengue severo complicado con falla renal aguda en 2-5% de los casos asociados a rabdomiólisis, hipotensión y hemorragias ocasionando una gran mortalidad38. En este estudio no están incluidos pacientes que fallecieron lo que explicaría que sólo uno de los pacientes estudiados presentó alteración del perfil renal de forma persistente.
Horvath et al constataron proteinuria en 74% de los pacientes con dengue hemorrágico. En esta cohorte un paciente tuvo 10,8 g/día de proteinuria y fue diagnosticado como síndrome nefrótico38. Nosotros constatamos proteinuria en orina simple en 62,9% de los pacientes, de los cuales 3 pacientes (8,82%) presentaron rango nefrótico y 23 (67,65%) cifras elevadas de proteinuria en orina de 24 hs. Estos hallazgos coinciden con la gravedad de nuestros casos en que más del 50% presentaban signos de hemoconcentración. Esta alteración podría explicarse por fuga capilar así como pudiera ocurrir en la pared endotelial glomerular. En ese contexto evaluamos otros signos de fuga capilar en los pacientes que contaban con ecografía abdominal, un método útil en detectar la fuga capilar que es inicialmente focal y ocurre principalmente en espacio pleural y peritoneal8. Encontramos que más de la mitad de nuestros pacientes presentaban ascitis, derrame pleural y edema de pared vesicular, lo que apoyaría la hipótesis mencionada.
Se encuentran también casos documentados de glomerulonefritis asociada al dengue confirmadas por biopsia como causa de proteinuria23,25,38. Así, la presencia de hematuria fue reportada en 12,5% de los pacientes con dengue hemorrágico por Futrakul et al. En nuestro estudio 50,7% de los pacientes presentó hematuria39.
En los niños con dengue la sospecha de glomerulonefritis se ve afianzada por la hipertensión arterial que acompaña al cuadro, habiendo varios reportes de estos casos23,38. Dado que nuestros pacientes son adultos y portadores de comorbilidades, como la hipertensión arterial, tal vez sea menos evidente este fenómeno, a pesar de ello constatamos hipertensión arterial en 53 pacientes (39,26%) que no portaban o no se conocían portadores de esta patología. La biopsia confirmaría esta sospecha pero es un método cruento y al ser el dengue una infección aguda, la mayoría de las manifestaciones hipertensivas cedían al alta.
También hay reporte de un caso de dengue asociado a nefritis por lupus eritematoso sistémico (LES) el cual presentó proteinuria. En nuestra serie, una de las pacientes es portadora de LES y presenta una proteinuria de 470 mg/dL; desconocemos si está alteración ya tenía la paciente o fue desencadenada por el dengue.
El perfil fisicoquímico de la orina simple de estos pacientes se caracterizó por el aspecto ligeramente turbio en 64,5% de las muestras, el color amarillo en 43%, pH medio 5,8±0,6 (rango 5 a 8), densidad media 1016±9,06 (rango 1000 a 1045). Otros parámetros de orina simple alterados, como el urobilinógeno en 42 pacientes (31%), cetonas en la misma proporción, bilirrubinuria en 15 pacientes (11%) y glucosuria en 11 pacientes (8,14%), se podrían atribuir a la permeabilidad vascular glomerular, ya que pacientes no portadores de diabetes mellitus o con glicemia dentro de rango normal, presentaron glucosuria, así como pacientes sin hiperbilirrubinemia exhibieron bilirrubina en orina. No encontramos algún trabajo similar para comparar nuestros hallazgos.
Además estudiamos parámetros de dengue grave como la plaquetopenia severa (= 20.000/uL) que fue encontrada en 29 pacientes (21,64%), hepatitis (enzimas hepáticas 10 veces sobre el valor normal) en 15 pacientes (11,90%), hemoconcentración del hematocrito (aumento = 20% del hematocrito basal) en 48 pacientes (35,82%) y hemoconcentración de la hemoglobina (aumento = 20% de la hemoglobina basal) en 44 pacientes (32,84%). Todos estos hallazgos anormales, aunque presentes en menos del 50% de los pacientes, nos indican la afectación multisistémica de estos casos.
Tal vez la proteinuria sea más sensible que otros marcadores de fuga capilar como la hemoconcentración del hematocrito o de la hemoglobina. Considerando que estos marcadores de forma aislada no son certeros, ya que se desconoce el valor del hematocrito basal al ingreso y porque en muchas poblaciones se desconoce la media del hematocrito, la proteinuria debería ser también considerada como parámetro de fuga capilar. Más aún, ya que las proteínas no se alteran por la hemorragias que estos pacientes pueden sufrir13.
Otro instrumento de medición utilizado para medir la proteinuria de forma reciente es el índice proteinuria/creatininuria el cual ha detectado asociación significativa con el desarrollo posterior de dengue hemorrágico en pacientes adultos ambulatorios y hospitalizados18. Este índice no fue calculado por haber utilizado la orina simple para evaluar otras alteraciones de la misma y porque la orina 24 hs es considerada el gold estándar en la detección de proteinuria, aunque existe excelente correlación entre ambos parámetros38.
Sería interesante incorporar un test de detección sensible y específico de proteínas en orina en todo paciente con sospecha de dengue8,30.
En estos casos de gran afectación renal se deberían descartar otras probables causas de glomerulopatía como las postinfecciosas, hepatitis B, hepatitis C. Además, se deberían medir títulos de antiestreptolisina (ASTO), marcadores inmunológicos y niveles de C3 y C4 para atribuir estas nefritis al virus del dengue31. Nosotros no realizamos estas mediciones debido al gran flujo de pacientes que requerían un rápido giro de camas, el tiempo que demora obtener resultados de estos estudios y su costo elevado.
La limitación de este estudio fue la ausencia de biopsia renal para documentar y confirmar la glomerulonefritis por dengue aunque esto está discutido debido a la naturaleza autolimitada del proceso. Además, faltaría el seguimiento de los pacientes para evaluar la remisión completa de la afectación renal debido a que los pacientes una vez estabilizados eran dados rápidamente de alta o trasladados a un centro de menor complejidad.
CONCLUSIONES
El dengue se caracterizó por afectar con igual proporción a varones y mujeres, edad media 43±18 años y presentar como principales comorbilidades a la hipertensión arterial y diabetes mellitus. El nivel medio de proteinuria 24 hs 768±1057 mg/día. Se halló proteinuria elevada en 67,6% y proteinuria en rango nefrótico en 8,8%.
Las características de la orina simple fueron pH medio 5,8±0,6; densidad media 1016±9,06. El aspecto ligeramente turbio fue el predominante así como el color amarillo. Entre los hallazgos químicos alterados sobresale la proteinuria en 63% seguido de la hematuria en 50,4%.
En menor proporción fueron hallados alterados otros parámetros de orina simple como la presencia de urobilinógeno (31,1%), cetonas (31,1%), bilirrubina (11,1%) y glucosa (8,1%).
La albuminemia media de toda la muestra fue 2,9 ± 0,48 mg/dL. La proteinemia media fue 5,9 ± 0,8 mg/dL.
Se constató signos de fuga capilar por ecografía en más de la mitad de los pacientes.
En 39,26% se presentaron cifras elevadas presión arterial sistólica, aún sin antecedentes de hipertensión arterial.
Otros parámetros de gravedad detectados fueron: plaquetopenia severa = 20.000/uL (21,64%), enzimas hepáticas 10 veces sobre el valor normal (11,90%), aumento = 20% del hematocrito basal (35,82%) y aumento = 20% de la hemoglobina basal (32,84%).
Un solo paciente presentó aumento persistente de urea y creatinina al alta.
REFERENCIAS
1. Paraguay. Ministerio de Salud Pública y Bienestar Social. Dengue: guía de manejo clínico 2012 (visitado 2014 Feb 9). Disponible en: http://www.mspbs.gov.py. [ Links ]
2. Velandia M, Castellanos J. Virus del dengue: estructura y ciclo viral. Infectio. 2011;15(1):33-43. [ Links ]
3. Hoyos A, Pérez A. Actualización en aspectos epidemiológicos y clínicos del dengue. Revista Cubana de Salud Pública. 2013;36(1):149-164. [ Links ]
4. Zhang H, Li W, Wang J, Peng H, Chen X, Zhou Y. NS1-based tests supplying a diagnostic utility for confirming dengue infection: a meta-analysis. Int J Infect Dis. 2014;10(2):1-10. [ Links ]
5. Villar L, Gélvez R, Rodríguez J, Salgado D, Parra B, Osorio L. Biomarcadores pronósticos de gravedad del dengue. Biomédica. 2013 Sept;33(1):108-116. [ Links ]
6. Brito C, Albuquerque M, Lucena-Silva N. Evidência de alterações de permeabilidade vascular na dengue: quando a dosagem de albumina sérica define o quadro?. Revista da Sociedade Brasileira de Medicina Tropical. 2007 Mar-Abr;40(2):220-223. [ Links ]
7. Centros para el Control y la prevención de Enfermedades. Atlanta. Hoja de datos dengue. (visitado 2013 Mar 3). Disponible en http://www.cdc.gov/spanish/enfermedades/dengue/HojaDatos.htm [ Links ]
8. Gubler D. Dengue/dengue haemorrhagic fever: history and current status. Novartis Found Symp. 2006;277:3-16. [ Links ]
9. Paraguay. Ministerio de Salud Pública y Bienestar Social. Departamento de Prensa. Evaluación-dengue: situación de la epidemia de dengue en Paraguay, en cifras. (visitado 2013 Mar 3). Disponible en: http://www.mspbs.gov.py/v2/18532-EVALUACIN--DENGUE-Situacin-de-la-epidemia-de-Dengue-en-Paraguay-en-cifras [ Links ]
10. Agencia de Información Paraguaya. Reconocen a Paraguay por lograr corte epidémico del dengue. Gobierno Nacional. Abril, 2014. [visitado 2013 Mar 3]. Disponible en: http://www.ip.gov.py [ Links ]
11. Center for Infectious Disease Research and Policy. University of Minnesota. Minneapolis. Researchers identify fifth dengue subtype. [visitado 3 Nov 2013]. Disponible en: http://www.cidrap.umn.edu/news-perspective/2013/10/researchers-identify-fifth-dengue-subtype [ Links ]
12. Fajardo G, Meljem J, Vicente E, Venegas F, Mazón B, Aguirre H. El dengue en México. Rev Med Inst Mex Seguro Soc. 2012;50(6):631-639. [ Links ]
13. Real R, Rojas G, Correa D, Aldama F, Barrios A, Irala G. et al. Manifestaciones sistémicas del Dengue. Rev Nac (Itauguá). 2013 Dic.;5(2):8-16. [ Links ]
14. Marquetti M, Suárez S, Bisset J, Leyva M. Reporte de habitats utilizados por Aedes aegypti en Cuidad de La Habana. Rev Cubana Med Trop. 2005 Agos;57(2):159-16. [ Links ]
15. Rodrígues R. Estrategias para el control del dengue y del Aedes aegypti en las Américas. Rev Cubana Med Trop. 2002;54(3):189-201. [ Links ]
16. Martinez E. Dengue. Estud. av. 2008 Dec;22(64):33-52. [ Links ]
17. Pelaez O, Sánchez L, Mas-Bermejo P, Pérez S, Kouri G, Guzmán M. Prevalencia de sindromes febriles en la vigilancia del dengue. Rev Cubana Hig Epidemiol. 2010 Abr;48(1)3-14. [ Links ]
18. Rodrigues RS, Brum AL, Páez MV, Póvoa TF, Basilio-de-Oliveira C, Marchiori C, et al. Lung in Dengue: Computed Tomography Findings. PLoS One. 2014 May 16;9(5)e96313. [ Links ]
19. Araya S, Duarte C, Sanabria M, Apodaca G, Lovera D, Arbo A. Comportamiento clínico del dengue en niños en los últimos años en Paraguay. Rev. Inst. Med. Trop. 2010;5(1):14-19. [ Links ]
20. Lee I, Lee W, Liu J, Yang K. Acute myocarditis in dengue hemorrhagic fever: a case report and review of cardiac complications in dengue-affected patients. International Journal of Infectious Diseases 2010;14(10):919-922. [ Links ]
21. Salgado D, Rodríguez J, Lozano L, Zabaleta T. Dengue perinatal. Biomédica. 2013 Sept;33(Supl 1):14-21 [ Links ]
22. Zhang F, Kramer C. Corticosteroids for dengue infection. Cochrane Database Syst Rev. 2014 Jul;1(7):CD003488. [ Links ]
23. Alvarez L, Briceño A, Oviedo M. Resistance to Temephos in populations of Aedes aegypti of the west of Venezuela. Rev Colombiana de Entomología. 2006;32(2):172-175. [ Links ]
24. Mesquita M, Basualdo W, Benítez M. Miositis aguda benigna por Dengue: reporte de un caso en un paciente pediátrico. Pediatr. (Asunción) 2012;39(01):39-42. [ Links ]
25. Escalante-Gómez C, Zeledón-Sánchez F, Ulate-Montero G. Proteinuria, fisiología y fisiopatología aplicada. AMC. 2007 Abril-Junio;49(2):83-89. [ Links ]
26. Arévalo J, Azaña J, Balsa J, Berdel A, Contreras J, Gaudó J, et al. Proteinuria (y microalbuminuria). Green Book. Diagnóstico y tratamiento médico. Marbán. 2012;1669-1671. [ Links ]
27. Vasanwala F, Thein T, Leo Y, Gan V, Hao Y, Lee L, et al. Predictive Value of Proteinuria in Adult Dengue Severity. PLOS Neglected Tropical Diseases. 2014 Feb;8(2)e2712. [ Links ]
28. Basu A, Umesh U. Vascular endothelium: the battlefield of dengue viruses. FEMS Immunol Med Microbiol. 2008 Agos;53(3):287-299 [ Links ]
29. Lizarraga K, Nayer A. Dengue-associated kidney disease. J Nephropathol. 2014;3(2):57-62. [ Links ]
30. Jiménez C, Gutierrez M. Disfunción renal aguda relacionada con dengue hemorrágico: reporte de un caso. Revista de Asociación Mexicana de Medicina Crítica y Terapia Intensiva. 2006;20(2):93-95. [ Links ]
31. Repizo L, Malheiros D, Yu L, Barros R, Burdmann E. Biopsy proven acute tubular necrosis due to rhabdomyolisis in a dengue fever patient. A case report and review of the literature. Rev Inst Med Trop Sao Paulo. 2014 Jan-Feb;56(1):85-88. [ Links ]
32. Vasanwala F, Puvanendran R, Suhail S. Two cases of self-limiting nephropathies secondary to dengue haemorrhagic fever. Singapore Med J. 2009 Jul;50(7):e253-5. [ Links ]
33. Vasanwala F, Puvanendran R, Fook-Chong S, Suhail S, Lee K. Could peak proteinuria determine whether patient with dengue fever develop dengue hemorrhagic/dengue shock syndrome? - A prospective cohort study. BMC Infectious Diseases. 2011 Ago 5;11:212. [ Links ]
34. Correa D, Real R, Rojas G, Aldama F, Barrios M, Fridman V, et al. Proteinuria en dengue. Rev. virtual Soc. Parag. Med. Int. 2014 (visitado 2013 Mar 3);1(1):19-21. Disponible en: http://www.revista.spmi.org.py/archivos/Revista%20SPMI%20Febrero/index.html#/18/ [ Links ]
35. Horvath R, McBride W, Hanna J. Clinical features of hospitalised patients during Dengue-3 epidemic in far north Queensland 1997-1999. Dengue Bulletin. 1999;23(9):24-29 [ Links ]
36. Martínez E, Polanco A, Pleites E. ¿Por qué y cómo mueren los niños con dengue? Rev Cubana Med Trop. 2008 (visitado 2013 Mar 3);60(01):40-7. Disponible en: http://scielo.sld.cu/pdf/mtr/v60n1/mtr06108.pdf [ Links ]
37. Huy T, Giang T, Duy D, Kikuchi M, Hien T, Zamora J, Hirayama K, et al. Factors Associated with Dengue Shock Syndrome: A Systematic Review and Meta-Analysis. PLOS Neglected Tropical Diseases. 2013 Sep;7(9)e2412. [ Links ]
38. González Cascán YM, Torres de Taboada E. Correlación entre el cociente proteinuria/creatininuria en una orina al azar y la proteinuria de 24 horas. Rev. virtual Soc. Parag. Med. Int. 2015;2(1):75-93. Disponible en: http://www.revista.spmi.org.py/archivos/Revista%20SPMI%20Mar-2015/index.html#/74/ 2015 03 02 [ Links ]
39. Futrakul P, Poshyachinda V, Mitrakul C, Kun-Anake C, Boonpucknavig V, Boompucknavig S, Bhamarapravati N. Renal involvement and reticulo-endothelial-system clearance in dengue hemorrhagic fever. J Med Assoc Thai. 1973 Jan;56(1):33-9. [ Links ]
1. Médico Residente de Medicina Interna. Universidad Nacional de Itapúa. Encarnación, Paraguay.
2. Médico Internista. Departamento de Medicina Interna. Hospital Nacional. Ministerio de Salud Pública y Bienestar Social (Itauguá, Paraguay)
Correo electrónico: daianacorrea585@gmail.com
Artículo recibido: 25 de marzo de 2015. Artículo Aprobado: 04 de abril de 2015.