Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista del Nacional (Itauguá)
Print version ISSN 2072-8174
Rev. Nac. (Itauguá) vol.6 no.2 Itauguá 2014
ARTICULO ORIGINAL
Uso de colistina en Pediatría
Use of colistin in Pediatrics
Chantal Marie Real Aparicio1, Patricia Abigail Arias Yrazusta1, Gloria Samudio2
RESUMEN
Introducción: la colistina es un antibiótico de reciente reintroducción en el tratamiento de gérmenes multiresistentes. Objetivo: describir las indicaciones clínicas y resultados obtenidos con el uso de la colistina. Material y métodos: estudio observacional descriptivo retrospectivo realizado en el Dpto. de Pediatría del Hospital Nacional en niños tratados con colistina entre los años 2011 y 2013. Resultados: se incluyeron 28 pacientes. Las comorbilidades más frecuentes fueron las cardiopatías congénitas (10%), desnutrición severa (10%) e insuficiencia renal crónica (10%). El diagnóstico más frecuente fue IAAS (infección asociada a la atención en salud) en 50%. La indicación fue empírica en 61%. Se realizaron 11 aislamientos bacterianos, predominando Acinetobacter baumannii en 63%. Los sitios de aislamiento fueron orina (27%), sangre (18%) y secreción traqueal (18%). Hubo multirresistencia en 10 de los 11 aislamientos (91%). La urea aumentó en 78% y la creatinina en 57%. Buen estado al alta en 82%. Conclusiones: la indicación clínica más frecuente para la administración de colistina fueron las infecciones asociadas a la atención en la salud (50%). El germen tratado con mayor frecuencia fue Acinetobacter baumannii. El efecto tóxico predominante fue la nefrotoxicidad. El estado al alta fue satisfactorio en la mayoría de los casos.
Palabras claves: colistina, multirresistencia a antibióticos, Acinetobacter baumannii, infección asociada a la atención en salud
ABSTRACT
Background: Colistin is an antibiotic of recent reintroduction in the treatment of multiresistant germs. Objective: To describe the clinical indications and the results with the use of colistin. Material and methods: We conducted a retrospective observational study in the Department of Pediatrics, National Hospital, in children treated with colistin between 2011 and 2013. Results: We included 28 patients. The most frequent comorbidities were congenital heart disease (10%), severe malnutrition (10%) and chronic renal failure (10%). The most frequent diagnosis were infections associated with health care (50%). The indication was empirical in 61%. Eleven bacterial isolates were performed, predominantly Acinetobacter baumannii (63%). Isolation sites were urine (27%), blood (18%) and tracheal secretion (18%). There were multidrug resistance in 10 of the 11 isolations (91%). Urea increased by 78% and creatinine in 57%. At discharge, most were in good condition (82%).Conclusions: The most frequent clinical indication for colistin administration were infections associated with health care (50%). The most frequent agent was Acinetobacter baumannii. The predominant toxicity was nephrotoxicity. The status at discharge was satisfactory in most cases.
Keywords: colistin, multidrug resistance to antibiotics, Acinetobacter baumannii, infections associated with health care
INTRODUCCIÓN
Las infecciones intrahospitalarias son un problema para el médico debido a su creciente frecuencia y, sobre todo, a la rápida aparición de bacterias que obligan al uso de antibióticos no convencionales como la polimixina1-3. Los importantes efectos nefrotóxicos y neurotóxicos observados en los años 60 han discontinuado su uso, pero la necesidad de nuevos antibióticos han hecho emerger a este fármaco4.
Entre dichos gérmenes sensibles destacan los bacilos Gram negativos no fermentadores como Pseudomonas aeruginosa, Acinetobacter baumannii y Klebsiella pneumonie, caracterizados por su perfil de multirresistencia y a veces de panrresistencia antibiótica. Su presencia en septicemias por neumonías asociadas a ventilación mecánica asistida, heridas operatorias, drenajes quirúrgicos ventriculares cerebrales, etc, es muy común5.
La colistina (polimixina E) es un antibiótico que forma parte del grupo de las polimixinas producido por Bacillus polymyxa subspecies colistinus. Su estructura básica es la de un anillo peptídico policatiónico hidrofólico compuesto de 10 aminoácidos y una cola de ácidos grasos hidrofóbicos. Su peso molecular es de alrededor de 1200 Daltons. Es, por lo tanto, una molécula amfifílica con muy escasa penetración intracelular pero muy buena distribución homogénea en el agua extracelular4. Es un compuesto catiónico cíclico que actúa como detergente de la membrana bacteriana y que, a altas concentraciones, tiene un efecto bactericida.6 Este efecto sobre la membrana celular es independiente del metabolismo bacteriano y explica, en parte, el retraso en la aparición de resistencia al mismo4.
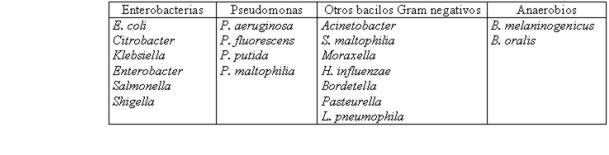
Su espectro de actividad es muy reducido, actúa exclusivamente sobre bacterias Gram negativas. Es útil como esquema de salvamento en el tratamiento de las infecciones por microorganismos multiresistentes como Stenotrophomonas maltophilia, especies de Acinetobacter o P. aeruginosa, cuando se han agotado las demás opciones6-10. Típicamente, las especies Proteus, Providencia, Burkholderia y Serratia son resistentes a la polimixina11.(tabla 1).
Tabla 1. Espectro de sensibilidad a la colistina4
No se absorbe por vía oral. Se ha utilizado por vía endovenosa, en nebulizaciones, en forma intratecal o tópica para tratar neumonías, bacteriemias, infecciones intra-abdominales, infecciones urinarias, meningitis o ventriculitis12. Su uso en nebulizaciones puede verse disminuida por la presencia de biopolímeros en los tubos endotraqueales5,13.
No atraviesa la barrera hematoencefálica ni pasa con facilidad a líquido pleural o sinovial, por lo que su administración en infecciones sistémicas requiere la vía parenteral y la intratecal en casos de infecciones del sistema nervioso central.5,14 La penetración al liquido cefalorraquídeo es de apenas 5%, pero en meninges inflamadas aumenta hasta 25-60%14.
La dosis diaria oscila entre 1,2 y 2,5 mg/kg de peso15,16. En caso de falla renal, las dosis son ajustadas de acuerdo con el siguiente esquema: para valores de filtración glomerular de 30 a 50 mL/min: 2,5 mg/kg/día; para valores entre 10 y 30 mL/min: 1,5 mg/kg/día y para cifras < 10 mL/min: 1 mg/kg cada 1 ó 2 días5,17.
Entre los efectos adversos se encuentra la nefrotoxicidad, siendo ésta dosis dependiente y se ve potenciada con el uso de aminoglucósidos, vancomicina, anfotericina B y algunas cefalosporinas. Este efecto colateral es evidenciado por el sedimento urinario anormal y el aumento progresivo de la creatinina7,14. La frecuencia de efectos nefrotóxicos oscila entre 15 y 55%15, 14.
Entre los efectos neurológicos se encuentra la parestesia perioral, vértigo, ataxia, debilidad y parálisis muscular, aunque estos efectos son mucho menos frecuentes que la nefrotoxicidad13. Las parestesias son las manifestaciones neurotóxicas más frecuentes (27%) aunque siempre son reversibles.
Otros efectos colaterales, aunque menos frecuentes, son las trombofleitis en el sitio de inyección, las urticarias, eosinofilia, fiebre medicamentosa8,15. El uso en forma de nebulizaciones se asocia ocasionalmente a broncoespasmo, tos y odinofagia8,18.
La emergencia de bacilos Gram negativos, multi o pan-resistentes y la casi ausencia de nuevas alternativas terapéuticas, ha obligado al creciente uso de colistina endovenosa en diferentes centros del mundo. Su asociación a otros antibióticos ha sido recomendada pues es mejor que su administración aislada19.
OBJETIVOS
Determinar las indicaciones del uso de colistina en el Departamento de Pediatría del Hospital Nacional en el periodo de 2011-2013.
Determinar las indicaciones del uso de colistina y el perfil bacteriológico de los gérmenes aislados.
Describir las características clínicas de los niños tratados con colistina y los efectos colaterales observados.
MATERIALES Y MÉTODOS
Diseño: observacional, descriptivo, transversal, retrospectivo
Población de estudio: niños y niñas menores de 16 años que recibieron tratamiento con colistina en el Departamento de Pediatría del Hospital Nacional durante los años 2012 y 2013
Criterios de inclusión:
- contar con aislamiento bacteriano y sensibilidad antimicrobiana
- tratamiento mínimo con colistina de 48 hs
- internación en cualquier Servicio del Departamento de Pediatría
Criterios de exclusión:
- fichas clínicas incompletas
- pacientes remitidos de otro hospital en tratamiento con colistina
Muestreo: no probabilístico de casos consecutivos
Variables
- demográficas: edad, sexo, lugar de internación,
- clínicas: sitio de infección, comorbilidades, mejoría clínica, estado al alta (vivo o muerto), duración de la antibióticoterapia, uso concomitante de otros antibióticos, efectos colaterales renales.
- bacteriológicas: germen aislado, fluido de aislamiento (sangre, líquido cefalorraquídeo, orina, heces, secreción traqueal), sensibilidad y resistencia antibiótica.
Reclutamiento
Se recurrió inicialmente a los registros de infecciones asentados en el libro de actas de Infectología. Posteriormente se extrajeron los datos de los expedientes clínicos obrantes en archivo
Gestión de datos: las variables se registraron en una planilla electrónica y fueron tomados por las autoras. Se realizó estadística descriptiva con el programa Epi Info 7.1. Las variables cualitativas se expresan en porcentajes y las variables cuantitativas en medias y desvío estándar.
Cálculo del tamaño de muestra: se utilizó el programa estadístico Epi Info 7.1. En un universo de 30 pacientes en 2 años se esperó una prevalencia de mejoría clínica de 70%.4,8 Para un efecto de diseño= 1, error alfa=5%, intervalo de confianza=95%, el tamaño mínimo calculado fue 27 casos.
Aspectos éticos
Se respetó la confidencialidad de los datos. Al trabajarse con expedientes clínicos no se requirió consentimiento informado.
RESULTADOS
Ingresaron al estudio 28 pacientes, incluyendo 6 neonatos, 10 lactantes menores y 11 adolescentes, internados principalmente en la Unidad de Cuidados Intensivos Pediátricos (tabla 2).
Tabla 2. Procedencia de pacientes con uso de colistina (n 28)
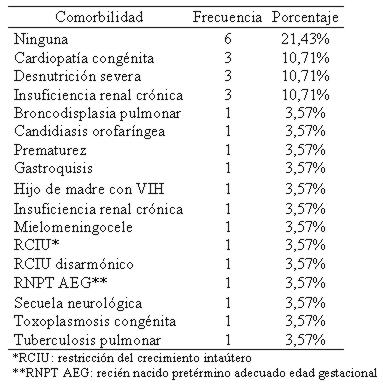
Hubo leve predominio del sexo femenino: 15 casos (55%). Se detectaron comorbilidades en 22 casos, predominando las cardiopatías congénitas (10%), desnutrición severa (10%) e insuficiencia renal crónica (10%) (tabla 3).
Tabla 3. Comorbilidades de pacientes en tratamiento con colistina (n 28)
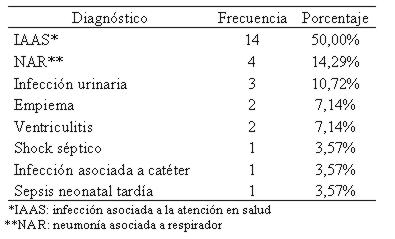
El diagnóstico más frecuente fue IAAS en 14 casos (50%) y el motivo de uso de la colistina fue empírico en 17 casos (61%) (tabla 4).
Tabla 4. Indicaciones del uso de colistina en Pediatría (n 28)
Se realizaron 11 aislamientos bacterianos, predominando Acinetobacter baumannii en 7 casos (63%), Acinetobacter baumannii/calcoaceticus complejo en 2 niños (18%), Acinetobacter sp. y Pseudomonas aeruginosa en 1 caso cada uno (9%).
El sitio de aislamiento más frecuente fue la orina (27%) (tabla 5)
Tabla 5. Sitios de aislamiento de gérmenes tratados con colistina (n 11)
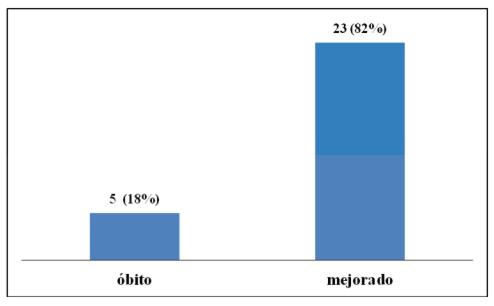
Se detectó multirresistencia en 10 de los 11 aislamientos (91%). El antecedente de uso previo de antibióticos fue elevado: 26 casos (93%). La media de uso de antibióticos fue 17±10 días y para la colistina fue 14±8 días. La urea aumentó en la mayoría de los pacientes: 22 casos (78%), así como la creatinina: 16 casos (57%). La mediana de días de internación fue 49 días (rango 20-82 días). El estado al alta fue mejorado en la mayoría: 23 casos (82%) (gráfico 1).
Gráfico 1. Estado al alta de pacientes tratados con colistina (n 28)
DISCUSIÓN
La colistina en un antibiótico de uso limitado, utilizado más frecuentemente en casos de infección asociada a cuidados de la salud, de forma empírica o dirigido en su mayoría a infecciones por Acinetobacter baumannii multirresistente, como fue observada en este estudio2,8.
Las infecciones asociadas a la atención en salud (IAAS) anteriormente llamadas nosocomiales o intrahospitalarias son aquellas adquiridas durante durante la internación y que no se habían manifestado ni estaban en período de incubación al ingreso a la institución. Este concepto también incluye a las infecciones adquiridas por el personal de salud durante el ejercicio de su profesión en las instituciones sanitarias. En este estudio representan la más frecuente indicación del uso de colistina. Se relacionan a factores como uso de dispositivos médicos, procedimientos quirúrgicos o invasivos, contacto entre pacientes y con trabajadores de la salud, administración de antibióticos, etc. Este tema debería investigarse para determinar el riesgo relativo de cada uno de ellos en próximos estudios20.
De los casos estudiados, el principal sitio de aislamiento de gérmenes sensibles fue el urocultivo, posiblemente por el uso frecuente de sondaje vesical en nuestros pacientes y por ser estos gérmenes Gram negativos originarios del área urogenital.
El promedio de días de tratamiento fue de 14 días, alterándose principalmente la urea más que la creatinina. En el estudio de Fica et al, el tiempo medio de tratamiento con colistina fue ligeramente menor (12 ± 5 días), posiblemente porque la cuarta parte de sus pacientes incluidos ya se hallaban en tratamiento dialítico. En coincidencia con este reporte, casi todos nuestros pacientes ya habían recibido otros antibióticos previamente5.
Aun así no se puede establecer si las alteraciones renales se deben al uso de colistina o al propio estado séptico de los pacientes, requiriéndose otros estudios. De igual manera se debe evitar el uso concomitante con otros fármacos nefrotóxicos, mantener buen volumen vascular, ajustar dosis según peso y función renal5,8. La frecuencia de nefrotoxicidad en múltiples series, expresada por el aumento del 50% del nivel basal de creatinina, oscila entre 7 y 30%.4 La mayoría de los reportes coinciden con nuestra observación de la mejoría de la nefrotoxicidad13. Se ha descrito que el uso de diuréticos y otras sustancias nefrotóxicas aumentan el riesgo de desarrollar estas complicaciones8.
La neurotoxicidad, que se manifiesta habitualmente como parestesias, bloqueo neuromuscular o apneas, no fue reportada en esta serie5,13.
La mayoría de los pacientes tuvo una evolución favorable (82%), en comparación con otras series donde se obtuvieron mejoría entre 50 y 70%5,8. Estas diferencias pueden ser debidas por la gravedad de los pacientes incluidos, la infección tratada, la oportunidad en el inicio del esquema, la dosis utilizada, el uso de antimicrobianos concomitantes con posible efecto sinérgico, etc. A pesar de la alta tasa de mejoría y coincidiendo con otros autores, no se recomienda el uso aislado de colistina en forma empírica en todas las infecciones nosocomiales sino combinada a rifampicina o carbapenems5,21. La reciente experiencia con la tigeciclina en el tratamiento de infecciones por Acineobacter baumannii no ha demostrado superioridad en comparación con la colistina obligando al uso de este antiguo "nuevo" antibiótico12,21,22.
CONCLUSIONES
La indicación clínica más frecuente para la administración de colistina fue la infección asociada a la atención en salud (50%). El germen tratado con mayor frecuencia fue Acinetobacter baumannii (63%). El efecto tóxico predominante fue la nefrotoxicidad. El estado al alta fue satisfactorio en la mayoría de los casos (82%).
REFERENCIAS
1. Bhattacharya S. Early diagnosis of resistant pathogens: how can it improve antimicrobial treatment? Virulence. 2013 Feb 15;4(2):172-84. [ Links ]
2. Balaji V, Jeremiah SS, Baliga PR. Polymyxins: Antimicrobial susceptibility concerns and therapeutic options. Indian J Med Microbiol. 2011 Jul-Sep; 29(3): 230-42. [ Links ]
3. Rossi F. The challenges of antimicrobial resistance in Brazil. Clin Infect Dis. 2011 May; 52(9): 1138-43. [ Links ]
4. Boisson M, Gregoire N, Couet W, Mimoz O. Colistin in critically ill patients. Minerva Anestesiol. 2013 Feb; 79(2): 200-8. [ Links ]
5. Fica CA, Céspedes JI, Gompertz GM, Jalón VM, Sakurada ZA, Sáez LE. Colistín en infecciones nosocomiales por bacilos gramnegativos pan-resistentes. Rev Chil Infect 2007; 24 (5): 360-367 [ Links ]
6. Velkov T, Roberts KD, Nation RL, Thompson PE, Li J. Pharmacology of polymyxins: new insights into an 'old' class of antibiotics. Future Microbiol. 2013 Jun; 8(6): 711-24. [ Links ]
7. Falagas ME, Kasiakou SK, Tsiodras S, Michalopoulos A. The use of intravenous and aerosolized polymyxins for the treatment of infections in critically ill patients: a review of the recent literature. Clin Med Res. 2006 Jun; 4(2): 138-46. [ Links ]
8. Falagas ME, Kasiakou SK. Toxicity of polymyxins: a systematic review of the evidence from old and recent studies. Crit Care. 2006 Feb; 10(1): R27. [ Links ]
9. Falagas ME, Vouloumanou EK, Rafailidis PI. Systemic colistin use in children without cystic fibrosis: a systematic review of the literature. Int J Antimicrob Agents. 2009 Jun; 33(6): 503.e1-503.e13. [ Links ]
10. Hartzell JD, Kim AS, Kortepeter MG, Moran KA. Acinetobacter pneumonia: a review. Med Gen Med. 2007 Jul 5; 9(3): 4. [ Links ]
11. Bergen PJ, Landersdorfer CB, Zhang J, Zhao M, Lee HJ, Nation RL, Li J. Pharmacokinetics and pharmacodynamics of 'old' polymyxins: what is new? Diagn Microbiol Infect Dis. 2012 Nov; 74(3): 213-23. [ Links ]
12. Khawcharoenporn T, Apisarnthanarak A, Mundy LM. Intrathecal colistin for drug-resistant Acinetobacter baumannii central nervous system infection: a case series and systematic review. Clin Microbiol Infect. 2010 Jul; 16(7): 888-94. [ Links ]
13. Nation RL, Li J. Colistin in the 21st century. Curr Opin Infect Dis. 2009 Dec; 22(6): 535-43. [ Links ]
14. Yahav D, Farbman L, Leibovici L, Paul M. Colistin: new lessons on an old antibiotic. Clin Microbiol Infect. 2012 Jan; 18(1): 18-29. [ Links ]
15. Mendes CA, Burdmann EA. Polymyxins - review with emphasis on nephrotoxicity. Rev Assoc Med Bras. 2009 Nov-Dec; 55(6): 752-9. [ Links ]
16. Couet W, Grégoire N, Marchand S, Mimoz O. Colistin pharmacokinetics: the fog is lifting. Clin Microbiol Infect. 2012 Jan; 18(1): 30-9. [ Links ]
17. Pérez-Pedrero MJ, Sánchez-Casado M, Rodríguez-Villar S. Utilización de la colistina nebulizada en la colonización e infección respiratoria por Acinetobacter baumannii en pacientes críticos. Med Intensiva. 2011; 35(4):226-231 [ Links ]
18. Petrosillo N, Ioannidou E, Falagas ME. Colistin monotherapy vs. combination therapy: evidence from microbiological, animal and clinical studies. Clin Microbiol Infect. 2008 Sep;14(9):816-27. [ Links ]
19. Cai Y, Chai D, Wang R, Liang B, Bai N. Colistin resistance of Acinetobacter baumannii: clinical reports, mechanisms and antimicrobial strategies. J Antimicrob Chemother. 2012 Jul; 67(7): 1607-15. [ Links ]
20. Barriga J, Cerda J, Abarca K, Ferrés M, Fajuri P, Riquelme M et al. Infecciones asociadas a la atención en salud (IAAS) en pacientes pediátricos post-operados de cardiopatías congénitas . Rev Chilena Infectol 2014; 31(1): 16-20 [ Links ]
21. Zavascki AP, Goldani LZ, Li J, Nation RL. Polymyxin B for the treatment of multidrug-resistant pathogens: a critical review. J Antimicrob Chemother. 2007 Dec; 60(6): 1206-15. [ Links ]
22. Linden PK, Paterson DL. Parenteral and inhaled colistin for treatment of ventilator-associated pneumonia. Clin Infect Dis. 2006 Sep 1; 43 Suppl 2: S89-94. [ Links ]
1. Médico Residente. Departamento de Pediatría, Hospital Nacional (Itauguá, Paraguay)
2. Departamento de Pediatría, Hospital Nacional (Itauguá, Paraguay)
Correo electrónico: chanti_real@yahoo.com.ar
Artículo recibido: 22 de octubre de 2014. Artículo aprobado: 24 de noviembre de 2014.