Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Revista del Nacional (Itauguá)
Print version ISSN 2072-8174
Rev. Nac. (Itauguá) vol.5 no.2 Itauguá Dec. 2013
ARTICULO ORIGINAL
Manifestaciones sistémicas del dengue
Systemic manifestations of dengue
Raúl Real1, Gustavo Rojas2, Daiana Correa2, María de los Ángeles Barrios2, Fabián Aldama2, Laura Pinchi3, Gustavo Irala3, Fabiola Cordero3, Soledad Rodríguez3, Lorena Alfonso3, Adriana Mendoza3, Lizi Vera3, Oscar Agüero3, Elías Fleitas3
RESUMEN
Introducción: el dengue es una infección que puede afectar múltiples órganos.Objetivo: determinar la afectación multisistémica por dengue. Metodología: estudio observacional, descriptivo, prospectivo realizado en sujetos adultos con dengue grave con signos de alarma internados en el Hospital Nacional entre diciembre 2012 y mayo 2013. La infección debía estar confirmada con antígeno NS1 y/o serología IgM (+). Resultados: se encontró 10,1% de hepatitis, 85,6% de transaminitis, 48% con relación CPKmb/CPK total >5%, 22,5% de alteraciones electrocardiográficas, 70,4% con proteinuria de 24 hs elevada y 9,3% con proteinuria en rango nefrótico. Conclusiones: la afectación multisistémica es frecuente, generalmente pasa desapercibida y en general es autolimitada aunque se requieren más estudios para evaluar la evolución a largo plazo en estos casos.
Palabras claves: dengue, hepatitis, miocarditis, proteinuria, Paraguay
ABSTRACT
Introduction: dengue is an infection that could affect multiple organs. Objective: to determine the multisystem involvement of dengue. Methodology: observational, descriptive, prospective study conducted in adult subjects with severe and warning signs of dengue admitted to the National Hospital between December 2012 and May 2013. Infection should be confirmed with NS1 antigen and / or IgM serology (+). Results: we found 10.1% of hepatitis, 85.6% of transaminitis the relation CPKmb / total CPK > 5% in 48%, electrocardiographic alterations in 22.5%, elevated proteinuria in 70.4% and nephrotic proteinuria in 9.3%. Conclusions: multisystemic involvement is frecuent, usually asymptomatic and generally self-limited although more studies are needed to evaluate the long-term outcome in these cases.
Keywords: dengue, hepatitis, myocarditis, proteinuria, Paraguay
INTRODUCCION
El dengue es una infección viral producida por un Arbovirus, afectando a regiones tropicales y subtropicales en todos los continentes. Los cuatro serotipos de dengue son infectantes para los seres humanos y capaces de producir formas graves, incluso letales. Tiene diferentes presentaciones clínicas y la mayoría se manifiesta en forma subclínica o asintomática (53-87%). En los sujetos sintomáticos, el cuadro clínico puede oscilar entre una fiebre leve hasta formas graves de choque y hemorragias mortales. A pesar de ser más grave en sujetos con comorbilidades, su evolución clínica es impredecible, lo que la hace peligrosa en cualquier situación1. La etiopatogenia de las formas graves se debe al aumento de la permeabilidad vascular y a los trastornos hemorrágicos causados por esta infección2.
El genoma RNA del dengue es una poli proteína consistente en tres proteínas estructurales (proteína C core, proteína M membrana y proteína capsular E) y siete proteínas no estructurales (NS1, NS2A, NS2B, NS3, NS4A, NS4B, NS5). La proteína NS1 es una glicoproteína de 50 kDA (353 o 354 aminoácidos) que no forma parte del virión pero que se libera de las células infectadas por el dengue3. (Wang SM). El rol del NS1 en la replicación viral es desconocido pero se demostró que es secretada por las células infectadas (sNS1) y que tiene importante actividad inmunológica4. Los anticuerpos contra NS1 podrían causar disfunción endotelial por reacción cruzada a las proteínas del huésped y al endotelio. Asimismo, puede ser un modulador en la vía del complemento y proteger al virus de la acción neutralizadora del mismo5.
El diagnóstico clínico del dengue tiene baja especificidad, por lo que el diagnóstico confirmatorio es únicamente laboratorial4. La detección de NS1 por ELISA o test rápidos tiene una sensibilidad entre 87 y 99% y especificidad entre 82 y 84% facilitando el diagnóstico precoz del dengue4,5,6,7. Los falsos negativos pueden deberse al aclaramiento de estas partículas por inmunoglobulinas presentes en los casos de infecciones secundarias. Los falsos positivos pueden deberse a reacciones cruzadas con anticuerpos dirigidos contra otros flavivirus (fiebre amarilla, encefalitis japonesa) o inmunocomplejos8. Otros estudios encontraron que los resultados de NS1 variaron de acuerdo al serotipo del virus del dengue, del estado inmunológico del paciente y de la severidad de la infección9.
Pasados los 5 días, la seroconversión de anticuerpos IgM e IgG por hemaglutinación o ELISA permite confirmar el diagnóstico. El aumento de IgM denota una infección reciente y la IgG una infección reciente o antigua. La vacunación reciente contra la fiebre amarilla puede dar resultados positivos1.
El principal órgano blanco del dengue es el endotelio vascular y los elementos formes de la sangre10,11. El daño funcional, no morfológico, de estas células se debe a la propia replicación viral intracelular y como consecuencia de la gran liberación de citoquinas, produciendo un aumento de la permeabilidad capilar con fuga plasmática al intersticio de todos los órganos12. Otros mecanismos del daño celular incluyen a los inmunocomplejos, efecto de los linfocitos T, reacción cruzada entre los anticuerpos circulantes y el endotelio vascular, aumento de los anticuerpos y complemento, mediadores solubles como las citoquinas, cepas extremadamente virulentas, pero el más reconocido es la gran liberación de anticuerpos y citoquinas cuando ocurre una segunda infección generando lo que se conoce como tsunami de citoquinas12. Característicamente, las manifestaciones clínicas de las complicaciones inician a partir del tercer día de enfermedad, cuando la fiebre cede y la viremia se halla en descenso, pero coincide con el aumento de las defensas inmunes del cuerpo12. Por otro lado, es bien sabido que pueden generarse fenómenos autoinmunes con diversos virus: HIV, hepatitis C, citomegalovirus, virus herpes simple, virus Epstein-Barr y virus del dengue.
Los anticuerpos dirigidos contra el antígeno NS1 muestran reactividad cruzada con las plaquetas humanas y las células endoteliales, lo que lleva a su inflamación y destrucción13.
Para el tratamiento del dengue no existen antivirales, sólo se realiza apoyo sintomático sobre todo el manejo adecuado de fluidos en relación a la magnitud de la fuga capilar y la trasfusión de plaquetas cuando la hemorragia es severa14. No existe ningún medicamento que reduzca la fuga capilar, los corticosteroides no han demostrado efectividad en este fenómeno ni en la plaquetopenia, por lo que están contraindicados15,16.
Muchas investigaciones se han propuesto para predecir la severidad del dengue usando parámetros clínicos y laboratoriales2,14. Entre los primeros están los signos de alarma propuestos por la OMS: dolor abdominal, vómitos, hemorragias, letargia o inquietud, hepatomegalia4. Estos parámetros tienen alta sensibilidad (95%), lo que evita enviar a la casa a pacientes graves. Sin embargo, la especificidad en baja (18%), es decir, hay muchos falsos negativos, lo que lleva a sobre internar a pacientes que no harán formas graves del dengue17.
Entre los parámetros laboratoriales de gravedad, aparte de la hemoconcentración y la plaquetopenia, se continúa buscando otros criterios diagnósticos rápidos, sencillos, sensibles y específicos que anuncien la severidad de esta infección4,18. El dengue puede tener una rápida evolución al choque y parece que el seguimiento de estos marcadores laboratoriales es más útil que una determinación aislada2.Como consecuencia de estos fenómenos es frecuente observar plaquetopenia, leucopenia, hemoconcentración superior al 20%5,19. Pero existen reportes de daños más o menos severos de diversos órganos20.
Afectación hepática
Es bien conocido el marcado tropismo del virus por los órganos del sistema monocítico y macrofágico, como son la médula ósea, bazo, nódulos linfáticos e hígado21. El dengue es hepatotropo, dado que han detectado antígenos del virus dengue en hepatocitos y partículas virales en muestras de biopsia de hígado. Otros mecanismos incluyen al daño por la gran circulación de citoquinas inflamatorias y a la isquemia hepática22.
El daño hepático se manifiesta con incremento significativo de la alanino aminotransferasa (GPT o ALT) y la aspartato aminotransferasa (GOT o AST). En el examen físico se constata dolor abdominal, ictericia y hepatomegalia, similar a lo encontrado en otras hepatitis causadas por virus hepatotropos clásicos. En la hepatitis por virus dengue los niveles de GOT son superiores que los de GPT, mientras que otros tipos de hepatitis virales se elevan más la GPT que GOT21.
El aumento de las enzimas hepáticas se observa en 60% y no siempre se relaciona con manifestaciones clínicas de disfunción hepática21. Se considera hepatitis cuando el aumento de las enzimas hepáticas sobrepasa 10 veces el valor normal23. Las transaminitis se presentan entre 17 y 44% y las hepatitis en 3,8%. Las enzimas aumentan hasta el 9° día de enfermedad y retornan a valores normales en las próximas tres semanas23. Es infrecuente la persistencia de síntomas y alteraciones analíticas pasadas los dos meses. La persistencia de hepatitis se relaciona a mecanismos inmunológicos24.
Las lesiones histopatológicas observadas fueron la necrosis centrolobulillar y de la zona media (zona 2), esteatosis, hiperplasia de las células de Kupfer, infiltración portal de monocitos y cuerpos acidófilos, además de partículas virales intracelulares. Necropsias hepáticas de ratones infectados experimentalmente han mostrado además eritrofagocitosis y hemorragias25.
Afectación cardiaca
El daño cardiaco es más frecuentemente observado en sujetos con dengue grave. Su patogenia no está bien aclarada pero se supone que interviene el daño celular por la replicación viral en el miocito o por el efecto de las citoquinas liberadas durante la infección. En los casos reportados, los serotipos 2 y 3 son los más citados26.
Las manifestaciones cardiacas varían considerablemente desde arritmias autolimitadas, desórdenes en la conducción auriculo-ventricular hasta severo daño miocárdico llevando a hipotensión arterial y edema de pulmón26. Es común que la miocarditis se confunda con infarto agudo de miocardio. La frecuencia de afectación cardiaca varía ampliamente en diferentes estudios. Así se han descrito 62% de alteraciones electrocardiográficas y 40% de alteraciones miocárdicas detectadas por escintigrafía26. En otra revisión prospectiva, la disfunción ventricular con fracción de eyección <50% se halló por centellografía en 16% de niños con dengue. Seguido en el tiempo, esta anormalidad se resolvió espontáneamente en el lapso de tres semanas27. Por ecocardiografía puede detectarse disfunción ventricular, hipoquinesia ventricular izquierda, regurgitación mitral y derrame pericárdico28,29. Estas elevadas frecuencias indican que la afectación cardiaca no es rara y que la mayoría de los casos pasan desapercibidos porque son oligosintomáticas y autolimitadas26.
Entre las alteraciones electrocardiográficas pueden verse bradicardia sinusal, prolongación del intervalo PR, bloqueo completo y de ramas del haz de His, cambios en el segmento ST, fibrilación auricular, taquicardia sinusal y arritmias ventriculares29. Estas alteraciones parecen estar relacionadas al nivel de citoquinas circulantes28. Afortunadamente, estas alteraciones son en su mayoría benignas, transitorias y autolimitadas30. Son debidas a miocarditis subclínica que se resuelven en 90% de los casos. En caso de persistencia de un bloqueo AV completo con repercusión hemodinámica, debe colocarse un marcapasos29. Se debe recordar que la bradicardia es característica del dengue y otras infecciones: fiebre tifoidea, malaria, enfermedad de los legionarios, psitacosis, tifus, leptospirosis y babesiosis28.
En nuestro medio se ha documentado por la clínica y laboratorio un caso de miocarditis por dengue en un sujeto adulto, con recuperación total en pocas semanas con medidas de sostén31. El estándar de oro del diagnóstico de una miocarditis es la biopsia endomiocárdica aunque la sospecha clínica y la resonancia nuclear magnética son de gran utilidad32.
Afectación renal
Algunos autores detectaron proteinuria en 22% de los pacientes con dengue33. Estudios realizados en niños con dengue, se ha detectado proteinuria en 12% de ellos, aún en ausencia de alteración de la función renal. En estos casos, la proteinuria no estaba asociada al descenso de plaquetas ni la hemoconcentración del hematocrito2. Sin embargo, otros investigadores han encontrado clara asociación entre proteinuria, plaquetopenia y formas graves de dengue2,33,34.
Por los glomérulos no sólo se filtra albúmina, sino otras moléculas como transferrina, antitrombina y glucosaminoglicanos34. Algunos autores han observado casos con rango nefrótico que se asocian a nefropatía IgA confirmada por estudios histopatológicos, debido a una glomerulonefritis por depósito de inmunocomplejos circulantes33. Otra investigación demostró la alteración en el glicocálix de las células endoteliales glomerulares en el aumento de la permeabilidad34.
Afortunadamente, no se vio que la proteinuria se relacione con deterioro severo de la función renal ni tampoco con la persistencia en un tiempo superior a 28 días33. La resolución de proteinurias severas se debería a la autolimitación de la infección, al escaso aumento de los inmunocomplejos circulantes y/o a la eliminación renal de los mismos18.
Afectación del sistema nervioso central
La prevalencia de afectación neurológica varía entre 0,5-6%35.La neuropatogénesis36,37 incluye diversos mecanismos:
- Por alteración metabólica, produciendo encefalopatía. Intervendrían el edema cerebral, el choque hipovolémico, la hemorragia cerebral, la anoxia, los trastornos electrolíticos y la encefalopatía hepática. En la encefalopatía por dengue no existe invasión viral directa del sistema nervioso38,39.
- Por invasión viral, manifestándose como encefalitis, meningitis, mielitis. Para el diagnóstico de encefalitis se requiere la presencia de cuadro clínico compatible con dengue, la presencia de partículas virales (NS1) o anticuerpos IgM en líquido cefalorraquídeo y la exclusión de otras etiologías36.
- Por reacción autoinmune, originando síndrome de Guillain Barré, neuritis óptica, neuromielitis óptica o mielitis aguda, síndrome opsoclono-mioclono35.
- También existen cuadros post dengue: amnesia, temblores, psicosis maniaca, demencia, epilepsia, síndrome de Reye39.
La reemergencia del dengue debe alertar a los profesionales de la salud ante cualquier cuadro neurológico, aún en ausencia de fiebre o cuadro clásico del mismo35,39,40. Así, un estudio de 209 cuadros de meningitis y encefalomielitis realizado en Brasil, halló al dengue como responsable de estos casos en 3,8%41.
Afectación pulmonarClínicamente, la manifestación torácica más frecuente es el derrame pleural por fuga capilar. Pero la afectación parenquimatosa pulmonar es la hemorragia intra alveolar, que se manifiesta por infiltrados pulmonares tipo consolidación neumónica. Los hallazgos necrópsicos muestran neumonía intersticial asociada a congestión alveolar localizada o difusa, aumento del número de macrófagos, linfocitos y plaquetas19. Afortunadamente es rara la hemorragia pulmonar masiva asociada a plaquetopenia y choque42,43. La hemoptisis se describe en 1,4% de los pacientes con dengue19.
En el endotelio vascular, en los macrófagos del parénquima pulmonar y en los monocitos circulando en los vasos pulmonares también se han detectado partículas del ARN viral utilizando técnicas de inmunohistoquímica e hibridización in situ. Esto demuestra que el antígeno viral es posiblemente secuestrado por pinocitosis por numerosas células parenquimatosas, que no pertenecen al sistema reticuloendotelial10.
Afectación del músculo esquelético
Las mialgias son muy frecuentes en el dengue. Un estudio que evaluó a 39 pacientes de una epidemia en 2010 encontró media de CPK de 837 U/L, electromiografía con potenciales motores de corta duración en algunos casos y la biopsia muscular en tres de ellos mostró hemorragia intersticial con necrosis y miofagocitosis, sin evidencia de vasculitis. Toda esta serie mejoró espontáneamente en 15 días44.
La elevación de las enzimas musculares es un predictor de dengue, aún sin fiebre ni mialgias. Su valor predictivo positivo fue 84% y valor predictivo negativo fue 98% en una serie de pacientes con dengue, aunque esta elevación no predice la severidad de la miositis. Esta afectación se debe a la replicación viral en las fibras musculares y al efecto miotóxico del Factor de necrosis tumoral que se libera en gran cantidad durante esta infección. En ocasiones la mioglobinuria por rabdomiólisis ocasiona falla renal aguda15,37. La asociación entre miositis y miocarditis por dengue severo ya fue descrita en muchas epidemias45. La rabdomiólisis debe sospecharse ante la presencia de gran debilidad muscular y orina oscura15.
Muchas veces la causa de la debilidad muscular es la hipokalemia46. Las causas de este trastorno electrolítico incluyen a la pérdida por vía digestiva, la afectación tubular renal con pérdida aumentada por orina y el aumento de las catecolaminas que inducen el ingreso del potasio a las células35,47.
La gravedad de estos órganos dañados es muy variable y no existen factores predictores conocidos de severidad. Se cree que infecciones previas con otros serotipos del virus predisponen a una gran liberación de citoquinas que persisten en la memoria inmunológica11. Podrían también intervenir comorbilidades como la diabetes mellitus, hipertensión arterial, desnutrición, obesidad, edades extremas de la vida y otros estados de inmunosupresión.
El propósito de este estudio fue investigar el daño de diversos órganos ocurrido durante una epidemia de dengue por serotipo 2 en el verano del 2012-2013 en el Paraguay, de modo a alertar a los profesionales de la salud sobre la afectación extravascular que muchas veces pasa desapercibida.
OBJETIVOS
Describir las características demográficas de pacientes con dengue
Determinar la afectación sistémica del dengue, sobre todo en hígado, riñón, corazón y músculo esquelético
Correlacionar la afectación sistémica del dengue con las manifestaciones de fuga capilar
MATERIAL Y METODOS
Diseño: estudio observacional, descriptivo, prospectivo, de corte transverso
Población de estudio: varones y mujeres, mayores de edad, internados por dengue en el Dpto. de Medicina Interna del Hospital Nacional entre diciembre 2012 y mayo 2013.
Criterios de inclusión: dengue confirmado por antígeno NS1 y/o serología IgM
Muestreo: no probabilístico, de casos consecutivos
Variables: demográficas (edad, sexo, procedencia) y clínicas (datos laboratoriales, radiográficos, ecográficos y electrocardiográficos). Todos los datos clínicos se obtuvieron en el periodo crítico o postfebril. La hemoconcentración de la hemoglobina se calculó utilizando el mayor y el menor valor obtenidos durante la internación, expresándose en porcentaje. Se consideró hemoconcentración significativa si sobrepasaba el 20%. Se procedió de la misma manera para calcular la hemoconcentración del hematocrito17,48,49.
Reclutamiento: los pacientes que ingresaban con fiebre y sospecha de dengue eran recibidos en la sala de Urgencias del Hospital Nacional. Según el tiempo de duración de la fiebre eran sometidos al test NS1 o IgM para dengue. Al mismo tiempo eran clasificados según su gravedad, presencia de comorbilidades o de síntomas de alarma en tres grupos4,50. Los pacientes estables y sin comorbilidades (grupo 1) recibían tratamiento ambulatorio. Los que presentaban comorbilidades o signos de alarma (grupo 2) quedaban internados para hidratación parenteral y proseguir con estudios laboratoriales y de imágenes. Los pacientes muy graves (grupo 3) eran rápidamente remitidos a sala de reanimación o terapia intensiva. Todos eran tratados según el protocolo de hidratación sugerido en la Guía de Manejo Clínico 2012 del MSP y BS/OPS14. Los pacientes del grupo 2, una vez estabilizados, eran trasferidos a una sala de contingencias del Departamento de Medicina Interna, donde se continuaban los estudios y tratamiento. La muestra se extrajo de esta sala.
Cálculo de tamaño de muestra: se utilizó el programa estadístico Epi Info©. Para una prevalencia esperada de 60% de afectación hepática23, precisión 6%, intervalo de confianza 95%, el tamaño mínimo calculado fue 196 sujetos.
Gestión de datos: las variables fueron registradas en fichas técnicas y trascriptas a planilla electrónica por los autores. Los cálculos estadísticos se realizaron con el programa Epi Info©. Las variables nominales se expresaron en porcentajes y las cuantitativas en medias ± DS. Para el análisis bivariado se utilizó la prueba Chi2 para comparar las variables nominales. Se consideró significativa toda p<0,05.
Aspectos éticos: se respetaron los Principios de la Bioética. Se mantuvo la confidencialidad de los sujetos. No se requirió consentimiento informado por tratarse de un estudio observacional.
RESULTADOS
Ingresaron al estudio 202 sujetos, con edad media 43±19 años y leve predominio del sexo masculino (50,5%). La mayoría procedía de ciudades circunvecinas: Itauguá (22%), Capiatá (14%), Itá (13%), JA Saldívar (11%), Ypacaraí (8%), San Lorenzo (6%), Asunción (5%) y otras (21%). Las comorbilidades estaban presentes en 77 casos, siendo las principales la hipertensión arterial (66%), diabetes mellitus e hipertensión arterial (14%), diabetes mellitus (6%) y edad añosa (6%).
El hemograma al ingreso se caracterizó por leucocitos con una mediana de 3.300/mm3 (rango 1.100-10.900/mm3), plaquetas con una mediana de 40.000/mm3 (rango 4.000-306.000/mm3), hemoglobina con una media de 15±1,8 g/dL y hematocrito con una media de 43,9±5,3 %.
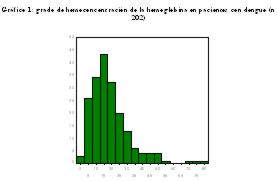
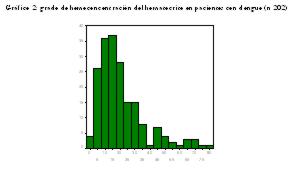
El nivel medio del grado de hemoconcentración de la hemoglobina fue 18,8±13,9 % (gráfico 1) y el nivel medio del grado de hemoconcentración del hematocrito fue 19,9 ±15,4 % (gráfico 2). Estableciendo 20% como punto de corte para considerarla significativa, se detectó que 34% y 37% de los pacientes estaban gravemente hemoconcentrados según la hemoglobina y hematocrito, respectivamente.Gráfico 1
En relación a la afectación hepática, por ecografía se halló hepatomegalia en 36 de 100 sujetos (36%), edema de pared vesicular en 46 de 84 sujetos (54,8%), ascitis en 46 de 84 sujetos (54,8%). En 188 sujetos se obtuvieron hepatogramas completos y la mediana de GOT fue 143 UI/L (rango 22-4128 UI/L), la mediana de GPT fue 88 UI/L (rango 11-1829 UI/L), la mediana de LDH fue 378 UI/L (rango 5,5-1332 UI/L), la media de bilirrubina total fue 0,9 ±0,8 mg/dL, el tiempo medio de protrombina fue 89±23% y la media de la albuminemia fue 2,9±0,5 mg/dL. Considerando al aumento de las enzimas hepáticas por 10 veces el valor normal como indicativo de daño hepático severo, los hallazgos corresponden a 10,1% de hepatitis y 85,6% a transaminitis. Sólo 4,3% no presentaron alteración del hepatograma.
<Las enzimas musculares se dosaron en 106 sujetos, encontrándose valores de CPK total aumentados en 32 sujetos (30%), con valor medio de 464±423 mg/dL. La CPKmb se medió en 89 pacientes y estaba aumentada en 34 sujetos (38%), con valor medio de 58±93 mg/dL. El dímero D no pudo determinarse en muchos pacientes pues no formaba parte del protocolo aplicado. Aún así, si se considera la relación CPKmb/CPK total >5%, la misma se halló elevada en 48% de los casos. Se practicó electrocardiograma a 93 pacientes, hallándose alteraciones en 21 de ellos (22,5%). Estas alteraciones electrocardiográficas fueron: bradicardia sinusal (8,3%), bloqueo auriculoventricular de primer grado (7,4%), intervalo QT prolongado (5,6%), síndrome PR corto (4,3%). En ningún caso se observó alteración significativa del segmento ST. Como medida de afectación renal se midió la proteinuria de 24 hs en 54 pacientes, encontrándose un valor medio de 926 ±1105 mg/día (rango 13 - 5000 mg/día). Al considerar un valor normal hasta 160 mg/día y rango nefrótico a partir de >2 g/día, la proteinuria se pudo considerar normal en 11 casos (20,4%), proteinuria elevada en 38 casos (70,4%) y rango nefrótico en 5 casos (9,3%). Entre los pacientes con rango nefrótico, sólo uno tenía comorbilidad: hipertensión arterial. Ningún paciente presentó alteración significativa del clearance de creatinina. Los pacientes con insuficiencia renal crónica estaban excluidos de esta investigación. Correlacionando la proteinuria con la albuminemia, no se obtuvo un valor significativo (r +0,03).
La afectación neurológica se caracterizó por dos casos de síndrome de Guillain Barré, confirmados por electromiografía y tratados exitosamente con inmunoglobulina intravenosa.
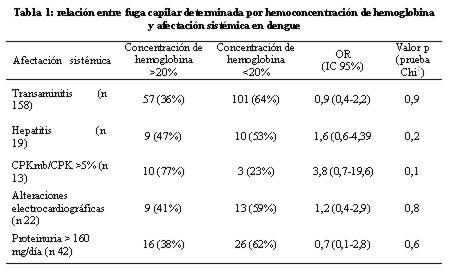
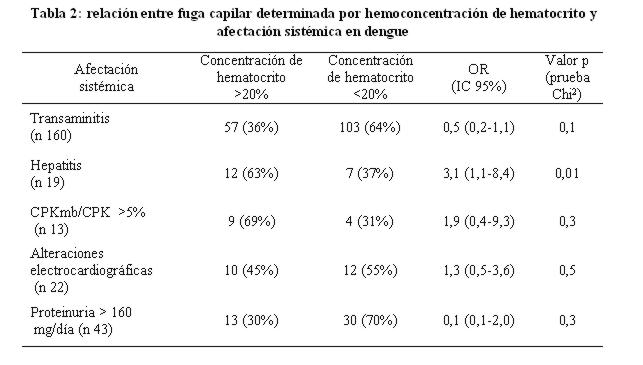
El grado de fuga capilar fue determinado por el nivel de hemoconcentración de la hemoglobina y del hematocrito, considerándose significativa toda proporción ≥ 20%. Se relacionó esos niveles de hemoconcentración con el daño de algunos órganos. La presencia de hepatitis se relacionó significativamente con la hemoconcentración del hematocrito >20% (tablas 1 y 2).
El tiempo medio de internación fue 5±2 días. El alta era rápida aún en pacientes con alguna afectación sistémica pues había gran demanda de camas durante el brote epidémico, los pacientes se hallaban estables y solicitaban su alta. El seguimiento ambulatorio post alta fue muy escaso pues los pacientes no volvían a control. Ningún paciente presentó hemorragia severa, tampoco hubo óbitos en esta muestra.
DISCUSIÓN
Las características demográficas de esta muestra resultan inusuales pues el dengue afecta en Sudamérica con más frecuencia a las mujeres, debido al hábito domiciliario del vector51.
Los hallazgos en el hemograma son usuales en el dengue, a tal punto que constituyen claves para sospechar dengue en todo paciente que ingresa por fiebre, sobre todo en periodos epidémicos2,4,18. La hemoconcentración significativa (>20%) de la hemoglobina y del hematocrito afectaba al tercio de los pacientes, lo que indica que los criterios clínicos de gravedad y que sugieren la necesidad de internación, estaban bien aplicados en la clasificación utilizada al ingreso en la sala de urgencias en los pacientes febriles4,50. La elevada frecuencia de afectación hepática detectada por la ecografía y el hepatograma en esta muestra coincide con los hallazgos citados por otros autores21,24. Afortunadamente, las alteraciones enzimáticas detectadas han sido transitorias, aunque se observó un caso de hepatitis fulminante, no incluido en esta serie52. En regiones epidémicas, la aparición de casos clínicos compatibles con hepatitis deben incluir en el diagnóstico diferencial al dengue53.
La alta proporción de derrames en espacios virtuales se debe a que la fuga capilar es inicialmente focal y ocurre principalmente en espacio pleural y peritoneal11. Más de la mitad de nuestros pacientes presentaban ascitis, mientras que sólo un tercio tenía hemoconcentración significativa de la hemoglobina y del hematocrito, otra manera de detectar la fuga capilar. Esta discordancia demostraría que la ecografía es más útil en detectar este fenómeno vascular, tema que debería ser investigado en epidemias futuras.
Las enzimas CPK total y mb se encontraron elevadas en más tercio de esta muestra. Si bien estas determinaciones no indican necesariamente daño miocárdico sino también daño muscular esquelético, la elevada proporción (48%) de la relación CPKmb/CPK total >5% es sugestiva de las miocarditis. Misra UK observó en una epidemia de dengue una media de CPK de 837 UI/L, con rango entre 194 - 383244.
NO se dispuso que estos pacientes sean sometidos a determinación de las troponinas ni ecocardiografías pues se hallaban asintomáticos ni tenían clínica sugestiva de insuficiencia cardiaca. Esta afectación miocárdica también es otro tema que debería investigarse con protocolos especialmente diseñados para detectar miocarditis por dengue26,28,29.
Las alteraciones electrocardiográficas coinciden con las descritas por otros autores. Si bien 36% de estos sujetos eran portadores de hipertensión arterial, los hallazgos descritos no son los característicos ni atribuibles a esta enfermedad. Aún así, debería seguirse la evolución de estos hallazgos electrocardiográficos pues, si bien fueron asintomáticos, habría que demostrar que son transitorios, como mencionan otros autores26. La frecuencia de afectación electrocardiográfica observada en una epidemia in Sri Lanka fue 62%54.
La falta de signos electrocardiográficos de infarto de miocardio y la rápida recuperación de nuestros pacientes son muy sugestivos de una miocarditis. El aumento de las enzimas cardiacas que se ha observado es común a ambas patologías. Desafortunadamente no se dispuso de ecocardiografía, centellografía o coronariografía para llegar al diagnóstico certero de esta elevación enzimática específica del músculo cardiaco. Cuando se sospecha o confirma daño miocárdico se debe tener más cuidado en la infusión de fluidos, para evitar desencadenar edema agudo de pulmón26.
El electrocardiograma es un método ampliamente usado en el diagnóstico de miocarditis a pesar de su baja sensibilidad o muchos falsos positivos. Los hallazgos más comunes son los cambios en ST y T, aparición de onda Q o nuevos bloqueos32. Los biomarcadores (creatinquinasas y troponinas) tienen baja especificidad, es decir, presenta muchos falsos negativos. La ecocardiografía no muestra signos característicos pero ayuda a descartar otras causas. La biopsia endomiocárdica sigue siendo el gold estándar pero es un método invasivo y no disponible en todos los medios hospitalarios.
En cuanto a la recuperación, se ha visto que formas severas de miocarditis pero sin afectación hemodinámica tienen muy buen pronóstico y sin secuelas32. Las manifestaciones cardiacas del dengue pueden además jugar un rol en la patogenia del shock y pueden influir en el desenlace de esta enfermedad29.
La proteinuria fue observada por otros autores en muchos casos de dengue, aún sin evidencia de afectación renal, en ocasiones hasta en 15-37%46. La presencia y severidad de la microalbuminuria ha sido postulada como factor de riesgo potencial de un dengue severo, aunque hay poca información de la magnitud, tiempo de inicio y evolución de este fenómeno durante la infección2. Sería interesante incorporar un test de detección sensible y específico de proteínas en orina en todo paciente con sospecha de dengue33,34. Es más, sería recomendable la medición del complemento y biopsia renal en casos de síndrome nefrótico, para demostrar glomerulonefritis asociadas al dengue18.
Sería interesante para próximos estudios tratar de demostrar el hecho de que sucesivas infecciones por otros serotipos de dengue desencadenan formas graves y multisistémicas4,11,27.
Es importante reconocer los signos de alarma para actuar con presteza y limitar el daño multiorgánico15. No es posible distinguir clínicamente a los pacientes con dengue que desarrollarán complicaciones graves como el choque hipovolémico y las hemorragias severas, como así tampoco predecir quiénes presentarán afectación sistémica27. Por todo ello, es importante ampliar el protocolo de estudios del paciente con dengue para detectar afectación sistémica silente y seguirla en el tiempo, para evitar o minimizar futuras complicaciones orgánicas. Hasta tanto no se disponga de una vacuna efectiva contra el dengue55, la prevención será siempre el pilar fundamental contra esta enfermedad que no respeta edad, sexo ni condición socioeconómica.
CONCLUSIONES
El dengue de esta muestra se caracterizó por afectar con igual proporción a varones y mujeres, con edad media 43±19 años, proceder de áreas circunvecinas y presentar como principales comorbilidades a la hipertensión arterial y diabetes mellitus.
Las afectaciones sistémicas detectadas fueron: 10,1% de hepatitis, 85,6% de transaminitis, 48% con relación CPKmb/CPK total >5%, 22,5% de alteraciones electrocardiográficas, 70,4% con proteinuria de 24 hs elevada y 9,3% con proteinuria en rango nefrótico.
La hemoconcentración de la hemoglobina >20% y del hematocrito >20% se encontró en 34% y 37%, respectivamente. Al correlacionar la afectación sistémica del dengue con estas manifestaciones de fuga capilar, sólo la hepatitis se asoció significativamente a la hemoconcentración del hematocrito (OR 3,1 IC 95% 1,1-8,4 p 0,01).
REFERENCIAS
1. Simmons CP, Farrar JJ, Nguyen vV, Wills B. Dengue. N Engl J Med. 2012 Apr 12; 366(15): 1423-32 [ Links ]
2. Hanh Tien NT, Lam PK, Duyen HT, Ngoc TV, Ha PT, Kieu NT, Simmons C, Wolbers M, Wills B. Assessment of microalbuminuria for early diagnosis and risk prediction in dengue infections. PLoS One. 2013;8(1):e54538. [ Links ]
3. Wang SM, Sekaran SD. Evaluation of a commercial SD dengue virus NS1 antigen capture enzyme-linked immunosorbent assay kit for early diagnosis of dengue virus infection. J Clin Microbiol. 2010 Aug;48(8):2793-7 [ Links ]
4. Tang KF, Ooi EE. Diagnosis of dengue: an update. Expert Rev Anti Infect Ther. 2012 Aug;10(8):895-907. [ Links ]
5. Bäck AT, Lundkvist A. Dengue viruses: an overview. Infect Ecol Epidemiol. 2013 Aug 30;3. [ Links ]
6. Bisordi I, Rocco IM, Suzuki A, Katz G, Silveira VR, Maeda AY et al. Evaluation of dengue NS1 antigen detection for diagnosis in public health laboratories, São Paulo State, 2009. Rev Inst Med Trop Sao Paulo. 2011 Nov-Dec;53(6):315-20. [ Links ]
7. Pan-Ngum W, Blacksell SD, Lubell Y, Pukrittayakamee S, Bailey MS, de Silva HJ et al. Estimating the true accuracy of diagnostic tests for dengue infection using bayesian latent class models. PLoS One. 2013;8(1):e50765. [ Links ]
8. Fry SR, Meyer M, Semple MG, Simmons CP, Sekaran SD, Huang JX, McElnea C et al. The diagnostic sensitivity of dengue rapid test assays is significantly enhanced by using a combined antigen and antibody testing approach. PLoS Negl Trop Dis. 2011 Jun;5(6):e1199. [ Links ]
9. Gowri Sankar S, Dhananjeyan KJ, Paramasivan R, Thenmozhi V, Tyagi BK, John Vennison S. Evaluation and use of NS1 IgM antibody detection for acute dengue virus diagnosis: report from an outbreak investigation. Clin Microbiol Infect. 2012 Jan;18(1):E8-10. [ Links ]
10. Jessie K, Fong MY, Devi S, Lam SK, Wong KT. Localization of dengue virus in naturally infected human tissues, by immunohistochemistry and in situ hybridization. J Infect Dis. 2004 Apr 15;189(8):1411-8. [ Links ]
11. Patkar C, Giaya K, Libraty DH. Dengue virus type 2 modulates endothelial barrier function through CD73. Am J Trop Med Hyg. 2013 Jan;88(1):89-94. [ Links ]
12. Basu A, Chaturvedi UC. Vascular endothelium: the battlefield of dengue viruses. FEMS Immunol Med Microbiol. 2008 Aug;53(3):287-99. [ Links ]
13. Lin CF, Chiu SC, Hsiao YL, Wan SW, Lei HY, Shiau AL et al. Expression of cytokine, chemokine, and adhesion molecules during endothelial cell activation induced by antibodies against dengue virus nonstructural protein 1. J Immunol. 2005 Jan 1;174(1):395-403. [ Links ]
14. Ministerio de Salud Pública y Bienestar Social. Dirección General de Vigilancia de la Salud. Dengue: guía de Manejo Clínico 2012. Disponible en http://www.mspbs.gov.py/documentacion/Dengue_guia_2012.pdf [ Links ]
15. Karakus A, Banga N, Voorn GP, Meinders AJ. Dengue shock syndrome and rhabdomyolysis. Neth J Med. 2007 Feb;65(2):78-81. [ Links ]
16. Shashidhara KC, Murthy KA, Gowdappa HB, Bhograj A. Effect of high dose of steroid on platelet count in acute stage of dengue fever with thrombocytopenia. J Clin Diagn Res. 2013 Jul;7(7):1397-400. [ Links ]
17. Thein TL, Gan VC, Lye DC, Yung CF, Leo YS. Utilities and limitations of the World Health Organization 2009 warning signs for adult dengue severity. PLoS Negl Trop Dis. 2013;7(1):e2023. [ Links ]
18. Vasanwala FF, Puvanendran R, Ng JM, Suhail SM. Two cases of self-limiting nephropathies secondary to dengue haemorrhagic fever. Singapore Med J. 2009 Jul;50(7):e253-5. [ Links ]
19. Marchiori E, Ferreira JL, Bittencourt CN, de Araújo Neto CA, Zanetti G, Mano CM, Santos AA, Vianna AD. Pulmonary hemorrhage syndrome associated with dengue fever, high-resolution computed tomography findings: a case report. Orphanet J Rare Dis. 2009 Mar 5;4:8. [ Links ]
20. Souza LJ, Boulos M. Clinical experience in dengue: experience of specialized service. Rev Inst Med Trop Sao Paulo. 2012 Oct;54 Suppl 18:S7-9. [ Links ]
21. Valero CN, Reyes VI, Larreal EY, Maldonado EM. Aminotransferases serum levels in patients with Dengue type 3. Rev Med Chil. 2007 Oct;135(10):1304-12. [ Links ]
22. Viswanathan S, Iqbal N, Anemon PP, Kumar GS. Fatal fulminant hepatic failure in a diabetic with primary dengue. J Trop Med. 2010;2010: 413561 [ Links ]
23. Souza LJ, Alves JG, Nogueira RM, Gicovate Neto C, Bastos DA, Siqueira EW et al. Aminotransferase changes and acute hepatitis in patients with dengue fever: analysis of 1,585 cases. Braz J Infect Dis. 2004 Apr;8(2):156-63. [ Links ]
24. Tristão-Sá R, Kubelka CF, Zandonade E, Zagne SM, Rocha Nde S, Zagne LO et al. Clinical and hepatic evaluation in adult dengue patients: a prospective two-month cohort study. Rev Soc Bras Med Trop. 2012 Dec;45(6):675-81. [ Links ]
25. Paes MV, Lenzi HL, Nogueira AC, Nuovo GJ, Pinhão AT, Mota EM et al. Hepatic damage associated with dengue-2 virus replication in liver cells of BALB/c mice. Lab Invest. 2009 Oct;89(10):1140-51 [ Links ]
26. Lee IK, Lee WH, Liu JW, Yang KD. Acute myocarditis in dengue hemorrhagic fever: a case report and review of cardiac complications in dengue-affected patients. Int J Infect Dis. 2010 Oct;14(10):e919-22. [ Links ]
27. Pesaro AE, D'Amico E, Aranha LF. Dengue: cardiac manifestations and implications in antithrombotic treatment. Arq Bras Cardiol. 2007 Aug;89(2):e12-5. [ Links ]
28. Lateef A, Fisher DA, Tambyah PA. Dengue and relative bradycardia. Emerg Infect Dis. 2007 Apr;13(4):650-1. [ Links ]
29. Kaushik JS, Gupta P, Rajpal S, Bhatt S. Spontaneous resolution of sinoatrial exit block and atrioventricular dissociation in a child with dengue fever. Singapore Med J. 2010 Sep;51(9):e146-8. [ Links ]
30. Khongphatthallayothin A, Chotivitayatarakorn P, Somchit S, Mitprasart A, Sakolsattayadorn S, Thisyakorn C. Morbitz type I second degree AV block during recovery from dengue hemorrhagic fever. Southeast Asian J Trop Med Public Health. 2000 Dec;31(4):642-5. [ Links ]
31. Ibarrola D, Paredes G, Zarza A, Torales N, Escalada G, Cabral L. Miocarditis por dengue. A propósito de un caso. Revista CONAREC 2012;3(05 ): 401 -403 [ Links ]
32. Kindermann I, Barth C, Mahfoud F, Ukena C, Lenski M, Yilmaz A et al. Update on myocarditis. J Am Coll Cardiol. 2012 Feb 28;59(9):779-92. [ Links ]
33. Vasanwala FF, Puvanendran R, Fook-Chong S, Ng JM, Suhail SM, Lee KH. Could peak proteinuria determine whether patient with dengue fever develop dengue hemorrhagic/dengue shock syndrome?--a prospective cohort study. BMC Infect Dis. 2011 Aug 5;11:212. [ Links ]
34. Wills BA, Oragui EE, Dung NM, Loan HT, Chau NV, Farrar JJ, Levin M. Size and charge characteristics of the protein leak in dengue shock syndrome. J Infect Dis. 2004 Aug 15;190(4):810-8. [ Links ]
35. Verma R, Sharma P, Garg RK, Atam V, Singh MK, Mehrotra HS. Neurological complications of dengue fever: Experience from a tertiary center of north India. Ann Indian Acad Neurol. 2011 Oct;14(4):272-8. [ Links ]
36. Puccioni-Sohler M, Orsini M, Soares CN. Dengue: a new challenge for neurology. Neurol Int. 2012 Oct 5;4(3):e15. [ Links ]
37. Acharya S, Shukla S, Mahajan SN, Diwan SK. Acute dengue myositis with rhabdomyolysis and acute renal failure. Ann Indian Acad Neurol. 2010 Jul;13(3):221-2. [ Links ]
38. Muzaffar J, Venkata Krishnan P, Gupta N, Kar P. Dengue encephalitis: why we need to identify this entity in a dengue-prone region. Singapore Med J. 2006 Nov;47(11):975-7. [ Links ]
39. Kanade T, Shah I. Dengue encephalopathy. J Vector Borne Dis. 2011 Sep;48(3):180-1. [ Links ]
40. Goswami RP, Mukherjee A, Biswas T, Karmakar PS, Ghosh A. Two cases of dengue meningitis: a rare first presentation. J Infect Dev Ctries. 2012 Feb 13;6(2):208-11. [ Links ]
41. Araújo F, Nogueira R, Araújo Mde S, Perdigão A, Cavalcanti L, Brilhante R et al. Dengue in patients with central nervous system manifestations, Brazil. Emerg Infect Dis. 2012 Apr;18(4):677-9. [ Links ]
42. Sharma SK, Gupta BS, Devpura G, Agarwal A, Anand S. Pulmonary haemorrhage syndrome associated with dengue haemorrhagic fever. J Assoc Physicians India. 2007 Oct;55:729-30. [ Links ]
43. Setlik RF, Ouellette D, Morgan J, McAllister CK, Dorsey D, Agan BK et al. Pulmonary hemorrhage syndrome associated with an autochthonous case of dengue hemorrhagic fever. South Med J. 2004 Jul;97(7):688-91. [ Links ]
44. Misra UK, Kalita J, Maurya PK, Kumar P, Shankar SK, Mahadevan A. Dengue-associated transient muscle dysfunction: clinical, electromyography and histopathological changes. Infection. 2012 Apr;40(2):125-30. [ Links ]
45. Sangle SA, Dasgupta A, Ratnalikar SD, Kulkarni RV. Dengue myositis and myocarditis. Neurol India. 2010 Jul-Aug;58(4):598-9. [ Links ]
46. Lumpaopong A, Kaewplang P, Watanaveeradej V, Thirakhupt P, Chamnanvanakij S, Srisuwan K et al. Electrolyte disturbances and abnormal urine analysis in children with dengue infection. Southeast Asian J Trop Med Public Health. 2010 Jan;41(1):72-6. [ Links ]
47. Hira HS, Kaur A, Shukla A. Acute neuromuscular weakness associated with dengue infection. J Neurosci Rural Pract. 2012 Jan;3(1):36-9. [ Links ]
48. Simmons CP, Wolbers M, Nguyen MN, Whitehorn J, Shi PY, Young P et al. Therapeutics for dengue: recommendations for design and conduct of early-phase clinical trials. PLoS Negl Trop Dis. 2012;6(9):e1752 [ Links ]
49. Wolbers M, Kleinschmidt I, Simmons CP, Donnelly CA. Considerations in the design of clinical trials to test novel entomological approaches to dengue control. PLoS Negl Trop Dis. 2012;6(11):e1937. [ Links ]
50. Halstead SB. Dengue: the syndromic basis to pathogenesis research. Inutility of the 2009 WHO case definition. Am J Trop Med Hyg. 2013 Feb;88(2):212-5. [ Links ]
51. Halsey ES, Marks MA, Gotuzzo E, Fiestas V, Suarez L, Vargas J et al. Correlation of serotype-specific dengue virus infection with clinical manifestations. PLoS Negl Trop Dis. 2012;6(5):e1638. [ Links ]
52. Tan SS, Bujang MA. The clinical features and outcomes of acute liver failure associated with dengue infection in adults: a case series. Braz J Infect Dis. 2013 Mar-Apr;17(2):164-9 [ Links ]
53. Agarwal MP, Giri S, Sharma V, Roy U, Gharsangi K. Dengue causing fulminant hepatitis in a hepatitis B virus carrier. Biosci Trends. 2011;5(1):44-5. [ Links ]
54. Kularatne SA, Pathirage MM, Kumarasiri PV, Gunasena S, Mahindawanse SI. Cardiac complications of a dengue fever outbreak in Sri Lanka, 2005. Trans R Soc Trop Med Hyg. 2007 Aug;101(8):804-8. [ Links ]
55. Thomas SJ, Endy TP. Current issues in dengue vaccination. Curr Opin Infect Dis. 2013 Oct;26(5):429-34. [ Links ]
1. Departamento de Medicina Interna, Hospital Nacional, Ministerio de Salud Pública y Bienestar Social (Itauguá, Paraguay)
2. Médico Residente de Medicina Interna, Hospital Nacional, Ministerio de Salud Pública y Bienestar Social (Itauguá, Paraguay)
3. Interno de la Facultad de Ciencias Médicas, Universidad del Pacífico, Asunción (Paraguay)
Artículo recibido: 02 de setiembre de 2013. Artículo aprobado: 25 de octubre de 2013
Correo electrónico: raulemilioreal@yahoo.com.ar