Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista del Nacional (Itauguá)
versión impresa ISSN 2072-8174
Rev. Nac. (Itauguá) v.5 n.1 Itauguá jun. 2013
ARTÍCULO ORIGINAL
Prevalencia y características clínicas de la nefropatía diabética
Prevalence and clinical characteristics of diabetic nephropathy
Edgar Augusto Ortega Filártiga1
RESUMEN
Introdución: entre 20 y 40% de los diabéticos tipo 2 (DM 2) desarrollarán nefropatía diabética a lo largo de la evolución de su enfermedad, dependiendo de factores de riesgo asociados: genéticos, grado de control de la glicemia, tratamiento apropiado de la presión arterial, dislipidemia, tabaquismo, microalbuminuria o su progresión hacia proteinuria manifiesta, todo los cuales marcarán la evolución hacia la nefropatía establecida. Objetivos: determinar la prevalencia de la nefropatía diabética y describir sus características clínicas. Materiales y métodos: diseño observacional descriptivo de corte transverso. Fueron estudiados 148 adultos con DM 2 internados en el Departamento de Urgencias Adultos del Hospital Nacional (Itauguá) desde el 1° de enero de 2012 hasta el 31 de julio de 2012. Muestreo no probabilístico de casos consecutivos. Resultados: la edad media de los pacientes fue 61±11 años, predominó el sexo femenino 77 (52%). Se halló nefropatía en 62 pacientes (42%). La media de la proteinuria de 24 horas fue 904±90 mg y la del clearance de creatinina fue 74±48 ml/min. En cuanto al control metabólico, sólo 13 pacientes (21%) presentaban buen control metabólico. La media de HbA1c fue 10,4±4,3% y la de la glicemia fue 199±72 mg/dL. Los factores de riesgo asociados fueron: hipertensión arterial 53%, dislipidemia 41%, tabaquismo 23%. El filtrado glomerular fue menor a 60 ml/min en 50 pacientes (19%). Conclusiones: la prevalencia de nefropatía diabética fue elevada, se detectó mal control metabólico, elevadas cifras de presión arterial, así como también alto porcentaje de factores de riesgo para desarrollar nefropatía diabética: dislipidemia y tabaquismo. La incidencia de la nefropatía fue aumentando en relación a los años de evolución de la diabetes.
Palabras clave: Diabetes, nefropatía diabética.
ABSTRACT
Introdution: between 20 and 40% of type 2 diabetes (DM2) diabetic nephropathy develop over the course of the illness, depending on risk factors: genetic, degree of glycemic control, appropriate treatment of blood pressure, dyslipidemia, smoking, microalbuminuria or progression to overt proteinuria, all of which mark the evolution to overt nephropathy. Objetives: to determine the prevalence of diabetic nephropathy and describe their clinical characteristics. Materials and methods: descriptive observational design transverse. We studied 148 adults with DM 2 boarding in the Adult Emergency Department National Hospital (Itauguá) from 1 January 2012 to 31 July 2012. Non-probability sampling of consecutive cases. Results: the average age of the patients was 61 ± 11 years, 77 were females (52%). Nephropathy was found in 62 patients (42%). The mean 24-hour proteinuria was 904 ± 90 mg and creatinine clearance was 74±48 ml / min. In terms of metabolic control, only 13 patients (21%) had good metabolic control. The mean HbA1c was 10.4 ± 4.3% and blood glucose level was 199 ± 72 mg / dL. The risk factors were hypertension 53%, dyslipidemia 41%, smoking 23%. Glomerular filtration rate was less than 60 ml / min in 50 patients (19%). Conclusions: the prevalence of diabetic nephropathy was high, was detected poor metabolic control, high blood pressure, as well as high percentage of risk factors for developing diabetic nephropathy: dyslipidemia and smoking. The incidence of nephropathy was increased in relation to years of diabetes evolution.
Keywords: diabetes, debetic nephropathy.
INTRODUCCION
Según datos proporcionados en algunos estudios, entre el 20 al 40% de los diabéticos tipo 2 (DM 2) desarrollarán nefropatía diabética a lo largo de la evolución de su diabetes, dependiendo de la aparición de los factores de riesgo asociados, tales como: factores genéticos, grado de control de la glicemia, tratamiento apropiado de la presión arterial, dislipidemia, tabaquismo, aparición de microalbuminuria o su progresión hacia proteinuria manifiesta, lo que marcará la evolución hacia la nefropatía establecida1.
La enfermedad renal crónica, estadío final de la nefropatía diabética, constituye una de las principales causas de muerte en el mundo industrializado; y los pacientes que presentan proteinuria o una disminución del filtrado glomerular tienen una elevada prevalencia de complicaciones cardiovasculares2,3.
Hace aproximadamente 20 años se describió a la microalbuminuria (excreción de albúmina de 20 a 200 ug/min) como un predictor de nefropatía diabética en pacientes con diabetes mellitus tipo 1 (DM 1)4.
Actualmente existe evidencia suficiente para afirmar que la micro albuminuria no sólo predice la aparición de la nefropatía diabética, sino que constituye el primer signo clínico de daño renal en pacientes con DM 1 y DM2.5,6.
La nefropatía diabética es un síndrome clínico que se caracteriza por la presencia de: albuminuria persistente, aumento de la presión arterial, disminución del filtrado glomerular; asociados a un alto riesgo de morbilidad y mortalidad de causa cardiovascular7.
Prevalencia: la misma se ha incrementado en las dos últimas décadas como consecuencia del mejor abordaje terapéutico de las complicaciones cardiovasculares clásicas de la diabetes (cardiopatía isquémica y arteriopatía periférica), que ha permitido una prolongación en la esperanza de vida y un incremento del número de pacientes que tienen complicaciones más tardías como la nefropatía8.
Aproximadamente dos tercios de los pacientes diabéticos en programas de diálisis periódicas son de tipo 2.9. La prevalencia de la nefropatía diabética en diabéticos tipo 2 es muy variable; en el Reino Unido se han reportado cifras de 5 a 20%, en España 23,5%, en Brasil 37%10-12 . La prevalencia de la nefropatía varía también de acuerdo a diferencias raciales y étnicas; así, es más prevalente entre Afro americanos, asiáticos y Nativos americanos que entre Caucásicos13.
Epidemiología: existen evidencias que demuestran que aproximadamente el 30% de los pacientes con microalbuminuria evolucionarán a macroalbuminuria en el transcurso de 5 a 10 años14. Una vez instalada la macroproteinuria, el clearance de creatinina comienza a disminuir entre 10 a 12 ml/año de no instalarse medidas terapéuticas intensivas. Sin tratamiento, el paciente desarrollará inevitablemente una insuficiencia renal crónica por lo cual deberá ingresar a un plan de hemodiálisis crónica ó transplante renal15 .
La nefropatía diabética aparece en aproximadamente 15 a 40% de los pacientes con diabetes tipo 1 (DM 1) en promedio 15 a 20 años posteriores al diagnóstico de la enfermedad16.
El 20 a 40% de los pacientes con diabetes tipo 2 (DM 2) desarrollarán microalbuminuria 10 a 15 años luego del inicio de la enfermedad. La causa de muerte más frecuente en este grupo de pacientes es la enfermedad cardiovascular17.
Tamizaje: la detección de la nefropatía diabética debe ser llevada a cabo al tiempo del diagnóstico en diabéticos tipo 2 y a los 5 años del diagnóstico en diabéticos tipo 1. Si la microalbuminuria es negativa, la búsqueda debe repetirse anualmente en ambos tipos de pacientes18.
La detección de la nefropatía diabética puede realizarse por 3 métodos:19
- Muestra de orina minutada (normal <20 ug/minuto).
- Determinación del índice albúmina – creatinina en una muestra de orina aislada (normal <30 mg/gr).
- Cuantificando la excreción urinaria de albúmina en orina de 24 hs (normal <30 mg/24 hs).
La microalbuminuria se considerará patológica cuando dos de tres determinaciones consecutivas realizadas en un lapso de 3 a 6 meses sean positivas19.
La detección de la nefropatía diabética no debe realizarse en la presencia de condiciones que incrementan la excreción urinaria de albúmina, tales como: infección de vías urinarias, hematuria, cuadros febriles agudos, ejercicio vigoroso, hiperglicemia pronunciada, hipertensión arterial no controlada, insuficiencia cardíaca20.
Para llegar al diagnóstico de microalbuminuria se requieren valores de 20 a 199 ug/minuto en orina minutada; 30 a 299 mg/gr en orina aislada ó 30 a 299 mg en orina de 24 horas, mientras que para diagnosticar macroalbuminuria se necesitan valores iguales o mayores a 200 ug/minuto en orina minutada, mayores ó iguales a 300 mg/gr en orina de 24 horas.20 La nefropatía diabética establecida se define como la presencia de una proteinuria mayor a 500 mg/24 hs21.
Factores de riesgo: se pueden dividir en: factores de riesgo modificables y no modificables. Dentro de los factores no modificables tenemos: edad, sexo, raza, factores genéticos, peso al nacimiento, etiología de la enfermedad renal, grado de insuficiencia renal al momento del diagnóstico, etc. Los modificables son: mal control metabólico de la glicemia, hipertensión arterial (HTA), proteinuria, tabaquismo, obesidad, dislipidemia, anemia, uso de nefrotóxicos, etc22.
Un estudio llevado a cabo en E.E.U.U. durante 20 años demostró que la edad avanzada, la HTA, la diabetes mal controlada, el tabaquismo actual y el sexo masculino son factores de riesgo independientes para desarrollar nefropatía diabética23.
El estudio MDRD (Modification of Diet in Renal Disease Study) demostró que una mayor excreción de proteínas en la orina, el diagnóstico de poliquistosis renal, menor concentración de transferrina en suero, el aumento de la presión arterial media, la raza negra y el colesterol HDL disminuido predicen una disminución más rápida de la tasa de filtración glomerular24. En otro estudio realizado en España se observó que la función renal al inicio, así como la presión arterial media, el sexo masculino y la proteinuria eran variables independientes predictivas de la progresión a nefropatía diabética25.
En E.E.U.U. existe una tasa mayor de nefropatía diabética en la población de raza negra en comparación con la población de raza blanca. El bajo peso al nacer, con la consiguiente disminución de la reserva glomerular, conllevaría una hipertensión glomerular compensatoria que podría acelerar la evolución hacia la insuficiencia renal26.
Los Indios Pima de Arizona, E.E.U.U., tienen mayor susceptibilidad de desarrollar nefropatía diabética debido a un efecto genético en los cromosomas 3q, 7q, 18q y 20p27. Otros factores que contribuyen a la rápida progresión de la enfermedad renal en los Indios Pima son el volumen glomerular y la densidad de los podocitos. A mayor volumen glomerular y mayor densidad de los podocitos, mayor pérdida del filtrado glomerular28. También pueden existir otras alteraciones genéticas que favorezcan la rápida progresión de la nefropatía diabética: los portadores del genotipo DD del gen de la enzima convertidora de la angiotensina progresan más rápidamente que los portadores de los genotipos II o DI29.
El hábito de fumar y el aumento de la excreción urinaria de albúmina son predictores de nefropatía interrelacionados y favorecen la progresión de la nefropatía diabética en pacientes con diabetes tipo 2 a pesar de mejoría en el control de la presión arterial y la inhibición de la enzima convertidora de la angiotensina (ECA)30. El genotipo Pro/Pro y el tabaquismo fueron factores de riesgo independientes para la nefropatía diabética. Los posibles efectos sinérgicos de genotipo y fumar pueden agravar el estrés oxidativo y contribuir al desarrollo de la nefropatía diabética31.
En pacientes diabéticos tipo 2 con microalbuminuria y hipercolesterolemia, la enfermedad renal tiene un curso acelerado, en particular aquellos que presentan polimorfismo en el genotipo H+/H+ en el locus de la lipoprotein lipasa32.
Tratamiento de la DM: el control glucémico inadecuado se ha asociado con malos resultados en la diabetes. Los primeros estudios observacionales sugieren que un mejor control glucémico puede mejorar los resultados microvasculares en pacientes con diabetes tipo 1 y 2. Desde entonces, los grandes ensayos que evaluaron el efecto del control intensivo de la glucemia en la población diabética, tales como el DCCT (The Diabetes Control and Complications Trial Research Group)33, el UKPDS (UK Prospective Diabetes Study)34 y el estudio Kumamoto35 han aportado pruebas sólidas de que la terapia intensiva reduce la incidencia y progresión de los resultados microvasculares, incluyendo microalbuminuria, un marcador clave precoz de la nefropatía diabética.
El control glucémico influye significativamente en la tasa de progresión de la microalbuminuria a proteinuria y de la nefropatía manifiesta a insuficiencia renal crónica. Aunque los ensayos aleatorios grandes y de largo plazo sobre los efectos de un mejor control metabólico en la progresión de la nefropatía diabética no existen, se describe el concepto de que los períodos muy prolongados de buen control metabólico son necesarios para tener un impacto positivo en la progresión o incluso obtener la regresión de la nefropatía diabética36.
El control intensivo de la glucosa reduce el riesgo de microalbuminuria y macroalbuminuria comparado con el tratamiento convencional, pero no hay pruebas de que el control intensivo de la glucemia reduce el riesgo de resultados clínicos significativos renales, como la duplicación de la creatinina sérica, enfermedad renal terminal o muerte por enfermedad renal37.
Tratamiento de la hipertensión arterial y la proteinuria: la enfermedad cardiovascular es la complicación más costosa de la diabetes y es la responsable del 86% de las defunciones en pacientes con diabetes38. La hipertensión contribuye sustancialmente a la morbilidad y la mortalidad cardiovascular en las personas con diabetes. Por otra parte, la hipertensión y la diabetes son particularmente frecuentes en determinadas poblaciones, como los afroamericanos y nativos americanos39.
Existe suficiente evidencia de que se debe mantener cifras de presión arterial menores a 130/80 mm Hg con el fin de preservar la función renal de manera óptima y reducir los eventos cardiovasculares en personas con nefropatía diabética, y que más del 65% de las personas con diabetes e hipertensión requieren dos o más medicamentos antihipertensivos diferentes para alcanzar la meta de presión arterial sugerida de 130/80 mmHg39,40.
Los inhibidores de la ECA, que competitivamente bloquean el sistema renina-angiotensina, disminuyen la presión capilar glomerular y previenen la progresión de la microalbuminuria a proteinuria franca41. Los resultados de los ensayos clínicos sugieren que los inhibidores de la ECA reducen la pérdida de la función renal en personas con nefropatía diabética, por encima y más allá de cualquier efecto atribuible a una reducción de la presión arterial42,43. Posteriormente, tres estudios examinaron el uso de los bloqueantes de los receptores de la angiotensina II (ARA II) en sujetos con diabetes tipo 2 y nefropatía. Dos estudios evaluaron cohortes con albuminuria abierta y se encontró que los ARA II redujeron el número de pacientes que tuvieron progresión de la insuficiencia renal terminal o la duplicación de la creatinina sérica, independientemente de una reducción de la presión arterial44,45. El tercer estudio evaluó la progresión de microalbuminuria a macroalbuminuria e informó un efecto beneficioso asociado con ARA II, de nuevo de forma independiente de una reducción de la presión arterial46.
Un estudio clínico comparó directamente el efecto de un ARA II (telmisartán) con un inhibidor de la ECA (enalapril) en sujetos con diabetes tipo 2 y nefropatía temprana, que a corto plazo indicó que los dos fármacos redujeron la excreción urinaria de albúmina; y que las diferencias entre ambos fármacos no fueron significativas. Estos datos determinaron que telmisartán no es inferior al enalapril en la prevención de la progresión de la disfunción renal, medido como la disminución de la tasa de filtración glomerular47.
Si bien las drogas de primera línea en el tratamiento de la HTA y la proteinuria son los inhibidores de la ECA y los ARA II, hay otras alternativas en caso de intolerancia a estas drogas o llegado a sus dosis máximas, y entonces aparecen como antihipertensivos de segunda línea los calcio antagonistas (BCC) y diuréticos tiazídicos. El objetivo fundamental es el control de la tensión arterial, independientemente del fármaco utilizado, por lo que no existe un orden de preferencia para elegir el segundo hipotensor en la actualidad48. Los antagonistas de la aldosterona como la espironolactona son superiores a losartán para disminuir la proteinuria, pero producen más hiperpotasemia49. La eplerenona tiene igualmente una acción antiproteinúrica. Se debería limitar su uso en caso de filtrado glomerular menor de 60 ml/minuto con control estricto de los niveles de potasio50.
Recientemente se han publicado estudios que demuestran que la administración conjunta de un inhibidor de la renina- angiotensina (RA) y un BCC inhibe los eventos cardiovasculares en los pacientes no diabéticos, diabéticos y pacientes con enfermedad renal crónica, a diferencia del uso de un inhibidor de la RA más un diurético51,52.
Hace poco se publicó el estudio OLCA, que comparó combinaciones diferentes de ARA II y BCC en pacientes hipertensos no tratados con diabetes. Un grupo recibió olmesartán más azelnidipino (grupo OL) y el otro grupo recibió candesartán más amlodipino (grupo CA). La glucemia en ayunas, HbA1c y los niveles de albúmina urinaria disminuyeron significativamente en el grupo OL pero no en el grupo CA. Esto sugiere que los efectos en el sistema metabólico pueden diferir de acuerdo con la combinación de ARAII y BCC. Los resultados del estudio OLCA indican que, en los pacientes hipertensos complicados con diabetes mellitus, olmesartán en combinación con azelnidipina tiene efectos beneficiosos en términos de control de la presión arterial, el metabolismo de la glucosa y protección renal53.
Recientemente apareció un nuevo fármaco, el aliskiren, que es un inhibidor de la renina activo por vía oral, que se convirtió en el primer fármaco de su clase en recibir la aprobación regulatoria europea para el tratamiento de la hipertensión en 2007. Aliskiren inhibe la primera etapa en la cascada del sistema renina-angiotensina-aldosterona, la conversión de angiotensinógeno a angiotensina I, y de ese modo reduce la síntesis de todos los componentes posteriores de la cascada54 . Se ha demostrado que la reducción de la proteinuria con este bloqueo se asocia con un mejor pronóstico renal y cardiovascular55,56.
El estudio AVOID fue el primer estudio doble ciego, aleatorizado y controlado para demostrar la capacidad antiproteinúrica de aliskiren 300 mg una vez al día como un complemento al tratamiento estándar, incluyendo la dosis recomendada de un ARA II (losartán), en pacientes con diabetes tipo 2, hipertensión y nefropatía. Este estudio demostró que aliskiren como tratamiento añadido a la terapia estándar, incluyendo la dosis óptima del ARA II losartán, redujo la albuminuria y frenó el desarrollo de la disfunción renal más que el placebo en los diferentes niveles de filtrado glomerular en pacientes con diabetes tipo 2, hipertensión y nefropatía. La hiperpotasemia es más frecuente en los pacientes tratados con aliskiren con enfermedad renal crónica estadio 357.
Tratamiento de la dislipidemia: los efectos beneficiosos de las estatinas sobre la morbilidad y mortalidad cardiovascular no se pueden explicar solamente por su efecto sobre la lipoproteína de baja densidad. Los mecanismos no lipídicos que pueden estar involucrados se denominan efectos pleiotrópicos, tales como estabilización de la placa de lípidos, disminución de la inflamación, disminución de la trombogenicidad, el aumento de la distensibilidad arterial y la mejoría de la función endotelial58. Un metaanálisis sobre el tratamiento con estatinas entre los participantes con albuminuria y proteinuria encontró que las estatinas pueden reducir moderadamente la excreción patológica de albúmina dentro de una mediana de 6 meses después del inicio de la terapia59.
Tratamiento multifactorial: en pacientes con DM 2 y microalbuminuria, la intervención multifactorial sobre el estilo de vida, el control intensivo de glucemia y de tensión arterial con inhibidores de la ECA redujo en 50% las complicaciones macro y microvasculares en el grupo de tratamiento intensivo60. Con medidas dietéticas y ejercicio físico regular, insistir en el cese del hábito tabáquico y en la restricción de la ingesta de proteínas a 0,8-1 g/kg/día en estadios iniciales de insuficiencia renal y 0,8 g/kg/día en estadios más avanzados, se consiguen buenos resultados61.
OBJETIVOS
Hallar la prevalencia de la nefropatía diabética en una población de pacientes con diabetes tipo 2 internados en el Departamento de Urgencias Adultos del Hospital Nacional (Itauguá).
Determinar el grado de proteinuria, clearance de creatinina y el control metabólico de los pacientes con nefropatía diabética.
Describir la frecuencia de hipertensión arterial y dislipidemia, así como el tratamiento de los pacientes con nefropatía diabética.
Determinar el estadío de la nefropatía diabética según los años de evolución de la diabetes.
MATERIALES Y METODOS
Diseño: estudio observacional descriptivo de corte transverso.
Población de estudio: varones y mujeres, mayores de edad, portadores de DM 2 internados en el Departamento de Urgencias Adultos del Hospital Nacional (Itauguá) desde el 1º de Enero al 30 de Junio de 2.012.
Criterios de Exclusión:
Pacientes con diagnóstico de diabetes tipo 1.
Pacientes con infección de vías urinarias e insuficiencia cardiaca.
Expedientes clínicos incompletos.
Muestreo: no probabilístico de casos consecutivos.
Variables: edad, sexo; años de evolución de la diabetes, tipo de medicación, glicemia, HbA1c; proteinuria de 24 hs, clearance de creatinina, presencia de factores de riesgo para nefropatía diabética asociados (hipertensión arterial, dislipidemia y tabaquismo).
Instrumentos de medición: expedientes clínicos del Departamento de Urgencias Adultos del Hospital Nacional (Itauguá).
Cuestiones éticas: se respetaron los Principios de la Bioética. Se mantuvo el anonimato de los pacientes.
Definiciones Operacionales:
Diabetes tipo 2: pacientes conocidos diabéticos tipo 2 tratados con dieta, antidiabéticos orales, insulina ó sin tratamiento alguno. Pacientes no conocidos diabéticos tipo 2 con cifras de glicemia basal en dos ó más tomas consecutivas mayores ó iguales a 126 mg/dL; ó prueba de tolerancia oral a la glucosa con cifras de glicemia iguales ó mayores a 200 mg/dl a las 2 horas ó con HbA1c igual o mayor a 6,5%.
Hipertensión arterial: pacientes conocidos hipertensos en tratamiento con dieta ó fármacos antihipertensivos; ó no conocidos hipertensos, con cifras de tensión arterial sistólica (TAS) en decúbito iguales ó mayores a 140 mm/Hg y/ó tensión arterial diastólica (TAD) igual ó mayor a 90 mm/Hg.
Dislipidemia: cifras de colesterol total mayores a 200 mg/dL y triglicéridos superior a 160 mg/dL.
Tabaquismo: aquel que refiere antecedentes de consumo de tabaco (cigarrillos, puros, pipa) hasta 1 año antes de la fecha indicada en el estudio.
Nefropatía diabética establecida: proteinuria mayor ó igual a 500 mg en una muestra de orina de 24 horas.
Microalbuminuria: proteinuria entre 30-300 mg en una muestra de orina de 24 horas.
Normoalbuminuria: proteinuria menor a 30 mg en una muestra de orina de 24 horas.
Buen control metabólico: cifras de HbA1c menores a 7%.
Mal control metabólico: cifras de HbA1c iguales o mayores a 7%.
Análisis de datos: los datos fueron cargados en una planilla Excel 2007 y analizados con el paquete estadístico Epi Info 2000©. Los datos fueron sometidos a estadística descriptiva. Para la descripción de las variables se utilizaron proporciones para las variables cualitativas y media ±DS para las continuas.
RESULTADOS
Fueron estudiados 148 pacientes con diagnóstico de DM 2. La edad media de los pacientes fue de 61±11 años. Eran del sexo femenino 77 (52%) y masculino 71 (48%). Se encontraron 62 pacientes (42%) con nefropatía diabética.
La media de la proteinuria de 24 horas fue de 904±90 mg y el clearance de creatinina fue de 74±48 ml/min.
La media de la HbA1c fue de 10,4±4,3%. La media de la glicemia fue de 199±72 mg/dL.
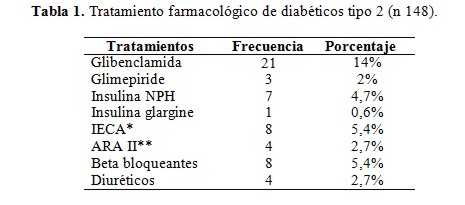
De acuerdo al tratamiento que recibían estos pacientes previamente a la internación, se encontró que 21 pacientes (35%) estaban tratados con glibenclamida. Se diagnosticó diabetes a 11 pacientes (17%) durante su internación y, por consiguiente, no estaban tratados (ver tabla 1).
Tabla 1. Tratamiento farmacologico de diabéticos tipo 2 (n 148)
En cuanto al control metabólico, 13 pacientes (21%) presentaban buen control metabólico y 49 pacientes (79%) con mal control metabólico. Presentaban HTA 33 pacientes (53%), predominando la HTA en estadío 2: 42 (54%). En cuanto al tratamiento de la HTA, la mayoría (27%) estaban sin tratamiento. Ninguno estaba tratado con 2 o más antihipertensivos (ver tabla 1).
Presentaron dislipidemia 25 pacientes (41%), predominado las formas mixtas: 14 pacientes (56%). Eran tabaquistas 14 pacientes (23%).
Se encontró a 12 pacientes con un filtrado glomerular menor a 60 ml/min (19%), y 50 pacientes con filtrado glomerular mayor a 60 ml/min.
Se dividió a los pacientes en 4 grupos teniendo como parámetro principal a la duración de la diabetes, tratando de correlacionarla con el grado de nefropatía que presentaban y se constató lo siguiente:
Diabéticos de reciente diagnóstico: en este grupo se encontraban 24 pacientes. Presentaron nefropatía diabética 2 pacientes (8%) y sin nefropatía diabética 22 pacientes (92%).
Diabéticos de menos de 5 años de evolución: en este grupo habían 55 pacientes. Presentaron nefropatía diabética 17 pacientes (31%) y sin nefropatía diabética 38 pacientes (69%).
Diabéticos de 6 a 10 años de evolución: en este grupo se hallaban 39 pacientes: con nefropatía diabética 23 pacientes (59%) y sin nefropatía 16 pacientes (41%).
Diabéticos de más de 10 años de evolución: a este grupo pertenecían 30 pacientes: con nefropatía diabética 20 pacientes (67%) y sin nefropatía 10 pacientes (33%).
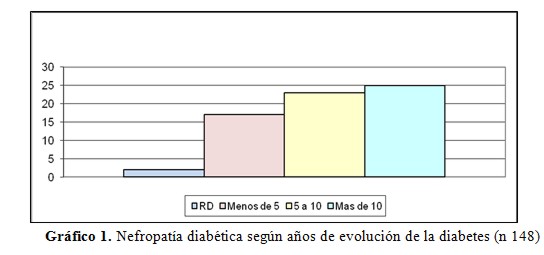
La prevalencia de nefropatía diabética fue aumentando en forma proporcional a los años de evolución de la diabetes (ver gráfico 1).
Grafico 1. Nefropatía Diabetica según años de evolución de la diabetes (n 148)
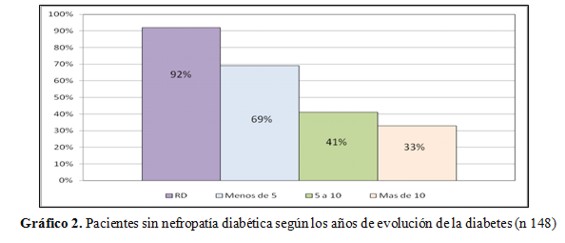
Inversamente, el porcentaje de pacientes diabéticos sin nefropatía fue disminuyendo en forma inversamente proporcional a los años de evolución de la diabetes (ver gráfico 2).
Grafico 2. Pacientes sin Nefropatía diabética según los años de evolucion de la diabetes (n 148)
DISCUSION
El presente trabajo demuestra que entre los pacientes diabéticos tipo 2 internados en el Departamento de Urgencias Adultos del Hospital Nacional existe una elevada prevalencia de casos de nefropatía diabética (42%), expresada por proteinuria importante en la muestra de orina de 24 horas. Esta cifra es superior a la encontrada en otros países10-12.
También se encontró una importante cantidad de pacientes con factores de riesgo: HTA, dislipidemia y tabaquismo, que sumados al mal control metabólico, pudieron contribuir a la elevada frecuencia de nefropatía diabética que presentaban estos pacientes durante su internación. Se sabe que el tratamiento de estos factores de riesgo, modificables con un tratamiento apropiado, con una intervención intensificada multifactorial tratando apropiadamente la hiperglucemia, la HTA, la dislipidemia y la microalbuminuria, se puede retrasar significativamente la progresión de la nefropatía diabética60.
Al constatar cifras medias de HbA1c elevadas se puede afirmar que el control metabólico de los pacientes estudiados es malo, lo cual coincide con lo reportado en la literatura, que aquellos pacientes con un mal control glicémico, desarrollan nefropatía precozmente, ya que los criterios de control glicémico de la Asociación Americana de Diabetes recomiendan en los diabéticos tipo 2 una HbA1c menor a 7% como control aceptable61.
El mal control metabólico de los pacientes estudiados podría deberse a que el 16% de ellos no se conocían diabéticos, y por consiguiente, no estaban tratados; además, el 31% de los que se conocían diabéticos no recibían ningún tipo de tratamiento, dietético ni farmacológico.
También es importante mencionar que más de la mitad de los pacientes estudiados eran hipertensos, y a su vez, más de la mitad de ellos tenían HTA estadío 2. Estas cifras de presión arterial elevada se pueden atribuir a que el 33% de estos pacientes estaban sin tratamiento, y ninguno de ellos estaban tratados con 2 o más antihipertensivos. Las guías apuntan a mantener la presión arterial menor a 130/80 en pacientes diabéticos hipertensos, y más de la mitad de ellos necesitan 2 o más fármacos antihipertensivos para llegar a esta meta39,40.
Los IECA y los ARA II son señalados en varios estudios como los más eficaces para retrasar la progresión de la enfermedad renal en los pacientes con nefropatía diabética incipiente o establecida, sugiriéndose su indicación como agentes de primera línea41-47. En los pacientes estudiados, ambos fueron utilizados solamente por pocos sujetos, lo que también podría justificar la elevada prevalencia de nefropatía diabética encontrada.
Al agrupar a los pacientes de acuerdo a los años de evolución de la diabetes se puede observar un ascenso progresivo en el porcentaje de pacientes con nefropatía diabética a medida que aumentan los años de evolución de la enfermedad, evolución similar, aunque más acentuada, como la encontrada en el estudio UKPDS10.
Inversamente a lo que ocurre con la nefropatía diabética, los pacientes sin nefropatía diabética se presentan con mayor frecuencia en los diabéticos recientemente diagnosticados, y van disminuyendo su frecuencia acorde a los años de evolución de la diabetes, evolución similar también, aunque más acentuada a la hallada el estudio UKPDS10.
En comparación con otros estudios descriptos en la literatura, realizados en el Reino Unido, España y Brasil,10-12 los pacientes estudiados en nuestra serie presentaron mayor prevalencia de nefropatía diabética y las cifras de HbA1c fueron mayores, si bien la frecuencia de HTA y dislipidemia fueron menores en comparación a estos estudios.
La edad de los pacientes estudiados fue mayor que en el Reino Unido y Brasil, pero menor que en España. La nefropatía fue más frecuente en hombres en el Reino Unido. Las cifras de tabaquismo fueron mayores que en España.
CONCLUSIONES
Los pacientes diabéticos internados en el Departamento de Urgencias Adultos del Hospital Nacional presentan un elevada prevalencia de nefropatía diabética, mal control metabólico, así como también un elevado porcentaje de factores de riesgo para desarrollar nefropatía diabética, tales como: dislipidemia y tabaquismo.
La prevalencia de la nefropatía fue aumentando en relación a los años de evolución de la diabetes.
REFERENCIAS
1. Martínez-Castelao A, De Álvaro F, Górriz JL. Epidemiology of Diabetic Nephropathy in Spain. Kidney Int 2005; 68(99): S20-S24. [ Links ]
2. Levin A, Djurdjev O, Barrett B, Burgess E, Carlisle E, Ethier J et al. Cardiovascular disease in patients with chronic kidney disease: getting to the heart of the matter. Am J Kidney Dis 2001 Dec; 38(6): 1398-407. [ Links ]
3. Collins AJ, Li S, Gilbertson DT, Chen SC, Herzog CA. Chronic kidney disease and cardiovascular disease in the Medicare population. Kidney Int Suppl. 2003 Nov; 64 (87): S24-S31. [ Links ]
4. Mogensen CE, Christensen CK. Predicting diabetic nephropathy in insulin-dependent patients. N Engl J Med. 1984 Jul 12; 311(2): 89-93. [ Links ]
5. Fioretto P, Steffes MW, Mauer M. Glomerular structure in nonproteinuric IDDM patients with various levels of albuminuria. Diabetes. 1994 Nov; 43(11): 1358-64. [ Links ]
6. Ruggenenti P, Remuzzi G. The diagnosis of renal involvement in non-insulin-dependent diabetes mellitus. Curr Opin Nephrol Hypertens. 1997 Mar; 6(2): 141-5. [ Links ]
7. Parving HH. Diabetic nephropathy: prevention and treatment. Kidney Int. 2001; 60(5): 2041-55. [ Links ]
8. Ritz E, Stefanski A. Diabetic nephropathy in type II diabetes. Am J Kidney Dis. 1996 Feb; 27(2): 167-94. [ Links ]
9. Collins AJ, Foley RN, Herzog C, Chavers BM, Gilbertson D, Ishani A et al. Excerpts from the US Renal Data System 2009 Annual Data Report. Am J Kidney Dis. 2010 Jan; 55(Suppl 1): S1-420 [ Links ]
10. Adler AI, Stevens RJ, Manley SE, Bilous RW, Cull CA, Holman RR; UKPDS GROUP. Development and progression of nephropathy in type 2 diabetes: the United Kingdom Prospective Diabetes Study (UKPDS 64). Kidney Int. 2003 Jan; 63(1): 225-32. [ Links ]
11. Marín R, Coca A, Tranche S, Rodríguez Mañas L, Abellán J, Moyá A. Prevalence of renal involvement in a population of type Ii diabetics followed up in primary care. Nefrologia. 2002; 22(2): 152-61. [ Links ]
12. Scheffel RS, Bortolanza D, Weber CS, Costa LA, Canani LH, Santos KG et al. Prevalence of micro and macroangiopatic chronic complications and their risk factors in the care of out patients with type 2 diabetes mellitus. Rev Assoc Med Bras. 2004 Jul-Sep; 50(3): 263-7. [ Links ]
13. Young BA, Maynard C, Boyko EJ. Racial differences in diabetic nephropathy, cardiovascular disease, and mortality in a national population of veterans. Diabetes Care. 2003 Aug; 26(8): 2392-9. [ Links ]
14. Ritz E, Orth SR. Nephropathy in patients with type 2 diabetes mellitus. N Engl J Med. 1999 Oct 7; 341(15): 1127-33. [ Links ]
15. Hovind P, Tarnow L, Rossing P, Jensen BR, Graae M, Torp I. Predictors for the development of microalbuminuria and macroalbuminuria in patients with type 1 diabetes: inception cohort study. BMJ. 2004 May 8; 328(7448): 1105 [ Links ]
16. Valmadrid CT, Klein R, Moss SE, Klein BE. The risk of cardiovascular disease mortality associated with microalbuminuria and gross proteinuria in persons with older-onset diabetes mellitus. Arch Intern Med. 2000 Apr 24; 160(8): 1093-100. [ Links ]
17. Molitch ME, DeFronzo RA, Franz MJ, Keane WF, Mogensen CE, Parving HH, Steffes MW. Nephropathy in diabetes. Diabetes Care. 2004 Jan; 27 Suppl 1: S79-83. [ Links ]
18. Mogensen CE, Vestbo E, Poulsen PL, Christiansen C, Damsgaard EM, Eiskjaer H et al. Microalbuminuria and potential confounders. A review and some observations on variability of urinary albumin excretion. Diabetes Care. 1995 Apr; 18(4): 572-81. [ Links ]
19. Kramer H, Molitch ME. Screening for kidney disease in adults with diabetes. Diabetes Care. 2005 Jul; 28(7): 1813-6. [ Links ]
20. Gross JL, de Azevedo MJ, Silveiro SP, Canani LH, Caramori ML, Zelmanovitz T. Diabetic nephropathy: diagnosis, prevention, and treatment. Diabetes Care. 2005 Jan; 28(1): 164-76 [ Links ]
21. García de Vinuesa S. Progression factors for chronic kidney disease. Secondary prevention. Nefrologia. 2008; 28 Suppl 3: 17-21. [ Links ]
22. Samaranayaka S, Gulliford MC. Trends in cardiovascular risk factors among people with diabetes in a population based study, Health Survey for England 1994-2009. Prim Care Diabetes. 2013 May 16. pii: S1751-9918(13)00051-X [ Links ]
23. Haroun MK, Jaar BG, Hoffman SC, Comstock GW, Klag MJ, Coresh J. Risk factors for chronic kidney disease: a prospective study of 23,534 men and women in Washington County, Maryland. J Am Soc Nephrol. 2003 Nov; 14(11): 2934-41. [ Links ]
24. Hunsicker LG, Adler S, Caggiula A, England BK, Greene T, Kusek JW et al. Predictors of the progression of renal disease in the Modification of Diet in Renal Disease Study. Kidney Int. 1997 Jun; 51(6): 1908-19. [ Links ]
25. Luño J, Garcia de Vinuesa S, Gomez-Campdera F, Lorenzo I, Valderrábano F. Effects of antihypertensive therapy on progression of diabetic nephropathy. Kidney Int Suppl. 1998 Dec; 68: S112-9. [ Links ]
26. Hsu CY, Lin F, Vittinghoff E, Shlipak MG. Racial differences in the progression from chronic renal insufficiency to end-stage renal disease in the United States. J Am Soc Nephrol. 2003 Nov; 14(11): 2902-7. [ Links ]
27. Imperatore G, Knowler WC, Nelson RG, Hanson RL. Genetics of diabetic nephropathy in the Pima Indians. Curr Diab Rep. 2001 Dec; 1(3): 275-81. [ Links ]
28. Lemley KV. A basis for accelerated progression of diabetic nephropathy in Pima Indians. Kidney Int Suppl 2003; (83): S38-S42. [ Links ]
29. Jacobsen P, Tarnow L, Carstensen B, Hovind P, Poirier O, Parving HH. Genetic variation in the Renin-Angiotensin system and progression of diabetic nephropathy. J Am Soc Nephrol. 2003 Nov; 14(11): 2843-50. [ Links ]
30. Chuahirun T, Khanna A, Kimball K, Wesson DE. Cigarette smoking and increased urine albumin excretion are interrelated predictors of nephropathy progression in type 2 diabetes. Am J Kidney Dis. 2003 Jan; 41(1): 13-21. [ Links ]
31. Liu L, Zheng T, Wang F, Wang N, Song Y, Li M, Li L, Jiang J, Zhao W. Pro12Ala polymorphism in the PPARG gene contributes to the development of diabetic nephropathy in Chinese type 2 diabetic patients. Diabetes Care. 2010 Jan; 33(1): 144-9. [ Links ]
32. Solini A, Passaro A, Fioretto P, Nannipieri M, Ferrannini E. Lipoprotein lipase gene variants and progression of nephropathy in hypercholesterolaemic patients with type 2 diabetes. J Intern Med. 2004 Jul; 256(1): 30-6. [ Links ]
33. The Diabetes Control and Complications Trial Research Group. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus. N Engl J Med. 1993 Sep 30; 329(14): 977-86 [ Links ]
34. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). UK Prospective Diabetes Study (UKPDS) Group. Lancet. 1998 Sep 12; 352(9131): 837-53. [ Links ]
35. Ohkubo Y, Kishikawa H, Araki E, Miyata T, Isami S, Motoyoshi S et al. Intensive insulin therapy prevents the progression of diabetic microvascular complications in Japanese patients with non-insulin-dependent diabetes mellitus: a randomized prospective 6-year study. Diabetes Res Clin Pract. 1995 May; 28(2): 103-17. [ Links ]
36. Fioretto P, Bruseghin M, Berto I, Gallina P, Manzato E, Mussap M. Renal protection in diabetes: role of glycemic control. J Am Soc Nephrol. 2006 Apr; 17(4 Suppl 2): S86-9. [ Links ]
37. Coca SG, Ismail-Beigi F, Haq N, Krumholz HM, Parikh CR. Role of intensive glucose control in development of renal end points in type 2 diabetes mellitus: systematic review and meta-analysis intensive glucose control in type 2 diabetes. Arch Intern Med. 2012 May 28; 172(10): 761-9. [ Links ]
38. Arauz-Pacheco C, Parrott MA, Raskin P. The treatment of hypertension in adult patients with diabetes. Diabetes Care. 2002 Jan; 25(1): 134-47. [ Links ]
39. Bakris GL, Williams M, Dworkin L, Elliott WJ, Epstein M, Toto R et al. Preserving renal function in adults with hypertension and diabetes: a consensus approach. National Kidney Foundation Hypertension and Diabetes Executive Committees Working Group. Am J Kidney Dis. 2000 Sep; 36(3): 646-61. [ Links ]
40. Chobanian AV, Bakris GL, Black HR, Cushman WC, Green LA, Izzo JL Jr et al. The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure: the JNC 7 report. JAMA. 2003 May 21; 289(19): 2560-72. [ Links ]
41. Brown NJ, Vaughan DE. Angiotensin-converting enzyme inhibitors. Circulation. 1998 Apr 14; 97(14): 1411-20. [ Links ]
42. Lewis EJ, Hunsicker LG, Bain RP, Rohde RD. The effect of angiotensin-converting-enzyme inhibition on diabetic nephropathy. The Collaborative Study Group. N Engl J Med. 1993 Nov 11; 329(20): 1456-62. [ Links ]
43. Ravid M, Savin H, Jutrin I, Bental T, Katz B, Lishner M. Long-term stabilizing effect of angiotensin-converting enzyme inhibition on plasma creatinine and on proteinuria in normotensive type II diabetic patients. Ann Intern Med. 1993 Apr 15; 118(8): 577-81. [ Links ]
44. Brenner BM, Cooper ME, de Zeeuw D, Keane WF, Mitch WE, Parving HH et al. Effects of losartan on renal and cardiovascular outcomes in patients with type 2 diabetes and nephropathy. N Engl J Med. 2001 Sep 20; 345(12): 861-9. [ Links ]
45. Lewis EJ, Hunsicker LG, Clarke WR, Berl T, Pohl MA, Lewis JB et al. Renoprotective effect of the angiotensin-receptor antagonist irbesartan in patients with nephropathy due to type 2 diabetes. N Engl J Med. 2001 Sep 20; 345(12): 851-60. [ Links ]
46. Parving HH, Lehnert H, Bröchner-Mortensen J, Gomis R, Andersen S, Arner P. The effect of irbesartan on the development of diabetic nephropathy in patients with type 2 diabetes. N Engl J Med. 2001 Sep 20; 345(12): 870-8. [ Links ]
47. Barnett AH, Bain SC, Bouter P, Karlberg B, Madsbad S, Jervell J. Angiotensin-receptor blockade versus converting-enzyme inhibition in type 2 diabetes and nephropathy. N Engl J Med. 2004 Nov 4; 351(19): 1952-61. [ Links ]
48. Mancia G, Laurent S, Agabiti-Rosei E, Ambrosioni E, Burnier M, Caulfield MJ et al. Reappraisal of European guidelines on hypertension management: a European Society of Hypertension Task Force document. J Hypertens. 2009 Nov; 27(11): 2121-58. [ Links ]
49. Mehdi UF, Adams-Huet B, Raskin P, Vega GL, Toto RD. Addition of angiotensin receptor blockade or mineralocorticoid antagonism to maximal angiotensin-converting enzyme inhibition in diabetic nephropathy. J Am Soc Nephrol. 2009 Dec; 20(12): 2641-50. [ Links ]
50. Epstein M, Williams GH, Weinberger M, Lewin A, Krause S, Mukherjee R et al. Selective aldosterone blockade with eplerenone reduces albuminuria in patients with type 2 diabetes. Clin J Am Soc Nephrol. 2006 Sep; 1(5): 940-51. [ Links ]
51. Jamerson K, Weber MA, Bakris GL, Dahlöf B, Pitt B, Shi V et al. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients. N Engl J Med. 2008 Dec 4; 359(23): 2417-28. [ Links ]
52. Weber MA, Bakris GL, Jamerson K, Weir M, Kjeldsen SE, Devereux RB et al. Cardiovascular events during differing hypertension therapies in patients with diabetes. J Am Coll Cardiol. 2010 Jun 29; 56(1): 77-85. [ Links ]
53. Daikuhara H, Kikuchi F, Ishida T. The combination of OLmesartan and a CAlcium channel blocker (azelnidipine) or candesartan and a calcium channel blocker (amlodipine) in type 2 diabetic hypertensive patients: the OLCA study. Diab Vasc Dis Res. 2012 Oct; 9(4): 280-6. [ Links ]
54. Staessen JA, Li Y, Richart T. Oral renin inhibitors. Lancet. 2006 Oct 21; 368(9545): 1449-56. [ Links ]
55. de Zeeuw D, Remuzzi G, Parving HH, Keane WF, Zhang Z, Shahinfar S et al. Proteinuria, a target for renoprotection in patients with type 2 diabetic nephropathy: lessons from RENAAL. Kidney Int. 2004 Jun; 65(6): 2309-20. [ Links ]
56. de Zeeuw D, Remuzzi G, Parving HH, Keane WF, Zhang Z, Shahinfar S et al. Albuminuria, a therapeutic target for cardiovascular protection in type 2 diabetic patients with nephropathy. Circulation. 2004 Aug 24; 110(8): 921-7. [ Links ]
57. Persson F, Lewis JB, Lewis EJ, Rossing P, Hollenberg NK, Parving HH. Impact of baseline renal function on the efficacy and safety of aliskiren added to losartan in patients with type 2 diabetes and nephropathy. Diabetes Care. 2010 Nov; 33(11): 2304-9. [ Links ]
58. Davignon J. Beneficial cardiovascular pleiotropic effects of statins. Circulation. 2004 Jun 15; 109(23 Suppl 1): 39-43. [ Links ]
59. Douglas K, O'Malley PG, Jackson JL. Meta-analysis: the effect of statins on albuminuria. Ann Intern Med. 2006 Jul 18; 145(2): 117-24. [ Links ]
60. Gaede P, Vedel P, Larsen N, Jensen GV, Parving HH, Pedersen O. Multifactorial intervention and cardiovascular disease in patients with type 2 diabetes. N Engl J Med. 2003 Jan 30; 348(5): 383-93. [ Links ]
61. American Diabetes Association. Standards of medical care in diabetes 2012. Diabetes Care. 2012 Jan; 35 Suppl 1: S11-63. [ Links ]
1Dr. Edgar Augusto Ortega Filártiga, Departamento de Urgencias Adultos, Hospital Nacional, Ministerio de salud Pública y Bienestar Social (Itauguá, Paraguay)
Artículo Recibido: 28 de noviembre de 2012. Artículo Aprobado: 24 de mayo de 2013
Correo electrónico: edgortegafila@gmail.com