INTRODUCCION
La escleroterapia es un procedimiento utilizado para tratar los vasos sanguíneos o las malformaciones vasculares y también las del sistema linfático. Se inyecta un medicamento en los vasos, lo que los hace encogerse. Se usa para niños y adultos jóvenes con malformaciones vasculares o linfáticas. En los adultos, la escleroterapia a menudo se usa para tratar las venas varicosas y las hemorroides 1.
Así mismo tanto quistes de epidídimo, abdominales, testiculares, ováricos, hepáticos, cerebrales y renales, entre otros, han sido tratados mediante la inyección de diversas sustancias con la propiedad de producir esclerosis, retracción y obliteración de las paredes del quiste logrando así su involución y evitando su recidiva 1-6. Asimismo, estas sustancias han sido también utilizadas para sellar várices de miembros inferiores, malformaciones linfáticas y venosas, hemorroides, várices esofágicas y linfoceles por la capacidad de generar esclerosis y oclusión de los vasos sanguíneos o linfáticos 7-9.
La esclerosis se caracteriza por la destrucción celular epitelial con apoptosis, inflamación estéril, fibrosis irreversible y disminución de la masa tisular por retracción con subsecuente obliteración de la luz de los quistes y/o vasos sanguíneos y la formación de trombo intravascular, denominado esclerotrombo, que sella la circulación 10-12.
Existen 3 grupos de sustancias esclerosantes: Los esclerosantes osmóticos como la solución salina al 30% o la solución dextro/sal hipertónica, que producen lisis de las células epiteliales por deshidratación 10-12. Los esclerosantes químicos irritantes como alcohol absoluto (etanol al 98%), el glicerol cromado y la iodina poliodinatada, que producen destrucción celular y necrosis por citotoxicidad; y los esclerosantes detergentes como el polidocanol (tetradecilsulfato de sodio al 3%), etanolamina y el clorhidrato de lapidium que interactúan con los lípidos de la membrana de las células epiteliales, produciendo la lisis celular por disminución de la tensión superficial resultando en esclerosis, retracción tisular y obliteración de los quistes y vasos sanguíneos 10-12.
En terapia fetal se ha intentado la inyección de alcohol absoluto, como estrategia terapéutica sencilla y económica, en casos de tumores fetales, tumores placentarios, secuestro pulmonar extralobar y gemelos acardios complicados con hidropesía 13-16. Los resultados de la escleroterapia percutánea con alcohol no han sido muy alentadores y se ha comunicado la muerte fetal post inyección de etanol en múltiples reportes 14-15. Los resultados reportados sugieren que el alcohol absoluto no representa una sustancia segura para ser usada en fetos. En contraste, nosotros y otros autores hemos comunicado múltiples casos exitosos de escleroterapia percutánea en casos de secuestro pulmonar intralobar y malformación adenomatoidea quística pulmonar mediante la inyección de polidocanol o etanolamina, sin muerte ni otras complicaciones fetales reportadas, con buenos resultados perinatales 17-20.
Las diferencias de los resultados publicados hacen pensar que la escleroterapia no es una técnica riesgosa si se escoge el esclerosante adecuado.
El objetivo de este estudio es determinar la efectividad y seguridad del Polidocanol versus alcohol absoluto como sustancia esclerosante.
MATERIALES Y MÉTODOS
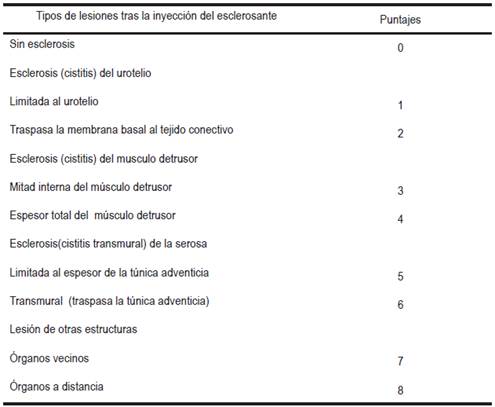
Previa aprobación por el Comité de Bioética de la Unidad de Perinatología del Hospital Universitario de Caracas, se planificó el estudio con 34 ratas Sprague-Dawley adultas hembras de 8 a 9 semanas. Se conformaron 3 grupos en forma aleatoria. Dos grupos experimentales y un grupo control con dos ratas. Grupo A: experimental con polidocanol, de los cuales 12 muestras fueron procesadas. Grupo B: experimental con alcohol absoluto, de los cuales 14 muestras fueron procesadas. Grupo C: control sin tratamiento. Cada rata fue sometida a anestesia general inhalatoria con halotano en cámara cerrada. Luego se realizó la cateterización vesical transuretral con sonda de 1,5 French de grosor. Después del vaciamiento urinario, se introdujo en la vejiga 1 ml. de solución de polidocanol en cada rata del grupo A y 1 ml de alcohol absoluto en cada rata del grupo B. Todas las ratas de cada grupo experimental fueron sacrificadas por pares escogidos al azar con sobredosis de halotano a las 12, 24, 48, 72, 96 y 120 horas respectivamente. Asimismo las 2 ratas del grupo control fueron sacrificadas según el protocolo. Se efectuó la autopsia de cada animal, con disección y estudio anatomopatológico. Se realizó el estudio macroscópico de las vías urinarias y de la cavidad toraco-abdominal de cada rata. Las ratas del grupo control fueron utilizadas para estandarizar los criterios de normalidad histológica, tamaño y grosor vesical. En las ratas de los grupos experimentales se registró el tamaño, los cambios en las paredes y en la luz de las vejigas. Se verificó la existencia de lesiones transmurales de órganos contiguos y de órganos distantes. Se tomaron las muestras para el análisis histológico. Los especímenes fueron fijados en buffer de formalina al 5% por 24 horas y luego fueron deshidratadas y embebidas en parafina. Se realizaron cortes histológicos del bloque de parafina de 4 micras y se realizó tinción con hematoxilina-eosina. Los cortes fueron revisados y documentados y se le adjudicó a cada caso un puntaje según la profundidad y extensión de los cambios histológicos de la esclerosis usando una escala numérica previamente diseñada para la clasificación, según los resultados obtenidos de la profundidad de las lesiones en los análisis de anatomía patológica, se detalla en la Tabla 1. Se tabularon los resultados según el puntaje obtenido en cada rata en hoja de Excel. Se determinó y comparó la eficacia de ambos esclerosantes según la capacidad de producir esclerosis vesical después de 24 horas de su aplicación. Mediante regresión logística se obtuvo el coeficiente de correlación entre el tiempo de acción y la profundidad de las lesiones producidas para cada esclerosante. Se determinó y comparó la seguridad de ambos esclerosantes según la aparición de lesiones transmurales, de órganos contiguos y/o la aparición de lesiones en órganos distantes por diseminación del esclerosante vía sanguínea y/o linfática. Se utilizó el test exacto de Fisher para comparar la profundidad de las lesiones y se estableció una p < 0.05 como significancia estadística y un CI del 95%. El análisis estadístico descriptivo se efectuó con el programa Statgraphics stadistical graphics system, versión 6.1.
RESULTADOS
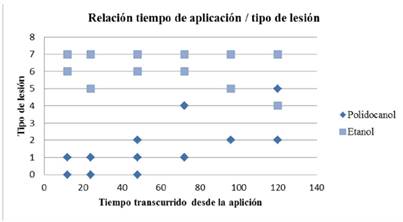
Los resultados de la acción de cada esclerosante según el tiempo de exposición se sintetizan en el Gráfico 1. Tanto el polidocanol como el alcohol fueron efectivos para producir esclerosis vesical. Ambas sustancias produjeron esclerosis caracterizada por descamación del urotelio, infiltrado de polimorfonucleares neutrófilos, áreas de hemorragia, retracción de las paredes vesicales con obliteración parcial en 100% de los casos sin diferencias estadísticas después de 24 horas de aplicación.
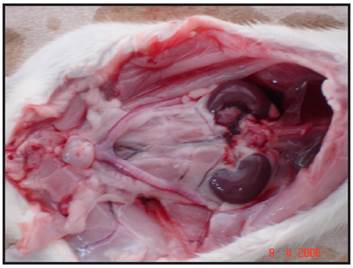
En el Grupo A, el polidocanol produjo esclerosis progresiva según el tiempo que transcurrió desde su aplicación, con coeficiente de correlación de 0.75, con un índice de probabilidad del 0.00183 con una p < 0.05 (Gráfico 2). En el Grupo B, el alcohol produjo esclerosis transmural en 83,34% de los casos, independientemente del tiempo de aplicación, con coeficiente de correlación de - 0.0465 e índice de probabilidad de 0.864 y p > 0.05 (Gráfico 3). En ningún caso del Grupo A (0%) se evidenció esclerosis extravesical, independientemente del tiempo de exposición mientras que en 83,33% de los casos del grupo B, el alcohol absoluto produjo esclerosis transmural y lesión de órganos contiguos (peritoneo, intestino, hígado, estómago, bazo y diafragma) en 50% de los casos. Al comparar la ocurrencia de lesiones transmurales y de órganos vecinos originadas por ambos esclerosantes con el test exacto de Fisher se obtuvo valor de p < 0.0001 con IC 95 % (Figura 1).
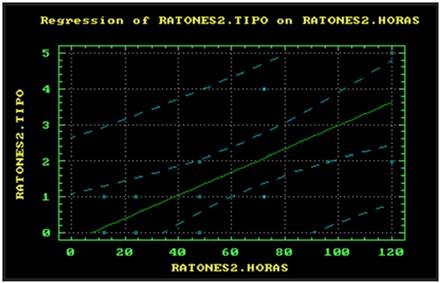
Gráfico 2. Análisis de regresión para el efecto del polidocanol según el tiempo de aplicación con coeficiente de correlación de 0.75 e índice de probabilidad de 0.00183 con p < 0.05.
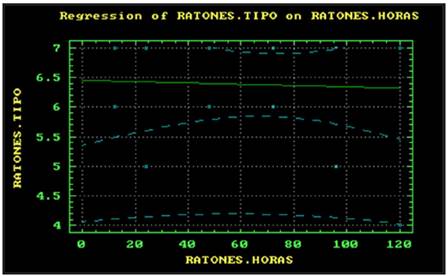
Gráfico 3. Análisis de regresión para el efecto del alcohol según el tiempo de aplicación con coeficiente de correlación de - 0.0465 e índice de probabilidad de 0.864 con p > 0.05
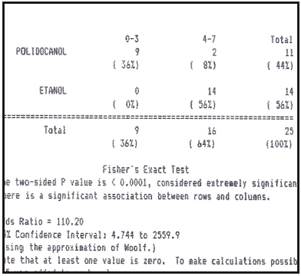
Figura 1. Seguridad de los esclerosantes establecida por el paso transmural de las sustancias con lesión de órganos vecinos y comparadas con test exacto de Fisher.
Con ninguna de las sustancias ocurrió migración del esclerosante ni lesión de órganos distantes independientemente del tiempo de aplicación.
DISCUSION
Los resultados demuestran que tanto el polidocanol como el alcohol absoluto son efectivos y produjeron esclerosis en nuestro modelo experimental animal, en las vejigas de las ratas después de 24 horas de su aplicación en 100% de los casos.
El polidocanol produjo esclerosis progresiva según el tiempo de acción y en ningún caso (0%) se presentaron lesiones transmurales de órganos contiguos, por lo cual parece ser una sustancia segura que limitó su acción biológica al sitio de aplicación en la totalidad de los casos. Adicionalmente, el polidocanol, como otros esclerosantes detergentes, no persiste en el tiempo porque es desactivado y consumido por la actividad celular 21 lo cual potencia su seguridad.
El alcohol absoluto se comportó de forma diferente al polidocanol. El alcohol produjo esclerosis transmural en 83,34% de los casos y se evidenciaron lesiones y necrosis de intestino, hígado, bazo y diafragma en 50% de los casos, independientemente del tiempo de aplicación, por lo cual el alcohol absoluto parece ser una sustancia peligrosa para ser utilizada como esclerosante en terapia fetal.
Ninguna de las 2 sustancias produjo lesiones en órganos distantes independientemente del tiempo transcurrido desde su colocación. Los esclerosantes producen daño endotelial vascular, retracción fibrótica y obliteración de los vasos sanguíneos y linfáticos 12. Los esclerosantes también inducen la formación de un esclerotrombo intravascular que ocluye los vasos imposibilitando su diseminación vía linfática o sanguínea 12, Por estos motivos parece improbable que los esclerosantes puedan migrar y producir lesiones a órganos distantes a través de estas vías. Sin embargo hay repostes de complicaciones severas con algunos esclerosantes con base alcohólica 22.
CONCLUSION
En nuestro modelo animal, tanto el polidocanol como el alcohol absoluto son sustancias efectivas para producir esclerosis. El polidocanol parece una sustancia segura ya que en todos los casos la acción biológica quedó limitada a la vejiga e independientemente del tiempo de exposición no se presentaron lesiones transmurales de órganos adyacentes. El alcohol absoluto no parece ser una sustancia segura porque produjo esclerosis transmural y de órganos contiguos. El riesgo de que los esclerosantes puedan diseminarse y ocasionar lesiones en órganos distantes parece improbable, ya que producen esclerosis, obliteración y oclusión trombótica de los vasos sanguíneos y linfáticos, lo cual imposibilita la migración de la sustancia a distancia.