Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Anales de la Facultad de Ciencias Médicas (Asunción)
Print version ISSN 1816-8949
An. Fac. Cienc. Méd. (Asunción) vol.48 no.1 Asunción June 2015
https://doi.org/10.18004/anales/2015.048(01)41-048
ARTÍCULO ORIGINAL
Efecto agudo de moringa oleífera sobre la hiperglucemia inducida por dexametasona en ratas Wistar
Moringa oleifera acute effect on dexamethasone-induced hyperglycemia in Wistar rats
Barreto S, Báez S, Malvetti V, Cardozo M, Gill A, Matto J, Mercado P, Ramirez R, Santa Cruz F.
Cátedra de Fisiopatología. Facultad de Ciencias Médicas. Universidad Nacional de Asunción.
RESUMEN
INTRODUCCIÓN: Se han atribuido muchos efectos beneficiosos a la moringa oleífera en varias publicaciones siendo de gran interés su efecto hipoglicemiante por disminución de la absorción intestinal de glucosa, aunque no está definido si su eficacia hipoglicemiante sería igual o mayor a algún hipoglicemiante oral conocido. El objetivo del presente estudio fue determinar el efecto agudo de moringa oleífera en hiperglucemia inducida por dexametasona en ratas Wistar hembras, así como comparar su efecto hipoglicemiante con la metformina. MATERIALES Y MÉTODOS: Estudio experimental, tres grupos de cinco ratas Wistar hembras, con peso de 188 ± 11 gramos. Se realizó la medición de la glucemia basal con glucómetro, después de 12 horas de ayuno, la inicial al principio del experimento, luego fueron tratadas con dexametasona 10 mg/kg/día, subcutánea, durante 10 días y se tomó la glicemia post dexametasona . Los días 11 a 14, recibieron el grupo 1 (suero fisiológico), grupo 2 (moringa oleífera 300 mg/kg/día) y grupo 3 (metformina 14,28 mg/kp/día), por sonda oro gástrica, el día 15 se tomó la glucemia post tratamiento. Se analizó el promedio, desviación estándar y la correlación mediante la prueba la prueba T de Student, se consideró P < a 0,05 como significativa. RESULTADOS: Grupo 1 (control): glucemia inicial (117 ± 21 mg/dl), post- dexametasona (445 ± 260 mg/dl) y post tratamiento (222 ± 5 mg/dL), Grupo 2 (moringa oleífera): glucemia inicial (95±27 mg/dl), post dexametasona (413 ± 184 mg/dl) y post tratamiento (102 ± 18 mg/dl) y del Grupo 3 (metformina): glucemia inicial (110 ± 5 mg/dl), post-dexametasona (470 ± 146 mg/dl) y post tratamiento (88 ± 11 mg/dL). La glucemia pos tratamiento mostró diferencias entre el grupo 1 y 2 (p < 0,0001), entre el grupo 1 y 3 (p < 0,0001) no hallándose diferencias entre los grupos moringa oleífera y metformina (p = 0,1). DISCUSIÓN: la moringa oleífera disminuye en forma aguda la hiperglucemia inducida por dexametasona en ratas hembras Wistar, con la misma eficacia que la metformina
Palabras clave: moringa oleífera, hiperglicemia, ratas Wistar, mefformina.
ABSTRACT
INTRODUCTION: It has been attributed many beneficial effects of moringa oleífera in various publications to be of great interest for its hypoglycemic effect due to decreased intestinal absorption of glucose; although it is not defined if his hypoglycemic efficacy would be equal to or greater than any known oral hypoglycemic agent. The objective of this study was to determine the acute effect of moringa oleífera on hyperclycemia induced by dexamethasone in female Wistar rats and compare its hypoglycemic effect with metformin. MATERIALS AND METHODS: Experimental study, wiht 3 groups of 5 female Wistar rats, weighing 188 ± 11 grams. Measuring the basal blood glucose meter was performed after 12 hours of fasting, the initial glycemia at the beginning of the experiment and were then treated with dexamethasone 10 mg / kg / day subcutaneously for 10 days, and post dexamethasone glycemia was taken. On 11 to 14, received the group 1 (normal saline), group 2 (moringa oleífera 300 mg / kg / day) and group 3 (14.28 mg metformin / kp / day) orally by gastric tube the day 15 became final analysis of fasting blood glucose, the post treatment glycemia. The mean, standard deviation and correlation test was analyzed by Student's t test, it was considered P <0.05 as significant. RESULTS: Group 1 (control group): initial glycemia (117 ± 21 mg / dl), post-dexamethasone (445 ± 260 mg / dl) and post treatment (222 ± 5 mg / dL), Group 2 (moringa oleífera group) initial glycemia (95 ± 27 mg / dl), post-dexamethasone (413 ± 184 mg / dl) and post treatment (102 ± 18 mg / dl) and Group 3 (metformin group): initial glycemia (110 ± 5 mg / dL) post-dexamethasone (470 ± 146 mg / dl) and post treatment (88 ± 11 mg / dL). Post treatment glucose (day 15) showed difference between group 1 and 2 (p <0.0001), between group 1 and 3 (p < 0.0001) finding no differences between groups moringa oleífera and metformin (p = 0,1). DISCUSSION: moringa oleífera acutely decreases dexamethasone-induced hyperglycemia in Wistar rats, with the same effectiveness that metformin.
Key Words: moringa oleífera , Hyperglycemia, Wistar rats, metformin.
INTRODUCCIÓN
Moringa oleífera lam, conocido como moringa, es un árbol originario de Kerala al norte de India en el sureste del Himalaya, crece en casi cualquier tipo de suelo, incluso en condiciones de sequía, usada como alimento y tradicionalmente en la medicina india para tratar diferentes dolencias, entre ellas la diabetes mellitus (1,2). Recientes investigaciones realizadas han demostrado la presencia en sus hojas de elementos traza como Cl, K, Ca, Ti, Cr, Mn, Fe, Co, Ni, Cu, Zn, Br y Sr en concentraciones variables pero siendo lo más relevante los altos niveles de Cr en su extracto (3).
Entre sus múltiples propiedades se han encontrado que el polvo seco de sus semillas posee un alcaloide denominado Moringine que es muy similar a la efedrina, por lo que relaja los bronquios pudiendo ser utilizado como una alternativa terapéutica para el tratamiento del asma (4).
Las semillas de moringa oleífera también contienen una lecitina soluble en agua en la que se describe un efecto hemoaglutinante que en dosis de 0.197mg/ml, se ha descrito que inhibe significativamente el crecimiento larvario del Aedes aegypti que ha desarrollado cierta resistencia a los insecticidas usado para combatir su reproducción (5).
Las hojas, cuyo consumo incluso en altas cantidades carecen de toxicidad, se han encontrado que poseen antioxidantes como las vitamina C y E, mejoran la memoria por medios nootropicos; se sospecha que podría ser utilizado para el tratamiento del Alzheimer según la investigación realizada por Obelesu M y col (6).
En el polvo seco de las hojas han sido encontrados polifenoles como quercetina, glucósidos de kaemferol, ácido clorogénico y caefenoilquinico, zeatina y beta – sitosterol (7), este polvo administrado a ratas como la Goto – Kakizaki y ratas Wistar mejora la tolerancia a la glucosa, dicho efecto podría estar mediado por la quercetina – tres glucósido y el glucósido de kaemferol, estas actúan a nivel del transportador sodio – glucosa que se sitúa en el duodeno – yeyuno como un inhibidor competitivo, disminuyendo de esta manera la absorción intestinal de glucosa (8).
También es destacable se ha encontrado que el extracto acuoso de las hojas de moringa oleífera a dosis de 200mg/kg produjo en animales normales (ratas Wistar) una reducción de la glucemia en ayunas de 26,7% y después de una prueba de tolerancia oral a la glucosa de 29,9% (9).
Se ha descrito que una alta proporción de bencilamina (moringina) a dosis de 3600 µmol/kg/día en extracto acuoso tiene propiedades hipolipemiantes y mejora la tolerancia a la glucosa en ratas con dieta rica en lípidos por lo que podría constituir una alternativa para el tratamiento del síndrome metabólico debido a que la bencilamina es metabolizada en los mamíferos por la monoamino oxidasa sensible a semicarbazida (10) produciendo un efecto similar a la insulina en los adipocitos ya que inhibe la lipólisis y estimula el trasporte de glucosa mediante el transporte de los GLUT – 4 a la superficie de los adipocitos (11).
La diabetes mellitus (DM) comprende un grupo de trastornos metabólicos frecuentes que comparten el fenotipo de la hiperglucemia. Existen varios tipos diferentes de DM debidos a una compleja interacción entre genética y factores ambientales. Los factores que contribuyen a la hiperglucemia pueden ser, deficiencia de la secreción de insulina, menor sensibilidad de los tejidos periféricos a la insulina o aumento de la producción hepática de glucosa (12).
La metformina es representativa de las biguanidinas usadas en el tratamiento de la diabetes mellitus tipo 2 (DM 2), reduce la producción hepática de glucosa (12) a través de la supresión de la producción hepática de glucosa por la fosforilación de CBP (13) o también se ha propuesto que activa a la quinasa de AMP mediante la inhibición de la AMP deaminasa (14) y puede mejorar ligeramente la utilización periférica de la glucosa, disminuye la glucosa plasmática y la insulina en ayunas, mejora el perfil lipídico y promueve una discreta pérdida de peso (12).
Está demostrado que la moringa oleífera y la metformina por diferentes mecanismos disminuyen la glicemia, la pregunta es si el extracto de moringa oleífera podría tener un efecto hipoglucemiante mayor que la metformina, el objetivo del estudio es comprobar la efectividad del extracto de moringa oleífera como hipoglucemiante, en ratas Wistar con hiperglucemia inducida por la dexametasona, y compararla con el efecto hipoglicemiante de la metformina.
MATERIALES Y MÉTODOS
Estudio experimental, en el cual se utilizaron 15 ratas Wistar hembras de dos meses de edad , puestas en jaulas comunes (cinco animales por caja), con agua de canilla ad libitum, alimento común para animales. Se aclimató a los animales por siete días en el hábitat del bioterio de la Cátedra de Fisiopatología de la Facultad de Ciencias Médicas de la UNA, con ciclos de luz y oscuridad de 12 horas y temperatura entre 19 °C – 23 °C. Entonces fueron divididas al azar en tres grupos:
Grupo 1 (control): administración de suero fisiológico por vía enteral a través de cánula orogástrica.
Grupo 2 (moringa oleífera): a dosis de 300 mg/kg/día por vía enteral a través de cánula orogástrica.
Grupo 3 (metformina): a dosis de 14mg/kg/día por VO por vía enteral a través de cánula orogástrica.
Se realizó la inducción de hiperglicemia mediante la administración subcutánea de dexametasona en la región escapular de las ratas en dosis de 10mg/kg/día durante 10 días. Luego de la misma se procedió al tratamiento con moringa oleífera, Metformina y suero fisiológico por vía enteral durante cinco días. Al grupo control se le administro solo suero fisiológico mientras que el grupo moringa oleífera recibió una dosis de 300 mg/kg/día de la planta medicinal. Se preparó usando 10 gramos de hojas secas y molidas de moringa oleífera por 100 ml de agua destilada hirviéndose durante cinco minutos y procediendo posteriormente al colado de la descocción. Al grupo metformina se le administró dicho fármaco a una dosis de 14mg/kg/día, el cual se preparó usando 400 mg de clorhidrato de metformina en 100 ml de suero fisiológico.
Variables: glicemia, peso.
Definición de variables
Glicemia Inicial (Día 0): es la determinación de la glicemia realizada antes de la administración de la dexametasona y corresponde al día 0 del protocolo.
Glicemia Post-dexametasona (Día 10): es la determinación de la glicemia realizada después de la administración de la dexametasona 10 mg/Kp/día y corresponde al día 10 del protocolo.
Glicemia Post-tratamiento (Día 15): es la determinación de la glicemia realizada después de la administración de metformina o moringa oleífera durante tres días y corresponde al día 15 del protocolo. La misma definición corresponde al peso inicial, post-dexametasona y post-tratamiento.
Determinación de la Glicemia
La determinación de la glucemia se realizó después de un periodo de ayuno de 12 horas y anestesia con sevoflurano, se tomó glucemia venosa con sangre de la cola, con glucómetro de la marca Accu-Chek; al mismo tiempo se determinó el peso de las ratas con una balanza de precisión de la marca Shimadzu.
Análisis estadísticos
Los datos fueron cargados en una hoja de cálculo de Microsoft Excel y se calculó el promedio, desviación estándar y la correlación mediante la prueba T de Student, se consideró p< 0,05 como significativa.
Asuntos éticos
Se cumplieron con los principios básicos de carácter internacional aplicables a las investigaciones biomédicas con animales elaborados por la CIOMS y el ICLAS.
RESULTADOS
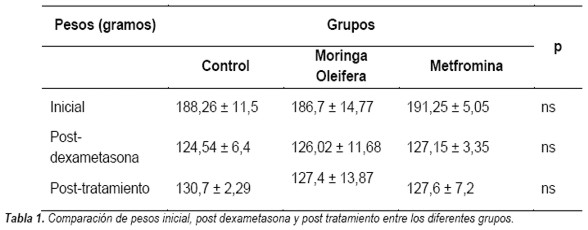
No hubo diferencias de pesos iniciales, post-dexametasona y post-tratamiento entre los 3 grupos de estudio (Tabla 1).
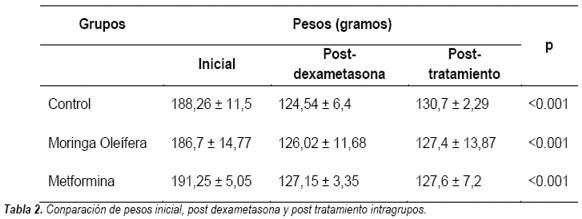
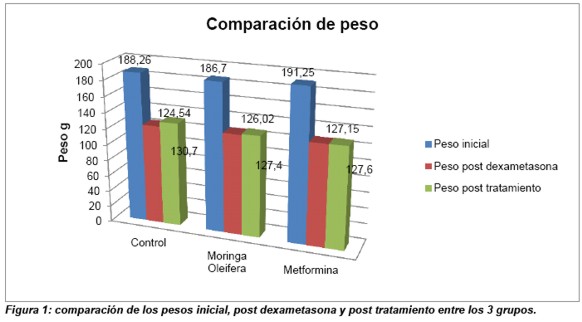
Si hubo diferencias significativas entre los pesos intragrupos, al comparar el peso inicial con el peso post-dexametasona, pero ya no se notó esta diferencia entre los pesos post-dexametasona y post-tratamiento (Tabla 2, Figura 1).
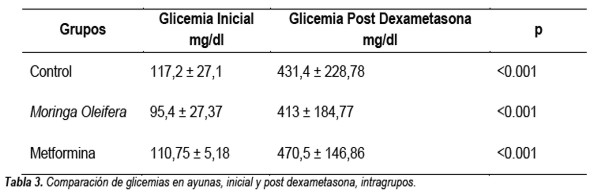
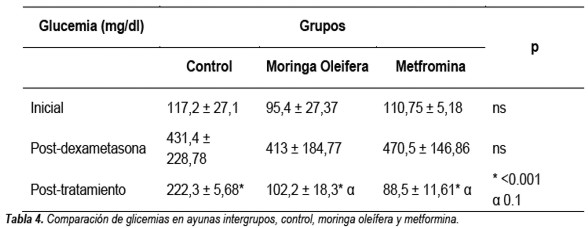
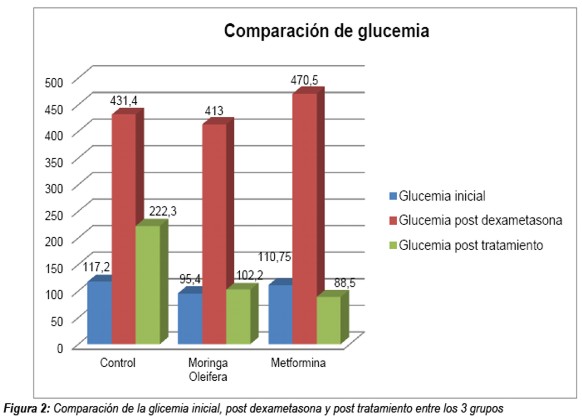
En relación a la glucemia en ayunas hubo un aumento después de 10 días de dexametasona a una dosis de 10 mg/Kp/día en los 3 grupos de estudios (Tabla 3). No hubo diferencias entre las iniciales y las post-dexametasonas según los diferentes grupos, en cambio se constató diferencia significativa al comparar la glicemia post-tratamiento entre grupo control y moringa oleífera, también entre grupos control y metformina, pero esta diferencia no se notó entre los grupos moringa oleífera y metformina (Tabla 4, Figura 2).
DISCUSIÓN
En este estudio constatamos un descenso de peso en las ratas después de la inducción de hiperglicemia por la dexametasona, probablemente sea el resultado de los efectos de la glicemia muy elevada y no tratada en las ratas durante dicha fase del protocolo.
La administración de dexametasona produce hiperglucemia, con cifras muy elevadas, a pesar de haber utilizado la dosis de dexametasona habitual para desencadenar hiperglicemia en ratas Wistar mencionadas en la literatura (15,16,17), este hecho puede ser explicado por el ayuno inadecuado de los animales, debido a la persistencia de alimentos balanceados entre las virutas de las cajas, los cuales no fueron retirados en el periodo de ayuno, previa a la extracción de la sangre para determinar la glicemia. La moringa oleífera produce un efecto hipoglicemiante, el cual es comparable con los niveles de disminución de glicemia obtenidos con el grupo metformina, aunque ligeramente de menor intensidad. Este efecto observado es agudo, ya que en este estudio se evaluó el efecto de la moringa oleífera solamente por 3 días, lo cual sugiere que esta planta medicinal puede ser útil cuando el objetivo es un descenso rápido de la glicemia, no sabemos si el efecto se mantiene a través del tiempo.
Los hallazgos han sido similares a los encontrados por Moussa N en ratas Goto, Kakizaki (8) y Jaiswal en ratas Wistar (9), ya que en ambos estudios se han constatado diferencias significativas entre la glicemia pre y post – tratamiento con moringa oleífera.
En conclusión podemos afirmar que se ha comprobado la efectividad de la moringa oleífera como hipoglicemiante, en hiperglicemia inducida por dexametasona en ratas hembras Wistar, de potencia similar a la metformina. Consideramos como limitaciones del trabajo el corto tiempo del tratamiento con la moringa oleífera y las cifras de glicemias muy elevadas que mantuvieron los animales; estudios posteriores en los mismos animales de laboratorio son necesarios, manteniendo cifras menores de glicemia y mayor duración de la administración de moringa oleífera para valorar efectos a largo plazo.
Finalmente se pueden diseñar estudios en humanos para evaluar el efecto de esta planta medicinal en personas con diabetes mellitus tipo 2.
REFERENCIAS BIBLIOGRÁFICAS
1. Modak M, Dixit P, Londhe J, Ghaskadbi S,. Devasagayam TPA. Indian Herbs and Herbal Drugs Used for the Treatment of Diabetes. J Clin Biochem Nutr. 2007; 40:163–173. [ Links ]
2. Shetty AJ, Choudhury D, Rejeesh, Nair V, Kuruvilla M, Kotian S. Effect of the insulin plant (Costus igneus) leaves on dexamethasone-induced hyperglycemia. Int J Ayurveda Res. 2010;1:100-2. [ Links ]
3. Gowrishankar R, Kumar M, Menon V, Divi SM, Saravanan M, Magudapathy P, Panigrahi BK, Nair KG, Venkataramaniah K. Trace Element Studies on Tinospora cordifolia (Menispermaceae), Ocimum sanctum (Lamiaceae), Moringa oleifera (Moringaceae), and Phyllanthus niruri (Euphorbiaceae) Using PIXE. Biol Trace Elem Res. 2010;133:357-63. [ Links ]
4. Babita A., Mehta A. Antiasthmatic activity of Moringa oleifera Lam: A clinical study. ndian J Pharmacol. 2008; 40: 28–31. [ Links ]
5. Coelho JS; Santos ND; Napoleao TH; Gomes FS; Ferreira RS; Zingali RB; Coelho LC; Leite SP; Navarro DM; Paiva PM. Effect of Moringa oleifera lectin on development and mortality of Aedes aegypti larvae. Chemosphere; 2009;77: 934-8. [ Links ]
6. Obulesu M, Dowlathabad MR. Effect of plant extracts on Alzheimer's disease: An insight into therapeutic avenues. J Neurosci Rural Pract. 2011;2:56-61. [ Links ]
7. Anwar F, Latif S, Ashraf M, Gilani AH. Moringa oleifera: a food plant with multiple medicinal uses. Phytother Res. 2007;21:17-25. [ Links ]
8. Moussa N, Mariko U, Shin-ichi K, and Kazuharu S. Effects of Oral Administration of Moringa oleifera Lam on Glucose Tolerance in Goto-Kakizaki and Wistar Rats. J Clin Biochem Nutr. 2007; 40: 229–233. [ Links ]
9. Jaiswal D, Kumar Rai P, Kumar A, Mehta S, Watal G. Effect of Moringa oleifera Lam. leaves aqueous extract therapy on hyperglycemic rats. J Ethnopharmacol. 2009;123:392-6. [ Links ]
10. Iffiú-Soltész Z, Wanecq E, Lomba A, Portillo MP, Pellati F, Szöko E, Bour S, Woodley J, Milagro FI, Alfredo Martinez J, Valet P, Carpéné C. Chronic benzylamine administration in the drinking water improves glucose tolerance, reduces body weight gain and circulating cholesterol in high-fat diet-fed mice. Pharmacol Res. 2010;61:355-63. [ Links ]
11. Zorzano A, Abella A, Marti L, Carpéné C, Palacín M, Testar X. Semicarbazide-sensitive amine oxidase activity exerts insulin-like effects on glucose metabolism and insulin-signaling pathways in adipose cells. Biochim Biophys Acta. 2003;1647(1-2):3-9. [ Links ]
12. Fauci A, Braunwald E, Kasper D, Hauser S, Longo D, Jameson J, Loscalzo J. Diabetes mellitus. In. McGrawHill editores. Harrison Principios de Medicina Interna. 17 ed. MéxicoD .F. 2008. p 2275–2305 [ Links ]
13. He L, Sabet A, Djedjos S, Miller R, Sun X, Hussain MA, Radovick A, Wondisford FE. Metformin and Insulin Suppress Hepatic Gluconeogenesis by Inhibiting cAMP Signaling Through Phosphorylation of CREB Binding Protein (CBP). Cell. 2009; 137:635–646.
14. Ouyang J; Parakhia RA; Ochs RS. Metformin activates AMP kinase through inhibition of AMP deaminase. J Biol Chem 2011; 286: 1-11. [ Links ]
15. Kaur N, Sharma N, Gupta AK. Effects of dexamethasone on lipid metabolism in rats organ. Indian J Biochem Biophy 1989;26:371-6 [ Links ]
16. Wiesenberg I, Chiesi M, Missbach M, Spanka C, Pignat W. Specific activation of the Nuclear Receptor PPARg and RORA by the Antidiabetic thiazolidinedione BRL 49653 and the Antiarthritic Thiazolidinedione Derivative CGP 52608. Mol Pharmacol 1998;53:1131-6 [ Links ]
17. Mahendran P, Shyamala Devi CS. Effect of Garcinia cambogia extract on lipids and lipoprotein composition in dexamethasone administered rats. Indian J Physiol Pharmacol 2001;45:345-50 [ Links ]