Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Anales de la Facultad de Ciencias Médicas (Asunción)
Print version ISSN 1816-8949
An. Fac. Cienc. Méd. (Asunción) vol.46 no.2 Asunción Dec. 2013
ARTICULO ORIGINAL
Detección inmunohistoquímica del virus de Epstein-Barr en pacientes con linfoma
Detection of Epstein- Barr virus for immunohistochemistry in patients with lymphoma
Navarro Trevisán NP1, Figueredo Thiel SJ1-2, Sánchez Martínez DF2, Espínola Cano AF1, Campos S1
1 Dpto. de Patología, Instituto de Investigaciones en Ciencias de la Salud, 2 Cátedra de Anatomía Patológica, Facultad de Ciencias Médicas, Universidad Nacional de Asunción.
RESUMEN
El virus de Epstein-Barr es un gammaherpes virus que infecta principalmente a linfocitos B permaneciendo en un estado de latencia en el interior del mismo, pudiendo también infectar a linfocitos T y células epiteliales. La persistencia de la infección viral inmortaliza a los linfocitos y favorece el desarrollo de procesos linfoproliferativos malignos como linfomas. Si bien se conoce que la relación entre la infección crónica del virus y el desarrollo de linfoma, varía de acuerdo al tipo histológico, se incrementa en pacientes inmunocomprometidos y de edad avanzada, la evidencia científica indica no sólo la importancia de este virus como agente infeccioso asociado con la etiología de esta neoplasia, sino también como un marcador asociado a respuesta refractaria y peor supervivencia. El objetivo de este estudio observacional descriptivo, fue detectar la presencia del Epstein-Barr virus por técnicas de inmunohistoquímica empleando anticuerpos monoclonales anti antígeno viral proteína latente de membrana en 86 pacientes con linfoma. La positividad para proteína en el total de pacientes con linfoma fue del 44%, correspondiendo el 20% a pacientes con linfoma de Hodgkin y el 24% a pacientes con linfoma no Hodgkin. La detección del virus en estas enfermedades, contribuye al manejo clínico de las mismas ya que el virus no sólo tiene un rol etiológico, sino además es un marcador pronóstico importante, incluso de interés terapéutico.
Palabras clave: Virus Epstein-Barr, Inmunohistoquímica, Linfoma.
ABSTRACT
The Epstein-Barr virus is a gammaherpes virus that infects mainly B lymphocytes staying inside it in a latent status, being able to infect a T lymphocytes and epithelial cells as well. The persistence of the viral infection immortalizes lymphocytes and favors the development of malignant lymphoproliferative processes like lymphomas. Even though it is known that the relationship between a chronic infection of the virus and the development of the lymphoma varies according to the histological type and that it increases in immunocompetent patients of advanced age, the scientific evidence indicates not only the importance of this virus as an infectious agent associated with the etiology of this neoplasm, but also as a marker associated to a refractory response and bad survivability. The goal of this descriptive observational study was to detect the presence of Epstein-Barr virus through immunohistochemistry using monoclonal antibody against the viral antigen Latent Membrane Protein in 86 patients with lymphoma. The positivity for this protein in the total patients with lymphoma was of 44%, corresponding 20% to patients with Hodgkin lymphoma and 24% to patients with no Hodgkin lymphoma. The detection of virus in these diseases contributes to the clinical handling of them because the virus not only has a role in the etiologic aspect but also is an important prognosis marker, even of therapeutic interest.
Key Words: Epstein-Barr virus, immunohistochemistry, lymphoma.
INTRODUCCION
El virus de Epstein-Barr (EBV) es un virus DNA que pertenece a la familia Herpesviridae, subfamilia Gammaherpesvirinae. La infección por el mismo está asociada al desarrollo de tumores linfoides y epiteliales, siendo los linfocitos B las células principalmente infectadas, además de células epiteliales y linfocitos T (1-3). El EBV infecta a los linfocitos B, ingresando a su interior mediante la glicoproteína de membrana CD21. Una vez internalizado, el genoma lineal del virus se circulariza para formar un episoma en el núcleo celular de los linfocitos B, de manera que quedan inmortalizados tras su infección latente y pueden proliferar indefinidamente en cultivos celulares. Este virus no es en sí oncogénico, pero actúa como un mitógeno en las células B, lo cual favorece la adquisición de translocaciones que favorecen el crecimiento de la célula afectada y la aparición de otras mutaciones que tienen como consecuencia la pérdida del control del ciclo celular normal, promoviendo el proceso neoplásico linfomatoso (4). La proteína latente de membrana 1 (LMP1), es una proteína transmembrana codificada por el gen BNRF1 y contiene 386 aminoácidos con una masa molecular de 63kDa, implicada en más de cuatro vías de señalización celular, e induce la expresión de múltiples marcadores de superficie y moléculas de adhesión celular (5,6). El LMP es la principal proteína de latencia capaz de transformar fibroblastos de roedores, esta no es expresada por las células B en la sangre periférica de individuos sanos pero es indispensable para la transformación de células B por EBV (7,8). Durante la fase de latencia el ADN del EBV permanece como un episoma dentro de la célula huésped y dirige la expresión de un número limitado de productos génicos virales. La expresión de esos genes se asocia a las manifestaciones de la infección por el EBV, incluyendo transformación e incremento de la supervivencia celular. En comparación con la expresión de otros genes de EBV durante la infección latente, LMP1 es el que presenta mayores efectos sobre el crecimiento celular, protegiendo a los linfocitos B de la apoptosis en parte por inducción de la expresión del gen bcl-2 cuyo producto es una proteína antiapoptótica. LMP1 también induce la agregación homotípica de células B por activación e inducción de moléculas de adhesión como LFA-1, LFA-3 e ICAM-1(9).
Además LMP1 tiene una función homóloga con el receptor constitutivo CD40 de las células B, ambos están asociados al receptor del factor de necrosis tumoral (TNF) que activa la transcripción del factor NF-kB, LMP1 parece proveer una señal más potente y sostenida que el CD40, por lo cual es posible que a través de este mecanismo permita a las células B infectadas del centro germinal escapar a la apoptosis (7,8). Los mecanismos de latencia del EBV han sido examinados ampliamente pues constituyen una estrategia para la evasión del sistema inmunológico del huésped, además de relacionarse con condiciones oncológicas asociadas a la persistencia viral, como lo son en particular los procesos linfoproliferativos entre ellos los linfomas (10-13). Entre los procesos linfoproliferativos de células B asociados al EBV se encuentran los linfomas de Hodgkin y los linfomas no Hodgkin. Entre estos últimos, se citan como más frecuentemente asociados al EBV, a los linfomas de células B como el linfoma de Burkitt y aquellos asociados a inmunocompromiso. Se citan también a algunos linfomas no Hodgkin de células T como el angioinmunoblástico y el linfoma nasal extranodal tipo NK, entre otros (14,15). La asociación del EBV con las neoplasias es variable dependiendo del área geográfica de origen del paciente. En este contexto se encuentran por ejemplo el linfoma de Burkitt endémico africano o algunos subtipos morfológicos del linfoma de Hodgkin, siendo los más frecuentemente asociados a la infección por EBV los subtipos celularidad mixta y esclerosis nodular (7,8). La frecuencia de linfoma de Hodgkin asociado a EBV oscila entre un 30% y 50% y la supervivencia en estos casos, ya sea en pacientes inmunocomprometidos o en ancianos es mala (16). El linfoma de Hodgkin asociado a infección por el EBV afecta en mayor medida a niños y ancianos que a adultos jóvenes. Recientemente, en un estudio se ha indicado, que en pacientes con linfoma de Hodgkin clásico asociado al EBV y con edad mayor a 50 años, la respuesta a la terapia es pobre, lo que sugiere además, que el deterioro del sistema inmunitario contribuye al desarrollo de la enfermedad neoplásica linfomatosa con positividad para el EBV (17,18).
Existe evidencia que indica que la infección por el EBV constituye un marcador pronóstico significativo en pacientes con linfoma que puede tener relevancia terapéutica (19). En el caso de los linfomas no Hodgkin asociados al EBV, éstos se describen como tumores agresivos caracterizados por crecimiento rápido y necrosis, asociándose en particular en los linfomas de células Natural Killer (NK) y linfomas T a hemofagocitosis concomitante. Aquellos individuos con alguna inmunodeficiencia primaria o secundaria son susceptibles de desarrollar neoplasias linfoproliferativas de células B. Los linfomas asociados a la infección por el EBV en pacientes sin inmunodeficiencias incluyen los de fenotipo citotóxico como los linfomas no Hodgkin de células NK y de células T, algunos casos esporádicos de linfomas no Hodgkin de células B y la granulomatosis linfomatoide. Estas enfermedades responden pobremente a la quimioterapia estándar y los tratamientos inmunoterápicos y nuevas estrategias farmacológicas contra el EBV están siendo investigadas (20). Debido a que la infección por el EBV permanece latente, muchos individuos portan células infectadas por el virus, por ello la mera infección por el virus en individuos que tienen un tumor no es suficiente para establecer una relación causal entre el tumor y la infección viral. Esta relación requiere la detección incuestionable de ácidos nucleicos o proteínas virales en las células tumorales (21). Las técnicas como el Western Blot, la citometría de flujo y el enzimoinmunoanálisis, pueden detectar y medir selectivamente ciertas proteínas virales, para las cuales existen anticuerpos disponibles, sin embargo la técnica más informativa es la inmunohistoquímica pues permite localizar las proteínas o antígenos virales en el contexto histopatológico, facilitando la evaluación de la significancia médica de la infección (22).
En el país, aún no existen datos que evalúen la presencia de infección por el EBV en células neoplásicas de pacientes con linfoma por lo que los objetivos de este estudio fueron determinar la frecuencia de detección del virus de Epstein Barr (EBV) por técnicas de inmunohistoquímica en biopsias de pacientes con linfomas, en los últimos cinco años, describir las características clínico-demográficas de los pacientes y determinar con qué frecuencia de positividad del EBV según subtipo histológico de linfomas clasificados según criterios de la OMS dentro del contexto histopatológico. El conocimiento de estos datos resulta de gran relevancia para la incorporación de la detección de LMP1 en los paneles de inmunohistoquímica; para la tipificación de los linfomas; para el diagnóstico, tratamiento y seguimiento de pacientes e incluso podría tener implicancia en el pronóstico de grupos definidos de pacientes. Todo esto ayudará, además, al médico tratante a enfocarse a utilizar los esquemas terapéuticos adecuados mejorados en cada caso.
MATERIALES Y METODOS
Se realizó un estudio observacional descriptivo de corte transverso temporalmente retrospectivo, que incluyó 86 muestras biópsicas de pacientes con diagnóstico anatomopatológico de linfoma, con muestreo no probabilístico de casos consecutivos. Para el reclutamiento se revisaron las bases de datos e informes anatomopatológicos del Departamento de Patología del Instituto de Investigaciones en Ciencias de la Salud de la Universidad Nacional de Asunción (IICS-UNA) y de la Cátedra de Anatomía Patológica de la Facultad de Ciencias Médicas-UNA. Se identificaron las muestras de tejido incluidas en bloques de parafina determinándose cuáles estaban en condiciones óptimas para el estudio. Se incluyeron a pacientes de cualquier edad y sexo, con diagnóstico anatomopatológico de linfoma, excluyéndose aquellas muestras no óptimas para el estudio. A fin de determinar la presencia del EBV en cortes de las biopsias de tejido incluidos en parafina, se utilizó la técnica de inmunohistoquímica empleando anticuerpos primarios contra el antígeno viral del EBV denominado LMP1 (Proteína latente de membrana1). La recuperación antigénica se realizó por calor en vaporera a pH alto e incubación con anticuerpo primario según indicación del fabricante. El método utilizado para la visualización de la reacción fue el de avidina-biotina-peroxidasa y como sustrato revelador se empleó la di-amino-bencidina (DAB).
La técnica de inmunohistoquímica, optimizada para las condiciones de trabajo, se realizó en el Laboratorio del Dpto. de Patología del IICS-UNA. Los datos fueron analizados por métodos de estadística descriptiva y distribución de frecuencias empleando para ello el paquete de datos Epi INFO 7.
Asuntos éticos: El protocolo de investigación ha sido aprobado por el Comité de Ética IICS-UNA, utilizándose además para el trabajo, un cuestionario de investigación estructurado y pre-codificado de manera a asegurar en todo momento la confidencialidad de los datos y resultados de los pacientes a lo largo de toda la investigación.
RESULTADOS
Se estudiaron muestras biópsicas de 86 pacientes con linfoma, correspondiendo 45 casos (52%) a pacientes del sexo femenino y 41(48%) al sexo masculino. El rango de edad estuvo entre los 2 y 93 años (media: 44 años; mediana: 48 años). Las muestras biópsicas fueron enviadas mayormente del Hospital de Clínicas (49%), del Hospital General Pediátrico Niños de Acosta Ñu (19%) y del Instituto de Previsión Social (15%) al Dpto. de Patología, IICS-UNA.
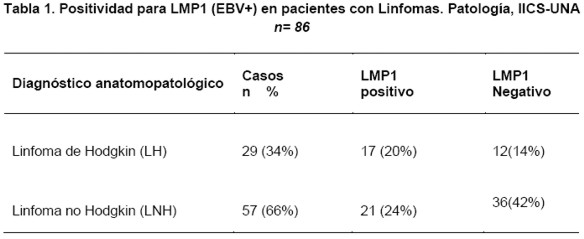
Del total de los 86 pacientes estudiados, 29 (34%) tuvieron diagnóstico anatomopatológico de Linfoma de Hodgkin, en este grupo el rango de edad fue de 2 a 88 años (media: 24; mediana: 18 años), en su mayor (62%) parte de sexo femenino (16 pacientes). Cincuenta y siete pacientes (66%) tuvieron diagnóstico anatomopatológico de Linfoma no Hodgkin, con rango de edad comprendido entre 3 y 93 años (media: 54 años; mediana: 58 años) con similar frecuencia entre pacientes de sexo masculino (49%) y de sexo femenino (51%), predominando también aquí el sexo femenino. La frecuencia de positividad para el EBV en cuanto a la proteína latente de membrana (LMP1) en el total de casos estudiados fue de 44% (38 casos), correspondiendo 17 casos (20%) a pacientes con Linfomas de Hodgkin y 21 casos (24%) a pacientes con Linfomas no Hodgkin (Ver Tabla 1).
Entre los 29 casos de linfomas de Hodgkin, clasificados histopatológicamente según criterios de la OMS, el tipo inmunofenotípico predominantemente encontrado fue el Linfoma de Hodgkin Clásico, en 27 casos (93%). Entre ellos el subtipo histopatológico de esclerosis nodular fue el más frecuentemente hallado 72% (21 casos) seguido por el subtipo celularidad mixta en 17% (5 casos) y un caso del subtipo depleción linfocítica (4%).
Se encontraron además, un caso de Linfoma de Hodgkin no clásico, subtipo histopatológico a predominio linfocitario y un caso con una localización muy rara localizado como tumor medular espinal extradural, el cual presentó inmunofenotipo de Linfoma de Hodgkin Clásico pero no pudo subclasificarse específicamente desde el punto de vista histopatológico.
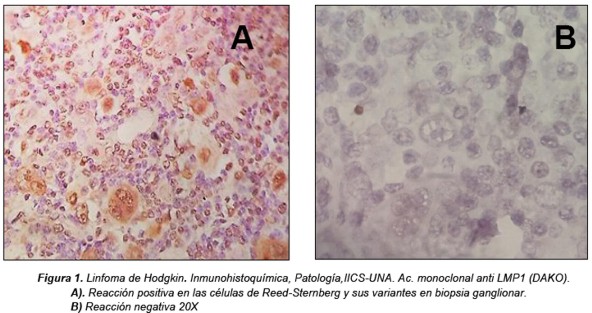
Del total de los 29 casos de Linfomas de Hodgkin, 17 casos (59%), mostraron positividad para el marcador LMP1 del EBV en las células neoplásicas de tipo Reed-Sternberg y sus variantes monolobuladas de Hodgkin como puede observarse en la Figura 1. De éstos, 14 casos correspondieron a pacientes pediátricos con edades comprendidas entre 2 y 18 años.
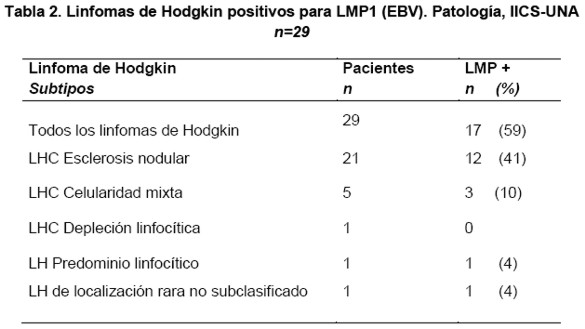
Doce casos positivos de Linfomas de Hodgkin (41%) correspondieron al subtipo histológico esclerosis nodular, tres casos (10%) al subtipo celularidad mixta y un caso al subtipo depleción linfocitaria. El caso de linfoma de Hodgkin de localización muy inusual que no fue clasificado histológicamente, también fue positivo para LMP1 del EBV. Estos resultados se detallan en la Tabla 2.
En relación a los 57 casos diagnosticados como Linfomas no Hodgkin, los subtipos más frecuentemente encontrados, fueron los linfomas de alto grado de células grandes B correspondientes al 23% (18 casos), seguidos por linfomas de bajo grado de células B con el 16% (9 casos). Entre estos grupos se encontraron los linfomas no Hodgkin B de tipo folicular con el 14% (8 casos) y los linfomas de Burkitt con el 12% (7 casos).
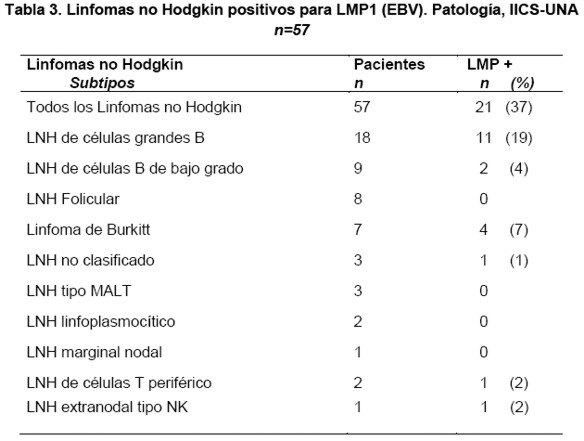
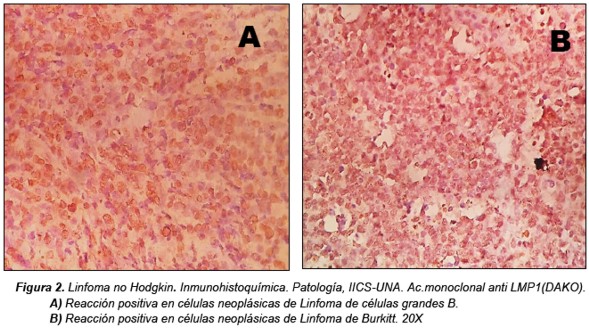
De todos los Linfomas no Hodgkin estudiados 21 casos (37%) fueron positivos para LMP1, la mayor parte (11 casos positivos=19%) correspondieron al tipo de linfoma no Hodgkin de células grandes B, cuatro casos (7%) a Linfomas de Burkitt, además de otros subtipos B y Linfomas no Hodgkin T hallados en menor frecuencia que son presentados en la Tabla 3 y Figura 2.
DISCUSIÓN
La presencia de la proteína viral del virus de Epstein Barr expresada en las células neoplásicas ha apoyado la evidencia científica que implica al EBV en la patogenia de los estos desórdenes linfoproliferativos (7,15) y en este sentido, en este estudio fue detectada su presencia, por inmunohistoquímica empleando anticuerpos monoclonales anti-LMP1, en el 44% de las muestras biópsicas de pacientes con linfomas en el que de los 29 pacientes, el 59% de pacientes con Linfomas de Hodgkin fueron positivas para LMP1, siendo esta proporción semejante a la descrita por Niedobitek y col (7) y Gandhi y col (16), donde se describe una frecuencia de 20 a 50% de linfomas de Hodgkin asociados al EBV. También esta proporción es cercana a los datos obtenidos en Argentina, en donde un 41% (49 casos) positivos fueron encontrados por Preciado y col (23). Como lo describen Gandhi y col. (16), la frecuencia de detección de EBV en Linfomas de Hodgkin es mayor en niños que en adultos jóvenes, puesto que de 17 casos positivos para LMP1, 14 pertenecieron a pacientes con edades comprendidas entre 2 y 18 años, datos similares, que también se han encontrado en este estudio realizado en Paraguay. En relación a la positividad de la LMP1 en los distintos subtipos de Linfomas de Hodgkin, en Paraguay, en este estudio, se observó mayor frecuencia en pacientes con LH clásico subtipo esclerosis nodular, seguido de pacientes con LH clásico subtipo celularidad mixta, si bien en la literatura se encuentra que la mayor parte de los casos asociados a EBV pertenecieron al tipo LH Clásico subtipo celularidad mixta (16,21,23,24). Esto probablemente se deba a que el número de pacientes con linfoma de Hodgkin incluidos no fue lo suficientemente grande y que la frecuencia de subtipos histológicos encontrada fue también mayor para la esclerosis nodular. Posiblemente teniendo un mayor número de casos podrían posteriormente compararse y equipararse las frecuencias con otras áreas geográficas.
De los 57 materiales de biopsias de pacientes con Linfomas no Hodgkin, el 37% presentó positividad para LMP1 siendo en su mayoría neoplasias de alto grado, y menos frecuentemente en neoplasias de bajo grado. Este comportamiento también lo describe Delecluse y col, en su investigación (21), en que también hallaron frecuencias mayores para linfomas no Hodgkin de alto grado. Teniendo en cuenta esto se observó que de los siete casos de linfomas de Burkitt, incluidos en este estudio, cuatro presentaron positividad para LMP1. En este sentido, se reporta que sólo una minoría de los linfomas de Burkitt esporádicos se hallan asociados al EBV, y que la proporción aumenta en el caso de pacientes inmunocomprometidos (15,21). Los casos de linfomas de Burkitt incluidos en este estudio aunque no fueron muchos, no presentaron inmunosupresión concomitante, pero se podría decir que para contrastar los resultados con los descritos por otros grupos de investigadores, la condición de inmunodepresión en los pacientes deberían estudiarse en un mayor grupo de pacientes de edades extremas, lo cual se realizará en un trabajo posterior. De los 18 casos de linfomas de células grandes B, llamativamente 11 casos correspondientes al 61% de casos de células grandes B fueron positivos para LMP1, describiéndose que un 10% a 35% de los linfomas de células grandes B están relacionados con la infección por el EBV (20) por lo que una inclusión de mayor número de casos de este subtipo inmunológico sería importante para analizar dichas frecuencias. De todas maneras se los datos encontrados aquí coinciden con la literatura correspondiente a mayor frecuencia de la presencia del EBV en linfomas no Hodgkin de alto grado como ser los de células grandes b y el linfoma de Burkitt. Entre los linfomas no Hodgkin de células T y NK, el único caso de LNH extranodal tipo NK también presentó positividad para LMP1, en concordancia con la evidencia científica que recalca que el EBV está presente en prácticamente todos los casos de linfoma extranodal tipo NK (25).
Otras neoplasias linfoproliferativas en las cuales se obtuvo positividad para LMP1 en este trabajo, incluyen un caso de LNH de células T periférico y un caso de LNH de células T anaplásico, reportándose también casos de linfomas no Hodgkin de células T asociados a EBV, según lo descrito por Carbone y col. (15). Si bien se obtuvieron datos importantes acerca de la presencia del EBV relacionada a las neoplasias linfoproliferativas de Hodgkin y no Hodgkin, será menester el estudio de mayor número de pacientes con linfoma a fin de afianzar estos hallazgos y lograr una significancia estadística. Así mismo su relación con el componente de inmunodepresión, que afecta a la frecuencia de las neoplasias linfomatosas asociadas a EBV y su pronóstico. En este trabajo no se tuvieron pacientes HIV positivos para estudio. La incorporación de la detección de LMP1 a los paneles de inmunohistoquímica para la inmunofenotipificación obligatoria de los linfomas, ofrece al médico una información de relevancia en el diagnóstico, tratamiento y seguimiento; e incluso, podría tener implicancia en el pronóstico de grupos definidos de pacientes.
AGRADECIMIENTO
A la Dirección General de Investigación Científica y Tecnológica del Rectorado de la UNA por posibilitar la realización de este trabajo gracias a la financiación otorgada a través del concurso previo realizado en la Dirección de Investigaciones de la Facultad de Ciencias Médicas de la Universidad Nacional de Asunción.
CONFLICTO DE INTERES
Los investigadores declaran no tener conflictos de intereses.
REFERENCIAS BIBLIOGRÁFICAS
1. Kasprzak A, Spachacz R, Wachowiak J, Stefanska K, Zabel M. Epstein-Barr virus (EBV) infection in B-cell non-Hodgkins lymphomas in children: virus latency and its correlation whith CD21 and CD23 molecules. Folia histochemicaetcytobiologica. 2007; 45(3):169-79. [ Links ]
2. Michelow P, Wright C, Pantanowitz L. A review of the Cytomorphology of Epstein-Barr Virus-Associated Malignancies. ActaCytologica. 2012;56:1-14. [ Links ]
3. Jaffe E, Harris N, Stein H, Isaacson P. Clasification of lymphoid neoplasms: the microscope as tool for disease discovery. Blood.2008; 112(12):4384-4399. [ Links ]
4. Kumar V, Abbas A, Fausto N. Robbins y Cotran Patología estructural y funcional. 7ma ed. España: Elsevier. 2005. [ Links ]
5. Vera Sempere F, Burgos J, Botella M, Córdoba J, Gobernado M. Inmunohistochemicalexpression of Epstein-Barr virus-encodedlatentmembraneprotein (LMP-1) in paraffinsections of EBV-associatednasopharyngeal carcinoma in Spanishpatients. Oral Oncol, Eur J Cancer. 1996;32B:163-8. [ Links ]
6. Baumforth K, Young L, Flavell K, Constandinou C, Murray P. The Epstein-Barrvírus and itsassociationwhit human cancers [review]. J ClinPathol: Mod Pathol.1999;52:30722. [ Links ]
7. Niedobitek G, Meru N, Delecluse H. Epstein-Barr virus infection and human malignancies. J. Exp. Path. 2001;82:149-70. [ Links ]
8. Jarrett R. Viruses and Hodgkin´s lymphoma. Annals of Oncology. 2002;13 Suppl1:23-9. [ Links ]
9. Laherty C, Hu HM, Opipari A, Wang F, Dixit V. The Epstein-Barr Virus LMP1 gene product induces a 20 Zinc finger protein expression by activating nuclear factor ?B. The journal of Biological Chemistry. 1992;267(34):157-160. [ Links ]
10. Pizzigallo E, Racciatti D, Gorgoretti V. EBV Chronic Infections. Medit J Hemat Infect Dis. 2010;2(1):e2010022.doi:10.4084/MJHID.2010.022. [ Links ]
11. Gottschalk S, Rooney C, Heslop H. Post-transplant lymphoproliferative disorders. Annu Rev Med. 2005;56:29-44. [ Links ]
12. Cohen Jl. Bening and malignant Epstein-Barr virus-associated B-cell lymphoproliferative diseases.Semin Hematol. 2003;40:116-123. [ Links ]
13. Young LS, Rickinson AB. Epstein-Barr virus: 40 years on. Nat Rev Cancer 2004;4:757-68. [ Links ]
14. Vereide D,Sugden B. Lymphomas differ in their dependence on Epstein-Barr virus. Blood. 2011;117(6):1977-85. [ Links ]
15. Carbone A, Gloghini A, Dotti G. EBV-Associated Lymphoproliferative Disorders: Classification an Treatment. The Oncologist. 2008;13:5-85. [ Links ]
16. Gandhi M,Tellam J, Khanna R. Epstein-Barr virus-associated Hodgkin´s lymphoma. British Journal of Haematology. 2004;125: 267-81. [ Links ]
17. Shimoyama Y, Oyama T, Asano N, Oshiro A, Suzuki R, Kagami Y. et al. Senile Epstein-Barr Virus-Associated B-Cell Lymphoproliferative Disorders: a Mini Review. J. Clin. Exp. Hematopathol.2006;46(1):1-3. [ Links ]
18. Shimoyama Y, Yamamoto K, Asano N, Oyama T, Tomohiro K, Nakamura. Age-related Epstein-Barr virus-associated B-cell lymphoproliferative disorders: Special referentes to lymphomas surrounding this newly recognized clinicopathologic disease. Cancer Sci.2008;99(6):1085-91. [ Links ]
19. Keegan T, Glaser S,Clarke C, Gulley M, Craig F, DiGiuseppe J, et al. Epstein-Barr Virus. As a Marker of Survival After Hodgkin´s Lymphoma: A Population – Based Study. J. Clin Oncology.2006;23(30):7604-13. [ Links ]
20. Heslop H. Biology and Treatment of Epstein-Barr Virus-Associated Non-Hodgkin Lymphomas. Hematology.2005: 260-66. [ Links ]
21. Delecluse HJ, Feederle R, O`Sullivan B, Taniere P. Epstein-Barr virus-associated tumors: an update for the attention of the working pathologist. J Clin Pathol.2006;60:1358-64. [ Links ]
22. Gulley ML, Tang W. Laboratory Assays for Epstein-Barr Virus-Related Disease. JMD. 2008;10(4):279-92. [ Links ]
23. Preciado MV, De Matteo E, Diez B, Grinstein S. Epstein-Barr virus latent membrane protein (LMP) in tumour cells of Hodgkins disease in pediatric patients. Med PediatrOncol. 1995; 24: 1-5. [ Links ]
24. Weinreb M, Day PJ, Niggli F, Powell JE, Raafat F, et al. The rol of Epstein-Barr virus in Hodgkins disease from different geographical areas. Archives of Disease in Childhood. 1996; 74:27-31. [ Links ]
25. Rickinson AB, Kieff ED. Epstein- Barr virus. In: Knipe DM HP, Griffin DE, Lamp RA, Martin MA, Roizman B, Straus SE, eds. Field virology, 5thedn, Philadelphia: Lippincott Williams & Wilkins. 2007:2655-700. [ Links ]