Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Anales de la Facultad de Ciencias Médicas (Asunción)
versión impresa ISSN 1816-8949
An. Fac. Cienc. Méd. (Asunción) v.2011 n.1 Asunción jun. 2011
ARTÍCULO ORIGINAL
Glucemia como factor de riesgo en pacientes internados en la Unidad de Cuidados Intensivos de Adultos del Hospital de Clínicas.
Glycemia as risk factor in adult patients admitted at Critical Care Unit of the Hospital de Clínicas.
Benítez Garcia A 1, Bueno E 1, Bianco H 2, Figueredo B 2, Ayala C 2, Cáceres M 1, Giménez F 1, Vera J 1 1 Dpto. de Endocrinología y Diabetes. Segunda Cátedra de Clínica Médica. 2 Unidad de Cuidados Intensivos de Adultos. Hospital de Clínicas. Facultad de Ciencias Médicas Universidad Nacional de Asunción
RESUMEN
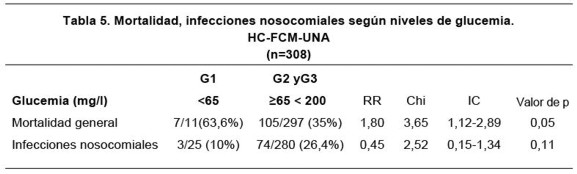
Objetivo: Determinar la relación entre glucemias al ingreso y la evolución de los pacientes admitidos a la Unidad de Cuidados Intensivos de Adultos (UCIA). Material y Métodos: estudio de cohorte retrospectivo de pacientes en la UCIA, tomando un muestreo, según distintos estratos de glucemia en mg/dL (Gl=65; G2 66 a 79; G3 80 a 199 y G4=200). Resultados: 413 pacientes, con edad media 48.89 años ±19; glucemia media al ingreso de 168.8 mg/dL (±93). 11.9% eran diabéticos conocidos. Al ingreso el Apache II fue 16±9, con una mortalidad global de 39.7%. Se constataron infecciones intrahospitalarias en 22.8%. La mortalidad en G4 fue de 49,5% vs. 35.4% en G3 (RR 1,41 p=0.008); en cirugías programadas fue en G4 de 30.6% y 14.7% en G3 (RR 2,07 p=0,04), con una tendencia significativa en las cirugías cardiacas (RR 2,33 p=0,11) y neurológicas (RR 3,33 p=0,26); la mortalidad en las cirugías de urgencia fue en G4 44,4% vs. 44,1% en G3 (RR 1,01 p=0,97). Los cuadros médicos en general presentaron una mortalidad de 76 % en G4 vs. 45% en G3 (RR 1,53 p=0,004). Los cuadros coronarios reportaron una mortalidad en G4 de 42 % vs. 10% en G3 (RR 7,13 p=0,001); en cuanto a hipoglucemia, existió una tendencia a mayor mortalidad general en G1 en comparación a G2 y G3 (35% vs. 63,6%) (RR 1,80 p=0,05) Conclusiones: La mortalidad general, de cirugías programadas y síndromes coronarios agudos fue mayor en forma significativa cuando la glucemia de ingreso fue =200 mg/dL.
Palabras clave: Glucemia, factor de riesgo, Unidad de Cuidados Intensivos.
ABSTRACT
Objective: to determine relation between glycemia to the admitions and the evolution of the adult patients admitted to UCIA (Adult Intensive Care Unit) Methods: retrospective cohorte study of patients files admitted in the UCIA, taking sampling of evaluation of the patients according to different levels of glycemia in mg/dL (Gl=65, G2 66 to 79, G3 80 to 199 and G4>200). Results: We evaluate 413 patients admitted UCIA, mid age was 48,89±19 years; mean glycemia at admition was 168,8 mg/dL ±93. Were diabetic knowned 11.9% Score Apache II mean 16 (±9), a global mortality in 39.7%; intrahospital infections were found in 22.8%. Mortality in G4 group was of 49.5% versus 35.4% in G3 (RR 1.41 p= 0.008). Intrahospital infections in G4 was 16,2% versus 26,4% in G3 (RR 0.54 p=0.03) Mortality in programmed surgeries in G4 was 30,6% versus 14.7% in G3 (RR 2.07 p=0.04).Had significant tendency in the cardiac surgeries (RR 2.33 p=0.11) and neurological (RR 3.33 p=0,26) bud non-significant in abdominal programmed surgeries G4 12.5% versus 10% in G3 (RR 0,83 p=0.85). Mortality in urgency surgeries was in G4 44,4% versus 44.1% in G3 (RR 1.01 p=0.97). In medical cases, non-surgically treated, mortality was 76,3% in G4 versus 45% in G3 (RR 1.53, p=0.004). Among coronary events, mortality was observed as significantly different comparing G4 vs G3 (42% and 10% respectively, RR 7.13 p=0.001). Regarding hypoglycemia general mortality was higher in those in group G1<65mg/dL the in comparison to groups G2 and G3 (RR 1.80, p=0.05) Conclusions: Greater general mortality was observed among the programmed surgery population and those with acute coronary events, specially in those patients admitted with >200 mg/dL of glycemia.Keywords: Glycemia, risk factor, Critical Care Unit.
INTRODUCCION
La asociación entre hiperglucemia y la mala evolución de los pacientes hospitalizados en general y en particular en los internados en UCIA ha llamado la atención de los médicos últimamente (1). Estudios observacionales demostraron claramente que existe una fuerte asociación entre hiperglucemia y morbi-mortalidad aumentada. En un trabajo, publicado en el año 1998, siguieron a 97 pacientes con diabetes sometidos a procedimientos quirúrgicos, una glucemia de ingreso mayor a 220 mg/dl, en el primer día del post-operatorio predijo en un 85%, el desarrollo de infecciones nosocomiales. El riesgo relativo (RR) de infecciones post-operatorias severas, incluidas sepsis, neumonía e infecciones de heridas operatorias fue de 5,7 en este grupo (2). Umpiérrez y su grupo de Atlanta, revisaron 1886 admisiones a salas generales de cirugía y clínica médica, en búsqueda de hiperglucemia; encontraron un 12% de personas con nueva hiperglucemia y 26% con diabetes conocida previa al ingreso. Los resultados dieron una mortalidad en los diabéticos conocidos de 2,7 y en los nuevos hiperglucémicos 18 veces más, que en el grupo normoglucémico. Comparando los tres grupos, apareció una tendencia significativa de mayor ingreso a UCI en los dos grupos hiperglucémicos (29 y 14% vs. 9% respectivamente, diferencia estadísticamente significativa) (3). Bolk y cols., en una cohorte de 14 meses, analizaron la glucemia de admisión de 336 sujetos (20% diabéticos). La mortalidad a un año en pacientes con glucemias menores a 100 mg/dl, fue de 19,3% y subió a 44%, con glucemias mayores a 199 mg/dl. La mortalidad fue más alta en pacientes con diabetes conocida que en aquellos sin diabetes conocida previamente (40 vs. 16%, p<0,05) (4).Se sabe que la hiperglucemia produce desequilibrios en una amplia gama de variables, que tienen que ver con el pronóstico de las personas internadas con cuadros críticos. Así, se reconoce una tendencia aumentada a las infecciones, teniendo como problema primario la disfunción fagocitaria de los neutrófilos y macrófagos causada por calcio citosólico elevado y ATP bajo (5).
Las alteraciones en la vía de la aldosa reductasa, en la generación de productos finales de glucosilación, de especies reactivas de oxígeno y en la vía de la proteína-kinasa C han sido vinculadas con esta disfunción (6-11). Otras alteraciones en el sistema inmune han sido descriptas, como la glicación de inmunoglobulinas y reducción del número de linfocitos T, tanto CD4 como CD8 que retornan a niveles normales luego de la normalización de la glucemia (12).
En el sistema cardiovascular, la hiperglucemia altera al reacondicionamiento post-isquémico. El tamaño del infarto aumenta y la circulación colateral se ve reducida. La hiperglucemia induce la muerte de los miocitos por apoptosis. Se han descrito, además, aumento de la presión sistólica, diastólica, del pulso, de la liberación de catecolaminas y prolongación del intervalo QT del electrocardiograma (13-16). Múltiples estudios en animales de experimentación y en humanos han vinculado la hiperglucemia con trastornos de la hemostasia que favorecen la aparición de trombosis. Así, se describieron actividad fibrinolítica disminuida y reducción de la actividad del activador tisular del plasminógeno (PAI-1) como aumento de la adhesión y agregación plaquetaria, con aumento del nivel de factor de von Willebrand (17-18). La hiperglucemia produce trastornos vasculares, por mediación del estímulo en la producción de citoquinas inflamatorias (IL6, FNT, IL18) (19). Otro mecanismo que explicaría la mala evolución cardiovascular de los pacientes con hiperglucemia es la disfunción endotelial (20-21). Finalmente en el sistema nervioso hay evidencia de que la hiperglucemia produce disminución en la capacidad de recuperación de las áreas isquémicas que rodean al territorio del infarto en los accidentes vasculares cerebrales. Esto obedece a la acidosis tisular y niveles de lactato aumentados (22-24).
En la diabetes tipo II, la hiperglucemia es el resultado de un largo proceso, que incluye grados variables de insulinorresistencia y falla de células beta, condicionados ambas genéticamente y desencadenados o empeorados por estímulos ambientales (15). En la enfermedad aguda la respuesta inmuno-hormonal al stress es hiperglucemiante. La epinefrina produce resistencia a la insulina alterando la señal post-receptor, aumentando la neoglucogénesis y la glucogenólisis hepática y muscular. El glucagón hace lo propio con la neoglucogénesis y la glucogenoslisis hepática y los corticoides inducen proteolisis, lipólisis que aumentan el sustrato para la neo-glucogénesis (25).
La evidencia de los estudios observacionales clínicos y de la experiencia en el laboratorio ha abonado la idea que la hiperglucemia más que un simple fenómeno reactivo, es un factor deletéreo más, en la cascada de eventos que llevan a morbi-mortalidad aumentada a estos pacientes y que controlarla podría llevarlos a un mejor pronóstico. El comportamiento de esta variable y su repercusión en la evolución de los pacientes que ingresan a UCIA es el motivo de este estudio, cuyo objetivo es determinar la relación entre la glucemia al ingreso y la evolución de los pacientes admitidos a la UCIA.
MATERIALES Y MÉTODOS
Estudio observacional analítico de cohortes retrospectivo, de 413 pacientes internados en la UCIA del Hospital de Clínicas desde el año 1999 al 2003. Criterios de inclusión: pacientes de ambos sexos, mayores de 15 años, ingresados a la UCIA del Hospital de Clínicas, con una internación prevista de por lo menos 72 horas. Criterios de exclusión: pacientes en los que no se pudieron completar las variables estudiadas.Muestreo no probabilístico de casos consecutivos. Las mediciones se realizaron evaluando las siguientes variables predictivas de ingreso: edad, sexo, diagnóstico previo de diabetes, glucemia, score apache II.
Variables resultantes de desenlace: mortalidad, necesidad de asistencia respiratoria mecánica (ARM) al ingreso, presencia o no de infecciones nosocomiales. Glucemia. Las comparaciones se hicieron a partir de cortes de glucemia. Se formaron 4 grupos: los que tenían valores menores a 65mg/dL (G1), un grupo entre 65 y menores a 80mg/dL (G2), uno entre 80 y 199mg/dL (G3) y los que tenían glucemias mayores a 200 mg/dL (G4). Esta estratificación se hizo en base a un análisis preliminar de las fichas, considerando los niveles de glucemia al ingreso de los pacientes, haciendo cortes arbitrarios de 10mg/dL, constatando la mortalidad de los sujetos en cada nivel. De esta observación, el rango donde aparentemente había menor mortalidad y variabilidad de este fenómeno fue entre 80 y 199mg/dL (G3), tomándose entonces este rango como controles y, como casos, los niveles anteriormente citados. Score Apache II. Score que de acuerdo a una serie de parámetros entre los que se encuentran la edad, enfermedad crónica, el score de Glasgow, el nivel de leucocitos, hematocrito, creatinina, sodio, potasio, ph sanguíneo, presión parcial de oxígeno, frecuencia cardiaca y respiratoria, presión arterial, y temperatura rectal, puede predecir el porcentaje de mortalidad (26). Interpretación: 0-4 puntos alrededor de 4 % de mortalidad; 5-9 puntos alrededor de 8 % de mortalidad; 10-14 puntos alrededor de 15 % de mortalidad; 15-19 puntos alrededor de 25 % de mortalidad; 20-25 puntos alrededor de 40 % de mortalidad; 26-29 puntos alrededor de 55 % de mortalidad; 30-34 puntos alrededor de 75 % de mortalidad; más de 34 puntos alrededor de 85 % de mortalidad.
Asuntos estadísticos: Los datos obtenidos de cada paciente fueron cargados y procesados en un programa de informática EPIINFO V-6. Se aplicó estadística analítica utilizándose cruces de variables con el propósito de determinar las asociaciones por medio de tablas de contingencia 2x2. Se consideró significativo a un valor de p menor de 0,05.
RESULTADOS
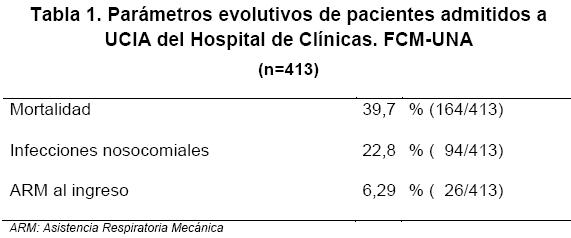
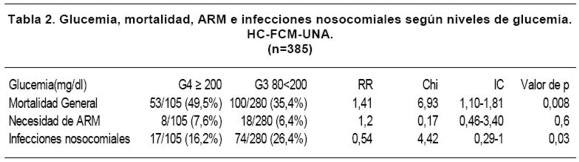
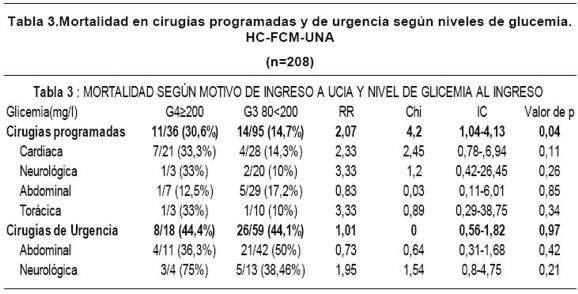
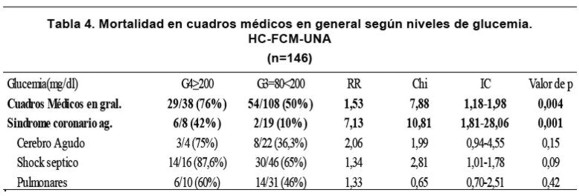
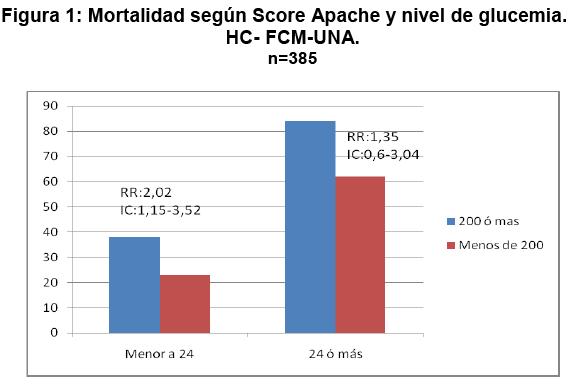
Fueron evaluados 413 pacientes, con una edad media de 48,89 (±19) años. Pertenecieron al sexo femenino el 46,7% (193/413) y al sexo masculino el 53,3% (220/413). El 11,9% (49/413) se conocían diabéticos. El tiempo medio de internación fue de 7,5 (0-77) días. El 55% (227/413) de los reclutados ingresaron para monitoreo post-operatorio y 45% (186/413) por causas clínicas. La mortalidad general fue de 39,7% (164/ 413). El porcentaje de infecciones nosocomiales estuvo en el orden del 22,8% (94/413). El 6,29% (26/413) de los pacientes requirieron ARM al ingreso. Ver Tabla 1. La media de la glucemia de ingreso fue de 168,8 (± 93) mg/dL. Relacionando la mortalidad con la glucemia al ingreso encontramos que en el G3, 100 de 280 (35,4%) pacientes en esta franja fallecieron y en el G4, lo hicieron 53 de 105 (49,5%) (RR:1,41, IC:1,10-1,81,Chi: 6,93, p=0,008). El 6,4% (18/280) de los reclutados, requirieron ARM y el 26,4% (74/280) presentaron infecciones nosocomiales en el G3 en comparación con el 7,6% (8/105) y el 16,2% (17/105) en el G4, respectivamente (RR:1,2 IC:0,46-3,40 Chi:0,17 p=0,6) y (RR:0,54,CI:0,29-1,Chi:4,42, p=0,03). Ver Tabla 2. La mortalidad en cirugías programadas en el G4 fue de 30.6% (11/36) y de14.7% (15/95) en el G3 (RR:2.07 Chi:4,2 IC:1,04-4,13, p=0.04), apareciendo una tendencia significativa en las cirugías cardiacas (33,3% vs 14,3%) (RR:3,Chi:2,33,IC0,78-694,p=0.11) y neurológicas (33% vs. 10%), respectivamente (RR:3,33,Chi:1,2 IC:042-26,45,p=0.26). Los resultados no resultaron significativos en las cirugías programadas abdominales (G4 12.5% vs.G3 17%) (RR:0,83, Chi:0,89,IC:0,29-38,75, p=0.34). La mortalidad en las cirugías de urgencia fue en G4 44.4% vs. 44.1% en G3 (RR:1,01 2Chi:O,IC:0,31-1,82, p:0.97) Ver Tabla 3. Los cuadros médicos en general presentaron una mortalidad de 76% (29/38) en G4 vs. 50 %(54/108) en G3 (RR:1,53,Chi:7,88,IC:1.18-1,98,p:0.004). Entre estos, la más significativa diferencia se observó en los cuadros coronarios con una mortalidad en el G4 de 42% (6/8) en comparación al 10% (2/19) en el G3 (RR: 7,13, Chi: 10,81,IC:1,81-28,06,p: 0.001). No hubo diferencias significativas en los cuadros cerebrales agudos, shock séptico y cuadros pulmonares. Tabla 4. El APACHE II medio de la población estudiada fue de 16(±9). Se encontró una tendencia a mayor mortalidad en el G4 con respecto a G3 si este score fue menor a 24 (40% vs. 22%.) RR: 2,02, IC 1,15-3,52, p: 0,08). Esto no se registró en el grupo con score mayor a 24 (84% vs.62%, RR: 1,35, IC: 0,6-3,04, p: 0,5) Figura 1. Comparando el grupo de hipoglucemia (G1= 65mg/dl) con la asociación de grupos G2 y G3, existió una mayor mortalidad general en el primer grupo de 63,6% (7/11) en contrapartida a 35% (105/297) del segundo (RR:1,80, IC 1,12-2,89) p=0.05). Ver Tabla 5.DISCUSIÓN
Mucho se ha hablado en estos últimos años sobre la hiperglucemia como elemento de mal pronóstico en los pacientes hospitalizados y en particular en aquellos de unidades de cuidados intensivos (1). Persistentemente se ha relacionado este fenómeno con la insulinorresistencia y la hiperinsulinemia secundaria a los fenómenos reactivos hormonales contrarreguladores generados por el stress de las enfermedades agudas. En este contexto, el ambiente hiperglucémico puede ser tóxico para la célula beta, produciendo disminución de la tasa de secreción de insulina en respuesta a la glucemia, generando apoptosis y disminuyendo la capacidad de captar las variaciones de glucemia del ambiente. Además los glucocorticoides - elementos básicos en la respuesta al stress - pueden inducir falla de célula beta en la producción de insulina por mecanismos independientes a la glucotoxicidad (25).Esta experiencia en la Unidad de Cuidados Intensivos de nuestro hospital, en una muestra de 413 sujetos de 4 años de evolución, mayoritariamente individuos que ingresaron para control post-operatorio de cirugía general, encuentra mayor mortalidad entre pacientes con glucemias de ingreso iguales o mayores a 200 mg% (49,5% vs. 35,4% p: 0,01). Estas cifras se dieron, sobre todo entre los pacientes operados en forma programada, con cuadros clínicos en general y en particular en aquellos con síndromes coronarios agudos. Igual tendencia, aunque no significativa, se observó en cirugías programadas cardiacas, neurológicas y en las de cirugías neurológicas de urgencia. Estos datos no se evidenciaron en las cirugías de urgencia en general. No se encontraron diferencias en cuanto a la necesidad de ARM e infecciones nosocomiales en ambos grupos. Estos resultados son similares a los presentados, anteriormente por Pomposelli y Umpiérrez (2-3), publicados en el año 1998 y 2002 respectivamente. La tendencia de mayor mortalidad en los pacientes que ingresaron con glucemias mayores a 200 mg/dl se mantuvo independientemente del antecedente de diabetes, de la edad y del Score Apache de ingreso.
Pero la hiperglucemia no lo es todo, nuestro trabajo también demuestra que la hipoglucemia de ingreso es un factor independiente de mortalidad en el grupo estudiado. Las personas que ingresaron con glucemias iguales o menores a 65 mg/dl (63,6%), fallecieron en mayor número que aquellas que lo hicieron con glucemias mayores (35%), diferencia estadísticamente significativa.
Este estudio suma su aporte a la evidencia pre-existente sobre la hiperglucemia como factor de riesgo deletéreo en la evolución de pacientes críticos y nos señala algunas direcciones sobre las poblaciones que se beneficiarían de conductas de intervención en términos de optimización del control de este parámetro metabólico. De acuerdo a los resultados y las consideraciones hechas con anterioridad, podríamos concluir que existe relación entre el pronóstico de los pacientes críticos y los niveles de glucemia al ingreso de los mismos. Sumado a esto, la glucemia igual o mayor a 200mg/dl se relacionan en forma significativa a la mayor mortalidad entre pacientes críticos de nuestra unidad de cuidados intensivos.
REFERENCIAS BIBLIOGRÁFICAS [ Links ]
2. Pomposelli J, Baxter J, Babineau T, Pomfret E, Driscoll D, Forse R, Bistrian B: Early postoperative glucose control predicts nosocomial infection rate in diabetic patients. J Parenter Enter Nutr1998. 22:77–81. [ Links ]
3. Umpierrez GE, Isaacs SD, Bazargan N, You X, Thaler LM, and Kitabchi AE: Hyperglycemia: an independent marker of in-hospital mortality in patients with undiagnosed diabetes. J Clin Endocrinol Metab.2002; 87:978–82. [ Links ]
4. Bolk J, van der Ploeg T, Cornel JH, Arnold AE, Sepers J, Umans VA: Impaired glucose metabolism predicts mortality after a myocardial infarction. Int J Cardiol 2001; 79:207–14. [ Links ]
5. Alexiewicz J, Kumar D, Smogorzewski M, Klin M, Massry S: Polymorphonuclear leukocytes in non-insulin-dependent diabetes mellitus: abnormalities in metabolism and function. Ann Intern Med. 1995; 123:919–24. [ Links ]
6. Sheetz M, King G: Molecular understanding of hyperglycemias adverse effects for diabetic complications. JAMA 2002; 288:2579–88. [ Links ]
7. Oldenborg P, Sehlin J: Hyperglycemia in vitro attenuates insulin-stimulated chemokinesis in normal human neutrophils: role of protein kinase C activation. J Leukocyte Biol 1999; 65:635–40. [ Links ]
8. Liu BF, Miyata S, Kojima H, Uriuhara A, Kusunoki H, Suzuki K, Kasuga M: Low phagocytic activity of resident peritoneal macrophages in diabetic mice: relevance to the formation of advanced glycation end products. Diabetes 1999; 48:2074–82. [ Links ]
9. Ortmeyer J, Mohsenin V: Inhibition of phospholipase D and superoxide generation by glucose in diabetic neutrophils. Life Sciences .1996; 59:255–62. [ Links ]
10. Perner A, Nielsen S, Rask-Madsen J: High glucose impairs superoxide production from isolated blood neutrophils. Intensive Care Med 2003; 29:642–45. [ Links ]
11. Sato N, Kashima K, Ohtani K, Shimizu H, Mori M: Epalrestat, an aldose reductase inhibitor, improves an impaired generation of oxygen-derived free radicals by neutrophils from poorly controlled NIDDM patients. Diabetes Care 1997; 20:995–98. [ Links ]
12. Bouter KP, Meyling FH, Hoekstra JB, Masurel N, Erkelens DW, and Diepersloot RJ: Influence of blood glucose levels on peripheral lymphocytes in patients with diabetes mellitus. Diabetes Res 1992; 19:77–80. [ Links ]
13. Kersten J, Schmeling T, Orth K, Pagel P, Warltier D: Acute hyperglycemia abolishes ischemic preconditioning in vivo. Am J Physiol 1998; 275:H721–25. [ Links ]
14. Verma S, Maitland A, Weisel R, Li S, Fedak P, Pomroy N, Mickle D, Li R, Ko L, Rao V: Hyperglycemia exaggerates ischemia-reperfusion-induced cardiomyocyte injury: reversal with endothelin antagonism. J Thorac Cardiovasc Surg 2002; 123:1120–24. [ Links ]
15. Ceriello A, Quagliaro L, DAmico M, Di Filippo C, Marfella R, Nappo F, Berrino L, Rossi F, Giugliano D: Acute hyperglycemia induces nitrotyrosine formation and apoptosis in perfused heart from rat. Diabetes 2002;51:1076–82. [ Links ]
16. Marfella R, Nappo F, Angelis LD, Siniscalshi M, Rossi F, Giugliano D: The effect of acute hyperglycaemia on QTc duration in healthy man. Diabetologia 2000;43:571–75. [ Links ]
17. Pandolfi A, Giaccari A, Cilli C, Alberta M, Morviducci L, Filippis ED, Buongiorno A, Pellegrini G, Capani F, Consoli A: Acute hyperglycemia and acute hyperinsulinemia decrease plasma fibrinolytic activity and increase plaminogen activator inhibitor type 1 in the rat. Acta Diabetologica 2001; 38:71–7. [ Links ]
18. Davi G, Catalano I, Averna M, Notarbartolo A, Strano A, Ciabattoni G, Patrono C: Thromboxane biosynthesis and platelet function in type II diabetes mellitus. N Engl J Med 1990; 322:1769–74. [ Links ]
19. Meldrum DR, Dinarello CA, Shames BD, Cleveland JC, Jr., Cain BS, Banerjee A, Meng X, Harken AH: Ischemic preconditioning decreases postischemic myocardial tumor necrosis factor-alpha production: potential ultimate effector mechanism of preconditioning. Circulation 1998;II 214–I18. [ Links ]
20. Tedgui A: Expression of interleukin-18 in human atherosclerotic plaques and relation to plaque instability. Circulation 2001; 104:1598–1603. [ Links ]
21. Kawano H, Motoyama T, Hirashima O, Hirai N, Miyao Y, Sakamoto T, Kugiyama K, Ogawa H, Yasue H: Hyperglycemia rapidly suppresses flow-mediated endothelium-dependent vasodilation of brachial artery. J Am Coll Cardiol 1999; 34:146–54. [ Links ]
21. Brodsky SV, Morrishow AM, Dharia N, Gross SS, Goligorsky MS: Glucose scavenging of nitric oxide. Am J Physiol Renal Physiol 2001; 280:F480–86.
22. Pulsinelli WA, Waldman S, Rawlinson D, Plum F: Moderate hyperglycemia augments ischemic brain damage: a neuropathologic study in the rat. Neurology 1982; 32:1239-46.
23. Hoxworth JM, Xu K, Zhou Y, Lust WD, LaManna JC: Cerebral metabolic profile, selective neuron loss, and survival of acute and chronic hyperglycemic rats following cardiac arrest and resuscitation. Brain 1999; Res 821:467–79.
24. Hotamisligil GS, Spiegelman BM. Tumor necrosis factor alpha: a key component of the obesity-diabetes link. Diabetes 1994; 43:1271-78.
25. Knaus WA, Draper EA, Wagner DP, Zimmerman JE: APACHE II: a severity of disease classification system. Crit Care Med 1985; 13:818–2.