Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Anales de la Facultad de Ciencias Médicas (Asunción)
versão impressa ISSN 1816-8949
An. Fac. Cienc. Méd. (Asunción) v.41 n.1-2 Asunción jun. 2008
Artículo de Interés
Fiebre amarilla en Paraguay año 2008
Yellow fevering in Paraguay year 2008
Prof. Dr. Adolfo Humberto Galeano Jimenez1
1) Prof. Titular Farmacología. Infectólogo. Director del Hospital de Clínicas. Asunción - Paraguay.
INTRODUCCIÓN
La fiebre amarilla es una hepatitis viral aguda atípica e infrecuente en la práctica clínica de nuestros días previos. Es una zoonosis típica de gran territorio tropical de las Américas y África (1).
Acostumbrados en los tiempos modernos al éxito de prevenir con un lento retroceso de la hepatitis A debido a la inmunización (2), y, donde los sinónimos de enfermedad hepática que causan estragos en la población mundial son otras hepatitis contemporáneas como la B, la C y la delta, algunas evitables con inmunizaciones masivas, de pronto irrumpe la fiebre amarilla en el escenario de las viejas enfermedades renovadas como re-emergentes (3), tras años de silencio para muchas generaciones de profesionales de la salud y de población en general.
CONCEPTOS GENERALES
Causado por un virus ARN del género flavivirus, familia flaviridadae, pequeño de 40 a 60 nm, con envoltura, capaz de replicarse en el citoplasma de las células infectadas, (3) es un típico arbovirus, esto significa virus transmitido por un artrópodo invertebrado minúsculo, en este caso, un mosquito.
Es capaz de causar una hepatitis acutísima y asombrosa como breve, con gran letalidad que puede llegar al 50 % en los casos típicamente ictéricos con diverso y oscilante comportamiento de tal forma que puede tener solo 5 % de letalidad en poblaciones indígenas endémicamente afectados hasta una cifra oscilantes entre 20 y 50 % (1) en poblaciones vírgenes con ataque epidemiológico tardío como podría ser catalogado nuestra población.
DISTRIBUCIÓN GEOGRÁFICA
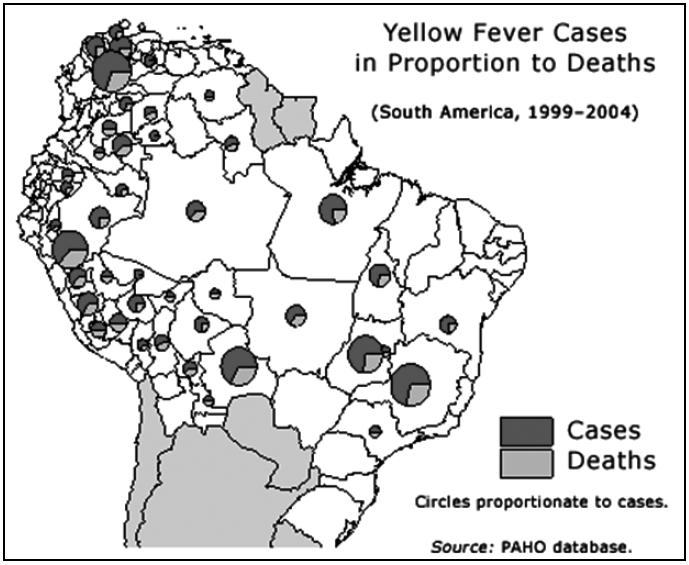
Distribuida ampliamente en el cinturón tropical del globo terráqueo, todo el área caluroso comprendido entre las latitudes 15 norte y 10 del sur (1), sobretodo en América del Sur y África, comparte con otro flavivirus, el virus dengue, un transmisor común invertebrado: el mosquito de la familia Aedes, astuto, urbano y casero, con dos componentes muy eficaces, el aegypti y el albopictus. Enfermedades asociadas a la transmisión por estos mosquitos tienden impelidos por el cambio climático mundial a diseminarse cada año más al sur en un fenómeno denominado meridionalización o australización, lo que implica en América del Sur, la penetración en Argentina y Uruguay en este lustro si no se emprende una enérgica campaña de erradicación o control efectivo a niveles de infestación ínfimos a dichos mosquitos.
Geográficamente la forma selvática se distribuye en Sud América desde Colombia (246 casos), Venezuela (57), Guayana Francesa (1), Guyana, Surinam, Trinidad y Tobago, pasando por Ecuador (93), Perú (1939), Brasil (539), Bolivia (684) y ahora a Paraguay (20 casos). Su existencia es conocida desde la época del descubrimiento de América, pero la actual deforestación salvaje y desmedida, por quemazones de extensas zonas selváticas, consiguiente disminución del hábitat arborícola, probablemente han empujado y arrinconado a la población de monos a lugares cada vez más cercanos a la población de humanos precipitando la desaparición de zonas de grises de transición y facilitando el encuentro con los humanos que ingresan a la selva por razones culinarias y económicas, desembocando en el actual brote paraguayo que tiene una diseminación en racimos dispersos, es decir a puntos geográficos distantes e inesperados.
HISTORIA BREVE
Históricamente se recuerda que los primeros casos de fiebre amarilla en América aparecieron en 1494 en la isla Española (actual Santo Domingo) en españoles conquistadores que se extendieron a la población indígena y asolando inmisericorde por 2 años hasta 1496 (6) con gran mortalidad de los nativos, son famosos los barcos procedentes del viejo mundo o los barcos "negreros" (con cargamentos de esclavos negros procedentes de Brasil o África) (7) con tripulación afecta de la enfermedad del "vómito negro" que eran sometidos a cuarentenas a cierta distancia de la costa a fuerza de cañonazos, para evitar diseminar la enfermedad entre los habitantes de los colonias del Nuevo Mundo. En los 500 años de vida conquistada se han sucedido numerosas epidemias con cuantiosos costos en vidas humanas en todas las Américas. En Paraguay se menciona el último caso conocido de fiebre amarilla en el año 1974, aislado caso único selvático importado aparentemente de un país vecino por lo tanto no autóctono (dato proporcionado por la Dirección de Vigilancia Epidemiológica del MSP del Paraguay).
CICLO DE LA FIEBRE AMARILLA
La fiebre amarilla tiene 2 ciclos bien conocidos de transmisión endémica y epidemiológica: una selvática y otra urbana. La selvática es persistente y diseminada. La urbana prácticamente ha estado desaparecida desde hace más de 50 años, los focos aislados que aparecieron en Brasil y Paraguay son los conocidos actualmente.
La fiebre amarilla selvática ataca a primates no humanos - monos aulladores y arañas (1), marsupiales y humanos ocasionales, siendo los agentes mosquitos de los géneros Haemogogus y Sabethes (4), con casos febriles leves de escasa mortalidad pero gran eficacia de elaboración y transmisión del virus, perpetuando la enfermedad en los santuarios de la floresta y aguardando a humanos que invaden el área para extender la infección a las áreas limítrofes a los bosques, y de ahí con suma posibilidad a través de esos humanos cargados de virus, por la migración interna provocada por el tráfico comercial (agricultores o intermediarios de materia prima que van a los centros urbanos) y profesional (veterinarios, agrónomos, ingenieros, etc.) que vuelven de sus áreas de labor ocasional) a áreas urbanas cercanas (poblados dormitorios) o distantes (ciudades de residencia familiar), con la rapidez que imprime el uso de vehículos modernos, cuando halla el otro agente transmisor urbano: el Aedes. Otro medio podría ser el transporte de formas adultas de mosquitos infectados en la cabina de vehículos o entre cargas, de larvas en recipientes contaminados o de propios huevos adheridos a los vehículos u otros objetos que eclosionarían al contacto con agua de las lluvias copiosas de verano o al atravesar aguadas que cortan los caminos troncales. Se ha estado comentando insistentemente que el ingreso masivo de plantas ornamentales procedentes del Amazonas, exhibidas en las principales avenidas adyacentes, transportaron huevos de Aedes o Haemogogus infectadas que pudieron haber sido el causal de la aparición en la vecindad de Asunción. La generación espontánea no cabe por lo que un agente vivo o inerte debe estar involucrado troncalmente en la transmisión.
La fiebre amarilla urbana se produce en áreas pobladas organizadas cuando confluyen una serie de condiciones concomitantes:
a) población humana susceptible,
b) carencia de inmunización vacunal de dicha población,
c) paciente transportador con alta carga viral
d) alta densidad de infestación de Aedes aegypti y/o albopictus,
e) circulación viral a través de dicho invertebrado
f) presencia en el área de infectado con viremia concentrada
EPIDEMIOLOGÌA
Los reservorios son distintos según el ciclo sea en la selva o en el ambiente urbano.
En la fiebre amarilla selvática los reservorios comúnmente son monos, algunos marsupiales (1) y mosquitos de la familia Haemogogus y Sabathes en tanto que en la urbana son los humanos y mosquitos de la familia Aedes aegypti y albopictus.
El ciclo urbano se inicia cuando el virus ingresa a una persona de la ciudad procedente de una persona que adquirió en la selva.
El virus de la fiebre amarilla es de un solo serotipo que es "antigénicamente conservado" es decir sufre poca mutación (3).
Epidemiológicamente en el Paraguay, la secuencia hipotética sería: invasión humana a la selva para cacería furtiva, picadura por Haemogogus con alta carga viral, gran eficacia de transmisión al humano y susceptibilidad inmunológica del mismo, humanos no inmunizados y no protegidos con repelentes habitualmente, desarrollo de casos asintomáticos, leves y algunos graves, regreso a la zona urbana de los casos con circulación sanguínea viral, picadura a éstos de Aedes, maduración en estos invertebrados en 12 días y nuevas diseminación a humanos de la zona, ya en el área urbana, primero en áreas semiurbanas como parajes, compañías o asentamientos precarios con silencio epidemiológico propio de poblaciones curtidas por el sacrificio de la sobrevivencia diaria, incluso con defunciones no registradas o subregistradas con diagnósticos distantes a la cruda realidad para luego extenderse a las grandes concentraciones urbanas de los pueblos o ciudades de que son satélites o tributarios, donde nuevamente sin el diagnóstico oportuno asolan como epidemias de "gripe o fiebres indeterminadas", algunas hasta mortales pero de etiología no esclarecida, al existir numerosos vías de comunicación, a través de automotores circulan por diversas áreas mas distantes. En horas un agricultor o un profesional veterinario o ingeniero agrónomo o forestal puede desplazarse del monte a ciudades circunvecinas o a la misma Asunción, portando el virus, la presencia pasajera o permanente y en contacto con zonas de alta infestación de Aedes, se expone a las picaduras, adquisición de virus por estos mosquitos locales y eclosión de nuevos focos metastáticos distantes y heterográficos, completándose el ciclo necesario para la situación actual.
CLÍNICA
Clásicamente en las clases de infectología se la denomina con una tetrada abreviada:" enfermedad febril de ictericia-hemorrágica intensa con vómito negro y bradicardia".
Pueden presentarse formas asintomáticas e inespecíficas, leves y graves que son ictéricas y hemorrágicas. Existe un gráfico conocido como el iceberg de la fiebre amarilla donde la base son las formas sintomáticas, el segundo peldaño lo constituyen estados febriles inespecíficos, los febriles con ictericia el tercer peldaño y las formas febriles ictéricas hemorrágicas la cúspide, siendo esta la mas grave, rica semiológicamente y con letalidad que puede ser hasta el 70 % (68 % en Colombia por ej.).
La evolución comprende tres estadios clínicos muy notorios: infección, remisión y de intoxicación.
El período de infección o de incubación aparece luego de la picadura del mosquito infectado (puede inocular aproximadamente 1000 partículas virales) (3), dura de 3 a 6 días en el que aparece fiebre elevada 39 o mas ºC), escalofríos, náuseas, mareos, cefalea, algias diversas en nuca, occipucio, espalda, lumbar, piernas, congestión facial y conjuntival a veces con bradicardia que es el famoso signo de Faget, hay leucopenia con neutropenia, trombocitopenia, albuminuria, elevación de las transaminasas y una altísima viremia. Puede durar de 3 a 6 días.
En el período de remisión los síntomas febriles y algias ceden y engañosamente el paciente se siente mejor, dura entre 2 horas y 2 días, -situación muy similar al dengue por aquella famosa curva febril en camello, en las formas leves el paciente inicia un periodo de recuperación que dura de 2 a 4 semanas. Persiste una viremia residual escasa pero peligrosa y detectable. En los casos severos hay manifestaciones hemorrágicas persistentes como el sangrado de las zonas de venopunción u otras espontáneas. Estos períodos son muy bizarros y difíciles de clasificarlas como fiebre amarilla si no existe un nexo epidemiológico sugerente.
El período de intoxicación aparece en el 15 a 25 % de los casos con ictericia franca, epistaxis, hemorragia gingival, hematemesis - el famosos vómito negro- , melena, oligoanuria, falla renal progresiva. En una palabra el paciente tiene insuficiencia hepática y renal concomitante con elevación de los marcadores hepáticos y renal, GPT, GOT, urea, creatinina, disminución del tiempo de protrombina, el paciente puede desarrollar hemorragias graves, CID, choque, muerte. La letalidad es variable pero puede llegar al 50 %.
El periodo de transmisibilidad de la sangre del paciente para el mosquito es de horas antes del inicio de los síntomas hasta 3 a 5 días de la enfermedad instalada (1) (periodo en el que es útil el mosquitero). El mosquito es capaz de trasmitir el virus a otros humanos en los siguientes 9 a 12 días de haber succionado la sangre infectada.
Desde el comienzo de un caso hasta la aparición de otro caso-nexo- dependiente del mismo es de 12 a 18 días más o menos.
LABORATORIO
A- Pruebas de diagnóstico diferencial con otras afecciones febriles ictéricas y hemorrágicas:
Hepatitis A,B,C: IgM, IgG, anti VHA, HBsAg, IgM anti HBc, HBe, anti VHC,anti VHD.
Leptospirosis: macro aglutinación
Dengue: IgM (MAC ELISA para captura), IgG, RCP, cultivo viral
Sepsis: Hemocultivos 3 tomas en periodos febriles
Hantavirus si el paciente procede de zonas endémicas
Paludismo: gota gruesa
Pedir en todo caso aunque el laboratorio no puede responder (lo que significa que se pensó en ellos): Fiebres hemorrágicas americanas (Junìn, Guanarito, Mapuche) si el paciente procede de zonas endémicas (Argentina, Venezuela, Bolivia)
Encefalitis Japonesa en pacientes procedentes de Japón con cuadros encefalíticos (no hay reactivos)
Pruebas generales y sus alteraciones mas frecuentes:
1- Hemograma inicialmente sin anemia pero aparece pos-hemorrágica, evolutiva y muy dinámica
2- Leucopenia con neutropenia
3- Plaquetopenia
4- Disminución del tiempo de protrombina
5- A veces leucocitosis en presencia de infección secundaria
6- Elevación de GPT y GOT, Bb total a expensas de la directa
7- Elevación de urea y creatinina
CRITERIOS LABORATORIALES DE CONFIRMACIÓN DE CASOS
1- Aislamiento viral
2- RCP posistiva
3- IgM positiva específica para fiebre amarilla
4- IgG elevada en control de sueros pareados comparados con 2 semanas de extracción del paciente.
5- Anatomía patológica con lesiones histopatológicas (cuerpos de Councilman, necrosis, etc.) compatibles con fiebre amarilla
6- Detección de antígenos virales de fiebre amarilla por métodos inmunhistoquímicos por estudio de anatomía patológica
DIAS RECOMENDADOS PARA LA EXTRACCIÓN DE SANGRE PARA RESULTADO EXITOSO:
Aislamiento viral: de sangre extraída en los 5 primeros días de síntomas (generalmente fiebre).
RCP (reacción de cadena de polimerasa): primeros 5 días de la enfermedad.
IgM: a partir del séptimo día de la enfermedad.
IgG: después de 7 y 21 días para controles pareados de resultados.
CRITERIOS PARA CONFIRMACIÒN DE CASOS:
Caso sospechoso: "toda persona con enfermedad caracterizada por fiebre de comienzo brusco seguida de ictericia en las dos semanas posteriores al inicio de los síntomas, y uno de los siguientes síntomas: 1) sangrado por la nariz, las encías, la piel o el tracto digestivo, o 2) muerte dentro del perídodo de tres semanas a partir del inicio de los síntomas."
Caso confirmado: "todo caso sospechoso que haya sido confirmado por laboratorio o presente nexo epidemiológico con un caso confirmado por el laboratorio".
Brote: "presencia de por lo menos un caso confirmado".
MANEJO Y TRATAMIENTO
El tratamiento es sintomático, de hecho no existe tratamiento específico tales como en gripe, VIH o herpes.
Casos leves: si se detectan internar e intensificar estudios serológicos o aislamiento viral y observancia de de aparición de signos de alerta como ictericia o falla renal y/o hemorragias. Implementación en el entorno familiar y vecindario (aún como caso sospechoso o probable) de medidas tales como fumigación e inmunización de bloqueo más combate del vector (adultos, larvas y huevos).
Atención de signos de deterioro porque los mismos se instalan muy rápidamente.
Casos graves (ictéridos con falla renal y/o trastornos hemorrágicos):
1- Interacción en sala con preferencia de cuidados intermedios, a criterio del médico a UTI.
2- Hidratación y electrolitos cuidadosos, previendo restricción según diurésis y distrés respiratorio
3- Prevención cuidadosa de hipoglicemia
4- Asistencia respiratoria mecánica según evolución bajo sedación con administración de oxígeno en permanencia
5- Manitol y anticonvulsivantes en edema cerebral
6- Sedación del paciente
7- Uso de mosquiteros en los primeros 5 días de la enfermedad
8- Sonda nasogástrica en caso de distensión abdominal o hemorragia con dilatación gástrica
9- Drogas vasoactivas para combatir la hipotensión del choque
10- Antibióticos preventivos en caso de infecciones respiratorias hipostáticas
11- Transfusión de sangre total o paquete de plaquetas según choque o hemorragias
12- Hemostasia de las zonas de hemorragia por venopunción o abordamientos necesarios
13- Control estricto de diurésis
14- Diuréticos o hemodiálisis según evolución de la falla renal
15- No tiene tratamiento específico, se ha preconizado la riba virina como en otras virosis sin posibilidades de éxito, inexistencia en el mercado y con numerosos efectos colaterales.
MEDIDAS DE PREVENCIÓN, INTERVENCION y VIGILANCIA EPIDEMIOLOGICA:
A) A favor de la población humana: 1. Inmunización masiva de la población en riesgo (100 %) (responsabilidad gubernamental)
a) Expuestos directos
b) Zonas de focos de brotes
c) Zonas de endemia selváticas
2. Evitar el ingreso selvático de humanos no inmunizados.( responsabilidad personal).
3. Igual conducta con vacunados con menos de 10 días de vacunación (responsabilidad personal).
4. Uso de ropas largas, repelentes y mosquiteros en forma permanente (responsabilidad personal).
5. Tela metálica protectora de aberturas como ventanales y puertas (responsabilidad personal).
6. Educación intensiva de la población con probable exposición (cazadores furtivos, agricultores, turistas, ecoturistas, veterinarios, ingenieros, agrónomos, visitantes, etc.) para la vacunación. (responsable gubernamental, municipal, ONG, personal) (1).
B) En contra de vector
1. Rociamiento intensivo para combatir las formas adultas de mosquitos durante semanas hasta que solo persistan formas ovo larvarias (tarea gubernativa).
2. Combate inmisericorde de los presuntos, posibles o supuestos criaderos de huevos o larvas hasta su eliminación final para evitar nuevas generaciones de mosquitos (contraparte municipal y sobretodo comunitaria). Disminuir el índice de infestación a 1 % o menos inclusive, es la piedra angular de eliminar dengue y fiebre amarilla. (responsabilidad comunitaria) .
3. Determinación periódica del índice de infestación aédica, por las propias comisiones vecinales que pueden ser capacitadas para el mismo. (responsabilidad conjunta).
4. Control de la circulación viral en simios selváticos a través de captura directa u observancia de la mortalidad de monos con estudios necrópsicos de los mismos o por lo menos de material hepático. (responsabilidad del gobierno u ONG ambientalistas).
C) Biopsias hepáticas y necropsias compulsivas en pacientes febriles ictéricos con sospecha de fiebre amarilla, basadas en el Código Sanitario para esclarecer con rigor científico y confirmación de los casos sospechosos y probables de fiebre amarilla (responsabilidad gubernamental conjunta con profesionales sanitarios y legistas).
Básicamente el control de la fiebre amarilla es totalmente complementario con el del dengue lo que se consigue manteniendo los niveles de infestación del Aedes por debajo o igual a 1 %, con la adición de que la fiebre amarilla posee una vacuna preventiva pero no exenta de efectos colaterales y limitaciones relativas pero limitaciones al fin.
La implementación de ambas estrategias asegura un logro sanitario posible.
ALGUNAS CONSIDERACIONES SOBRE LA VACUNA CONTRA LA FIEBRE AMARILLA:
Es una vacuna de virus vivos atenuados. Se la considera segura y eficaz (4) más de 60 años de uso. Inmunidad duradera tal vez toda la vida. Desarrollada Por Max Theiler a fines de los años 30 del siglo pasado en los laboratorios de la Fundación Rockefeller, tiene su origen en la cepa origina 17D (1,4).
CARACTERISTICAS:
Liofilizada y termoestable, obtenidos de huevos embrionados de pollos, requieren de un paciente proceso de 9 meses para la obtención final a partir el pedido normal.
Se aplica por vía subcutánea en una sola dosis de 0,5 mL en la parte superior del brazo derecho o izquierdo. Se puede aplicar también por vía intramuscular pero nunca por vía intravenosa (4) Se ha demostrado una eficacia superior a los 90 %.
CONTRAINDICACIONES DE LA VACUNA:
1- Personas afectas de síndrome febril agudo con compromiso del estado de salud.
2- Alérgicos al huevo de gallinas o sus derivados.
3- Alérgicos a la neomicina.
4- Inmunodeprimidos por cáncer, linfomas, leucemias, sida, etc.
5- Uso crónico de corticosteroides e inmunosupresores en reumáticos, etc.
6- Timectomizados o afectos de enfermedad del timo.
7- Menores de 6 meses.
8- Mujeres embarazadas (4) sobretodo primer trimestre (1).
REACCIONES ADVERSAS:
Leves: dolor en el sitio de inyección, fiebre, cefalea, congestión conjuntival, artralgias y mialgias, inapetencia. El tratamiento es sintomático: reposo, baños para la fiebre, reposo y dipirona tal vez pero no paracetamol por su potencial hepatotóxico (10) (11).
Graves: Hipersensibilidad en menores de 9 meses provocando encefalitis pos vacunal (9).
Enfermedad multisistémica denominada viscerotrópica (8) que tiene mayor probabilidad de aparecer en mayores de 60 años, es un síndrome con las mismas características de la enfermedad natural con relativa gravedad y una letalidad mínima.
PRECAUCIONES:
Pueden aplicarse pacientes POVIH (portadores de VIH) es asintomáticos.
Pueden aplicarse menores de 1 año en situaciones excepcionales (1).
Se recomienda no aplicar a mujeres embarazadas "por razones teóricas" (4). En mayores de 60 años en regiones enzoóticas se debe evaluar en forma individual. (4)
INCOMPATIBILIDAD DE LA VACUNA CON OTRAS
Prácticamente es compatible con todas las vacunas de virus avivo atenuados como anti sarampionosa, rubéola y paperas, pero se sugiere un intervalo de 4 semanas con el de cólera y fiebre tifoidea. La única vacuna que no se debe administrar simultáneamente es la del cólera (4). No se recomienda la revacunación antes de los 10 años.
BIBLIOGRAFÍA
1- Abram S. Berenson, Editor. Informe oficial de la Asociación Estadounidense de Salud Pública. OPS. Manual para el control de las enfermedades transmisibles. Publicación científica Nº 564, 16ª Edición. [ Links ]
2- Krugman, Ward, Katz. Enfermedades infecciosas. Sexta Edición. Interamericana. [ Links ]
3- COMITE DE INFECCIONES EMERGENTES. Fiebre amarilla. Rev. chil. infectol., 2001, vol.18, no.1, p.64-68. [ Links ]
4- Control de la fiebre amarilla. Guía práctica. OPS. 2005. [ Links ]
5- Documento de la Dirección de Epidemiología del Ministerio de Salud de la Nación (República Argentina). Riesgo de transmisión de fiebre amarilla en Brasil (actualización). Fecha de alerta: 10-01-08. Semana epidemiológica 02-2008. [ Links ]
6- Toledo Curbelo, Gabriel José. La otra historia de la fiebre amarilla en Cuba. 1492-1909. Historia de la medicina. Formato PDF. Instituto Superior de Ciencias Médicas de La Habana. Facultad de Ciencias Médicas "10 de Octubre". Departamento de Salud. 27-04-2000. [ Links ]
7- Neyra J. La fiebre amarilla su pasado en el Perú, revisión histórica. En: Imágenes históricas de la medicina Peruana. Neyra J. Lima: Fondo Editorial UNMSM; 1997. p. 195-203. [ Links ]
8- Kitchner S. Viscerotropic and neurotropic disease following vaccination with de yellow fever 17D. Vaccine ARILVAX. Vaccine 2004; 22: 2103-5[ [ Links ]STANDARDIZEDENDPARAG]
9- WHO "Global Advisory Comnmittee on Vaccine Safety (2-3 December 2004)". Wkly Epidemiol Rec: 2005 jan 7; 80(1); 3-7. [ Links ]
10- Alonso Llamazares, A. Reacciones adversas a paracetamol. Hospital Universitario San Carlos. Madrid. España. [ Links ]
11- Barreda P. El mal uso del paracetamol: riesgo de una grave intoxicación. [online]. Disponible en : URL: http://www.pediatral/intoxi_paracetamol.htm[ [ Links ]STANDARDIZEDENDPARAG]
12- Vasconcellos. Conferencia en Hotel "Villa Morra Suites" 21-02-08. [ Links ]