Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Anales de la Facultad de Ciencias Médicas (Asunción)
versão impressa ISSN 1816-8949
An. Fac. Cienc. Méd. (Asunción) v.38 n.1-2 Asunción abr. 2005
ARTÍCULO ORIGINAL
Diagnóstico citohistoquímico sistemático en biopsias de médula ósea y citologías hematológicas en el Paraguay (1)
Sistematic Cytohistochemical diagnose of bone marrow biopsies and hematological cytologies in Paraguay
Dra. Susy Jacqueline Figueredo Thiel (*)
1) Tesis aprobada en el año 2004.
(*) Médica hematopatóloga, Docente Investigadora Jefa del Departamento de Patología del Instituto de Investigaciones en Ciencias de la Salud y Docente de la Cátedra de Anatomía Patológica de la Facultad de Ciencias Médicas. Universidad Nacional de Asunción
RESUMEN
Las técnicas de citoquímica enzimática utilizadas en citología hematológica, mundialmente aceptadas para clasificar leucemias agudas se adaptaron a biopsias de médula ósea descalcificadas e incluidas en parafina. Estas técnicas se introdujeron en el Paraguay en 1997 en la Sección de Hematopatología del Departamento de Patología del Instituto de Investigaciones en Ciencias de la Salud para el estudio anatomopatológico cito e histológicos de las patologías hematológicas, concentrándose actualmente casi la totalidad del material del país. Se describen los hallazgos morfológicos y citohistoquímicos en 374 biopsias de médula ósea, 167 aspirados medulares y 114 frotis de sangre periférica en 5 años (1997-2002), de 370 pacientes hematológicos de distintos hospitales del país. Se utilizan diferentes esquemas citohistoquímicos enzimáticos analizando la sensibilidad, especificidad y la concordancia diagnóstica entre los métodos clínico-hematológicos y anatomopatológicos. La mayor parte de pacientes fueron varones adultos y las patologías mas frecuentes procesos linfoproliferativos crónicos, linfomas no Hodgkin y de Hodgkin (58 casos), aplasias medulares (47 casos), leucemias agudas linfoblásticas(40 casos) y mieloides(47 casos), mieloproliferativo crónico 31 casos), mielodisplasias(14 casos), metástasis(10 casos) y gammapatías monoclonales(7 casos). 98 hiperplasias medulares reactivas y 12 normales. Se excluyeron materiales hemorrágicos o pequeños <5mm. La concordancia entre los diagnósticos clínico-hematológicos y anatomopatológicos fue baja (índice kappa 38%), la sensibilidad del método clínico-hematológico de 54,58% y la especificidad de 5,55%, lo que demuestra la importancia del estudio de la biopsia de médula ósea y citologías hematológicas en forma conjunta con técnicas especiales sistemáticas para llegar al diagnóstico final preciso y confirmatorio en una gran parte de patologías hematológicas.
Palabras claves: histoquímica enzimática, biopsias de médula ósea, hematopatología
SUMMARY
Techniques of enzymatic cytochemistry used in hematologic cytology and widely accepted in the classification of acute leukemias, were adapted to biopsy material of decalcified bone marrow included in paraffin. In Paraguay, the Hematopathology Section of the Department of Pathology of the Health Sciences Research Institute (IICS) introduced these techniques for the study of cyto and hystological materials of hematologic pathologies. Currently, almost all the material is concentrated for the anatomopathological study of these pathologies in the country. This study describes the morphological and cytohistochemical findings in 374 biopsies of bone marrow, 167 bone marrow aspirates and 114 peripheral blood smears during five years (1997-2002) of 370 hematological patients of different hospitals of the country using different enzymatic cytohistochemical schemes. Besides, the sensitivity, specificity and diagnostic concordance between the clinico-hematologic and anatomopathological methods were analysed. Most patients were male adults and the most frequent pathologies were: chronic lymphoproliferative processes, Hodgkin's and non-Hodgkin's lymphomas (58 cases), bone marrow aplasias (47 cases), acute lymphoblastic leukemias (40 cases), myeloid leukemias (47 cases), chronic myeloproliferative diseasses (31 cases), myelodysplasias (14 cases), metastasis (10 cases) and monoclonal gammapaties (7 cases). Ninetyeight cases corresponded to reactive bone marrow hyperplasias and 12 were normal. Hemorrhagic and small (< 5 mm) materials were excluded. The concordance between the clinico-hematologic and anatomopathological diagnostic methods was low (kappa index 38%), the sensitivity of the clinico-hematologic method was 54.58% and the specificity was 5.55% which show the importance of the use of bone marrow biopsies and hematologic cytology together with special and systematic techniques to achieve precise, final and confirmatory diagnosis in great part of the hematologic pathologies.
Key words: enzymatic cytochemistry, bone marrow biopsies, hematopathology
INTRODUCCIÓN
El estudio morfológico en patología hematológica a lo largo del tiempo se ha basado principalmente en el análisis cuali y cuantitativo de alteraciones celulares en extendidos de sangre periférica o de aspirados de médula ósea1, 2 Para evidenciar las alteraciones celulares en estos materiales se utilizaron diferentes técnicas, desde la tinción policromática hematológica básica, basada en el efecto Romanowsky, como el May Grünwald Giemsa (MGG) o Pappenheim (PAPP) de la literatura anglosajona,3, 4 seguidas de técnicas de citoquímica enzimática que evidencian gránulos celulares específicos, utilizada para la clasificación de las leucemias agudas, complementada en algunos casos con técnicas ultraestructurales para diagnósticos definitivos5, 6, 7, 8, 9.
Inicialmente todos estos procedimientos se han realizado solo en materiales citológicos10 En las últimas décadas, gracias al estudio exhaustivo de la histología normal de la médula ósea, se conoció su compleja estructura, sus funciones y la relación que tienen las células estromales y hematopoyéticas, valorándola realmente como el tejido que es. Se reconoce una arquitectura histotopográfica normal, la cual se altera en los procesos patológicos hematológicos o extra-hematológicos que la afectan y que es muy importante reconocer para evaluar las lesiones a la hora de examinar preparados histológicos11, 12.
Con el correr de los años la biopsia de médula ósea pasó a constituir una herramienta metodológica complementaria utilizada cada vez más y con mayor importancia en el diagnóstico de enfermedades hematológicas. Consecuentemente se han desarrollado diferentes instrumentos de extracción biópsica y técnicas de procesamiento para estudios histológicos13, 14. Se logra así, la adaptación de técnicas de citoquímica enzimática, que comúnmente se utilizaban sólo en citologías, a cortes histológicos de cilindros medulares óseos descalcificados y procesados en parafina15, 16,17, 18, 19.
Actualmente la práctica biópsica medular es de uso corriente y cada vez más necesaria para evaluar los cambios patológicos tisulares en pacientes con enfermedades hemato-oncológicas que asociada al uso sistemático de técnicas especiales citohistoquímicas para interpretación, constituye un instrumento valioso para diagnóstico, pronóstico, indicación acertada de esquemas terapéuticos, evolución y verificaciones post-tratamiento12, 13, 14, 15, 16, 17, 18, 19.
En Paraguay, desde 1997 con la apertura de la Sección de Hematopatología en el Dpto. de Patología del Instituto de Investigaciones en Ciencias de la Salud (IICS-UNA), se desarrollaron e incorporaron las diferentes técnicas citohistoquímicas específicas para estudios histológicos de biopsias de médula ósea, aplicándolas en forma sistemática y conjunta a citologías de sangre periférica, aspirados medulares y tejidos linfoides20. Se estudian así, todos los casos reclutados en los primeros cinco años, procedentes de centros asistenciales de todo el país, para demostrar la importancia y relevancia del estudio anatomopatológico histo y citológico conjunto con la aplicación sistemática de esta metodología, que amplían mucho las posibilidades del diagnóstico precoz y definitivo, pronóstico, evaluación de conductas terapéuticas y seguimiento de pacientes, de gran ayuda para clínicos, hematólogos y oncólogos20.
Este trabajo que, además, analiza la situación actual del país, contribuye en gran medida con la medicina hemato-oncológica, ya que estas técnicas facilitan en primer lugar, el trabajo del médico en el diagnóstico, manejo y tratamiento de pacientes; en segundo lugar, es importante para la investigación, ya que a través de ella se pueden realizar estudios científicos aplicados y, en tercer lugar, contribuye con la docencia médica universitaria de pre y post-grado, ya que todos los materiales son utilizados también para este fin.
OBJETIVOS
MATERIAL Y MÉTODOS
Pacientes
Total de 655 materiales anatomopatológicos con 374 biopsias de médula ósea, 167 extendidos de aspirados medulares y 114 extendidos de sangre periférica de 370 pacientes portadores o sospechosos de enfermedad hematológica de los principales centros médicos asistenciales del país, como las Cátedras de Clínica Médica y Pediatría del Hospital de Clínicas; el Instituto de Previsión Social; el Centro de Hematología y Hemoterapia; el Hospital Central de las Fuerzas Armadas; el Hospital Nacional de Itauguá; el Instituto Nacional del Cáncer y el Hospital Pediátrico de San Lorenzo. Todos con estudios anatomopatológicos cito e histológicos especializados en la Sección de Hematopatología del Dpto. de Patología del Instituto de Investigaciones en Ciencias de la Salud (IICS) de 1997 a 2002. Materiales escasos, hemorrágicos, cartilaginosos y óseos sin hematopoyesis evaluable, excluídos.
Aplicación citohistoquímica enzimática sistemática y conjunta en materiales anatomopatológicos citológicos(extendidos sanguíneos, aspirados o improntas medulares) e histopatológicos (cortes de parafina de biopsias de médula ósea y ganglios). Las técnicas se introducen al país en 1997 en el IICS, para diagnóstico e investigación de patologías hematológicas20 y se basan en investigaciones realizadas en el laboratorio de médula ósea del Instituto de Patología de Freiburg-Alemania por el Prof.Dr. Hans Schaefer con quién el autor realizó su formación y entrenamiento técnico en hematopatología14, 15, 16, 17.
Esta metodología tiene como finalidad la interpretación diagnóstica que relaciona a la vez criterios morfológicos y citoquímicos en citologías hematológicas y cortes histológicos de biopsias de médula ósea, y es utilizada especialmente por la escuela de patólogos que realiza el diagnóstico mediante el estudio conjunto de materiales cito e histológicos.
Sistemáticamente todas las muestras se fijaron, descalcificaron y procesaron con el mismo procedimiento. Al extraer las biopsias de médula ósea, se realizaron improntas de los cilindros, para exprimir material de estudio citológico, haciéndolos rodar suavemente sobre láminas de vidrio previamente lavadas y secadas al aire. Biopsias y extendidos se fijaron en soluciones neutras de fijador universal(pH 6,8 a 7) y la descalcificación en solución de etilendiaminotetracetato disódico (EDTA) también neutra,15, 20 requisito básico fundamental para evitar la degranulación hematopoyética imprescindible para asegurar el éxito de las reacciones enzimáticas. Esto no resulta con fijadores comunes como formol al 10% y descalcificadores con pH ácido, utilizados de rutina en los laboratorios de patología20.
Desparafinación de cortes de 3µ y coloraciones citohistoquímicas de mieloperoxidasa (MPOX) y naftol AS-D cloroacetato esterasa (NACE) para granulocitos; alfa naftil acetato (ANAE) o butirato esterasa (ANBE) para monocitos; esterasa plaquetaria (PE) para megacariocitos en parafina; fosfatasa ácida (FAC) para linfocitos y plasmocitos y fostatasa ácida tartrato resistente (FATR) específicamente para tricoleucocitos y osteoclastos. Azul de Prusia de Perls para hierro, impregnación argéntica de Gomori para fibras reticulínicas, Azán para colágeno, ácido periódico de Schiff (PAS) para linfoblastos, eritroblastos y megacariocitos y rojo Congo para amiloide15. Muestreo inicial con hematoxilina y eosina (HE) en cortes histológicos y May-Grünwald-Giemsa (MGG) en extendidos. De acuerdo al caso, citohistoquímica enzimática con diferentes esquemas: a. Para mieloproliferativos: MPOX, NACE, PAS, ANAE, ANBE, PE y b. Para linfoproliferativos: MPOX, PAS, ANAE, FAC, FATR. El esquema básico para cualquier biopsia medular incluyó Giemsa, NACE, azul de Prusia y Gomori20.
Todos los preparados utilizados para diagnóstico y las fotografías de este trabajo fueron realizados personalmente por el autor.
Estudio observacional descriptivo transverso y analítico de pruebas diagnósticas. Tamaño de muestra calculado para una sensibilidad esperada de 90%, amplitud del intervalo de confianza (W) 0,15 y nivel de confianza (NC) 95%, requiriéndose mínimo 139 pacientes con enfermedades hematológicas44. Variables patológicas: cuadros hematológicos clonales como linfoproliferativos crónicos y agudos, mieloproliferativos crónicos y agudos, mielodisplasias, gamapatías monoclonales, metástasis y aplasias medulares. Variables reactivas: hiperplasias reaccionales, carenciales y normales. Variables anatomopatológicas: cambios morfológicos y citohistoquímicos cuali y cuantitativos en biopsias y aspirados de médula ósea y sangre periférica. Variables demográficas: edad, sexo, procedencia para estadística descriptiva.
Estadística analítica bivariada dicotómica no paramétrica para sensibilidad y especificidad diagnóstica del método clínico-hematológico inicial (DCH) con respecto al método diagnóstico anatomopatológico final (DAP), valores predictivos y razón de probabilidad positiva y negativa. Variable predictora:DCH inicial con aspirados medulares y/ o frotis de sangre periférica, datos clínicos y laboratoriales, cualitativa dicotómica positiva de 1 si se llegó al diagnóstico de la enfermedad y negativa de 2 si no se llegó al diagnóstico. Variable resultante: DAP final(prueba de referencia) en biopsias de médula ósea y/ o citologías hematológicas analizadas sistemáticamente con técnicas citohistoquímicas, cualitativa dicotómica positiva de1 si se llegó al diagnóstico y negativa de 2 si no se llegó al diagnóstico. Se consideró, además, el acierto diagnóstico clínico-hematológico con respecto al anatomopatológico desde el punto de vista del diagnóstico general por grupos patológicos (clonales o reactivos) y desde el punto de vista diagnóstico específico de subtipos en cada grupo.
La concordancia entre ambos métodos (clínico-hematológico-DCH y anatomopatológico-DAP) se analizó con el índice kappa de Cohen del programa de análisis epidemiológico de datos tabulados EPIDAT versión 2.0 Windows. Hipótesis nula (Ho): No existen diferencias entre los resultados diagnósticos por el método clínico-hematológico inicial y el anatomopatológico final en las pruebas diagnósticas y en la prueba de la concordancia. Hipótesis alternativa (Ha): Existen diferencias entre los resultados diagnósticos por ambos métodos en ambas pruebas.
RESULTADOS DISCUSIÓN CONCLUSIONES AGRADECIMIENTOS BIBLIOGRAFÍA
De 655 materiales anatomopatológicos en 370 pacientes hematológicos en cinco años, el 57% fueron biopsias de médula ósea con 374 cilindros; el 25% aspirados medulares con 167 extendidos y el 18% restante 114 frotis de sangre periférica. 27 casos (6,8%) fueron coágulos, cortical o cartílago sin hematopoyesis que fueron excluidos, excepto, tres casos con nuevas biopsias, aspirados y sangre.
Mayormente los cilindros medulares fueron de 1 a 1,5 cm. de longitud (78 casos) o 2 a 2,5 cm (34 casos) media de 1,3 cm. todos con conclusiones acertadas en los que el 75% presentó excelente material para evaluación morfológica. En 102 casos se recibieron sólo aspirados medulares y frotis de sangre periférica para estudio morfológico y citoquímico.
Los pacientes fueron mayormente adultos (72%-265 casos), varones (59%-157 casos) de 19 a 90 años, media de 54 y pediátricos (28%=105 casos), de 2 meses a 18 años, media 8, incluyendo lactantes, escolares y adolescentes; también más frecuentes en varones (59%-62 casos). Pacientes mayores adultos con dos picos etarios, de 50 y 70 años y pediátricos en la primera década.
El 64% fue de procedencia urbana, el 36% rural. Relacionando variables demográficas y cuadros clínico-hematológicos se observó preponderancia de varones, excepto los extra-hematológicos con sexo de igual frecuencia, como metástasis de neuroblastomas en niños y carcinomas y sarcomas en adultos.
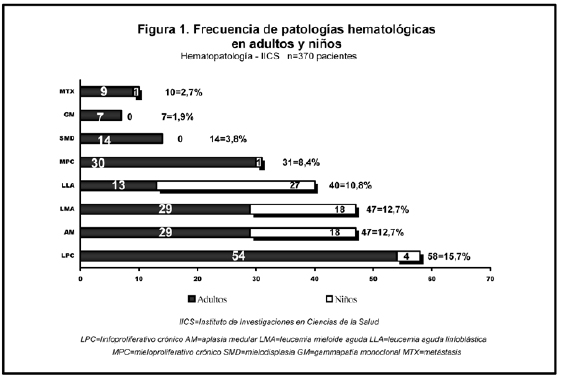
Cuadros frecuentes fueron hiperplasias medulares reactivas y carenciales (26,5%-98 casos), linfoproliferativos (15,7%) incluyendo leucémicos crónicos e infiltraciones linfomatosas y aplasias medulares (12,7%), todos con indicación obligatoria de biopsia medular para estadificación y diagnóstico. Leucemias agudas mieloides (12,7%) y linfoblásticas (10,8%), 31 hemopatías mieloproliferativas crónicas (8,4%), 14 mielodisplasias (3,8%), 10 metástasis (2,7%) y 7 gamapatías monoclonales (1,9%) El 3,2 % fue normal y el 1,6% con otras patologías como histoplasmosis, necrosis o fibrosis medulares (Figura 1).
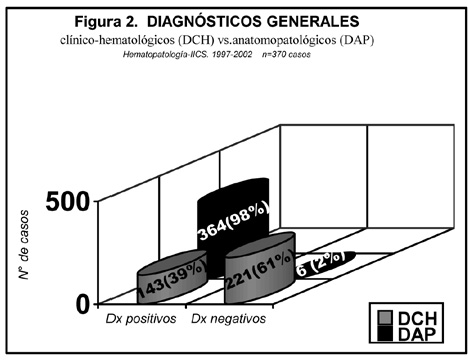
Los resultados diagnósticos generales positivos acertados por la clínica-hematológica fueron confirmados por la anatomía patológica y sus técnicas(patrón de referencia) coincidiendo los diagnósticos en 143 casos (39%). En los 221 casos restantes se llegó al diagnóstico final de certeza sólo por medio de métodos anatomopatológicos con técnicas especiales sistemáticamente utilizadas (61%) En 6 casos (2%) no se llegó al diagnóstico final clínico-hematológico ni anatomopatológico, necesitándose de técnicas citogenéticas y/ o de biología molecular para un diagnóstico definitivo (Figuras 2 y 3).
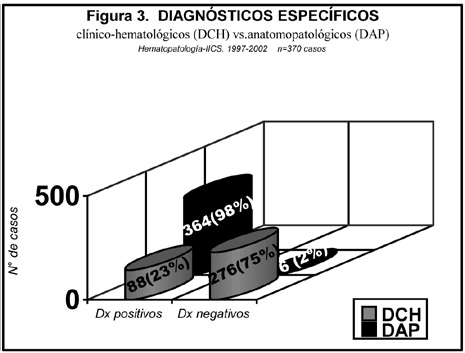
Al subclasificar y estatificar los resultados diagnósticos específicos clínico-hematológicos no acertados fueron 276 casos (75%) Estos debieron ser complementados con técnicas anatomopatológicas para la confirmación diagnóstica final específica. Comparando los datos de las figuras 2 y 3 se observó diferencia de acierto diagnóstico con respecto al diagnóstico clínico-hematológico inicial general y específico y los diagnósticos finales anatomopatológicos. El acierto clínico-hematológico general fue de 39% sobre el total, el cual disminuyó a 23% cuando se intentó subclasificar y estadificar los procesos patológicos (Figura 4).
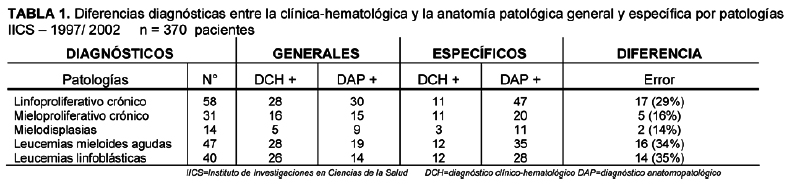
Agrupadas las patologías, el acierto diagnóstico clínico-hematológico desde el punto de vista general fue de 50 a 65% en casos de leucemias agudas linfoblásticas y mieloides, en aplasias medulares, enfermedades mieloproliferativas y en linfoproliferativas crónicas. Desde el punto de vista específico para clasificar y subclasificar se observaron diferencias diagnósticas notables entre los métodos diagnósticos clínico-hematológicos general y específico, en la mitad de los grupos de patologías estudiadas (diferencia significativa p<0,0001), siendo más afectadas las leucemias agudas linfoblásticas con un error diagnóstico/ clasificatorio de 35%(14 casos); las mieloides agudas de 34% (16 casos); las linfoproliferativas crónicas 29%(17 casos); las mieloproliferativas crónicas en 16%(5 casos) y las mielodisplasias de 14%(2 casos).
En la tabla 1 se ilustran las diferencias entre la clínica-hematológica y la anatomía patológica en cuanto a los diagnósticos generales propuestos y específicos comprobados, encontrándose un margen de error de 14 a 35% de casos en los grupos patológicos afectados indicando la necesidad de estudios biópsicos y/ o citológicos con técnicas especiales anatomopatológicas complementarias para diagnósticos confirmatorios, definitivos e imprescindibles en estos casos.
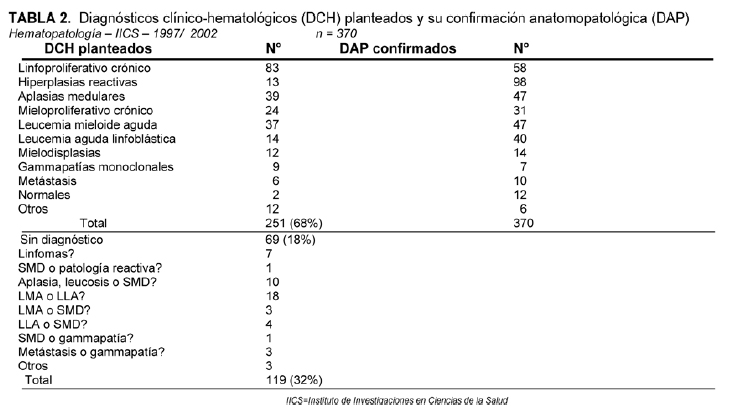
La tabla 2 desglosa el total de diagnósticos clínico-hematológicos presuntivos enviados para confirmación y/ o clasificación con estudios anatomopatológicos especiales.
En el estudio de pruebas diagnósticas, la sensibilidad del método clínico-hematológico o capacidad para detectar resultados positivos en pacientes enfermos (verdaderos positivos), en los casos analizados en este trabajo, fue de 54,58% (143/ 262 casos positivos), intervalo de confianza de 50,74 a 58,42%. Estos correspondieron a los resultados diagnósticos del aspirado medular y frotis de sangre periférica en correlación con el examen clínico y laboratorial de rutina, con respecto a los resultados del método anatomopatológico final en las biopsias de médula ósea y/ o citologías hematológicas con técnicas especiales, consideradas como prueba de referencia.
La proporción de resultados falsos negativos o riesgo de que existan enfermedades sin ser diagnosticadas por el método clínico (error beta) fue de 45,41% correspondientes a 119 casos de 262 positivos totales.
La especificidad del método clínico-hematológico o la capacidad del método para detectar resultados negativos en pacientes no enfermos (verdaderos negativos), con respecto a la prueba de referencia anatomopatológica fue muy baja de 5,55%. La proporción de falsos positivos o el riesgo de que existan resultados positivos en pacientes sin enfermedad (error alfa) fue de 94,44% correspondientes a 102 de 108 casos del total de negativos. La probabilidad de que un paciente con resultado diagnóstico positivo por el método clínico-hematológico padezca en realidad la enfermedad propuesta (valor predictivo positivo) fue de 58,36% correspondiente a 143 de 245 casos positivos. Al mismo tiempo la probabilidad de que un paciente con resultado negativo no padezca en realidad esa enfermedad (valor predictivo negativo) fue muy baja (4,80%) (Tabla 3).
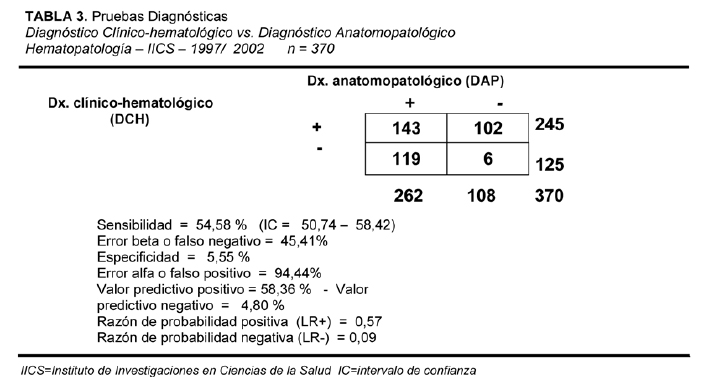
Estos datos indican que sólo en el 58% de los casos serán diagnosticados los pacientes con la enfermedad que padecen y que en el 95% de los casos no se detectarán aquellos que verdaderamente se encuentren sin enfermedad.
La razón de probabilidad positiva (LR+) o cociente entre la sensibilidad del método clínico-hematológico y los resultados falsos positivos fue de 0,57 con respecto al método anatomopatológico. La razón de probabilidad negativa (LR-) o cociente entre la especificidad del método clínico-hematológico y los resultados falsos negativos fue de 0,09.
Estos valores nos demuestran que la prueba clínica-hematológica es insuficiente para emplearla sola o en forma aislada en estos casos y que la misma debe acompañarse del estudio complementario anatomopatológico.
Para evaluar la concordancia entre el diagnóstico clínico-hematológico inicial y el resultado anatomopatológico final en los casos estudiados se asumió como hipótesis nula (H0) la ausencia de diferencias entre los resultados de ambos métodos, la que fue rebatida (p < 0.00001) por el resultado del índice kappa (IK) de Cohen de 0,3812 indicando que hay una diferencia significativa entre ambos métodos. Anexo Tabla 4. Teniendo en cuenta que el índice kappa (IK) puede adoptar valores entre –1 (desacuerdo) y +1 (acuerdo total) y que los rangos aceptados son considerados buenos cuando son mayores a 0,60 (IK bueno: 0,61 a 1), vemos que existe concordancia entre ambos métodos pero que ésta es mínima (IK= - 0,3812).
El valor global de la prueba o probabilidad de que un individuo sea clasificado correctamente por ella, en este caso por el método clínico-hematológico fue, sólo del 40%.
Todos estos valores nos indican que existe acuerdo entre los métodos diagnósticos utilizados, pero al ser mínima la concordancia diagnóstica, estos casos necesariamente deben acompañarse del estudio conjunto y complementario anatomopatológico con técnicas especiales. El hallazgo de estos datos se reduce al tipo de casos estudiados en este trabajo, en los que se necesitaron realizar biopsias/ citologías de médula ósea con técnicas especiales para llegar al diagnóstico final de certeza y/ o en el momento de subclasificar, pronosticar y cuantificar los cambios patológicos o la evolución, indicados por la clínica-hematológica.
La utilidad de las técnicas de citoquímica enzimática fue demostrada y aceptada mundialmente sobre todo para clasificación diagnóstica de las leucemias agudas en sucesivos trabajos científicos desde Naegeli, Bennett, Catovsky y otros7, 8, 9, 12. La adaptación de estas técnicas al material de biopsia de médula ósea incluida en parafina, también, fue estandarizada posterior y definitivamente por Schaefer15 – 18.
En el Paraguay, a partir de 1997 se introdujeron estas técnicas para el estudio de las patologías hematológicas, en materiales cito e histológicos, en la Sección de Hematopatología del Departamento de Patología del Instituto de Investigaciones en Ciencias de la Salud con un análisis de los primeros 28 casos20.
Actualmente esta sección constituye el punto de referencia para el estudio anatomopatológico de las patologías hematológicas con técnicas especiales en el Paraguay, concentrando materiales de pacientes provenientes de los distintos centros asistenciales de todo el país.
Mediante la utilización sistemática de este tipo de técnicas en cortes histológicos de biopsias de médula ósea junto al estudio citológico de aspirados medulares y sangre periférica, se pueden visualizar y cuantificar hallazgos morfológicos en patologías hematológicas. Esto permite en primera instancia definir la/ las líneas celulares hematopoyéticas alteradas, clasificando y subclasificando específicamente el tipo de enfermedad. Este punto resulta de capital importancia en la distinción entre leucemias agudas linfoblásticas y no linfoblásticas o mieloides, sobre todo para la subclasificación morfológica en estas últimas, lo que constituye aún actualmente una de sus mayores indicaciones 9, 14, 31, 41.
En nuestro material se analizaron y clasificaron 87 leucemias agudas enviadas para diagnóstico, confirmación diagnóstica o subclasificación. La subclasificación se basó en los parámetros morfológicos y citoquímicos utilizados por la FAB 9 con los criterios actualizados de la OMS41 y se realizó utilizando un esquema citoquímico constituido por MPOX, PAS, ANAE, ANBE, NACE y FAC. En las leucemias agudas linfoblásticas, MPOX obligadamente negativas, se recomendó su obligatoria correlación con marcadores fenotípicos (LLA, B, pre-B, común o T) si bien, las de origen T pudieron evidenciarse ya mediante la reacción ANAE positiva puntiformedot-like en los linfoblastos T, como indican otros trabajos en este campo11 - 18.
Del mismo modo en las leucemias agudas mieloides de tipo M0, M7 y en las probablemente bifenotípicas se indicó su necesaria correlación con los marcadores inmunofenotípicos para diagnóstico diferencial con las linfoblásticas. En leucemias mieloides agudas M1, M2, M3, M4, M5 y M6 de FAB, el estudio citoquímico sigue siendo de suma importancia para el diagnóstico y clasificación; no así en las M0, M7, bifenotípicas y linfoblásticas en que la citohistoquímica sola, aunque sugiere la mayor parte de los diagnósticos, necesita de técnicas complementarias como el inmunofenotipo, la citogenética o la biología molecular9, 14, 41, 45.
Teniendo en cuenta los conceptos actualizados en cuanto al reordenamiento de patologías clonales incluidas en la clasificación unificada de la OMS,41 para el grupo de leucemias agudas de cualquier tipo, deben tenerse en cuenta además del diagnóstico morfológico citoquímico subclasificatorio también el inmunofenotipo, especialmente en las linfoblásticas, así como la citogenética sobretodo en las mieloides para el pronóstico y tratamiento adecuados. En nuestros casos hemos recomendado la obligatoria correlación de los resultados morfológicos con el inmunofenotipo y la citogenética.
En caso de las aplasias medulares panmielopáticas o globales que fue el segundo grupo de enfermedades más frecuentes, en todos los pacientes se realizaron biopsias de médula ósea para confirmación diagnóstica, lo que constituye de hecho una indicación precisa 12, 24, 31. Ante la presunción clínico-hematológica de aplasia medular, en el 60% de los casos se confirmó el diagnóstico por la anatomía patológica, encontrándose en el 40% restante, otras patologías, como mielodisplasias hipocelulares, procesos fibróticos o leucemias a células peludas.
En este punto cabe resaltar que esta última enfermedad, clasificada dentro del grupo de síndromes linfoproliferativos crónicos22-27 se presentó con un cuadro clínico-hematológico citopénico con punción aspirativa medular seca, no sospechándose su diagnóstico inicialmente a la clínica en varios de ellos. En las biopsias medulares y en las improntas citológicas se observó material hipercelular constituido por proliferación de células con morfología tricoleucémica y reacción positiva multigranular y difusa a la FATR, obligadamente negativas a NACE, con un patrón de infiltración medular intersticial, aleatorio o difuso y fibrosis reticulínica grado 2 a 3.
La morfología asociada a las características citohistoquímicas en la biopsia de médula ósea, improntas y aspirados medulares así como en sangre periférica, y, en un caso en material de esplenectomía y cuña de hígado, llevó al diagnóstico final de tricoleucemia con el estudio conjunto y el empleo sistemático de las técnicas especiales anatomopatológicas. Es otro ejemplo de la importancia de la anatomía patológica y de las técnicas histoquímicas enzimáticas, como ayuda diagnóstica en casos clínicos semejantes, aunque, totalmente diferentes desde el punto de vista diagnóstico, pronóstico y terapéutico.
Otras afecciones como las leucemias linfocíticas crónicas presentan la ventaja de poder reconocer mediante la biopsia de médula ósea, el patrón de infiltración neoplásico, que no puede realizarse en materiales citológicos, aunque un buen observador podría presumirlo. En estos casos se identifican los patrones como intersticial, nodular, mixto y difuso, este último, considerado de mal pronóstico y necesario como criterio en la estadificación y en la conducta terapéutica, así como su diferenciación de procesos reactivos linfoides nodulares 31, 42, 46.
Se destaca, además, en este punto como conducta obligatoria, a la biopsia de médula ósea, la estadificación de todos los procesos proliferativos, especialmente los linfoproliferativos hodgkinianos y no hodgkinianos nodales o extranodales, acompañados o no expresión leucémica.
Notándose una diferencia significativa marcada entre el acierto diagnóstico clínico-hematológico general y específico con respecto a la anatomía patológica para los procesos linfoproliferativos, se evidencia que esta última, con la utilización sistemática de técnicas citohistoquímicas, es de suma importancia para el diagnóstico, estadificación y pronóstico, constituyéndose en un arma valiosa, complementaria e indispensable para el hematólogo en el manejo de sus pacientes.
Para el grupo de las enfermedades mielodisplásicas el diagnóstico clínico-hematológico fue positivo en una tercera parte de los casos, necesitándose de la biopsia de médula ósea en la mayor parte de ellos. En estos, los materiales fueron enviados inicialmente por sospecha clínica, para confirmación y subclasificación o en forma de diagnóstico diferencial clínico-hematológico propuesto entre mielodisplasia y eritroleucemia o entre mielodisplasia y aplasia medular, una de las mayores dificultades diagnósticas encontradas en el diagnóstico presuntivo.
Son criterios morfológicos histológicos que pueden confirmar una mielodisplasia como la alteración de la distribución topográfica pancelular normal de la médula ósea, con la presencia de localización anormal de grupos de células granulocíticas precursoras y/ o blásticas (ALIP) en forma central no peritrabecular endosteal,12, 39 así como la presencia de la paraneutrofilia acompañante evidenciada por el defecto granular de granulocitos a la naftol AS-D cloroacetato esterasa (NACE) demostrado por Schaefer en el estudio de biopsias de médula ósea incluídas en parafina, especialmente en casos de anemia refrectaria con exceso de blastos de tipo 1 o 214, 15.
Estos conceptos, además de ser criterios diagnósticos, son los que se buscan en las biopsias de médula ósea para indicar el pronóstico sombrío y la evolución hacia un cuadro próximo de transformación a leucemia aguda secundaria a tenerse en cuenta en estos pacientes16 – 18.
Es importante destacar aquí que el estudio morfológico y citohistoquímico conjunto en aspirados medulares, frotis de sangre y biopsias de médula ósea, tiene su mayor aplicación y utilidad en el diagnóstico y clasificación de las mielodisplasias, que además, permite aplicar técnicas de inmunohistoquímica en la biopsia para la detección y cuantificación de blastos CD34+14, 15, 31, 41.
En el grupo de gamapatías monoclonales, casi todos los mielomas se diagnostican por métodos clínico-hematológicos simplemente por el aspirado medular y los criterios clínicos. En los demás trastornos correspondientes a este grupo no siempre es posible un diagnóstico y una clasificación acertada, requiriéndose de la biopsia de médula ósea para definirlos.
Esto ocurre preferentemente con las infiltraciones de linfomas linfoplasmacíticos, gamapatías monoclonales de significado indeterminado, amiloidosis y la diferenciación obligatoria de cuadros reactivos como plasmocitosis marcadas. Todos los casos que se han estudiado fueron enviados para esclarecimiento diagnóstico entre infiltraciones medulares por linfomas linfoplasmacíticos y mielomas, los cuales, no han presentado los criterios clínico-hematológicos; o porque se obtuvieron punciones secas en casos que resultaron ser mielomas esclerosantes acompañados de fibrosis reticulínica de grado 3 o 4 evidenciada con tinciones argénticas en la biopsia de médula ósea.
Otros casos de sospecha mielomatosa que no presentaron criterios clínicos, secretantes, hematológicos o morfológicos evidentes en el aspirado medular, fueron plasmocitosis reactivas o gamapatías monoclonales de significado indeterminado. El diagnóstico en estos casos se basó, desde el punto de vista morfológico en criterios cuali y cuantitativos, siendo confirmados inmunohistoquímicamente por la expresión positiva de cadenas livianas kappa o lambda en biopsias de médula ósea. En estos casos se recomendó el seguimiento evolutivo obligatorio de los pacientes.
Lo mismo sucedió con las patologías extra-hematológicas, en que sólo un caso fue diagnosticado por la clínica y el aspirado medular, confirmado con la biopsia de médula ósea, encontrándose en los demás aspirado medular con material insuficiente; o se presentaban con cuadro clínico de anemia no determinada; o simplemente sin diagnóstico clínico presuntivo. En estos casos se demostró carcinomas o sarcomas metastáticos con anemia ferropénica tumoral reactiva acompañante, en la biopsia medular ósea.
En la mayoría de los materiales enviados, correspondientes a pacientes sin diagnóstico clínico evidente inicial (18%), o que consultaban por anemia cuyo origen no se determinó hematológicamente, o como síndrome febril prolongado, o estadificación neoplásica linfoproliferativa, se encontraron hiperplasias hematopoyéticas reactivas, anemias carenciales, ferropénicas, plasmocitosis reactivas y siderosis acompañantes en fumadores. Así también se encontraron procesos infecciosos leucopénicos en los que se constató dengue en uno de los casos o pacientes VIH positivos.
Los procesos hiperplásicos mayormente se encontraron como hiperplasias de tipo inflamatorio-tumoral acompañante en cuadros infecciosos crónicos o neoplásicos, enviados para estadificación sin constatarse infiltración neoplásica medular. En cuanto a los materiales hematológicos, el 72% del total estuvo constituido por cilindros biópsicos de médula ósea, la mayor parte acompañado de sus extendidos de aspirado medular y sangre periférica. Estos fueron enviados al departamento para diagnóstico histopatológico y citohistoquímico en casos de estadificación de procesos linfoproliferativos, confirmación de aplasias medulares, gamapatías monoclonales y metástasis, así como para la clasificación e índice pronóstico de enfermedades mieloproliferativas crónicas y mielodisplasias14, 31, 41.
El 28% del material restante correspondiente a extendidos de aspirados medulares y sangre periférica fueron enviados al departamento para estudio citoquímico enzimático, diferenciación y subclasificación de leucemias agudas mieloides y linfoblásticas y de mielodisplasias. Cabe recalcar aquí que el estudio anatomopatológico que incluye tanto el aspecto histológico de la biopsia como el citológico de los extendidos con la aplicación de esta metodología citoquímica sistemática y conjunta permite obtener todos los criterios morfológicos necesarios para diagnosticar, clasificar, pronosticar y cuantificar las alteraciones, lo que resulta de gran ayuda al patólogo en la interpretación de cada caso en particular13-20.
En los casos con informes de material insuficiente para evaluación con necesidad de repetir el procedimiento, se notó que sólo en 3 casos, se repitió la biopsia, no se aclararon los motivos. En cuanto al tamaño de los cilindros, la longitud de la mayor parte fue menor a 2 cm, lo que indica que aunque se llegó a una interpretación diagnóstica confirmada es recomendable mejorar la longitud de la biopsia en el procedimiento de extracción, llegando a los valores estandarizados de 2 a 3 cm de longitud12, 14, 15.
La frecuencia urbana de pacientes, en su mayor parte capital y alrededores, obedece probablemente a su condición socioeconómica, así como a la facilidad de consulta con profesionales especialistas en este ámbito. Los casos rurales fueron remitidos por profesionales generales.
Los datos de frecuencia de aparición de las enfermedades hematológicas encontradas en nuestra casuística son equiparables a los de la literatura 24, 31, 41 siendo los procesos linfo 42, 46, 48, 49 y mieloproliferativos crónicos,14, 31 las mielodisplasias y gamapatías monoclonales 31, 47 de presentación muy frecuente en adultos, así como las metástasis de adenocarcinomas con primarios mamarios, prostáticos o digestivos para adultos y los neuroblastomas para niños40. Las leucemias agudas linfoblásticas de presentación más frecuente en niños pequeños y las mieloides en adultos, encontradas también en la literatura12, 13, 14, 24, 31, 41, 43.
Del análisis estadístico de casos enviados, con distintas presunciones diagnósticas clínico-hematológicas, ya sean para confirmación diagnóstica anatomopatológica y/o análisis de factores pronósticos y/o clasificación de subtipos, comparando los métodos clínico-hematológicos con los anatomopatológicos se constató un acierto diagnóstico general sólo en un tercio de los casos (39%), los cuales presentaron presunciones clínicas acertadas confirmadas por la anatomía patológica. Este acierto fue aún menor (23%) en el diagnóstico específico en el momento de clasificación o estadificación, necesitándose del estudio anatomopatológico con técnicas especiales en la mayor parte de los casos. Como prueba diagnóstica, con una sensibilidad de 54,58%, una especificidad de 5% y altos porcentajes de falsos negativos (45%) y falsos positivos (95%), el método clínico-hematológico con aspirados medulares y/ o frotis de sangre periférica solos podrá diagnosticar solamente la mitad de los casos.
La concordancia diagnóstica mínima encontrada entre los métodos (IK = 0,38) implica que los aspirados medulares y frotis de sangre periférica resultan insuficientes cuando son utilizados aisladamente, para el diagnóstico definitivo en gran parte de casos, necesitándose estudios complementarios con técnicas anatomopatológicas especiales confirmatorias.
Se demuestra de esta manera la utilidad y la imperiosa necesidad de combinar los procedimientos clínico-hematológicos con la biopsia de médula ósea y el estudio con técnicas especiales aplicadas sistemáticamente para llegar a un diagnóstico final correcto en este tipo de enfermedades, resultando imprescindibles en los casos leucopénicos y con aspirados medulares hipocelulares, en que prácticamente no existe de por sí, material extraíble para evaluación citológica morfológica diagnóstica. La indicación acertada de biopsia de médula ósea, así como el análisis anatomopatológico con técnicas especiales enzimáticas utilizadas sistemática y conjuntamente en materiales histo y citológicos, contribuyó en gran medida a proporcionar datos pronósticos y a esclarecer o confirmar el diagnóstico final en casi todas las patologías.
En el 2% de casos (6 de 370 casos) En estos no se llegó al diagnóstico final por ninguno de los métodos, necesitándose de otras técnicas complementarias como marcadores celulares, citogenética o biología molecular para una confirmación o clasificación diagnóstica. En nuestra serie, estos correspondieron a una mastositosis sistémica con asociación hematológica clonal de células no mastocíticas, comprobada por inmunohistoquímica con triptasa mastocítica positiva, descartándose un proceso linfoproliferativo y a la patología mieloproliferativa acompañante como leucemia mieloide crónica con eosinofilia, por citogenética y biología molecular. Esta presentó resultados negativos para el cromosoma Philadelphia y para la fusión del gen BCR/ ABL. No pudo clasificarse inicialmente, sino posteriormente, con estudios complementarios y con la evolución, como una leucemia mielomonocítica crónica. En la clasificación actual de la OMS41 se encuentra a esta entidad como una mastocitosis sistémica con asociación clonal hematológica de células no mastocíticas.
Otros casos como leucemias agudas LMA-M3 variante microgranular, LMA-M7, LMA-M0 con mielodisplasia anterior, necesitaron marcadores celulares, citogenética y biología molecular para diagnóstico definitivo; una aplasia selectiva bilineal de series eritroblástica y megacariocítica, en la que se indicó el estudio citogenético para diferenciarla de una mielodisplasia, aunque en biopsias secuenciales, no se encontraron criterios morfológicos e histoquímicos de mielodisplasia; y un probable caso de síndrome de Sézary no característico a la clínica ni al frotis de sangre periférica que resultó ser una farmacodermia con linfocitosis T reactiva.
A la Prof. Dra. Elena Kasamatsu y al Prof. Dr. Alfredo Boccia Paz por el asesoramiento tutorial de esta tesis. Al Dr. José Ferreira Nizza por el apoyo constante, de siempre, a la Sección de Hematopatología del IICS siendo uno de sus mayores propulsores y colaboradores. Al Prof. Dr. Esteban Ferro y a la Dra. Graciela Velázquez por las sugerencias, correcciones y por sus contribuciones a mi formación en metodología de la investigación. Al Prof. Dr. Hans Eckardt Schaefer del Instituto de Patología de Freiburg-Alemania por el entrenamiento en hematopatología con el compromiso de utilizar los conocimientos en la asistencia, docencia e investigación en nuestro país. A todos los hematólogos y oncólogos de los distintos centros asistenciales del país, que envían sus materiales para estudio al departamento. A los Pacientes, a quienes servimos con humildad, brindándoles lo mejor de nuestra formación, haciendo todo lo que está a nuestro alcance, pasando sobre trabas económicas y burocráticas para solucionar los problemas diagnósticos que a diario encontramos en nuestro medio. A ellos les damos las gracias porque nos permiten enriquecernos en la experiencia médica diaria, en la investigación y por lo tanto aportar conocimientos a la docencia.
1. Lafuente R, Woessner S. Métodos de estudio de órganos hematopoyéticos. En: Sans Sabrafen J. Hematología Clínica. Segunda edición. Barcelona. España. Ediciones Doyma. 1987; 2-3: 19-42[ [ Links ]STANDARDIZEDENDPARAG]
2. Brunning R. Bone marrow Specimen Processing. En: Knowles DM. Neoplastic Hematopathology. Primera edición. New York. USA: Ediciones Williams & Wilkins. 1991; 35: 1081-1097[ [ Links ]STANDARDIZEDENDPARAG]
3. Ehrlich P. Üeber die specifischen Granulationes des Blutes. En: Ehrlich P. Editores. Untersuchungen zur Histologie und Klinik des Blutes. Gesammelte Mitteilungen. Berlin. 1891; 5-17[ [ Links ]STANDARDIZEDENDPARAG]
4. Pappenheim A. Panoptische Universalfärbung der Blutpräparate. Med Klin 1908; 4: 1244-48[ [ Links ]STANDARDIZEDENDPARAG]
5. Brandenburg K. Über die Reaction der Leukocyten auf die Guajaktinctur. Münch Med Wochenschr 1900; 6: 183-6[ [ Links ]STANDARDIZEDENDPARAG]
6. Naegeli O. Üeber rothes Knochenmark und Myeloblasten. Dtsch Med Wochenschr 1900; 26: 287-90[ [ Links ]STANDARDIZEDENDPARAG]
7. Naegeli O. Blutkrankheiten und Blutdiagnostik. Berlin: Springer. 1923[ [ Links ]STANDARDIZEDENDPARAG]
8. Bennett JM, Catovsky D, Daniel M et al. Proposals for the classification of the acute leukaemias. Br J Haematol 1976; 33: 451-8[ [ Links ]STANDARDIZEDENDPARAG]
9. Bennett JM, Catovsky D, Daniel MT et al. Proposed revised criteria for the classification of acute myeloid leukemia. A report of the French-American-British Cooperative Group. Ann Med 1989; 103: 6205-12[ [ Links ]STANDARDIZEDENDPARAG]
10. Schaefer HE. Histologie und Histochemie am Paraffinschitt. Verh Dtsch Ges Pathol 1983; 67: 6-7[ [ Links ]STANDARDIZEDENDPARAG]
11. Schaefer HE. Citology and Histology of the normal human bone marrow. En: Lennert K. Hübner K, editores. Pathology of the bone marrow. Stutrgart: Fischer. 1984; 33-53[ [ Links ]STANDARDIZEDENDPARAG]
12. Catovsky D. The Leukemic Cell. Segunda edition. London UK: Ed Churchill Livingstone. Medical Division of Longman Group UK Limited; 1991[ [ Links ]STANDARDIZEDENDPARAG]
13. Remmele W und Schaefer HE. Erythropoese, Leukopoese und myeloproliferative Erkrankungen. En: Herausgegeben von W. Remmele. Pathologie 1. Sringer Verlag: Germany. 1984: 5-6: 273-452[ [ Links ]STANDARDIZEDENDPARAG]
14. Mufti GJ, Flandrin G, Schaefer HE, Sandberg AA and Kanfer E (eds). An Atlas of Malignant Haematology. Cytology, Histology and Cytogenetics. Martin Dunitz Ltd. London; 1996[ [ Links ]STANDARDIZEDENDPARAG]
15. Schaefer HE. Die histologische Bearbeitungstechnik von Beckenkammbiopsien auf der Basis von Entkalkung und Paraffineinbettung unter Berücksichtigung osteologischer und hämatologischer Fragestellungen. Pathologe 1995; 16: 11-27[ [ Links ]STANDARDIZEDENDPARAG]
16. Schaefer HE. Methoden zur histologischen, zytologischen und zytochemischen Diagnostik von Blut und Knochenmark. En: Remmele W (Hrsg.) Pathologie. Bd 1. Springer: Verlag. Berlin 1984; 6: 435-452[ [ Links ]STANDARDIZEDENDPARAG]
17. Schaefer HE. How to fix, decalcify and stain paraffin embedded bone marrow biopsies. Cytology and histology of the normal human bone marrow. En: Lennert K, Hübner eds. Pathologie of the bone marrow. Fischer: Stuttghart 1984; 33-53[ [ Links ]STANDARDIZEDENDPARAG]
18. Schaefer HE. Zytologische Hämatopathologie unter besonderer Berücksichtigung histochemischer Methoden. Basel: Karger. Beitr Onkol, 1990; 38: 196-260[ [ Links ]STANDARDIZEDENDPARAG]
19. Böck P. (Hrsg.) Mickroskopische Technik/ Romeis. Urban und Schwarzenberg. München; 1989[ [ Links ]STANDARDIZEDENDPARAG]
20. Figueredo SJ. Utilización y aplicación de técnicas de citohistoquímica enzimática en biopsias de médula ósea. Anales de la Facultad de Ciencias Médicas. Asunción–Paraguay. 1997; 30 (1-2): 81-97[ [ Links ]STANDARDIZEDENDPARAG]
21. McFarland W and Dameshek W. Biopsy of bone marrow with the Vim-Silverman needle. JAMA 1958; 166: 1464-1466[ [ Links ]STANDARDIZEDENDPARAG]
22. Duhamel G. Histopathologie Clínique de la Moelle Osseuse. Monographies d´histopathologie publiées sous la direction de Jean de Brux. Masson & C, Éditeurs. Paris. France; 1974[ [ Links ]STANDARDIZEDENDPARAG]
23. Wittels B. Surgical pathology of Bone Marrow-Core Biopsy Diagnosis. Vol 17 in the series Major problems in pathology. Ed. W B Saunders Company. USA; 1985[ [ Links ]STANDARDIZEDENDPARAG]
24. Nieto L Hernández y Rozman C. Biopsia medular en la clínica hematológica. Salvat Editores, S.A. Barcelona: España; 1980[ [ Links ]STANDARDIZEDENDPARAG]
25. Jamshidi K and Swain W. Bone marrow biopsy with unaltered architecture. J Lab Clin Med 1971; 77: 33-42[ [ Links ]STANDARDIZEDENDPARAG]
26. Goldenberg AS and Tiesinga JJ. Clinical experience with a new specimen capturing bone marrow biopsy needle. Am J Hematol 2001; 68: 189-193[ [ Links ]STANDARDIZEDENDPARAG]
27. Dacie SJV and Lewis SM. Practical Haematology. Churchill Livingstone Longman Group limited. London and New York; 1984[ [ Links ]STANDARDIZEDENDPARAG]
28. Wickramasinghe SN. Bone Marrow. En: Histology for Pathologists. Stephen S Sternberg. Raven Press Ltd. New York. 1992; 1: 1-31[ [ Links ]STANDARDIZEDENDPARAG]
29. Juneja SK, Wolf MM and Cooper IA. Value of bilateral bone marrow biopsy specimens in non-Hodgkins lymphoma. J Clin Pathol 1990; 43: 630-632[ [ Links ]STANDARDIZEDENDPARAG]
30. Hayhoe FGJ and Quaglino D. Haemathological Cytochemistry. Churchill Livingstone Longman Group limited. London and New York; 1980[ [ Links ]STANDARDIZEDENDPARAG]
31. Knowles DM. Neoplastic Hematopathology. Segunda edición. New York. USA: Williams & Wilkins; 2001[ [ Links ]STANDARDIZEDENDPARAG]
32. Bhatia M, Bonnet D, Murdoch B, Gan O and Dick J. A newly discovered class of human hematopoietic cells with SCID-repopulating activity. Nature Medicine 1998; Vol 4: 1038-1045[ [ Links ]STANDARDIZEDENDPARAG]
33. Young NS and Maciejewski J. The pathophysiology of acquired aplastic anemia. The New England Journal of Medicine 1997; 336 (19): 1365-1372[ [ Links ]STANDARDIZEDENDPARAG]
34. Peichev M, Naiyer AJ, Pereira D, Zhu Z et al. Expression of VEGFR-2 and AC133 by circulating human CD34+ cells identifies a population of functional endothelial precursors. Blood 2000; 95: 952-958[ [ Links ]STANDARDIZEDENDPARAG]
35. Kennedy M, Firpo M, Chol K, Wall C et al. A common precursor for primitive erythrpoiesis and definitive haematopoiesis. Nature 1997; 386: 488-493[ [ Links ]STANDARDIZEDENDPARAG]
36. Francis K, Ramakrishna R, Holloway W and Palsson B. Two new pseudopod morphologies displayed by the human hematopoietic KG1a progenitor cell line and by primary human CD34+ cells. Blood 1998; 92: 3616-3623[ [ Links ]STANDARDIZEDENDPARAG]
37. Penchansky L. Hematopoietic System. I Bone Marrow and Peripheral Blood in Potters Pathology of the fetus and infant. Enid Gilbert-Barness. Mosby-Year book, Inc. USA. 1997; 23: 936-979[ [ Links ]STANDARDIZEDENDPARAG]
38. Farhi Diane C. Germinal centers in the Bone Marrow. Hematologic Pathology 1989; 3 (3): 133-136[ [ Links ]STANDARDIZEDENDPARAG]
39. Thiele J. Introduction to bone marrow pathology. Slide seminar. En: the XIX Brazilian Congress of Pathology of the Brazilian Society of Pathology. Junio, 1993[ [ Links ]STANDARDIZEDENDPARAG]
40. Brunning RD and McKenna RW. Tumors of the Bone Marrow. Atlas of Tumor Pathology. Juan Rosai Editor. New York; 1994[ [ Links ]STANDARDIZEDENDPARAG]
41. Jaffee E, Harris N, Stein H and Vardiman J. Pathology and genetics of tumours of haematopoietic and lymphoid tissues. World Health Organization Classification of Tumours. WHO. OMS. Published by IARC Press, International Agency for Research on Cancer. 150 cours Albert Thomas, F-69008 Lyon, France; 2001[ [ Links ]STANDARDIZEDENDPARAG]
42. Schaefer HE. The histotopography of bone marrow involvemeny in low malignant B-Cell lymphoma. En: Hara H (de) Contributions in Celebation of the 65th Published by The First Departament of Pathology, Kochi Medical School, Shinkodo Printing Company, Kochi: Japan; 1995: 115-150[ [ Links ]STANDARDIZEDENDPARAG]
43. Riede UN, Herbst EW und Schaefer HE. Hämatopoetisches und lymphatisches System. En: Allgemeine und Spezielle Pathologie. Georg Thieme Verlag. Stuttgart: Germany. 1995; 10: 526-586[ [ Links ]STANDARDIZEDENDPARAG]
44. Hulley SB and Cummings SR. Diseño de la Investigación Clínica. Reimpresión. Apéndice 13.E.1. 1997; 236[ [ Links ]STANDARDIZEDENDPARAG]
45. Bain BJ. Routine und specialised techniques in the diagnosis of haematological neoplasms. J Clin Pathol 1995; 48: 501-8[ [ Links ]STANDARDIZEDENDPARAG]
46. Bennet JM, Catovsky D, Daniel M et al. Proposal for the Classification of chronic (mature) B and T lymphoid leukaemias. J Clin Pathol 1989; 42: 567-84[ [ Links ]STANDARDIZEDENDPARAG]
47. McCurley TL, Cousr JB, Stanley E et al. Plasma Cell Iron - Clinical and Morphologic Feactures. Am J Clin Pathol 1984; 81: 312-316[ [ Links ]STANDARDIZEDENDPARAG]
48. Nieto LH, Lampert IA and Catovsky D. Bone Marrow Histologycal Patterns in B Cell Prolymphocytic Leukaemia. Hemat Pathol 1989; 3 (2): 79-84[ [ Links ]STANDARDIZEDENDPARAG]
49. Pangalis GA y col. B-Chronic Lymphocytic Leukaemia. Prognostic Implication of bone marrow histology in 120 Patients. Experience from a Single Hematology Unit.Cáncer 1987; 59:767-71[ [ Links ]STANDARDIZEDENDPARAG]
50. Figueredo SJ. Diagnóstico anatomopatológico de las leucemias a células peludas en el Paraguay. Monografía presentada para título de especialista en Anatomía Patológica por la Escuela de Postgrado de la Facultad de Medicina de la Universidad Nacional de Asunción. Año 2002. Mem. Inst. Invest. Cienc. Salud /publicación periódica en línea/ 2003 /citada 2004 setp 15/; 2 (1) en: http://www.iics.una.py/memorias.htm[ [ Links ]STANDARDIZEDENDPARAG]














