INTRODUCCIÓN
Las investigaciones basadas en el registro de electrogramas locales auriculares anormalmente prolongados y fraccionados durante el ritmo sinusal y su distribución característica en la aurícula derecha de pacientes con disfunción del nódulo sinusal (DNS) han aportado un conocimiento importante sobre las propiedades electrofisiológicas de la aurícula patológica1-4. Estudios patológicos detallados y cuantitativos realizados en pacientes con DNS Tipo III de Rubenstein han demostrado una fibrosis extensa del miocardio auricular en la vecindad del nódulo sinusal y en los tractos internodales. Cuando las fibras musculares auriculares se encuentran separadas por tejido conjuntivo, las propiedades de conducción pueden alterarse debido a los efectos sobre la resistencia axial, creando una propagación discontinua y anisotrópica5-8.
Cuando las paredes auriculares se encuentran marcadamente alteradas por fibrosis, la onda de despolarización debe cambiar frecuentemente de dirección respecto de la orientación longitudinal de la fibra miocárdica. Esto provocaría bloqueos unidireccionales, conducción lenta y dispersión de los periodos refractarios en determinados sitios, generando los elementos fundamentales del mecanismo de la reentrada y desarrollando episodios de arritmias auriculares y fibrilación auricular (FA) (9-13. Es nuestra intención presentar un paciente con diagnóstico documentado de DNS Rubenstein tipo III por episodios paroxísticos de FA intercalados con episodios de bradicardia sinusal extrema. Se documentó una estenosis severa proximal de la arteria coronaria derecha como posible causa isquémica de la disfunción nodal. No obstante, la revascularización exitosa de la coronaria derecha con angioplastia e implante de stent medicado que restableció el flujo sanguineo adecuado a la arteria del nódulo sinusal, no produjo una mejoría de la función del nódulo sinusal.
Caso clínico:
Paciente de sexo masculino, 59 años de edad, hipertenso sin tratamiento y con antecedente de síncope en 2 oportunidades en los últimos 4 meses. Acudió al servicio de urgencias por cuadro de inicio brusco y de minutos de duración de palpitaciones, mareos, sudoración fría, opresión torácica y pre-síncope. Al ingreso se constató una presión arterial de 120/70 mmHg, una frecuencia cardiaca de 280 lat/min, y una frecuencia respiratoria de 24 por min. Al examen físico presentaba una taquicardia regular, sin congestión pulmonar, sudoración fría. El electrocardiograma (ECG) reveló un flutter auricular típico con conducción auriculo-ventricular (AV) 1:1, que luego pasa a una conducción AV 2:1 con el inicio de una carga y mantenimiento de Amiodarona (Figura 1) y posteriormente revierte a ritmo sinusal a una FC de 60 latidos/minuto. Un Holter de 24 horas demostró un ritmo sinusal predominante, episodios paroxísticos de fibrilación auricular con respuesta alta (FARVA), bradicardia sinusal (FC mínima de 47 latidos/minuto), con pausas sinusales significativas (Figura 2). Se realizó el diagnóstico de enfermedad del nódulo sinusal, Rubenstein tipo III (Síndrome Bradicardia-Taquicardia). La ecocardiografía Doppler demostró una cardiopatía hipertensiva con fracción de eyección conservada y sin trastornos de la motilidad segmentaria. Se realizó una coronariografía para descartar una cardiopatía isquémica como causa de la disfunción del nódulo sinusal. Se constató una estenosis del 80% en el segmento proximal de la arteria coronaria derecha con componente espástico (Figura 3). La arteria del nódulo sinusal emerge del segmento proximal de la coronaria derecha. Se realiza una angioplastia exitosa con stent medicado (Figura 4) y el paciente es dado de alta con amlodipina y mononitrato de isosorbide como tratamiento vasodilatador, además de antiplaquetarios y estatinas. Otro estudio Holter de 24 horas de control pos-angioplastia registró nuevamente episodios paroxísticos de FARVA y episodios de pausas de hasta 3.100 milisegundos por lo que se indica finalmente la implantación de un marcapasos bicameral y farmacoterapia para control de frecuencia de las taquiarritmias.
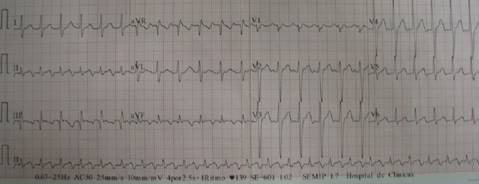
Figura 1: Electrocardiograma de 12 derivaciones que demuestra un flutter auricular con conducción AV de 2:1 a una frecuencia ventricular de 150 lat/min. Se trata de un flutter típico con ondas P negativas en la cara inferior debido a la despolarización antihoraria del septum interauricular.
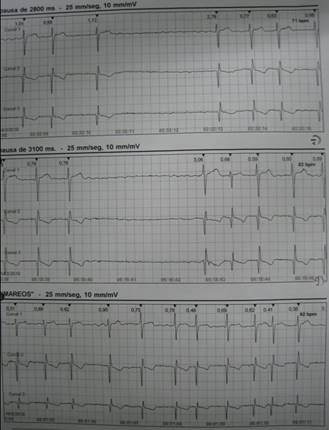
Figura 2: Registro electrocardiográfico ambulatorio Holter de tres canales demostrando el síndrome bradicardia-taquicardia, disfunción del nódulo sinusal, Rubenstein tipo III. En el panel superior se observa una pausa sinusal de 2,78 segundos. En el panel del medio se observa una pausa sinusal de 3,05 segundos. En el panel inferior se observa una fibrilación auricular con una frecuencia ventricular de 112 lat/min.
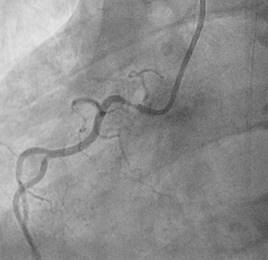
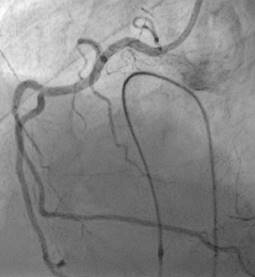
Figura 3: Coronariografía de la arteria coronaria derecha. Se observa una estenosis severa en el segmento proximal.
DISCUSIÓN
La clave para llegar al diagnóstico de esta entidad nosológica es establecer una correlación entre los síntomas clínicos descritos por los pacientes y los hallazgos electrocardiográficos. Un ECG convencional de rutina o un monitoreo Holter de 24 horas pueden confirmar el diagnóstico de disfunción del nódulo sinusal si los hallazgos electrocardiográficos típicos pueden correlacionarse con los síntomas (10-12.
Los hallazgos electrocardiográficos típicos son uno o más episodios de bradicardia sinusal extrema (Rubenstein Tipo I), o pausas sinusales, paro y bloqueo de salida sinoatrial (Rubenstein Tipo II), o episodios de bradicardia y/o pausas alternantes con taquiarritmias auriculares (Rubenstein Tipo III)8. Sin embargo, en algunos pacientes, es posible que se requieran pruebas diagnósticas adicionales y no se debe diagnosticar la DNS hasta que se hayan identificado y tratado las causas secundarias potencialmente reversibles, que incluyen el uso de fármacos, isquemia miocárdica, hipotiroidismo y desequilibrio autonómico8-10. En nuestro paciente pudimos descartar todas estas causas secundarias de DNS. Si bien la coronariografía demostró una estenosis severa en el segmento proximal de la arteria coronaria derecha como posible causa isquémica, la angioplastia coronaria demostró que al menos no se trataba de una causa aguda de isquemia tisular. A pesar del restablecimiento de un buen flujo sanguíneo adecuado a la arteria del nódulo sinusal con la angioplastia de la coronaria derecha no se obtuvo una mejoría de la disfunción del nódulo sinusal. Como nuestro paciente ya tenía como antecedente dos episodios de síncope en los últimos 4 meses, al documentarse el síndrome bradicardia-taquicardia en el Holter, y al observarse la irreversibilidad de la DNS al restablecerse un flujo sanguíneo adecuado al nódulo sinusal se implementó un tratamiento definitivo. Le implantamos un marcapasos bicameral e iniciamos farmacoterapia para control de la frecuencia de las taquiarritmias.
La incompetencia cronotrópica en las pruebas de esfuerzo, es decir, un aumento subnormal en la frecuencia cardíaca después del ejercicio puede ayudar a identificar a las personas con función anómala del nódulo sinusal que pueden beneficiarse de la implantación de un marcapasos (12. Los estudios electrofisiológicos permiten determinar ciertos parámetros que hablan de la DNS como por ejemplo el tiempo de recuperación del nódulo sinusal, y el tiempo de conducción del nódulo sinusal. Por lo tanto, este estudio invasivo podría considerarse especialmente en aquellos pacientes que persisten sintomáticos y en quienes no se han documentado las alteraciones electrocardiográficas descritas (10. Los estudios electrofisiológicos en pacientes con disfunción del nódulo sinusal Tipo III de Rubenstein presentan ciertas limitaciones. Debido a la facilidad con que estos pacientes desarrollan fibrilación auricular mediante la estimulación cardíaca programada durante el estudio electrofisiológico en el laboratorio, no se puede realizar un análisis detallado de las propiedades electrofisiológicas del miocardio auricular ya que la fibrilación auricular no permite la realización de las mediciones correspondientes. Por ende, los datos obtenidos mediante el mapeo endocárdico auricular durante ritmo sinusal adquieren una incuestionable importancia en el conocimiento del sustrato electrofisiológico auricular (13-15. Las investigaciones basadas en el registro de electrogramas locales auriculares anormalmente prolongados y fraccionados durante el ritmo sinusal y su distribución característica en la aurícula derecha de pacientes con disfunción del nódulo sinusal han aportado un conocimiento importante sobre las propiedades electrofisiológicas de la aurícula patológica (16-18.
Hemos observado que los electrogramas auriculares endocárdicos anormalmente prolongados y fraccionados registrados en la aurícula derecha denotan una conducción auricular irregular; que se registran frecuentemente en pacientes con disfunción del nódulo sinusal Tipo III de Rubenstein2-4. El mapeo endocárdico auricular en pacientes con fibrilación auricular paroxística ha proporcionado más conocimiento acerca del sustrato electrofisiológico de esta taquiarritmia. La implicancia clínica demostrada es que la detección de electrogramas auriculares anormales identifica a un grupo de pacientes, tales como nuestro paciente con DNS y episodios paroxísticos de fibrilación auricular, con vulnerabilidad auricular aumentada y con incidencia significativamente mayor de episodios espontáneos o inducidos de fibrilación auricular2-4.
En conclusión, hemos demostrado con nuestro paciente con disfunción del nódulo sinusal la importancia de estudiar adecuadamente la anatomía coronaria y descartar la posibilidad de isquemia miocárdica como causa secundaria de DNS. No obstante, la revascularización exitosa de una estenosis severa de la coronaria derecha que restablece el flujo sanguíneo adecuado a la arteria del nódulo sinusal, no garantiza el restablecimiento de la función del nódulo sinusal.