INTRODUCCIÓN
El virus de papiloma humano (VPH) es un virus ADN de doble hebra, su genoma posee aproximadamente 8000 pares de bases y en él se diferencian tres regiones:
La región reguladora larga (LCR) la cual es no codificante y posee secuencias que controlan la trascripción y replicación viral, ya que posee elementos cis necesarios para la replicación y transcripción del ADN viral1.
La región temprana E, que codifica para las proteínas E1, E2, E4, E5, E6 y E7, involucradas en múltiples funciones como transcripción, replicación y transformación celular. Las oncoproteínas E6 y E7 crean inestabilidad genómica e interfieren en vías de proteínas supresoras de tumores(2).
Y la región tardía L, que codifica para las proteínas estructurales L1 y L2 las cuales forman la cápside viral y participan en el ensamblaje del ADN viral. Las proteínas L1 y L2 se ensamblan en capsómeros para dar lugar a la cápside de forma icosaédrica que contiene el genoma viral1,3.
Actualmente se han descrito más de 150 tipos de VPH, de los cuales aproximadamente 50 infectan la mucosa genital. Los VPH de tropismo mucoso se clasifican en tipos de ‘alto’ (VPH-AR) y ‘bajo’ (VPH-BR) riesgo oncogénico, siendo los de bajo riesgo los causantes de lesiones benignas y los de alto riesgo los causantes de lesiones que pueden progresar a tumores malignos4-7.
Los genotipos incluidos en el grupo de virus de alto riesgo oncogénico son 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59 y 68. Esta clasificación obedece a su relación con el desarrollo de neoplasia intraepitelial cervical (CIN). Estudios previos han demostrado que los tipos 16 y 18 son los genotipos de alto riesgo más frecuentemente detectados en cáncer cervical; en aproximadamente el 50% y 20% de casos, respectivamente(3,4,8,9).
La infección persistente puede dar lugar a una lesión intraepitelial escamosa de bajo grado (LSIL) y ésta conducir a una lesión intraepitelial escamosa de alto grado (HSIL) y cáncer en un promedio de 5 a 14 años si no se detectan y se tratan. Es importante el tipo viral, ya que la persistencia viral constituye un factor de riesgo clave para el desarrollo de lesiones de alto grado y cáncer. La persistencia está genéticamente determinada y guarda relación con la patogenicidad3,10. Sin embargo, la progresión a cáncer ocurre solo en un pequeño porcentaje de mujeres infectadas, ya que la mayoría elimina la infección en 1-2 años11.
A nivel mundial se registraron aproximadamente 528.000 casos nuevos de cáncer de cuello uterino y 266.000 muertes en 201212. En Paraguay un estudio realizado en el 2012 por Kasamatsu et al. observó en 432 casos de cáncer cervical, una frecuencia de 64,6% de VPH 16, seguido de 8,5% por VPH 18 y 5,4% de VPH 4513.
Sin embargo, debido a que la mayoría de pruebas de VPH basadas en ADN tienen un bajo valor predictivo positivo para detección de CIN2 o más, se debe identificar a las mujeres en riesgo de desarrollar una infección persistente o lesión precursora de cáncer mediante pruebas de triage para evitar la sobrecarga al sistema de salud y la carga emocional que representa para la mujer14.
Debido a esto, se diseñó este estudio con el objetivo de estandarizar y determinar el límite de detección de una técnica de PCR convencional para la detección de VPH 16 y 18 que puede ser utilizada como triage con miras a su implementación en servicios de salud y para orientar el manejo clínico de mujeres positivas para VPH-AR.
MATERIALES Y MÉTODOS
Para la optimización de las PCR se utilizaron controles positivos de VPH 16 y VPH 18 provenientes del biobanco del Departamento de Salud Pública (IICS-UNA), previamente tipificados en estudios anteriores (14INVO36, P11/2010). Fueron utilizados controles puros y diluidos.
Para la extracción de ADN viral de los controles positivos se utilizó el kit comercial AccuPrep® Genomic DNA Extraction Kit (Bioneer, Corea) siguiendo las instrucciones del fabricante. El ADN extraído fue almacenado a -20°C hasta su procesamiento.
Optimización de PCR para VPH 16 y VPH 18
La detección del genoma de VPH 16 y VPH 18 se realizó amplificando un fragmento de la región LCR de controles positivos a través de reacciones de PCR descriptas por Ho et al. en 1991 para VPH 16, y Ong et al. en 1993 para la detección de VPH 18. Se utilizaron los primers 16a/16b para VPH 16, y 18a/18b para VPH 18, que amplifican un fragmento de 364 pares de bases y 320 pares de bases, respectivamente(15,16) (Tabla 1).
Cada tubo de reacción contenía 2 μL de buffer 10x, 1,6 μL de MgCl2 25 mM, 1,6 μL de dNTPs 2,5 mM, 1 μL de cada primer 16a/16b ó 18a/18b, 0,17 μL de Taq polimerasa 5 U/L (Thermo Scientific, EEUU), 9,63 μL de agua libre de Nucleasa (Thermo Scientific, EEUU) y 3 μL del control positivo para VPH 16 o VPH 18, para un volumen final de 20 μL. Las condiciones de termociclado fueron 40 ciclos de 3 minutos a 94 °C, luego 94 °C por 1 minuto, 65 °C por 1,5 minutos y 72 °C por 2 minutos, un paso final de 5 minutos a 72 °C.
La presencia del genoma del VPH se visualizó por electroforesis en gel de poliacrilamida teñido con nitrato de plata según el protocolo establecido por Sanguinetti et al., 1994. En cada corrida electroforética se utilizó un marcador de peso molecular 50 pares de bases (Thermo Scientific, EEUU)17,18.
Bajo estas condiciones se probó la reacción a tres concentraciones distintas de MgCl2: a 1,5mM; 2,0mM y 2,5mM. Para determinar la temperatura de alineamiento, se probó la reacción a 60 y 65°C.
Determinación del límite de detección
Posterior a la optimización de las PCR se determinó el límite de detección de las reacciones utilizando un control positivo de VPH 16 de 14,6ng/µL y un control positivo de VPH 18 de 21,7ng/µL. Se prepararon diluciones seriadas con factor de dilución de 10. Se seleccionaron las diluciones de 10-5 a 10-12 del control VPH 16 y, de 10-6 a 10-13 del control VPH 18, a fin de determinar hasta que título es detectable el genoma viral.
Todas las diluciones de los controles fueron sometidas a PCR por triplicado y posterior electroforesis. Se obtuvieron tres geles mediante los cuales determinó el límite de detección para cada tipo de VPH, concordando al menos dos de ellos en la última dilución en la que se detectó producto.
RESULTADOS
Optimización de PCR para VPH 16 y VPH 18
En relación a la concentración de MgCl2, para el control VPH 16 puros se observaron bandas a las tres concentraciones analizadas. Con el control diluido sólo se observaron bandas a 2 y 2,5 mM. Sin embargo, se optó por utilizar la concentración final de 2mM ya que se obtuvieron bandas nítidas tanto con el control puro como diluido.
Para el control VPH 18 puro se observaron bandas a 2 y 2,5mM, mientras que el control diluido sólo presentó banda a 2,0mM. Por lo tanto, se optó por utilizar la concentración final de 2mM. Estos resultados se aprecian en la Figura 1.
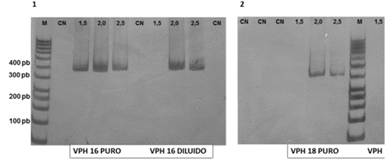
Figura 1: Electroforesis en gel de poliacrilamida al 5% de los productos amplificados para la región LCR de VPH 16 y 18 a distintas concentraciones de MgCl2. (M) Marcador de 50 pares de bases. (CN) Control negativo. (1,5) Control a 1,5 mM de MgCl2. (2,0) Control a 2,0 mM de MgCl2. (2,5) Control a 2,5 mM de MgCl2.
En cuanto a la temperatura de alineamiento, se probaron las reacciones a 60°C y 65°C. En la Figura 2 se observan los productos de amplificación de VPH 16 y VPH 18 a 60°C y 65°C, respectivamente. Con la primera temperatura analizada se observaron bandas nítidas tanto para el control de VPH 16 como para el control de VPH 18, mientras que a 65°C solo se visualizó una banda tenue correspondiente al control VPH 16 puro. Con base en esto se optó por la temperatura de 60°C en ambas reacciones.
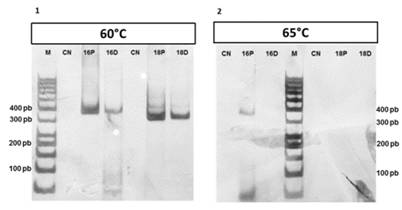
Figura 2: Electroforesis en gel de poliacrilamida al 5% de los productos amplificados para la región LCR de VPH 16 y 18 a 60 y 65°C. (M) Marcador de 50 pares de bases. (CN) Control negativo. (16P) Control VPH 16 puro. (16D) Control VPH 16 diluido. (18P) Control VPH 18 puro. (18D) Control VPH 18 diluido.
Límite de detección
En relación al límite de detección para VPH 16, en la Figura 3 se observa un resultado positivo hasta la dilución 10-11, es decir, hasta 14,6x10-11ng/µL.
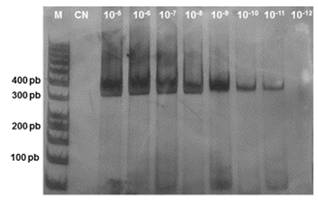
Para el control VPH 18, se observó resultado positivo hasta la dilución 10-12, es decir hasta 21,7x10-12ng/µL. Estos resultados se observan en la Figura 4.

Figura 4: Límite de detección para PCR VPH 18. Electroforesis en gel de poliacrilamida al 5% de los productos amplificados para la región LCR de VPH 18. (CN) Control Negativo. Carriles 2 al 9: diluciones del control positivo de VPH 18 desde 10-7 al 10-13. (M) Marcador de 50 pares de bases (ensayo realizado por triplicado).
En la Tabla 2 se encuentran resumidas las condiciones de PCR optimizadas.
DISCUSIÓN
Las infecciones persistentes por VPH-AR constituyen un factor de riesgo importante para el desarrollo de cáncer cervical11. En Paraguay, se observó una alta frecuencia de casos de cáncer invasor positivos para los genotipos 16 y 18(13,19). En este estudio se estandarizó y se determinó el límite de detección de una técnica de PCR convencional para la detección de VPH 16 y 18.
En ambas reacciones de PCR se optó por utilizar una concentración final de MgCl2 de 2 mM ya que se observaron bandas más nítidas. Esta concentración difiere de la reportada por Tornesello et al., 2000 20, donde se utilizó 2,5 mM para VPH 16 mientras que Arias-pulido et al., 2005 21) reportan 2,5 mM en la amplificación de VPH 18.
En relación a la temperatura de alineamiento, la seleccionada fue de 60°C para ambas reacciones. Este resultado concuerda con la temperatura de alineamiento calculada en base al porcentaje de G+C y A+T de los primers, la cual fue de 61°C para VPH 16 y de 57°C para VPH 1817. Esto difiere de lo reportado por Tornesello et al.20 para VPH 16, y Arias-pulido et al.21 para VPH 18, que reportan 55°C y 58°C respectivamente. Sin embargo Chow et al., 1990 reportaron 50°C para VPH 16 y 60°C para VPH 1822. Estos resultados sugieren que sería factible realizar una reacción multiplex con ambos, eventualmente.
Se observó un límite de detección de 14,6x10-11ng/µL para VPH 16 y de 21,7x10-12ng/µL para VPH 18. Estos resultados difieren de lo que reportan otros autores como Chow et al , 1990 22 que obtuvieron un límite de detección de al menos 0,01 µg de ADN genómico de líneas celulares Si-Ha (VPH16) y C4-1 (VPH18). Lo que sugiere que las reacciones son capaces de detectar pequeñas cantidades de ADN viral. Las diferencias en estos resultados pudieron deberse a diferentes condiciones en que fue determinado el límite de detección8.
En conclusión, el presente estudio permitió optimizar una PCR convencional que permite detectar bajas concentraciones de VPH 16 y 18 y que podrá ser utilizada como una potencial prueba de triage, con miras a identificar mujeres VPH-AR positivas que poseen más riesgo de desarrollo de lesiones de cuello uterino y cáncer y precisan de un control más cercano.
















