Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Memorias del Instituto de Investigaciones en Ciencias de la Salud
versão On-line ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud v.10 n.1 Asunción jun. 2012
ARTICULO ORIGINAL
Identificación molecular de linajes y sub-linajes de Trypanosoma cruzi en niños infectados congénitamente provenientes de áreas endémicas del Paraguay
Molecular identification of Trypanosoma cruzi lineages and sub lineages in congenitally infected children from endemic areas of Paraguay
*Sánchez Z, Russomando G
Departamento de Biología Molecular y Genética, Instituto de Investigaciones en Ciencias de la Salud, Universidad Nacional de Asunción (UNA) Paraguay
RESUMEN
La tripanosomiasis americana es una infección causada por un protozoario flagelar Trypanosoma cruzi que está diseminado por todo el continente Americano. T. cruzi es una especie heterogénea que comprende varias sub-poblaciones que circulan en hospederos vertebrados domésticos y salvajes, e invertebrados. Esta diversidad genética ha sido detectada con técnicas moleculares demostrándose que circulan clones mayoritarios en varios hospederos y en diferentes áreas geográficas de América Latina. Aislados de T. cruzi han sido divididos en dos grupos genéticos nombrados por consenso internacional T. cruzi I (linaje 2-asociado al ciclo enzoótico) y T. cruzi II (linaje 1-asociado al ciclo doméstico). La interacción de los clones infectivos de T. cruzi y el hospedero humano podrían determinar la morbilidad de la enfermedad. En este trabajo se empleó la técnica PCR para amplificar genes constitutivos de T. cruzi, como el gen 24Sa Ribosomal y el gen mini exón (ME) y se detectaron linajes de T. cruzi en 112 muestras (83%) de un total de 135 muestras de niños infectados provenientes de dos departamentos endémicos para la enfermedad de Chagas en Paraguay(Cordillera y Paraguarí). En cuanto a la procedencia de las mismas, 53 muestras eran de Paraguarí y 59 muestras de Cordillera. Los sub-linajes encontrados fueron: Paraguarí: 34TcIIc, 17 TcIId, 1 muestra TcIIb-IIe y 1 muestra ND (no determinada), En Cordillera: 37 TcIIc, 19 TcIId, 1 muestra TcIIb-IIe y 2 muestras no determinadas. No se encontró linaje I, selvático en ninguna de las 2 áreas estudiadas.
Palabras claves: Trypanosoma cruzi, lineages, vector.
ABSTRACT
American trypanosomiasis is an infection caused by the protozoan flagellate Trypanosoma cruzi that is spread throughout the Americas. T. cruzi is a heterogeneous species comprising several sub-populations circulating in domestic and wild vertebrate and invertebrate hosts. This genetic diversity has been detected with molecular techniques showing that there are major clones circulating in several hosts and different geographic areas of Latin America. T. cruzi isolates have been divided into two genetic groups named by an international consensus as T. cruzi I (lineage 2-associated with enzootic cycle) and T. cruzi II (lineage 1-associated with the domestic cycle). The interaction of infective clones of T. cruzi and human host could determine the morbidity of the disease. In this work, we used PCR technique to amplify constitutive genes of T. cruzi, 24Sa ribosomal gene and the mini exon (ME) gen. Lineages of T. cruzi were detected in 112 samples (83%) out of 135 samples of infected children from two Departments of Paraguay that are endemic for Chagas disease (Cordillera and Paraguarí). Regarding their origin, 53 samples were from Paraguarí and 59 samples from Cordillera. The sub-lineages found in Paraguarí were: 34TcIIc, 17 TcIId, 1 TcIIb-IIe and 1 ND sample (not determined). In Cordillera: 37 TcIIc, 19 TcIId, 1 TcIIb-IIe and 2 ND samples. Wild lineage I was not found in any of the two areas studied.
Keywords: Trypanosoma cruzi, lineages, vector.
INTRODUCCIÓN
La enfermedad de Chagas, causada por el parásito Trypanosoma cruzi, afecta aproximadamente a 15 millones de individuos. La enfermedad se encuentra presente en casi toda América Central y del Sur. Sus manifestaciones y características epidemiológicas son altamente variables entre una y otra zona endémica (1). En Paraguay se estima que aproximadamente 150.000 personas estarían infectadas (2). Existen áreas históricamente endémicas, como Paraguarí y Cordillera de la Región Oriental, donde la seroprevalencia en el grupo etáreo de 15 a 45 años es del 10 al 12% (3), mientras que en la Región Occidental o Chaco existen comunidades indígenas con prevalencias por encima del 50% (4) y a nivel nacional los bancos de sangre registran actualmente una prevalencia del 3,2% (2).
La transmisión de T. cruzi en humanos ha sido atribuida tradicionalmente a dos ciclos que se conectan entre sí y definidos como ciclos selvático y doméstico. En el ciclo doméstico los humanos se infectan inicialmente como resultado de la domiciliación de los vectores que traen los parásitos del ambiente selvático a las viviendas. El ciclo selvático involucra la interacción entre vectores silvestres y mamíferos selváticos incluyendo marsupiales, roedores, armadillos y otros animales. El ciclo doméstico es el resultado del contacto vector-humano debido a factores que permiten la colonización de ecotopos artificiales por los insectos que usan roedores, marsupiales y a veces perros y gatos como fuente de alimentación (5).
T. cruzi es una especie heterogénea, los aislados pueden clasificarse en diferentes niveles genéticos, desde sub-especies hasta sub-divisiones clonales. El análisis genético de aislados de diferentes regiones geográficas y de diferentes reservorios (vectores y humanos), ha sugerido que el T. cruzi tiene una estructura poblacional del tipo clonal, y muchas de las infecciones detectadas en vectores y mamíferos aparecen como una mezcla de varios clones (5).
La alta diversidad genética, y los aislados muestran distintas características biológicas, tal vez relacionadas con las diferentes presentaciones clínicas de la enfermedad de Chagas (forma indeterminada, manifestaciones cardiaca y digestiva). Los aislados de T. cruzi han sido divididos en dos grupos genéticos nombrados por consenso internacional T. cruzi I (linaje 2- asociado al ciclo enzoótico) y T. cruzi II (linaje 1- asociado al ciclo doméstico) (6), el T. cruzi II se divide a su vez en 5 sub-grupos (IIa-IIe). Estos dos grupos posiblemente representando sub-especies, fueron determinados por isoenzimas y técnicas moleculares (7).
Datos biológicos y epidemiológicos recientes, han demostrado una fuerte asociación entre el T. cruzi II y las manifestaciones clínicas en humanos, mientras que el T. cruzi I ha sido detectado preferentemente en el ciclo selvático (8). Breniere y colaboradores compararon los clones circulantes en humanos y en Triatoma infestans y demostraron la existencia de los 2 clones mayoritarios circulando en igual frecuencia en los insectos mientras que solo 1 de ellos era aparentemente más prevalente en la sangre de humanos. Hasta la fecha la identificación de estos clones se ha realizado en cultivos de aislados de T. cruzi provenientes de sangre de humanos, animales o de heces de triatominos. Este aislamiento y amplificación artificial podría de alguna manera seleccionar algunos clones, por lo que no se identificarían los verdaderos clones presentes en las muestras biológicas inicialmente (7).
Entre las técnicas moleculares que se emplean para la identificación de linajes y sub-linajes, se encuentran el PCR y el RAPD, que por su sensibilidad permiten identificar el parásito directamente en las muestras biológicas, sin cultivo previo, por lo que se proponen estas técnicas empleando como blanco los genes constitutivos de T. cruzi como: el gen ribosomal 24Sa rRNA (rDNA) y el gen mini-exón (ME) (9). Estos genes constitutivos han demostrado ser de gran valor en la investigación de la diversidad genética del mismo porque el gen ME posee regiones intergénicas divergentes y el gen 24Sa rRNA presenta dimorfismo en su dominio D7 (10,11).
En Paraguay se han llevado a cabo estudios sobre genotipos circulantes en el ciclo silvestre, principalmente en marsupiales y triatominos silvestres, detectándose el genotipo TcI involucrado en la trasmisión (14). Recientemente nuestro grupo publicó un trabajo sobre los genotipos circulantes en humanos que habitan en regiones endémicas y en ejemplares de T. infestans capturados en la misma región, encontrando que mayoritariamente circula el sub-linaje TcIId en ambas poblaciones (15).
MATERIALES Y MÉTODOS
Población: este estudio descriptivo de corte transverso se realizó sobre un total de 135 muestras de sangre de niños de ambos sexos, de 6 meses a 5 años de edad, infectados congénitamente con T. cruzi, detectados por serología y parasitemia directa y cuya procedencia fueron los departamentos endémicos de la Región Oriental del Paraguay: Cordillera y Paraguarí.
Extracción de ADN: se realizó con el método Fenol-Cloroformo, descrito por Sambrook y col. (13).
Identificación de linajes de T. cruzi y sub-linajes IIa, IIb, IIc, IId, IIe: se realizó empleando la técnica de la reacción de la polimerasa (PCR), con cebadores que amplifican genes constitutivos como el gen 24Saribosomal y con el espaciador intergénico del gen miniexón (ME) (10,11).
Los productos amplificados fueron analizados en geles de agarosa al 2%, teñidos con bromuro de etidio y visualizados bajo un transiluminador UV (10). Cada uno de estos ensayos se realizó por duplicado.
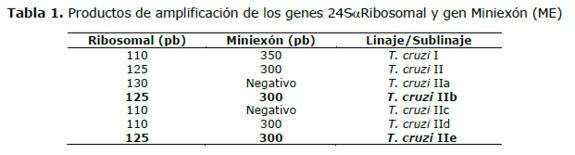
Para la determinación de los linajes y sub-linajes de T. cruzi se utilizó la siguiente clasificación (11), tabla 1.
Los linajes 1 (T. cruzi II) son domiciliares y el linaje 2 (T. cruzi I) es selvático.
Como se puede observar en la tabla 1, los productos de ribosomal y miniexón son del mismo tamaño (125pb y 300pb respectivamente) para T. cruzi IIb y T. cruzi IIe, una forma de diferenciarlos sería empleando cebadores que amplifiquen el gen 18Saribosomal, con los cuales se obtienen productos diferentes para ambos linajes, pero en éste trabajo no se utilizaron éstos cebadores.
CRITERIOS ÉTICOS
Para asegurar la confidencialidad de la identidad de los niños, se trabajó con muestras codificadas y con el consentimiento de los padres en forma verbal. El protocolo de investigación fue aprobado por los comités científico y ético del Instituto de Investigaciones en Ciencias de la Salud de la Universidad Nacional de Asunción. Los resultados no benefician en forma directa a los sujetos del estudio, pero aportan información sobre la epidemiología de la enfermedad.
RESULTADOS
De 135 muestras analizadas, 112 (83%) dieron linajes positivos, 53 muestras eran de Paraguarí y 59 muestras de Cordillera, procedentes de 14 distritos de cada departamento.
Los sub-linajes detectados fueron:
Paraguarí: 34 TcIIc, 17 TcIId, 1 muestra TcIIb-IIe y en 1 muestra no fue posible determinar el linaje.
Cordillera: 37 TcIIc, 19 TcIId, 1 muestra TcIIb-IIe y en 2 muestras no se pudo determinar los linajes.
No se encontró linaje I, selvático en ninguna de las 2 áreas estudiadas.
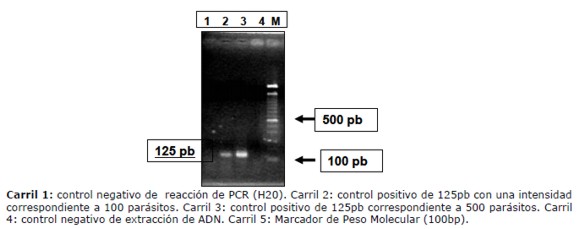
Estos resultados se pueden observar en la tabla 2, y la prueba de especificidad de uno de los cebadores para los linajes se puede observar en la figura 1.
DISCUSIÓN
La enfermedad de Chagas se considera un problema de salud pública en muchos países por la gran cantidad de personas infectadas y la variedad de manifestaciones clínicas con las que se presenta. Muchos estudios han llevado a inferir que dicha variación está ligada directamente al genotipo de los parásitos circulantes, ya que diferencias genéticas en las poblaciones del parásito hacen que estos presenten un tropismo diferencial por tejidos del hospedero durante la fase crónica de la enfermedad (16). Este trabajo realizado con muestras consideradas agudas, dio un panorama sobre los linajes de T. cruzi circulando en sangre humana de individuos procedentes de zonas endémicas del Paraguay. Los linajes de T. cruzi fueron detectados en un 83% de las muestras analizadas mediante la técnica empleada. Los sub-linajes TcIIc y TcIId fueron los predominantes en la muestra.
Muchas de las cepas naturales de T. cruzi son multiclonales y se encuentran compuestas de poblaciones del parásito tanto del grupo T. cruzi I como del grupo T. cruzi II. Sin embargo, este número de clones puede cambiar drásticamente a medida que trascurre el tiempo de infección, ya que en la fase crónica de la enfermedad ciertos clones del parásito son eliminados como resultado de factores inmunológicos del hospedero o debido a la capacidad de multiplicación o requerimientos nutricionales para cada clon (7).
Es importante destacar que diversos estudios han reportado el músculo esquelético como uno de los órganos que más se encuentra parasitado con T. cruzi tanto en la fase aguda como en la fase crónica de la enfermedad (15,16).
En éste trabajo, mediante la detección de linajes y sub-linajes de T. cruzi en muestras de la fase aguda de la enfermedad, se pudo tener información sobre los clones del parásito circulantes, y con la detección de los clones en muestras de la fase crónica de la enfermedad, se podrá conocer la evolución o selección hacía un determinado linaje, lo cual podrá a su vez ayudar a tener un mejor control del tratamiento de la enfermedad y al mismo tiempo tener información sobre la epidemiología de la enfermedad de Chagas.
Los amplificados de algunas muestras dieron productos con tamaños de bandas diferentes a lo esperado, esto podría deberse a linajes o sub-linajes circulantes que aún no fueron descritos. No se ha detectado en las regiones del estudio, presencia de T. cruzi I, o selvático.
Estos resultados son coincidentes con otros realizados en la región, lo que sugiere que el sub-linaje TcIId estaría fuertemente relacionado con las manifestaciones clínicas de la enfermedad de Chagas por ser el mayoritario detectado tanto en humanos como en vectores.
AGRADECIMIENTOS
Al Programa Nacional de Chagas del Ministerio de Salud Pública y Bienestar Social (bajo la jefatura de la Dra. Graciela Russomando) por la colecta y provisión de muestras.
A la Sra. Graciela Meza por su colaboración en el procesamiento de las muestras.
Fuentes de financiación: este trabajo recibió apoyo económico del Instituto de Investigaciones en Ciencias de la Salud–Universidad Nacional de Asunción- Paraguay.
REFERENCIAS BIBLIOGRÁFICAS
1. World Health Organization. Control of Chagas Disease. Second report of the WHO Expert Committee. Geneva: WHO; 2002. WHO Tecnical Report Series 905. [ Links ]
2. Organización Panamericana de la Salud. Estimación cuantitativa de la enfermedad de Chagas en las Américas. Montevideo: OMS. 2006. [ Links ]
3. Russomando G, Almiron M, Candia N, Franco L, Sánchez Z, de Guillen I. Implementación y evaluación de un sistema localmente sustentable de diagnóstico prenatal que permite detectar casos de transmisión congénita de la enfermedad de Chagas en zonas endémicas del Paraguay. Rev Soc Bras Med Trop. 2005;38(2):49-54. [ Links ]
4.Rojas de Arias A. Chagas disease in Paraguay. Washington, DC: Pan-American Health Organization. 1996. PAHO Document No. PAHO/HCP/HCT/72/ 96. [ Links ]
5. Souto R, Fernandes O, Macedo A, Campbell D, Zingales B. DNA markers define two major phylogenetic lineages of Tripanosoma cruzi. Mol Biochem Parasitol. 1996; 83(2):141-52. [ Links ]
6. Breniere SF, Bosseno MF, Tellería J, Carrasco R, Vargas F, Yacsik N, Noireau F. Field application of polymerase chain reaction diagnosis and strain typing of Tripanosoma cruzi in Bolivian triatomines. Am J Trop Med Hyg. 1995; 53(2):179-84. [ Links ]
7. Breniere SF, Bosseno MF, Tellería J, Bastrenta B, Yacsik N, Noireau F, et al. Different behaviour of two Tripanosoma cruzi major clones: transmission and circulation young Bolivian patients. Exp Parasitol. 1998;89(3):285-95. [ Links ]
8. Zingales B. Molecular epidemiology of American tripanosomiasis in Brazil base on dimorphisms of rRNA and mini-exon gen sequences. Int J Parasitol. 1998; 28(1):105-12. [ Links ]
9. Souto RP, Zingales B. Sensitive detection and strain classification of Tripanosoma cruzi by amplification of a ribosomal RNA sequence. Mol Biochem. Parasitol, 1993; 62: 45-52. [ Links ]
10. Fernández O, Souto R, Castro JA, Borges J, Carrara N, Junqueira CV, et al. Brazilian isolates of Trypanosoma cruzi from humans and triatomines classified into two lineages using mini-exon and ribosomal RNA sequences. Am J Trop Med Hyg. 1998;58(6):807-11. [ Links ]
11. Brisse S, Verhoef J, Tibayrenc. Characterisation of large and small subunit rRNA and mini-exon genes further supports the distinction of six Tripanosoma cruzi lineages. Int J Parasitol. 2001 Sep;31(11):1218-26. [ Links ]
12. Del Puerto F, Sánchez Z, Nara E, Meza G, Paredes B, Ferreira E, Russomando G. Trypanosoma cruzi Linages Detected in Congenitally Infected Infants and Triatoma infestans from the Same Disease- Endemic Region under Entomologic Surveillance in Paraguay. Am J Trop. Med Hyg. 2010; 82(3): 386-90. [ Links ]
13. Sambrook J, Fritsch E, Maniatis T. Molecular Cloning. A Laboratory Manual. New York: Cold Spring Harbor Laboratory Press. 1994. [ Links ]
14. Yeo M, Acosta N, Llewellyn M, Sánchez H, Adamson S, Miles GA, et al. Origins of Chagas disease: Didelphis species are natural hosts of Trypanosoma cruzi I and armadillos hosts of Trypanosoma cruzi II, including hybrids. Int J Parasitol. 2005; (35): 225–33. [ Links ]
15. Franco DJ, Vago AR, Chiari E, Meira FC, Galvao LM, Machado CR. Trypanosoma cruzi: mixture of two populations can modify virulencia and tissue tropism in rat. Exp. Parasitol 2003;104:54-61. [ Links ]
16. Cummings KL, Tarieton RL. Rapad quantitation of Trypanosoma cruzi in host tissue by real-time PCR. Mol Biochem Parasitol. 2003;129:54-9. [ Links ]
*Autor Correspondiente: Dra. Zunilda Sánchez, Dpto. de Biología Molecular.
Instituto de Investigaciones en Ciencias de la Salud. UNA. Paraguay.
Email:biomol@iics.una.py.
Fecha de recepción: marzo de 2012, Fecha de aceptación: mayo 2012.