Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Memorias del Instituto de Investigaciones en Ciencias de la Salud
versión On-line ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud v.7 n.2 Asunción dic. 2009
ARTICULO ORIGINAL
Actividad larvicida de extractos vegetales acuosos en larvas de Aedes aegypti (primeros ensayos)
Larvicidal activity of aqueous plants extracts on Aedes aegypti larva (first trials)
*Sanabria L, Segovia EA, González N, Alcaraz P, Vera de Bilbao N
Departamento de Medicina Tropical. Instituto de Investigaciones en Ciencias de la Salud. Universidad Nacional de Asunción (UNA).Paraguay
RESUMEN
El dengue es una enfermedad epidémica muy común en regiones tropicales y sub tropicales. La eliminación de criaderos y el control vectorial se encuentran entre las medidas en la lucha contra la enfermedad. Se han desarrollado diversas estrategias para mantener bajo índice poblacional del mosquito. Diversas investigaciones se han enfocado a la búsqueda de nuevos productos naturales, con actividad insecticida y larvicida, que puedan controlar la población de mosquitos, sin presentar riesgos al humano y animales domésticos. Realizamos una serie de bioensayos con extractos acuosos de plantas paraguayas, Annona muricata (chirimoya); Bulnesia sarmentoi (palo santo); Melia azederach (paraíso); Zanthoxylum chiloperone var. Angustifolium (tembetary hú) y Bixa orellana (urukú), para comprobar en cada planta, su actividad y eficacia como larvicida, contralarvas del mosquito Aedes agypti. Dichas larvas, fueron colectadas de diversas zonas de Asunción y el Gran Asunción, durante la epidemia de fiebre amarilla del año 2007. Las semillas de la Annona mucricata (chirimoya), presentaron una buena actividad larvicida, ya que a la mínima concentración del 5%, han tenido un efecto mortal para las larvas, comparable al observado en los controles positivos (que contenían temefos 1%). En cambio, M. aezsederach (paraíso) y Z. chiloperone (tembetary hú) no mostraron actividad larvicida a esa dosis, ni aún a otras superiores. Por otro lado B. sarmientoi (palo santo) y B. orellana (urukú), presentaron cierto efecto larvicida, eliminando al 18% de larvas a las 72 horas post-exposición. Se observó una marcada diferencia de actividad, entre el extracto de semillas chirimoya con los demás extractos probados.
Palabras claves: Aedes aegypti, dengue, extractos vegetales acuosos, bioensayos.
ABSTRACT
Dengue is an common epidemic disease in tropical and subtropical regions. The elimination of breeding sites and vector control are among the most widely used measures in the fight against the disease. Many strategies have been developed to keep low rates of mosquito populations. Several research studies have been focused on finding natural products with insecticide and larvicide activity that could effectively control these mosquito populations without risks for the human populations and domestic animals. In this work, we have performed a series of bioassays with aqueous extracts of Paraguayan plants: Annona muricata (cherimoya), Bulnesia sarmentoi (palo santo), Melia azederach (paradise), Zanthoxylum chiloperone var. Angustifolium (tembetary hú) and Bixa orellana (uruku) in order to check the effectiveness and activity as larvicide of each plant gainst Aedes aegypti larvae. The larvae were collected in various areas of Asuncion and Great Asuncion during the yellow fever outbreak of 2007. The seeds of A. mucricata (cherimoya or custard apple) showed good larvicidal activity, i.e. at the minimum concentration of 5%, showed lethality against larvae comparable to that observed in positive controls (containing 1% temephos). On the other hand, M. azederach (paradise) and Z. chiloperone (tembetary hú) did not show any larvicidal activity at the same dose and even at higher doses. B. sarmientoi (palo santo) and Bixa orellana (uruku) showed some larvicidal effect killing larva (18%) at 72 hours post-exposure. There was a marked difference in activity between the cherimoya seeds extract and the other extracts tested.
Keywords: Aedes aegypti, dengue, aqueous plants extracts, bioassays.
INTRODUCCIÓN
La fiebre del dengue y su forma más grave, el dengue hemorrágico, constituyen un grave problema de salud pública. Según la OMS, cada año se producen cerca de 50 millones de infecciones por dengue, incluidos unos 500.000 casos de dengue hemorrágico que requieren hospitalización. Alrededor de 21.000 defunciones por dengue hemorrágico ocurren por año afectando según las estadísticas a niños menores (1-3). El vector de la enfermedad es el mosquito Aedes aegypti,de origen africano, ubicado biogeográficamente en la región Etiópica (África), que nuclea la mayor cantidad de especies del subgénero Stegomyia, al cual pertenece este culícido (mosquito). Aedes aegypti inició, hace siglos una dispersión cosmopolita, acompañando los viajes del hombre a través del globo, convirtiéndose en eficaz vector de arbovirosis como fiebre amarilla y dengue. La ecología del mosquito representa una clara adaptación de una especie silvestre al ámbito humano, con criaderos, hábitat, fuente de alimentación, desplazamientos activos y pasivos, ligados al ambiente domiciliario, con lo cual representa un desafío del control y vigilancia epidemiológica del siglo XXI, (4-7). Hasta el momento no se dispone de ningún medicamento específico para el tratamiento del dengue, por lo que los únicos métodos para prevenir y controlar la enfermedad consisten en reducir el contacto humano con el vector y controlar los criaderos larvarios de este mosquito. A pesar que existen actualmente una variedad de métodos de control del A. aegypti, muchos de los cuales han demostrado ser eficaces en diferentes situaciones, sin embargo, el principal método de control sigue siendo el uso de los insecticidas de bajo volumen (IBV) para el control de mosquitos adultos. El inconveniente de esta estrategia, es que debe repetirse constantemente, siendo su costo elevado y su eficacia limitada (8,9). Asimismo se han reportado casos de reacciones alérgicas en individuos en contacto con los insecticidas especialmente en niños y ancianos a mas de otros trabajos que reportan que los insecticidas utilizados actualmente, además de eliminar al Aedes, también lo hace con su predador natural, otro mosquito no hematófago del género Toxorhynchites, que en su estado adulto se alimenta de las larvas del A. aegypti (1,4, 9,10). Las plantas y sus derivados, han mostrado actividad contra los insectos y sus larvas, desde los trabajos realizados con extractos acuosos de plantas por diversos autores, (10-13), Se ha incrementado a 140 la lista de especies de plantas con propiedades larvicidas, entre las cuales se destacan las del género Annona, A.bullata (Rich), A.densicoma (Mart) y A.muricata (Mill), que son activas contra A. aegypti y Anopheles spp(14-16). Estos ensayos se realizan en forma regular en el insectario, testando los extractos a distintas dosis, en diferentes tiempos de aplicación y controlando el microclima de las larvas, las condiciones ambientales y su alimentación. Se acostumbra realizar los ensayos con larvas del estadio III ya que este, demuestra mayor resistencia a los larvicidas y es la última etapa larvaria en que toma alimento, antes de surgir la pupa y el insecto hematólogo (17). De estas plantas se han extraído unos nueve principios activos con estructura de acetogeninas y alcaloides, que se encuentran en la corteza y las semillas. La mayoría de las investigaciones que se realizan actualmente sobre el uso de sustancias vegetales para el control de mosquitos están enfocadas a encontrar especies con alto potencial en la eliminación de larvas de mosquitos para poder implementar estrategias de control y manejo integrado de mosquitos, haciendo un mejor uso de los recursos naturales y reducir el uso de los insecticidas organosintéticos (17-20).Buscando, contribuir en la lucha contra la fiebre del dengue, la cual en su recurrencia con brotes epidémicos cada año, se torna en un problema de salud pública, este trabajo tiene como objetivo, ensayar, diferentes extractos acuosos de plantas nacionales, en procura de identificar su posible efecto larvicida con vistas a su uso en el futuro, como agente para controlar la población larval e impedir la emergencia del mosquito adulto, asumiendo que dichos extractos de plantas presenten baja toxicidad para la salud humana, bajo costo y buena disponibilidad.
MATERIALES Y MÉTODOS
Annona muricata (chirimoya)fue recolectada de la ciudad de Villa Elisa, en salidas de campo del equipo de trabajo, donde se encontró la planta con frutas en una casa particular fue; identificada taxonómicamente, con la ayuda de una clave botánica por los autores; Bulnesia sarmentoi (palo santo), Melia azederach (paraíso) y Bixa orellana (urukú), fueron adquiridos en; "yuyerías"; del mercado cuatro, donde estos, se venden como hierbas medicinales, para su consumo masivo. Zanthoxylum chiloperone var. Angustifolium (tembetary hú), fue obtenido a partir del material vegetal, que se encuentra disponible en el laboratorio de Medicina Tropical del IICS y se utiliza en otras líneas de investigación fitoquímica.
Captura de larvas de Aedes aegypti: fue realizada por el equipo de investigación en salidas de campo en lugares predeterminados en Asunción y el Gran Asunción, donde había un alto índice de densidad larvaria, en las mingas del mes de febrero del 2007 (durante la epidemia de fiebre amarilla), se localizaron las larvas en aguas estancadas y en aquellos lugares húmedos donde se crían las larvas del mosquito. La colecta se realizó, en campo con redes de malla fina de 0,3 mm y 30 cm. de diámetro, en los lugares de difícil acceso se utilizó el método de pipeteado (13). Las larvas colectadas fueron traídas al laboratorio donde luego de ser traspasadas a recipientes amplios con agua limpia libre de cloro, se procedió a su identificación taxonómica y posteriormente se seleccionaron aquellas larvas del estadio I y II de desarrollo, las que fueron mantenidas en condiciones de humedad y temperatura, alimentadas con alimentos de peces, hasta pasar al estadio III, losque se utilizaron para los bioensayos.
Obtención de los extractos vegetales acuosos: los extractos vegetales acuosos a las que fueron expuestas las larvas han sido preparados según la metodología de Lock (1994), con algunas modificaciones. El método establece que, una vez colectadas las plantas, se colocan sus partes (semillas, hojas y corteza) en papel periódico a la sombra para su secado, luego se pulveriza cada parte vegetal con un molino manual para obtener un polvo que será posteriormente hidratado. Los extractos acuosos fueron preparados aproximadamente a las concentraciones del: 5, 10 y 15%, (corresponden a las fracciones hidrosolubles) para esto, se disolvió 4.5 7.5 y 12.5.g. del polvo de la planta en 50 mL de agua destilada, respectivamente. Se dejaron 12 horas en reposo para la extracción de sus componentes hidrosolubles y al término de esto último se separó el sólido del líquido, dicho material líquido se utilizó en los ensayos.
Bioensayos
Las concentraciones de los extractos acuosos utilizados en los bioensayos se establecieron de acuerdo al protocolo de (13), para extractos acuosos, a una concentración de 5, 15 y 25% respectivamente. Se distribuyó un total de 420 larvas de Aedes aegyti, (larvas del III estadio) en 21 vasos de plástico con capacidad de 200 mL. cada uno, se colocaron en forma aleatoria 20 larvas por vaso, cada vaso contenía previamente unos 100mL. de agua destilada. El grupo control (+) fue expuesto a un larvicida de referencia (temefos al 1%), al otro grupo control (-) no se le aplicó ningún tratamiento, a los demás grupos se le aplicó 1 mL. de los extractos acuosos. En todos los grupos testados incluyendo sus controles positivos y negativos, se hicieron repeticiones por triplicado. A modo de réplica, se realizaron dos bioensayos, con los mismos extractos, en las mismas condiciones mencionadas. A las 24, 48 y 72 horas posteriores de la aplicación de los tratamientos se registró la mortalidad de las larvas. Fueron consideradas muertas aquellas que no presentaron movimiento alguno cuando se les tocó con un estilete en el mesotórax.
RESULTADOS
En la tabla 1, se presentan los lugares de colecta de larvas, en donde se destacan las cubiertas como los lugares de mayor productividad de las larvas.
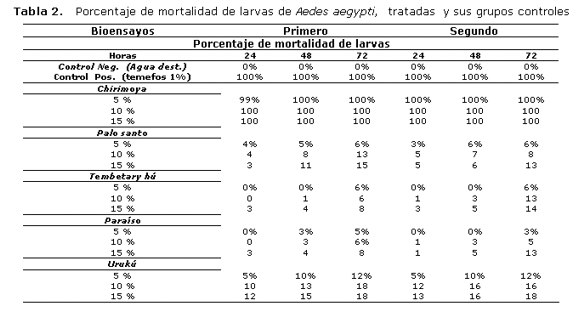
En la tabla 2, se presentan los porcentajes de mortalidad de las larvas de Aedes aegipti tratadas con los extractos vegetales en diferentes concentraciones.
DISCUSIÓN
Los resultados de los bioensayos con la semilla de la Annona mucricata (chirimoya), parece prometedor, pues, a partir de la concentración más baja del 5%, ha demostrado su efecto letal para las larvas, al tener una efectividad similar al larvicida de referencia, (temefos 1%), utilizado en el control positivo (tabla 1). En cambio se observó una menor tasa de mortalidad de larvas, en relación con sus controles para los extractos de: M. aezsederach (paraíso) y Z. chiloperone (tembetary hú), en ambos bioensayos a esas dosis. Por otro lado B. sarmientoi (palo santo) y B. orellana (urukú), presentaron efecto moderado como larvicida, con la preparación al 15%, luego de las 72 horas de exposición al tratamiento, (tabla 1). Se observó, una marcada diferencia entre el extracto de chirimoya con los demás extractos, estos hallazgos coinciden con otros trabajos como los de Pérez Pacheco R, Rodríguez C, Reyna JL et al (13). que obtuvieron resultados similares con especies de la misma familia y que se conocen en Centroamérica y el Caribe como “guanábana”. Otros investigadores como Sánchez M, González N, Bobadilla M. Zavaleta G, et al (2), han reportado haber aislado un principio activo de esta Mirtacea, un alcaloide fitoconstituyente que se encuentra en toda la planta y más concentrado en la semilla y que mostró una marcada actividad antilarvaria. En nuestro país, autores como (7,17) atribuyen a M. aezsederach (paraíso) propiedades de repelente e insecticida contra mosquitos; Z. chiloperone (tembetary hú), presenta propiedades antiparasitaria (tripanocida y leishmanicida) y antifúngicas (7); aunque no existen publicaciones al respecto de B. orellana (urukú), el común de la gente lo utiliza como repelente e insecticida. Por ser esta una prueba piloto no contamos con líneas de regresión dosis-respuesta, lo que requeriría ajustar las dosis hasta obtener las unidades Probit. (dosis-efecto). Se necesitan realizar nuevos ensayos y ajustar las dosis para buscar la LC 50 y 90 para conocer la efectividad de los extractos.
BIBLIOGRAFIA
1.OMS. Resistencia de los Vectores de Enfermedades a los Plaguicidas. Ginebra Suiza: 15º Informe del Comité de Expertos de la OMS en Biología de Vectores y Lucha Antivectorial (Serie de Informes Técnicos Nº 818); 1992. [ Links ]
2. Rotraut A, Consoli G. Principais Mosquitos de Importancia Sanitária no Brasil. 3ra. Edición. Rio de Janeiro. Brasil: Editorial Fiocruz; 1995. [ Links ]
3. Mangabeira A, Olivera G. Mosquitos Aedes no Brasil. 2da. Edición. San Pablo Brasil: Editorial da Rua; 1998. [ Links ]
4.Fradin, MS, Day JF. Comparative efficacy of insect repellents against mosquito bites. New England J Med 2002; 347(1): 13-18. [ Links ]
5. VHoss R. Cuaderno de Trabajo Guía metodológica: Uso de Extractos vegetales en la regulación de plagas. Lima Perú: Red de Acción de Alternativas al uso de Agroquímicos; 1992. [ Links ]
6.Lock O. Investigación fitoquímica. Métodos en el estudio de productos naturales. 2da edición. Lima Perú: Fondo Editorial de la Pontificia Universidad Católica del Perú; 1994. [ Links ]
7. Rojas de Arias A, Schmeda G. Feeding Deterrency and Insecticidal Effects of Plants Extracts on Lutzomyia longipalpis. Phytoth Rese 1992; 6: 64-7. [ Links ]
8. WHO. Guidelines for Laboratory and Field Testing of Mosquito Larvicides, Communicable disease control, prevention and eradication. Ginebra: WHO/CDS/WHOPES/GCDPP; 2005. [ Links ]
9. Espinosa PJ. Búsqueda de plantas del lago de Texcoco con actividad tóxica contra mosquitos Culex quinquefaciatus. Tesis de Licenciatura. Chapingo, México: Parasitología Agrícola, UACH. 1985. [ Links ]
10. Ho SH, Goh PM, Lee KM. Evaluation of two pine oil-based formulations of kitz against various life estages of Aedes aegypti. Inter Pest Cont 1992; 34(6): 180-1. [ Links ]
11. Mathur S. Prospects of using herbal products products in the control of mosquito vectors. Bull Indian Council Med Res 2003; 33(1): 1-10. [ Links ]
12. Mclaughlin J, Lingling R, Jon A. The use of biological assays to evaluate botanicals. Drug Information Journal 1998; 32: 513-24. [ Links ]
13.Pérez Pacheco R, Rodríguez C, Reyna JL, Montes R, Ramírez G. Toxicidad de Aceites, Esencias y Extractos Vegetales en Larvas de Mosquitos Culex quinqefasciatus (Diptera: culicidae). Act Zool Mexicana 2004; 20(1): 141-52. [ Links ]
14. Rodríguez HC, Lagunas A. Combate de los mosquitos Aedes aegypti y Culex quinquefasciatus (Díptera culicidae) con sustancias acuosas vegetales. Cuernavaca, Morelos: 1er. Encuentro Estatal sobre Entomología Médica y Veterinaria; 1989. [ Links ]
15. Alali F, Liu X, Laughlin JMC. Annonaceus acetogenis: Recent progress. J Nat Prod 1999; 62(3): 504-40. [ Links ]
16. Bobadilla M, Zavaleta G, Gil F, Pollack L, Sisniegas M. Efecto bioinsecticida del extracto etanólico de las semillas de Annona muricata Miller Chirimoya y A muricata Linneaus sobre larvas del IV estadio de Anopheles sp. Rev Peruana de Biología 2002; 9(2): 64-73. [ Links ]
17. Cataldo J. La Flora Medicinal Paraguaya. Segunda edición. Asunción Paraguay: Editorial Comuneros; 1980. [ Links ]
18. Rodríguez Barboza N. Pojhá Ñaná Plantas que Curan. 2º edición, Asunción Paraguay: Editorial Litocolor; 1985. [ Links ]
19. Sánchez MC, González N, González E. Efecto larvicida de extractos acuosos vegetales sobre Aedes aegypti. Manejo Integrado de Plagas 1997; 45: 30-3. [ Links ]
20. Soberón G, Rojas C, Saavedra J, Kato M, Delgado G. Acción Biocida de Piper tuberculatum Jacq. sobre Diartrea saccharalis (Lepidóptera, piralydae). Rev Peru de Biol 2006; 13(1): 107-12. [ Links ]
*Autor Correspondiente: Lic. Luis Sanabria,
Instituto de Investigaciones en Ciencias de la Salud. Río de la Plata y Lagerenza. Asunción-Paraguay
Email:luis-sanabria@hotmail.com