Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Memorias del Instituto de Investigaciones en Ciencias de la Salud
versão On-line ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud v.7 n.1 Asunción jun. 2009
COMUNICACIÓN CORTA
Inmunohistoquímica en el diagnóstico de la fiebre amarilla. Experiencia en el Dpto. de Patología, del Instituto de Investigaciones en Ciencias de la Salud y la Cátedra de Anatomía Patológica, Facultad de Ciencias Medicas, Universidad Nacional de Asunción
Immunohistochemistry in the diagnosis of yellow fever. Experience in the Department of Pathology, Health Sciences Research Institute and the Department of Pathology, Faculty of Medical Sciences, National University of Asuncion
*Campos SI, Figueredo Thiel SI-II, Bellassai JII, Rodríguez III
IDepartamento de Patología. Instituto de Investigaciones en Ciencias de la Salud. Universidad Nacional de Asunción (UNA).Paraguay
IICátedra de Anatomía Patológica. Facultad de Ciencias Médicas. Universidad Nacional de Asunción (UNA).Paraguay
RESUMEN
La fiebre amarilla (FA) es una enfermedad hemorrágica aguda, inmunoprevenible producida por un arbovirus cuyo órgano blanco es el hígado. Se presenta en forma epidémica y en dos formas epidemiológicas: la urbana y la selvática, ambas con características clínicas e histopatológicas semejantes. Para el diagnóstico se utilizan distintos métodos como serología, cultivo celular, biología molecular, histopatología e inmunohistoquímica (IHQ). La IHQ identifica, en las muestras obtenidas postmortem, la presencia, a nivel tisular, del antígeno viral causante de la enfermedad mediante una unión antígeno-anticuerpo altamente específica. El objetivo de este estudio fue determinar por IHQ la presencia del antígeno del virus de la FA en tejidos hepáticos de pacientes fallecidos con sospecha de FA en el Paraguay. Estudio descriptivo en muestras de tejido hepático (bloques de parafina) obtenidos postmortem, con autorización de los familiares, de 4 pacientes fallecidos con sospecha clínica de FA. Los bloques de parafina fueron enviados, codificados para respetar la confidencialidad de los pacientes, por la Cátedra de Anatomía Patológica de la Facultad de Ciencias Médicas de la Universidad Nacional de Asunción (UNA) al Dpto. de Patología del Instituto de Investigaciones en Ciencias de la Salud (IICS-UNA) para el análisis por IHQ. Se utilizó el anticuerpo primario anti-fiebre amarilla y la técnica del complejo avidina-biotina-peroxidasa, se agregaron cortes de control positivo y negativo para cada caso. Todas fueron positivas para FA. La positividad de la tinción se evaluó por microscopía óptica y en relación a los hallazgos histopatológicos, se consideró positivos aquellos casos en los que se observó una tinción marrón en el citoplasma de las células hepáticas. La positividad se observó en todos los casos sospechosos y en los controles positivos. Los controles negativos no presentaron esta tinción. La IHQ en conjunto con otras técnicas laboratoriales y los criterios clínicos contribuye al diagnóstico postmortem en los casos de FA, y se constituye en una herramienta de diagnóstico muy útil que permite realizar el diagnóstico retrospectivo, en los casos que no ha sido posible realizar otros estudios.
Palabras claves: Inmunohistoquímica, fiebre amarilla, tejidos, antígeno.
ABSTRACT
Yellow fever (YF) is an acute hemorrhagic disease, which is immuno-preventable, caused by an arbovirus whose target organ is the liver. It occurs epidemically and in two epidemiological forms: urban and wild, both with clinical and histopathological similar characteristics. Several methods are used for the diagnosis such as serology, cell culture, molecular biology, histopathology and immunohistochemistry (IHC). The IHC determines the presence of the viral antigen causing the disease at tissue level in post-mortem samples through a highly specific antigen-antibody binding. The objective of this study was to determine the presence of the YF viral antigen by IHC in the liver tissue of deceased patients with suspicion of YF in Paraguay. This is a descriptive study carried out on liver tissue samples (paraffin blocks), obtained post-mortem with the permission of the relatives, of four patients that died and had clinical suspicion of YF. Paraffin blocks were sent, coded to respect the patient confidentiality, by the Department of Pathology of the Faculty of Medicine-National University of Asunción (UNA) to the Department of Pathology of the Instituto de Investigaciones en Ciencias de la Salud (IICS-UNA) to be analysed by IHC. The anti-yellow fever primary antibody and the technique of avidin-biotin-peroxidase complex were used. Also, samples of positive and negative controls for each case were added. Positive staining was evaluated by optical microscopy, and in relation to the histopathological findings those with a brown staining in the cytoplasm of the hepatic cells were considered positive. Positivity was observed in all suspected cases and positive controls. The negative controls did not show any staining. The IHC techniques together with other laboratory techniques and the clinical criteria contribute to postmortem diagnosis in YF cases and represent a useful diagnostic tool which allows the performance of retrospective diagnosis in those cases where other studies could not have been made.
Keywords: Immunohistochemistry, yellow fever, tissue, antigen.
INTRODUCCIÓN
La fiebre amarilla (FA), mal de Siam o fiebre de Barbados, es una enfermedad zoonótica mantenida en la naturaleza por primates no humanos y mosquitos de hábitos diurnos. Es una enfermedad, tropical, aguda, de gravedad variable producida por un arbovirus de la familia Flaviviridae, genero flavivirus, cuyo órgano blanco es el hígado. Es transmitida por la picadura de mosquitos Haemogogus ssp en América y Aedes ssp en África (1,2).
La fiebre amarilla se presenta en forma epidémica en dos formas epidemiológicas: la urbana y la selvática, ambas con características clínicas e histopatológicas semejantes. A pesar de que se cuenta con una vacuna eficaz, la fiebre amarilla continúa siendo hoy en día una importante causa de morbi-mortalidad y afecta regiones tropicales y sub tropicales, principalmente de África y Sudamérica (2-4).
La mayoría de las infecciones son tan leves que no muestran ningún cuadro clínico y con frecuencia pasan inadvertidas. En los casos sintomáticos se pueden producir graves síntomas generales, ictericia, hematemesis, nefritis y alteraciones degenerativas del miocardio. La forma típica o clásica se observa en aproximadamente el 20% de los infectados y se caracteriza por una enfermedad de tipo dengue, de principio brusco, fiebre elevada entre 39 y 40ºC, malestar general, cefalalgia, intenso dolor lumbar, mialgias generalizadas, postración, náuseas, vómitos, escalofríos y dolor en las extremidades. Este período que corresponde a la fase virémica, es denominado período de infección febril o fase roja de la enfermedad y dura 3 a 4 días (3-5).
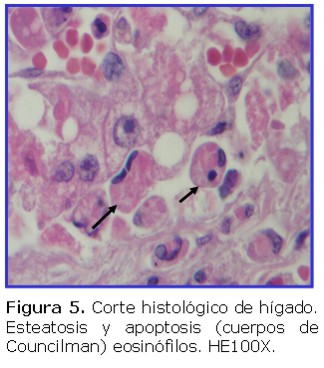
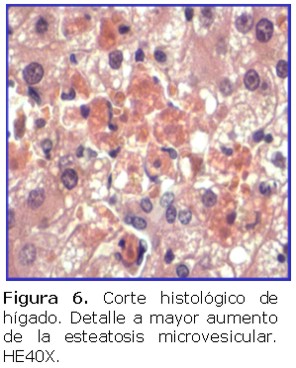
A partir del cuarto o quinto día, el paciente entra en el período de intoxicación o fase amarilla. Las manifestaciones gastrointestinales son más severas e incluyen vómito y dolor abdominal. Simultáneamente suelen aparecer síntomas hemorrágicos como púrpura, petequias y equimosis generalizadas, metrorragia, epistaxis y hemorragias bucales. La hemorragia gastrointestinal es la responsable de la hematemesis ("vómito negro") y melena, las cuales indican también un pronóstico desfavorable. Estas se deben a la falla hepática con disminución de varios factores de la coagulación. No hay tratamiento específico para la enfermedad. La terapéutica es básicamente sintomática y de soporte, orientada al control del equilibrio hidroelectrolítico y diálisis en pacientes con insuficiencia renal. La confirmación diagnóstica se realiza por laboratorio, utilizándose distintos métodos como aislamiento viral, serología, cultivo celular, biología molecular, histopatología e inmunohistoquímica. La biopsia hepática en pacientes vivos está contraindicada debido a la diátesis hemorrágica. El hígado de los fallecidos tiene una imagen histológica característica presentando necrosis de coagulación de los hepatocitos que predomina en la zona media del lobulillo, necrosis de algunos hepatocitos periportales, pericentrales y subcapsulares con la formación de cuerpos de Councilman, cambio graso microvacuolar y ausencia de inflamación (2-7). La inmunohistoquímica (IHQ) identifica, en las muestras obtenidas postmortem, la presencia, a nivel tisular, del antígeno viral causante de la enfermedad mediante una unión antígeno-anticuerpo altamente específica (9).
En el Paraguay durante la epidemia que se registró en el primer trimestre del 2008, las autoridades de salud notificaron en enero del 2008, la confirmación de los primeros cinco casos de fiebre amarilla selvática. La confirmación de un caso se realizó a través de técnicas moleculares. Los otros cuatro fueron confirmados por nexo epidemiológico. Hasta el 11 de febrero, otros 4 casos sospechosos de fiebre amarilla selvática han sido informados. Se amplió la vigilancia epidemiológica para detección e investigación de casos sospechosos y se intensificó la vacunación antiamarílica a la población general, y a aquellos que residen o ingresan a área de riesgo y no poseen antecedente de vacunación previa, ya que no se notificaban casos de FA en el país desde 1904 (8).
Este trabajo tuvo como objetivo identificar por inmunohistoquímica la presencia del antígeno del virus de la fiebre amarilla en tejidos hepáticos obtenidos de pacientes fallecidos con sospecha de FA, de manera a confirmar el diagnóstico de la enfermedad.
MATERIALES Y MÉTODOS
Estudio descriptivo de corte transverso en bloques de parafina en biopsias de tejido hepático obtenidos post mortem, con autorización de los familiares, de 4 pacientes fallecidos con sospecha clínica de FA durante la epidemia de fiebre amarilla en Paraguay en enero 2008.
Los bloques de parafina fueron enviados por la Cátedra de Anatomía Patológica de la Facultad de Ciencias Médicas-UNA, al Dpto. de Patología, IICS-UNA para identificar el antígeno específico de la fiebre amarilla por inmunohistoquímica. Se utilizó el anticuerpo primario anti-fiebre amarilla proveído por el Instituto Evandro Chagas, Belem - Brasil con la técnica del complejo avidina-biotina-peroxidasa (LSAB-2 Dako. Carpintería, California USA). Para cada caso se agregó un corte de hígado control positivo, muestra de hígado de un paciente con diagnóstico serológico e histopatológico de fiebre amarilla proveída por el Laboratorio de Patología, Instituto Nacional de Salud - Colombia y un corte de control negativo.
Los cortes de parafina de 3-4 µ de grosor fueron extendidos sobre láminas previamente tratadas con poli-l-lisina al 10% permitiendo una mejor fijación de los tejidos a la lámina. Posteriormente, los cortes se desparafinaron y se procedió al bloqueo de la peroxidasa endógena con solución de peróxido de hidrógeno al 30 %. Se procedió a la recuperación antigénica con solución de tris buffer 10mmol/l y EDTA 1mmol/l ph 9, en microondas al 50 % de potencia durante 10 minutos. Los cortes se lavaron en buffer y posteriormente se colocó el anticuerpo anti-fiebre amarilla en una dilución 1:200, por 30minutos. Se aplicó luego el sistema de visualización kit Dako LSAB+/HRP (cod. No K0679 Dako Carpintería California USA). Todo el proceso de incubación se realizó en cámara húmeda a temperatura ambiente.
Para evidenciar la unión antígeno anticuerpo, se utilizó el kit substrato cromógeno DAB líquido (Dako cod. K3466) y posteriormente se usó hematoxilina como coloración de contraste.
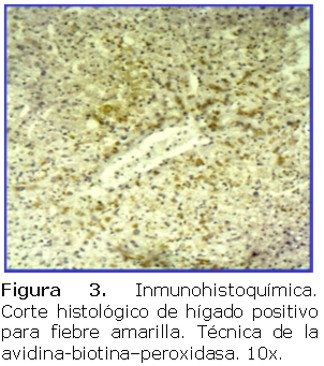
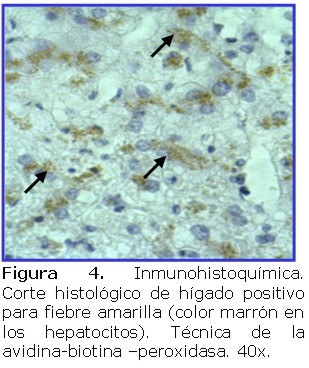
La positividad de la reacción se observó por microscopía óptica considerándose positivos a los casos en que se observó una tinción marrón en los hepatocitos, esto fue evaluado concomitantemente en relación a los hallazgos morfológicos histopatológicos observados en las muestras con la tinción de rutina hematoxilina eosina (HE).
RESULTADOS
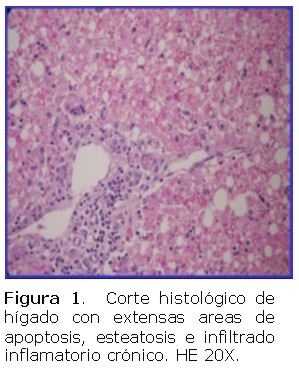
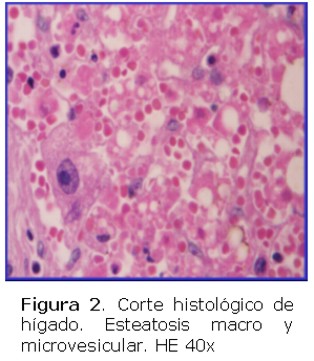
Se estudiaron biopsias hepáticas de cuatro pacientes cuyas edades estaban comprendidas entre 24 y 37 años, tres de ellos eran del sexo masculino. Todos habían fallecido con síntomas y diagnóstico clínico compatible con fiebre amarilla. Al momento de este estudio se contaba con la confirmación serológica IgM positiva para FA, en un solo caso. Histológicamente todas las biopsias estudiadas presentaban esteatosis micro y macrovacuolar, apoptosis o cuerpos de Councilman. Todas las muestras analizadas fueron positivas para fiebre amarilla por inmunohistoquímica en los cortes de parafina. La positividad se observó en todos los casos sospechosos y en los controles positivos (Ver figura 1,2,3,4,5,6).
DISCUSIÓN
Es difícil realizar un diagnóstico rápido y acertado de la fiebre amarilla ya que puede confundirse con otras patologías como hepatitis virales, malaria, otras fiebres hemorrágicas producidas por arbovirus como el dengue, infecciones bacterianas o enfermedades debidas a sustancias tóxicas (2,3). En los casos dudosos o difíciles, la técnica de inmunohistoquímica permite demostrar antígenos virales en el hígado, por medio de una unión antígeno-anticuerpo, que en conjunto con el estudio de las alteraciones histopatológicas confirman el diagnóstico de fiebre amarilla. Así el estudio histopatológico acompañado de la inmunohistoquímica en cortes de hígado es el método de elección para realizar el diagnóstico en los casos post mortem (2-4,6).
Las técnicas de inmunohistoquímica, si bien se utilizan principalmente en el área oncológica donde tienen múltiples aplicaciones como, identificar el origen celular del tumor, diferenciar entre una hiperplasia benigna y una neoplasia maligna, en algunos casos, inferir sobre la respuesta al tratamiento o tiempo libre de enfermedad así como determinar el pronóstico de las neoplasias, tienen además importante aplicación diagnóstica en los procesos infecciosos y son varios los autores que han demostrado diferentes antígenos virales en tejido por medio de esta técnica (9-15).
Sin embargo para obtener resultados satisfactorios se deben considerar diferentes aspectos como ser la correcta conservación de los anticuerpos, la dilución apropiada, el tiempo transcurrido entre el fallecimiento del paciente y toma de muestra, el uso de fijadores apropiados, tiempo y condiciones de incubación apropiados utilizándose diferentes variantes del método de la avidina-biotina como sistema amplificador de la reacción antígeno-anticuerpo (13-15).
Nuestros resultados con la utilización de la técnica de IHQ son satisfactorios y pueden ser comparados con los de otros autores, quienes han demostrado también antígenos del virus de la fiebre amarilla en tejidos embebidos en parafina (16-20).
En los casos que hemos estudiado, los resultados positivos para antígenos de fiebre amarilla por IHQ en muestras de tejido hepático, estuvieron estrechamente relacionados con los hallazgos histopatológicos, así como a las características clínicas. Si bien en el momento del estudio no se contaban aún con los resultados serológicos de tres pacientes, hemos confirmado en los mismos el diagnóstico de FA por medio de la inmunohistoquímica en muestras post mortem.
Esta confirmación diagnóstica reviste mayor relevancia en aquellos pacientes en quienes los estudios serológicos no arrojaron resultados concluyentes especialmente considerando las características clínicas y los hallazgos histopatológicos en las muestras de hígado de estos pacientes.
La inmunohistoquímica en conjunto con los criterios clínicos y el aspecto histopatológico confirma el diagnóstico de FA en casos post mortem. Constituye una herramienta muy útil permitiendo realizar el diagnóstico retrospectivo en los casos que no ha sido posible realizar otros estudios.
Agradecimiento
Los autores agradecen al Dr. Edgar Parra del Laboratorio de Patología, Instituto Nacional de Salud-Colombia quién gentilmente nos ha proporcionado los bloques de parafina con controles positivos, y material bibliográfico. Igualmente al Instituto Evandro Chagas, Belem - Brasil por el anticuerpo anti-fiebre amarilla para este trabajo.
BIBLIOGRAFÍA
1. Rodriguez G, Velandia M, Boshel J. Fiebre amarilla: La enfermedad y su control. Bogotá: Instituto Nacional de Salud; 2003. [ Links ]
2. Organización Panamericana de la Salud. Enfermedades infecciosas emergentes y reemergentes, Región de las Américas Fiebre amarilla selvática (FAS) en Brasil, Paraguay, Argentina. Boletín PAHO 2008; 5(4). [ Links ]
3.Monath TP. Yellow fever: an update. Lancet Inf Dis 2001;1:11-20. [ Links ]
4.Singh MK, Brillman J. Yellow Fever. eMedicine World Medical Library. (Online). (Consultado mayo 2009) Disponible en http://www.emedicine.com/emerg/topic645.htm. [ Links ]
5. Neyra J, Sipan F. La fiebre amarilla, pasado y presente en el Perú. Rev Diag. 1983; 12(03):86-95. [ Links ]
6. Cáceres DC. La fiebre amarilla y su vigilancia en salud pública. Inf Quin Epidemiol Nac 1999; 4:7-11. [ Links ]
7. Organización Panamericana de la Salud. Alternativas para la prevención y control del dengue y del dengue hemorrágico en los países de Centroamérica. Washington: OPS/OMS; 1995. [ Links ]
8. Paraguay. Ministerio de Salud pública y Bienestar Social. Fiebre Amarilla en Paraguay. Boletín Epidemiológico semanal. 9(6). [ Links ]
9.Bacchi CE, Grown AM, Bacchi MM. Detection of infectious disease agents in tissue by immunocytochemistry. Braz J Med Biol Res 1994; 27(12): 2803-20. [ Links ]
10.Jasani B, Schmid K. Immunocytochemistry in diagnosis of neoplastic diseases.En Jasani-Schmid, (Ed). Immunocytochemistry in diagnostic histopathology. London: Churchill Livingstone; 1993.p 31-125. [ Links ]
11.Sarmiento L, Rodríguez G, Boshell J. Diagnóstico immunohistoquímico del dengue en cortes de parafina. Biomed. 1995;15:10-5. [ Links ]
12.Brunnert SR, Dai Y, Kohn DF. Comparison of polymerase chain reaction and immunohistochemistry for the detection of Mycoplasma pulmonis in paraffin-embedded tissue. Lab Anim Sc. 1994; 44(3):257-60. [ Links ]
13.Ricaurte O, Sarmiento L, Caldas ML, Rodríguez G. Evaluación de un método inmunohistoquímico para el diagnóstico de la fiebre amarilla. Biomédica. 1993;13:15-9. [ Links ]
14. Pelegrino JL, Arteaga E, Rodriguez AJ, Gonzales E, Frontera MC, Guzmán MG. Normalización de técnicas inmunohistoquímicas para la detección de antígenos del virus dengue en tejidos embebidos en parafina. Instituto de Medicina Tropical "Pedro Kourí". Rev Cub Med Trop. 1997;49(2):86-93. [ Links ]
15. Faran ME, Romoser WS, Routier RG, Bailey ChL. Use of the avidin biotin-peroxidase complex immunocytochemical procedure for detection of Rift Valley fever virus in paraffin section of mosquitoes. Am J Trop Med Hyg. 1986; 35 (5): 1061-7. [ Links ]
16. Se Thoe SY, Sam CK, Cheng HM , Prasad U. Improved sensitivity of detection by avidin- biotin complex (ABC), immunocytochemistry in Epstein-Barr virus serology. J Med Virol. 1989; 29:311-4. [ Links ]
17. Muñoz E, Morón C, Kemper R, Román. Inmunohistoquímica en el diagnóstico de fiebre amarilla. An Fac Med Lima 2004; 65(3). [ Links ]
18. MonathTP, Ballinger ME, Miller BR, Salaum JJ. Detection of yellow fever viral RNA by nucleic acid hibridizatin and viral antigen by immunocytochemistry in fixed human liver. Am J Trop Med Hyg 1989; 40:663-8. [ Links ]
19. Méndez J, Parra E, Neira M, Rey G. Detección por reacción en cadena de la polimerasa de transcriptasa inversa del virus de la fiebre amarilla en monos silvestres: una herramienta sensible para la vigilancia epidemiológica. Biomédica 2007; 27:461-7. [ Links ]
20. Méndez J, Rodríguez G, Bernal M, Calavache D, Boshell. Detección molecular del virus de la fiebre amarilla en muestras de suero de casos fatales humanos y en cerebros de ratón. Biomédica 2003; 23:232-8. [ Links ]
*Autor Correspondiente: Dra. Soledad Campos, Departamento de Patología
Instituto de Investigaciones en Ciencias de la Salud. Río de la Plata y Lagerenza. Asunción-Paraguay
Email: patologia@iics.una.py