Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Memorias del Instituto de Investigaciones en Ciencias de la Salud
On-line version ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud vol.7 no.1 Asunción June 2009
ARTICULO ORIGINAL
Pruebas complementarias a la problemática del diagnóstico de la infección por los virus B y C en donantes de sangre
Complementary tests for the problem of B and C virus infection diagnosis in blood donors
*Echagüe GI-II, Sosa LI-II, Valdez RI, Ramírez AII, Ruiz III, Arce MI
IBanco de Sangre del Hospital de Clínicas. Universidad Nacional de Asunción (UNA).Paraguay
IIInstituto de Investigaciones en Ciencias de la Salud. Universidad Nacional de Asunción (UNA).Paraguay
RESUMEN
El objetivo de este trabajo es determinar si las transaminasas hepáticas tienen valor como pruebas complementarias que orienten el diagnóstico de hepatitis B y C, en donantes de sangre con anticuerpos positivos por el método ELISA a estas infecciones virales; teniendo en cuenta que las pruebas confirmatorias como el inmunoensayo recombinante (RIBA) o la prueba de ácidos nucleicos por técnicas moleculares como PCR (RNA HCV) para hepatitis C y DNA viral (PCR) para hepatitis B no se realizan aún en nuestro país debido a sus elevados costos. Se busca sumar esfuerzos en salud pública desde los bancos de sangre debido a la trascendencia de llegar a un diagnóstico en los donantes seropositivos, que hayan sido captados en el tamizaje, para prevenir la propagación de estas hepatitis. Se realizaron pruebas serológicas para hepatitis C, anticuerpos frente al antígeno del core de la hepatitis B y determinaciones de los niveles de GPT o ALT (Transaminasa Glutámica Pirúvica o Alanina Amino Transferasa), GOT o AST (Transaminasa Glutámico Oxalacética o Aspartato Amino Transferasa) en 236 donantes de sangre seropositivos para hepatitis B y C del Banco de Sangre del Hospital de Clínicas de la Universidad Nacional de Asunción-Paraguay. Las transaminasas elevadas fueron clasificadas de acuerdo a los marcadores serológicos positivos para hepatitis B y C, encontrándose niveles elevados en un 13.9% de individuos con anti-HBc, 40% en individuos con anti HCV y 2 de 7 casos en individuos con serología positiva para ambos marcadores serológicos. Casi la mitad de los donantes con marcador serológico positivo para anti HCV presentan elevación de las transaminasas.
Palabras claves: Aspartato aminotransferasa (GOT/AST), y alanino aminitransferasa (GPT/ALT), antígeno de superficie (HBsAg), anticuerpos frente al antígeno del core(anti-HBc), anti-HVC, donantes de sangre.
ABSTRACT
The aim of this study was to determine if liver transaminases had value as complementary tests to orientate the diagnosis of hepatitis B and C in blood donors with positive antibody to these viral infections by the EIA method, considering that confirmatory tests such as the recombinant immunoassay (RIBA) or nucleic acid test by molecular techniques such as PCR (HCV RNA) for hepatitis C and viral DNA (PCR) for hepatitis B are not performed in our country due to their high costs. We are looking for joining efforts in public health from the blood banks due to the importance of reaching a diagnosis of seropositive donors who have been detected in the screening to prevent the spread of hepatitises. Serologic tests for hepatitis C, antibodies against the core antigen of hepatitis B and determinations of the levels of ALT or GPT (Alanine aminotransferase or Glutamic pyruvic transaminase), AST or GOT (Aspartate aminotransferase or Glutamic oxalacetic transaminase) were carried out in 236 blood donors seropositive for hepatitis B and C of the Blood Bank of the Hospital de Clinicas, National University of Asuncion, Paraguay. Elevated transaminases were classified according to the positive serological markers for hepatitis B and C finding high levels in 13.9% in donors with anti-HBc, 40% in donors with anti HCV and two of seven cases in donors with positive serology for both serological markers. Almost half of the donors with positive serologic marker for anti HCV had elevated transaminases.
Keywords: Aspartate aminotransferase (GOT/AST), alanine aminotransferase (GPT/ALT), surface antigen (HBsAg), antibody to core antigen (anti-HBc), anti-HVC.
INTRODUCCIÓN
Las infecciones transmisibles por transfusión (ITT) son aquellas que pueden transmitirse a otras personas a través de donaciones de sangre o hemocomponentes, siendo los donantes de riesgo aquellos en quienes los análisis de su unidad de sangre dan resultados doblemente reactivos en pruebas de tamizaje (1).
Para evitar o disminuir la transmisión y diseminación de estas enfermedades a través de la transfusión de productos sanguíneos, los bancos de sangre deben obtener un producto terapéutico de mejor calidad y seguridad. También el mismo siempre se constituye en vigilancia epidemiológica e identifica el verdadero riesgo transfusional a que se exponen los receptores de sangre (1).
La OMS estima que 170 millones de personas en el mundo se encuentran infectadas por el virus de la hepatitis C (HCV) (2), datos que son obtenidos de donantes de sangre, que no reflejan la situación real de la infección en la población general. Esta, actualmente, se considera como la primera causa de transplante hepático en el mundo (3). Es muy poco expresiva desde el punto de vista clínico, y el 50 a 80% de las personas infectadas corren el riesgo de evolucionar hacía formas crónicas, y de éstos, cerca del 20% progresan a cirrosis que es la causa principal de transplante hepático. Entre 0,4 a 5% de los casos de cirrosis evolucionan a un carcinoma hepatocelular (4).
En 1990, la Food and Drug Administration (FDA) aprobó el test para detectar el anticuerpo del virus de la hepatitis C, el enzimainmunoensayo (ELISA)(3). La prueba inmunoenzimática de tercera generación (ELISA 3.0) para la detección del anticuerpo de hepatitis C (anti-HCV), incluye el antígeno NS5, lo cual la hace más sensible (99%) que las versiones previas (5,6).
La detección de anticuerpos anti HCV evalúa la respuesta inmunológica humoral del paciente infectado contra proteínas virales del HCV y es obligatoria utilizarla en bancos de sangre. Detecta anticuerpos de clase IgG, lo que explica la existencia de un periodo de ventana serológico (variable de un paciente a otro, en general de 1 a 3 meses, pudiendo llegar hasta los 6 meses) (7,8). Un resultado positivo indica el contacto actual o pasado del sistema inmune del paciente con HCV, impidiendo su utilización como marcador de infección aguda, salvo que se documente su seroconversión, la cual se comprobaría con el dosaje seriado de anticuerpos. La determinación de anticuerpos de tipo IgM no se utiliza, debido a su baja sensibilidad y especificidad (9,10).
La detección de anticuerpos anti HCV por RIBA (recombinant inmunoblot assay) es un ensayo suplementario al de ELISA que permite discriminar antígenos virales específicos, blancos de la respuesta inmunológica detectada en el ELISA (8,11).
En donantes de sangre en áreas de baja prevalencia para HCV (menor a 10%), como es el caso de Paraguay (11,12), el RIBA, que es más específico, es útil para determinar si el ELISA positivo es un verdadero o un falso positivo (8). Es habitual informar el anti-HCV positivo únicamente con base en el resultado de la prueba de tamizaje, aún cuando la recomendación internacional establece que antes de emitir el resultado se deben realizar pruebas complementarias a todas las personas con prueba de tamizaje positiva, especialmente en poblaciones con baja prevalencia de hepatitis C, en donadores de la población general (13,14). En poblaciones con baja prevalencia de hepatitis C, el anti-HCV es falso positivo en 40 % de los casos. Lo mismo ocurre en individuos con anti-HCV positivo, sin factores de riesgo para hepatitis C y Alanina Amino Transferasa (ALT) normal. En áreas de alta prevalencia y para pacientes con riesgo de padecer hepatitis C, el resultado del anti-HCV tiene un valor predictivo positivo alto, y, por tanto, es suficiente para el diagnóstico y hace innecesario el RIBA (13). Asimismo en pacientes con anti-HCV positivo en un programa de donación de sangre, la técnica molecular de PCR (RNA-HCV) positivo confirma el diagnóstico. En pacientes con PCR (RNA HCV) negativo indica un resultado falso positivo del anti-HCV o una infección con el virus C resuelta (13).
Los bancos de sangre en los Estados Unidos iniciaron tests a los donantes voluntarios para el anticuerpo dirigido contra el núcleo antigénico de la hepatitis B anti-HBc y alanina aminotransferasa (ALT) en 1986 y 1987 y para anti-HCV en 1990 (15,16).
Por otro lado, la hepatitis B (VHB) es la mayor causa de hepatitis aguda y crónica, cirrosis y carcinoma hepatocelular primario (17,18). Se reporta que un millón de personas en el mundo tienen evidencias serológicas de la infección (19), y se estima que trescientos cincuenta millones mantienen el estado de portador del virus, éstos se consideran como reservorios de la infección. La infección por VHB, induce una hepatitis aguda ictérica en uno de cada cinco casos, y evoluciona a la cronicidad en aproximadamente el 5% de los casos cuando se adquiere en la adolescencia o la edad adulta (20).
El antígeno de la hepatitis B (HBsAg) puede ser identificado en el suero a los 30 a 60 días después de la exposición al HBV y persiste por periodos variables dependiendo de la resolución de la infección (18). El anticuerpo para el núcleo antigénico de la hepatitis B (anti-HBc) se desarrolla en la infección aguda y crónica por hepatitis B y persiste indefinidamente. La Inmunoglobulina M (Ig M) del anti-HBc aparece tempranamente en la infección y persiste por 6 meses o más. Es un marcador de infección por HBV aguda. En un pequeño número de pacientes con HBV aparecen en circulación niveles de HBsAg indetectables, y el anti-HBc podría ser el único marcador detectable en esos casos (17,21).
Los test sensibles recomendados comercialmente para la detección de hepatitis B son radioinmuensayo (RIA) y enzimainmunoensayo (ELISA). Un pequeño número de individuos puede tener niveles indetectables de HBsAg y el test puede dar un falso negativo. La mayoría de estos bajos niveles de HBsAg, sin embargo, pueden ser detectados por el test de anti-HBc en las unidades de sangre o componentes sanguíneos para transfusión (17). El método de PCR es uno de los ensayos de elección por su alta sensibilidad y con amplios rangos de detección para poder evaluar correctamente la respuesta antiviral (22).
Los resultados deberían proveer la información de los test relacionados con el screening de hepatitis (anti-HBc, ALT y anti-HCV) a los donantes repetidamente reactivos o confirmación positiva del test de HBsAg. Esta información debería ser transmitida con facilidad a los donantes. La persistencia de HBsAg con elevados valores de transaminasas mayormente indicaría hepatitis B crónica (17,19).
El Centro para el Control y Prevención de Enfermedades (CDC-Atlanta, EE.UU.), (17) ha recomendado que una persona debe ser considerada con evidencia de infección de HCV si el resultado del tamizaje es positivo, debiendo ser verificado por un test serológico específico como el RIBA o PCR - RNA (nucleic acid test). De igual manera en los individuos con resultado positivo para hepatitis B es recomendado realizar test más específicos como el DNA viral (PCR) antes de reportar un resultado positivo (5,16).
Las pruebas complementarias revisten una especial importancia, en la identificación de donadores de sangre con alta probabilidad de hepatitis. Contreras afirma que ofrecen una "oportunidad de oro" para identificar personas asintomáticas antes del desarrollo de complicaciones (23). En este sentido es importante que el Banco de Sangre se comprometa con el sistema de notificación y con la derivación a la consulta del paciente detectado anti-HCV positivo, para la confirmación diagnóstica, seguimiento y/o eventual tratamiento (8).
El objetivo de este trabajo es determinar si las transaminasas hepáticas tienen valor como pruebas complementarias que orienten el diagnóstico de hepatitis B y C, en donantes de sangre con anticuerpos positivos por el método ELISA; teniendo en cuenta que las pruebas confirmatorias como el inmunoensayo recombinante (RIBA) o la prueba de ácidos nucleicos por técnicas moleculares como PCR (RNA HCV) para hepatitis C y DNA viral (PCR) para hepatitis B no se realizan aún en nuestro país debido a su elevado costo. Buscamos sumar esfuerzos en salud pública desde los bancos de sangre, debido a la trascendencia de llegar a un diagnóstico en donantes seropositivos, que hayan sido captados en el tamizaje, para prevenir la propagación de estas hepatitis.
MATERIALES Y METODOS
Estudio observacional, descriptivo de corte transverso en 3559 donantes del Banco de Sangre del Hospital de Clínicas FCM-UNA, desde agosto del año 2.005 a febrero del año 2.006, donde se encontraron 236 muestras consecutivas positivas para el virus de hepatitis B y/o C, con un 95% de confiabilidad y un error máximo del 5%. A los donantes con serología positiva se le dosaron los niveles de transaminasas en el Departamento de Análisis Clínicos del Instituto de Investigaciones en Ciencias de la Salud IICS-UNA, Se siguieron los criterios de selección del donante: evaluándose los antecedentes y el estado actual del donante, medicamentos, frecuencia de donación, edad, pulso, embarazo y menstruación, peso, altura, ayuno, inmunizaciones y vacunaciones, estilo de vida. Cada donante con resultado positivo participó voluntariamente, brindó su consentimiento informado y recibió el resultado de los análisis realizados en forma confidencial.
Los marcadores serológicos fueron determinados mediante la técnica de inmunoensayo enzimático (ELISA) de segunda generación, para el anticuerpo frente al antígeno del core (anti-HBc) IgG e IgM y el anticuerpo del virus de la hepatitis C (anti-HCV). Los niveles séricos de las transaminasas: aspartato aminotransferasa (AST), y alanino aminotransferasa (ALT), se realizaron por el método enzimático colorimétrico de Reitman Frankel, con un nivel de referencia menor a 12 UI/L (24).
RESULTADOS
En 3559 donantes de sangre estudiados, se encontró 236 muestras con serología positiva para anticuerpos de hepatitis B o C, de los cuales 172 correspondieron al anticuerpo anticore de la hepatitis B (anti-HBc) y 57 al anticuerpo contra el virus de la hepatitis C anti-HCV; 168 eran del sexo masculino y 68 del sexo femenino, con una edad promedio de 35 ± 10 años.
La distribución de los marcadores serológicos para hepatitis (anti-HBc y anti-HCV) fue la siguiente: 73% (172/236) presentó serología positiva para el marcador anti-HBcore de hepatitis B, 24% (57/236) serología positiva para anti-HCV de hepatitis C y 3% (7/236) serología positiva para anti-HBc y anti-HCV de hepatitis B y C respectivamente.
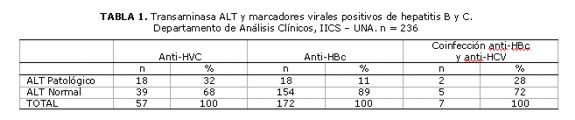
Las determinaciones de la enzima ALT fueron clasificadas en relación con la serología reactiva para anti-HCV y para anti-HBc de la siguiente forma: elevadas (patológico), 32% con anti-HVC, 11% con anti-HBc; normal, 68% con anti-HVC, 89% con anti-HBc. Tabla 1.
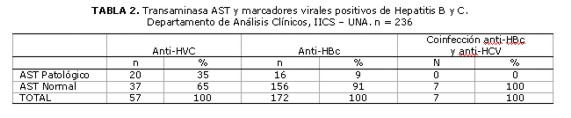
Las determinaciones de la enzima AST fueron clasificadas en relación con la serología reactiva para anti HCV y para anti-HBc de la siguiente forma: elevadas (patológico), 35 % con anti-HVC, 9% con anti-HBc; normal, 65 % con anti-HVC, 91% con anti-HBc. Tabla 2.
Las frecuencia de transaminasas elevadas ALT y/o AST según marcadores positivos de anti-HBcore fue del 13.9% (24 de 172 casos), la de anti-HCV fue del 40% (23 de 57casos) y 2 de 7 casos para la coinfección.
DISCUSIÓN
En nuestro estudio, casi la mitad de los donantes con anti-HCV reactivos presentaron elevación de ALT y/o AST (40%) en comparación con el porcentaje encontrado en individuos con serología positiva para anti-HBc (13.9%), La enzima ALT elevada se encontró con una frecuencia mayor en los donantes de nuestro estudio con ELISA repetidamente reactivos para anti-HCV (32%) en comparación a los que poseían serología repetidamente reactiva para anti-HBc (11%); la elevación de la ALT fue en su mayoría hasta dos veces con respecto a su valor normal,lo que podría sugerirnos posibles resultados reactivos con la prueba de RIBA o los test moleculares mientras que el resto de los donantes con serología positiva para anti-HCV y con transaminasas normales podrían tratarse de falsos positivos, de indeterminados o de positivos con ALT normal. En cuanto a la AST, las que resultaron elevadas, solo fueron ligeramente elevadas con respecto a su valor normal.Estudios realizados por Stevens et al, Koziol et al, Aach et al y Alter et al (17, 18, 19, 20) a finales de la década del 80, en los cuales se realizaron dosajes de ALT en donantes implicados en la transmisión de hepatitis "no A no B", encontraron ALT elevadas en comparación a los donantes no implicados en la transmisión de hepatitis no A no B, estos estudios sugirieron que la inclusión en el screening de los donantes, de marcadores indirectos, redujeron la incidencia de hepatitis post transfusional no A no B en un 50% (21).
La alaninoaminotransferasa (ALT o GPT) y la aspartatoaminotransferasa (AST o GOT) son enzimas que se encuentran en los hepatocitos. Son marcadores sensibles de lesión hepática, pero sólo la ALT es específica (AST también está en músculo cardíaco y esquelético, riñón, cerebro, páncreas, pulmones, leucocitos y hematíes). Su determinación es rápida y barata. La elevación de las transaminasas tiene un valor impredecible ya que un mismo valor puede corresponder a una variación de la normalidad o ser la primera evidencia de una enfermedad mortal. No obstante existen unos rangos de valores que nos pueden orientar como marcador indirecto por seropositividad de hepatitis B y/o C (29).
Si bien los test de ELISA de segunda y tercera generación poseen una alta sensibilidad (99,8%) para las hepatitis B y C y una ventana inmunológica reducida a aproximadamente 10 semanas, presentan ciertas limitaciones: no permiten discriminar entre los sujetos con infección aguda, crónica o pasada con recuperación, tampoco permiten la detección de una infección aguda y pueden presentar falsos positivos en población sana y de bajo riesgo como los donantes de sangre.(26) El CDC de Atlanta ha recomendado que los individuos no sean considerados portadores de HCV hasta que el resultado positivo obtenido por el screening sea confirmado por dos métodos diferentes. Sin embargo el alto costo que esto supone, aún más, si se debe realizar una confirmación por métodos moleculares, ha reducido la accesibilidad de los laboratorios a dichos procedimientos, haciéndose necesario alternativas accesibles en el costo para orientar hacia un diagnóstico. Este es el motivo por el cual hemos realizado las determinaciones de las transaminasas como método complementario al screening por ELISA.
Por otro lado, hemos encontrado un elevado porcentaje de donantes con serología positiva para hepatitis C que presentaban ALT normales (68%), que tampoco pueden ser descartados de estar infectados activamente por el HCV ya que la elevación de las transaminasas en estos individuos es intermitente (29) o podría tratarse de falsos positivos. Estas interrogantes podrían resolverse con la prueba de RNA HCV positiva y/o RIBA positivo para hepatitis C, que confirma la prueba de escrutinio positiva. El RNA HCV es detectable de 1 a 3 semanas postexposición.
En poblaciones de baja prevalencia para hepatitis C, como es el caso de nuestro país, las pruebas confirmatorias (RIBA o ARN HCV) son útiles para determinar si el ELISA repetidamente positivo, es un verdadero o un falso positivo (5). La prevalencia en donantes de Sangre del Hospital de Clínicas en el año 2005 fue de 1,36% para anti-HCV y 4,20% para anti-HBc, para el año 2007 se redujo la prevalencia del anti-HCV a 0,19%; creemos que gracias a las versiones mejoradas del ELISA (v3.0); en tanto que para el anti-HBc fue de 5,08% (Estadística del Servicio de Banco de Sangre del Hospital de Clínicas. Facultad de Ciencias Médicas, Universidad Nacional de Asunción. Datos no publicados).
Estos resultados nos sitúan entre los grupos de baja prevalencia (< 2%) para hepatitis C y de mediana prevalencia (2 a 7%) para el anti-HBc. Estudios realizados por Silveira, Tanaka et al encontraron una prevalencia en donantes de sangre para anti-HBc en Brasil de 7,9%, en Argentina 2,1%, República Dominicana de 21,4%, México 1,4%, Venezuela 3,2% y Chile de 0,6%.
En el 2.003 el CDC (Centro para el Control y Prevención de Enfermedades, EE.UU.) recomendó dos nuevos algoritmos. El uso de estos algoritmos ha sido de ayuda para simplificar el diagnóstico de la hepatitis C y bajar los costos. El algoritmo A se basa en la relación de la densidad óptica (OD) del ELISA anti-HVC sobre el punto de corte (CO): una razón OD/CO = 6 se reporta positivo y a una razón OD/CO < a 6 se le debe realizar el método del Inmunoblot anti-HCV. Esto minimizaría el número de muestras positivas del screening por ELISA que requieren un test suplementario confirmatorio para el diagnóstico. El algoritmo B sugiere realizar a todos los ELISA reactivos una PCR RNA HCV para el diagnóstico (6).
En nuestro trabajo, que fue realizado en el 2005, no fue posible utilizar el algoritmo A, y por ello hemos realizado la determinación de las transaminasas como marcador indirecto complementario, pero actualmente la mayoría de los resultados reactivos del screening por ELISA para HCV de nuestros donantes, poseen la razón OD/CO por debajo de seis, por lo cual se hace necesario la confirmación de los mismos por otros métodos para el diagnóstico.
En cuanto a las hepatitis B reactivas en nuestro estudio, el 73% se encontró con serología positiva para el anti-HBcore, lo que pone de manifiesto el elevado porcentaje de individuos que estuvieron en contacto con este virus. Si bien la prevalencia se mantiene intermedia (entre 2% y 7%) en los donantes del Banco de Sangre del H. de Clínicas, es importante ayudar a los médicos a llegar al diagnóstico de manera a prevenir la progresión de la enfermedad, detectada fortuitamente en donadores de sangre.
Debemos señalar que el Instituto Nacional de Salud de los EEUU definió los criterios diagnósticos utilizados hasta la fecha (31), comprendiendo el dosaje de las transaminasas, destacando el papel del DNA-VHB ante un falso positivo de HBsAg o negativo de anti-HBc, así como su medición en las tres fases de la infección, la fase de tolerancia inmune (correspondiente al periodo de incubación), la fase reactiva inmune (forma más activa de la enfermedad) y la fase no replicativa (fase de seroconversión).
Por otro lado hemos encontrado un 3% de coinfección de hepatitis C y B; cabe destacar que la infección combinada produce mayor lesión hepática que las infecciones por un solo virus. La mayoría de las veces una infección tiende a predominar, haciéndose indispensable para saber cual es la infección dominante la detección de RNA-VHC y DNA-VHB (31,32).
Por último, queremos concluir que aunque la ALT/GPT y la AST/GOT son marcadores de lesión hepática de determinación rápida y barata, su utilidad como marcador indirecto complementario en la confirmación del screening realizado para hepatitis B y C es muy limitada y debe ser utilizado en conjunto con las técnicas confirmatorias como el RIBA y técnicas moleculares, poco disponibles aún en nuestro país, que puedan clarificar el comportamiento de estas enfermedades, haciendo hincapié en la importancia de realizar un diagnóstico precoz de las hepatitis, en especial en aquellos individuos aparentemente sanos como los donantes de sangre, antes que se presenten alteraciones irreversibles.
BIBLIOGRAFÍA
1. Los Bancos de Sangre en la Vigilancia en Salud Pública. Instituto Nacional de Salud. Circular INS 003-2002. Disponible en: www.ins.gov.co [ Links ]
2. Falagán C, Váldez P, León A, Hechavarría X, Cabeza N. Donantes de sangre positivos al virus C de la hepatitis. MEDISAN. 2003; 7 (4):20-24. [ Links ]
3. Richter S. Laboratory Assays for Diagnosis and Management of Hepatitis C Virus Infection. J Clin Microbiol 2002; 40 (12): 4407-4412. [ Links ]
4. Beltrán M. Riesgo de Infección Transfusional de hepatitis C en Colombia. Rev Atreia. 2004; 17(3): 305. [ Links ]
5. Alter M, Kuhnert W, Finelli L. Guidelines for Laboratory testing and result reporting of Antibody to hepatitis C Virus. Centers for disease control and prevention. 2003; MMWR Recomm Rep 52: 1-13, 15. [ Links ]
6. Barreto AMEC, Takei K, Sabino EC, Bellesa MAO, Salles NA, Barreto CC, Nishiya AS, Chamone DF. Cost-effective analysis of different algorithms for the diagnosis of hepatitis C virus infection. Braz J Med Biol Res 2008; 41 (2). [ Links ]
7. Caetano M, Beck S. Importancia da deteccao de anticorpos anti-HBc na prevencao da transmissao do virus da hepatite B (VHB) em bancos de sangue. RBAC. 2006; 38 (4): 235-237. [ Links ]
8. Consenso Argentino Coinfección HIV-HCV. Acta Gastroenterol Latinoam 2005; 36(1). [ Links ]
9. Carithers RL Jr, Marquardt A, Gretch DR. Diagnostic Testing for Hepatitis. Semin Liver Dis. 2000; 20: 159-171. [ Links ]
10. Strader DB; Wright T, Thomas DL, Seeff LB. Diagnosis, Management and Treatment of Hepatitis C. Hepatology. 2004; p1147-1141. [ Links ]
11. Programa Nacional de Sangre. Hemovigilancia de las Hepatitis B y C en Bancos de Sangre Número 14; 2004. Boletín Mensual del Sistema Nacional de Información en Salud. Disponible en: www.sns.gov.bo. [ Links ]
12. Boletín Epidemiológico. Situación de seguridad en los bancos de sangre de los países del Caribe no Latino. Boletín Epidemiológico. 1999; 20(2). [ Links ]
13. Otero W, Pineda L, Beltrán L. Utilidad de la razón de verosimilitud (likelihood Ratio) en la práctica clínica. Rev Colom Gastroenterol. 2001; 6 (1): 33-36. [ Links ]
14. Farfán Y, Garzón M, Rey Tovar M, Molano JC, Lizarazu J, Marulanda JC. Prevalencia de hepatitis C por reacción en cadena de polimerasa (PCR) en donantes del banco de sangre. Rev Col Gastroentero. 2007; 22 (4). [ Links ]
15. Recommendations for Prevention and Control of Hepatitis C Virus (HCV) Infection and HCV-Related Chronic Disease. Atlanta, Ga.: Centers for Disease Control and Prevention, Epidemiology Program Office; Morbidity and Mortality Weekly Report, Recommendations and Reports, No. 19. October 16, 1998. [ Links ]
16. CDC. Hepatitis surveillance report, no. 53. Atlanta: Centers for Disease Control, Public Health Service, 1990. [ Links ]
17. Aach RD, Szmuness W, Mosley JW, et al. Serum alanine aminotransferase of donors in relation to the risk of non-A, non-B hepatitis in recipients: the Transfusion-Transmitted Viruses Study. N Engl J Med 1981;304:989-94. [ Links ]
18. Alter HJ, Purcell RH, Holland PV, Alling DW, Koziol DE. Donor transaminase and recipient hepatitis: impact on blood transfusion services. JAMA 1981;246:630-4. [ Links ]
19. Stevens CE, Aach RD, Hollinger FB, et al. Hepatitis B virus antibody in blood donors and the occurrence of non-A, non-B hepatitis in transfusion recipients: an analysis of the transfusion-transmitted viruses study. Ann Intern Med 1984;101:733-8. [ Links ]
20. Koziol DE, Holland PV, Alling DW, et al. Antibody to hepatitis B core antigen as a paradoxical marker for non-A, non-B hepatitis agents in donated blood. Ann Intern Med 1986;104:488-95. [ Links ]
21. CDC. Public Health Service inter-agency guidelines for screening donors of blood, plasma, organs, tissues, and semen for evidence of hepatitis B and hepatitis C. MMWR 1991;40(No. RR-4):1-17. Disponible en: http://www.cdc.gov/mmwr/preview. [ Links ]
22. Maynard JE, Kane MA, Alter MJ, Hadler SC. Control of hepatitis B by immunization: global perspectives. In: Zuckerman AJ, ed. Viral hepatitis and liver disease. New York: Alan R. Liss, Inc. 1988; p 967-9. [ Links ]
23. Santiesteban TJ, Alerm A, González G. Evaluación bioquímica-inmunológica de infectados crónicos por el virus de la hepatitis B. Comportamiento de la respuesta inmune en sus contactos familiares. Rev Cubana Invest Biomed. 2000; 19(1):14-27. [ Links ]
24. Pan American Health Organiazation. Normas y Estándares en Epidemiología: Lineamientos para la vigilancia epidemiológica. Boletín Epidemiológico. 1999; 20 (2). [ Links ]
25. Holland PV, Alter HJ. The clinical significance of hepatitis B virus antigens and antibodies. Med Cl No Amer. 1975; 59:849-55. [ Links ]
26. Muñoz G. Diagnóstico serológico y virológico de la hepatitis C y B: Aspectos Prácticos. Gastr Latinoam. 2006; 17 (2): 249-252. [ Links ]
27. Contreras AM. Anticuerpo a hepatitis C: ¿verdadero o falso positivo? Nuevas estrategias de diagnóstico. Rev Invest Clin. 2006; 58 (2): 153-160. [ Links ]
28. Frankel S. Gradwohl`s Clinical Laboratory Methods and Diagnostic. 7º Ed. Frankel, Reitman y Sonnenwirth; 1970. p. 123. [ Links ]
29. Romero MJ. Elevación de las Transaminasas. Guías Clínicas. 2001; 1 (42). Disponible en: www.fisterra.com/guias2/transaminasas.asp. [ Links ]
30. Zunino E. Epidemiología de la hepatitis B en Chile y esquemas de vacunación en Latinoamérica. Rev Chil Infect. 2002; 19 (3): 140-155. [ Links ]
31. Lok AS, Heathcote J, Hoofnagle. Management of Hepatitis B. Gastroenterology. 2001;120: 1828-1853. [ Links ]
32. Beltrán O, Rosas M, Garzón M. Hepatitis B: Diagnóstico y manejo. Rev Col Gastroenterol. 2005; 20 (2): 12-33. [ Links ]
*Autor Correspondiente:Dra. Gloria Echagüe,
Departamento de Análisis Clínicos, Instituto de Investigaciones en Ciencias de la Salud.
Río de la Plata y Lagerenza. Asunción-Paraguay
Email: aclinicos@iics.una.py