Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Memorias del Instituto de Investigaciones en Ciencias de la Salud
versão On-line ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud v.5 n.2 Asunción dez. 2007
ARTICULO ORIGINAL
Niveles de concordancia en el diagnóstico clínico – patológico de las enfermedades hematológicas
Levels of concordance in the clinical and pathological diagnosis of hematological diseases
*Figueredo Thiel SJ
Sección de Hematopatología del Dpto. de Patología. Instituto de Investigaciones en Ciencias de la Salud. Universidad Nacional de Asunción (UNA). Asunción-Paraguay
RESUMEN
En el diagnóstico hematopatológico los hallazgos clínicos(interrogatorio, examen físico, laboratorio, radiología u otros) se correlacionan con el examen morfológico cuanti-cualitativo de las células sanguíneas y hematopoyéticas en el frotis de sangre periférica y aspirados medulares. En caso de presunciones clínicas, para el diagnóstico final se tienen en cuenta los resultados anatomopatológicos considerados de certeza. Este trabajo de corte transverso, describe y analiza la concordancia diagnóstica entre la clínica-hematológica y la anatomía patológica en 370 pacientes provenientes de los grandes centros médicos del Paraguay, con 679 estudios anatomopatológicos citohistológicos analizados conjunta y sistemáticamente con técnicas especiales en la Sección de Hematopatología del Instituto de Investigaciones en Ciencias de la Salud entre los años 1997 y 2002. La concordancia, evaluada por el índice kappa, puede clasificarse en tres grupos: Grupo 1: concordancia buena (11% de casos) síndrome mieloproliferativo crónico (IK=0,48). Grupo 2: concordancia regular (47%) síndrome linfoproliferativo crónico (IK=022), leucemias agudas linfoblásticas (IK=020) y mieloides (IK=0,20). Grupo 3: concordancia baja (42%) aplasias medulares(IK=0,14), hiperplasias reactivas (IK=0,5) y mielodisplasias (IK=0,4) demostrándose la necesidad de estudios anatomopatológicos complementarios con técnicas especiales para llegar al diagnóstico de certeza como para estadificar, pronosticar y subclasificar las patologías hematológicas.
Palabras claves: Citohistoquímica enzimática, biopsia de médula ósea, hematopatología.
ABSTRACT
In the hemopathological diagnosis, clinical findings (patient physical examination, laboratory, radiology and others) are correlated to the quanti-qualitative morphological exam of blood and hematopoietic cells in peripheral blood smears and bone marrow aspirates. In the case of clinical presumptions, the anatomopathological results, considered accurate, have to be considered for the final diagnosis. This cross-sectional study describes and analyzes the diagnostic concordance between the hematological-clinical and the anatomopathological findings in 370 patients from the greatest medical centers of Paraguay. with 679 cytohystological and anatomopathological studies were systematically analyzed with special especial techniques of the Hematopathology Section of the Health Sciences Research Institute from 1997 to 2002. The concordance, evaluated by the Kappa index, could be divide in three groups: Group 1: good concordance (11% of cases) in chronic myeloproliferative syndromes (KI:0.40-0.60)). Group 2: regular concordance (47%) in chronic lymphoproliferative syndromes (IK=0.22), acute lymphoblastic leukemias (IK:0.20) and myeloid leukemias (IK=0.20). Group 3: low concordance (42%) in bone marrow aplasias (IK=0.14), reactive hyperplasias (IK=0.5) and myelodysplasias (IK=0.4). We demonstrated the necessity of anatomopathological studies complemented with special techniques to achieve an accurate diagnosis and dete4rmine the stage, prognosis and sub-classify hematological pathologies.
Keywords: Enzymatic cytochemistry techniques, bone marrow biopsy, hematopathology.
INTRODUCCIÓN
Las enfermedades hematológicas presentan diferentes grupos sindromáticos clasificados y subclasificados según su etiología, sus manifestaciones clínico-laboratoriales y su aspecto morfológico semejante, en relación a la proliferación clonal o no clonal de una, dos o tres de las líneas celulares hematopoyéticas. Entre los síndromes más frecuentes se encuentran los mielo y linfoproliferativos (agudos o crónicos), las mielodisplasias, los cuadros reactivos carenciales y las aplasias medulares(1-4).
Para el diagnóstico, se correlacionan los hallazgos clínicos (interrogatorio, examen físico, laboratorio, radiología u otros) con los exámenes hematológicos de acuerdo al aspecto morfológico cuantitativo y cualitativo de las células sanguíneas y hematopoyéticas en frotis de sangre periférica, como en extendidos de aspirados medulares. Se llega así, ya a un diagnóstico definitivo o, en su defecto, a una presunción diagnóstica clínica, la cual deberá ser confirmada por otros métodos antes de elegir la terapéutica adecuada(5-7).
Esta confirmación diagnóstica utiliza la mayoría de las veces como siguiente paso, a la biopsia de médula ósea, práctica necesaria, muy difundida y de uso corriente para evaluar los cambios patológicos del tejido hematopoyético en pacientes con enfermedades hematológicas. En sucesivos trabajos,(8-12) se ha demostrado que cuando la biopsia se asocia al uso sistemático de técnicas especiales, en conjunto y al mismo tiempo, con materiales citológicos para su interpretación, esta constituye un instrumento valioso para confirmar los diagnósticos, así como también para valorar los pronósticos, decidir los esquemas terapéuticos, realizar el seguimiento de pacientes y verificar la respuesta al tratamiento.
En nuestro país, desde 1997, se han incorporado y difundido las diferentes técnicas especiales para el estudio histológico de biopsias de médula ósea, conjuntamente con el estudio citológico de extendidos de sangre periférica, de aspirados medulares y de tejidos linfoides, ampliándose enormemente con ello, las posibilidades diagnósticas específicas(13).
En estudios previos en nuestro país,(14) se analizaron, aspectos morfológicos de las enfermedades hematológicas desde el punto de vista anatomopatológico, describiendo y clasificando los hallazgos con la aplicación sistemática de esta metodología especial y relacionándolos con los diagnósticos presuntivos clínico-hematológicos iniciales con los resultados anatomopatológicos finales. Estos estudios revelaron una sensibilidad y especificidad bajas de 54,58% y 5,55% respectivamente, así como una concordancia general mínima del 38% (IK=0,38), al examen clínico-hematológico utilizado sólo, sin tener en cuenta los hallazgos anatomopatológicos complementarios para llegar a diagnósticos definitivos en una mayor parte de los casos(14).
El objetivo de este trabajo fue determinar la concordancia entre el diagnóstico clínico-hematológico inicial y el anatomopatológico final, en este caso, específica por grupo sindromático de patologías hematológicas más frecuentes, para demostrar la relevancia del estudio anatomopatológico complementario en forma sistemática y conjunta, tanto cito e histológicas en materiales de sangre y médula ósea con técnicas citohistoquímicas especiales. Se estudian así todos los casos evaluados y diagnosticados en la Sección de Hematopatología del Dpto. de Patología, IICS-UNA en cinco años desde 1997 a 2002. Esta metodología contribuye y facilita el trabajo del médico en el tratamiento de los pacientes y resulta imprescindible para la clasificación y el diagnóstico final de certeza de las enfermedades hematológicas.
MATERIALES Y MÉTODOS
Población en estudio: Siguiendo un diseño observacional descriptivo de corte transverso con componente analítico, se evaluaron 370 pacientes hematológicos, con un total de 679 materiales anatomopatológicos que incluyeron a 413 biopsias de médula ósea, 155 aspirados medulares y 111 extendidos de sangre periférica. Los mismos fueron enviados de los principales centros médicos asistenciales del Paraguay, como ser los Dptos. de Hematología de las tres Cátedras de Clínica Médica de la Facultad de Medicina-UNA- Hospital de Clínicas, del Instituto de Previsión Social (IPS), del Centro de Hematología y Hemoterapia, del Hospital Central de las FFAA de Asunción, del Gran Hospital Nacional de Itauguá, del Instituto Nacional del Cáncer de Areguá, del Centro Materno Infantil de San Lorenzo y del Hospital Pediátrico Niños de Acosta Ñú de Reducto, con pacientes de todo el país. Se incluyeron a todos los pacientes portadores o sospechosos de enfermedad hematológica, de ambos sexos y de todas las edades, cuyos materiales anatomopatológicos se remitieron para estudio diagnóstico a la Sección de Hematopatología del Dpto. de Patología del Instituto de Investigaciones en Ciencias de la Salud, Universidad Nacional de Asunción, entre los años 1997 y 2002. Se excluyeron las muestras inadecuadas, como material escaso, hemorrágico, cartilaginoso u óseo sin tejido hematopoyético evaluable.
Técnicas anatomopatológicas, morfología y clasificación: Todos los materiales se analizaron en forma conjunta y sistemática con técnicas de citohistoquímica enzimática. La fijación se realizó con fijador universal neutro y los cilindros de médula ósea se procesaron mediante la técnica de inclusión adaptada a parafina. La descalcificación se realizó en solución neutra de etilendiaminotetra-acetato disódico (EDTA) y se siguieron los protocolos ya establecidos para cada tipo de patología(13-18).
Las variables hematológicas se clasificaron en base a hallazgos morfológicos en patológicas (síndromes linfoproliferativos crónicos y agudos o leucemias linfoblásticas; síndromes mieloproliferativos crónicos y agudos o leucemias mieloblásticas; aplasias medulares y mielodisplasias) y en reactivas (hiperplasias reaccionales y tejidos dentro de parámetros normales). Las variables morfológicas anatomopatológicas incluyeron los cambios patológicos morfológicos y citohistoquímicos cualitativos y cuantitativos en las biopsias y/ o aspirados de médula ósea y en los frotis de sangre periférica.
Análisis estadísticos: El análisis de la concordancia entre los métodos diagnósticos clínico-hematológicos (DCH-método 1) y anatomopatológicos (DAP-método 2) se realizó mediante el cálculo del índice kappa de Cohen (tabla de contingencia y test de chi2) con el programa de análisis epidemiológico de datos tabulados EPIDAT (Versión 2.0 para Windows) para variables dicotómicas, según el siguiente criterio: concordancia baja: IK:0,00-0,20; concordancia regular: IK:0,21-0,40; concordancia buena: IK:0,41-0,60; concordancia substancial IK:0,61-0,80; concordancia casi perfecta o perfecta IK:0,81-1,00(19). El tamaño de la muestra se estimó en 41 pacientes por grupo hematológico sindromático, en base a una concordancia esperada igual a 0,60 con una amplitud del intervalo de confianza (W) de 0,30 y un nivel de confianza (NC) de 95%(20).
Asuntos éticos: Este trabajo fue avalado por el Comité Científico y Ético de la Institución y los materiales utilizados comprenden aquellos enviados normalmente al Dpto. por indicación médica para estudios diagnósticos anatomopatológicos complementarios. Se aseguró la confidencialidad de los resultados de cada paciente y se los benefició con los estudios especiales realizados para llegar al diagnóstico correcto en cada caso.
RESULTADOS
La concordancia encontrada entre los diagnósticos clínico-hematológicos presuntivos iniciales y los resultados anatomopatológicos finales, en los distintos síndromes patológicos establecidos, clasificada en tres grupos o niveles según los resultados del índice kappa (IK), presentó en el grupo 1 una concordancia buena (IK>0,40) ycomprendió a los casos de patologías del síndrome mieloproliferativo crónico. El grupo 2 presentó una concordancia regular (40>IK>20), y comprendió a los casos de patologías linfoproliferativas crónicas, leucemias agudas linfoblásticas y agudas mieloides. El grupo 3 presentó una concordancia baja (IK<0,20), y comprendió a las aplasias medulares, a las hiperplasias reactivas y a las mielodisplasias. Véase Figura 1.
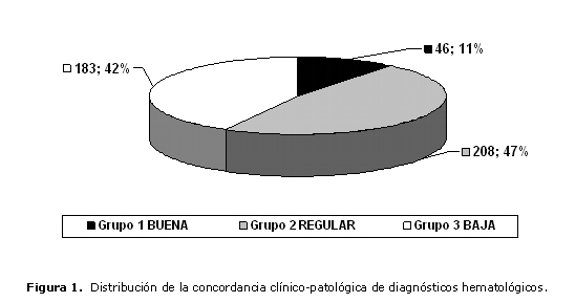
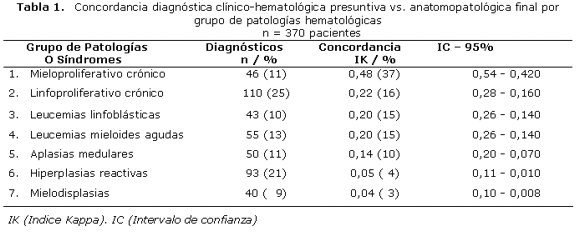
En cuanto a la distribución según el tipo de patología se encontró una mayor concordancia diagnóstica en las patologías del síndrome mieloproliferativo crónico, (IK=0,48) correspondiendo éstas solo al 11% del total de casos. Las patologías más frecuentes, como los procesos linfoproliferativos crónicos, linfomas leucemizados y no leucemizados, que corresponden al 47% del total de casos, presentaron una concordancia regular, seguidas de las biopsias de médula ósea con diagnóstico de hiperplasias reactivas con una frecuencia del 42% pero de una concordancia muy baja (IK=0,05). Véanse los detalles en la Tabla 1.
DISCUSION
Del análisis de los casos estudiados en la Sección de Hematopatología del Dpto. de Patología IICS-UNA, se evidencia que existe un nivel de concordancia bueno entre los diagnósticos clínico-hematológicos presuntivos o iniciales y los anatomopatológicos finales en las patologías del grupo 1, regular en las del grupo 2 y bajo en las del grupo 3.
El grupo 1, de concordancia buena corresponde sólo 11% del total de casos e integra a las patologías del síndrome mieloproliferativo crónico como la leucemia mieloide crónica, la policitemia vera, la trombocitemia esencial y la mielofibrosis idiopática, que tienen una clínica y morfología características. No obstante, fueron necesarios y están indicados, estudios anatomopatológicos complementarios para clasificar los estadíos de cada una de estas patologías, como para diferenciar las osteomielofibrosis idiopáticas primarias de las secundarias a infiltraciones linfomatosas hodgkinianas o no hodgkinianas, tricoleucemias, leucemias linfoblásticas agudas empaquetadas o procesos extrahematológicos, así como también para diferenciarlas en sus estadíos tempranos(2-4). Es importante recalcar, en este punto, que la indicación precisa de la biopsia de médula ósea con estudios especiales lo constituyen específicamente los casos leucopénicos o leucoeritroblásticos con aspirados medulares secos en los que no se llega a una conclusión desde el punto de vista clínico-hematológico por falta de células para evaluación(9,10,21). Esto ocurre a menudo con el síndrome mieloproliferativo crónico, debido al grado de fibrosis reactiva del estroma medular, que es evidenciado incipientemente en los grados 1 y 2, sólo por tinciones especiales para fibras reticulínicas en la biopsia de médula ósea (15, 22-27).
En las leucemias agudas ya sean éstas mieloides o linfoides (grupo 2 de concordancia regular), para llegar a una subclasificación exacta resulta imprescindible el estudio citoquímico enzimático seguido del inmunofenotípico según el caso. Cabe resaltar aquí, que la antigua citoquímica enzimática (14,28,29) con las insustituibles mieloperoxidasa, esterasas y fosfatasas siguen teniendo vigencia en la actualidad debido a su calidad, facilidad de realización y a su bajo costo, comparada a las inmunomarcaciones, que en nuestro país representan un problema grave para los pacientes de estratos socioeconómicos mayoritarios medio y bajo. Si bien estas inmunomarcaciones pueden realizarse en todos los casos, sería prudente en países en desarrollo como el nuestro, indicarlas obligatoriamente en los casos dudosos y en las estirpes celulares linfoides.
Así también dentro del grupo 2, en los casos linfoproliferativos crónicos sean estos leucemizados o tumorales (linfomas de Hodgkin y no Hodgkin), se impone obligatoriamente la biopsia de médula ósea para estadificación y estudios inmunofenotípicos de subclasificación precisa (2,11,24,25). En estos casos el aspirado medular por sí solo no es suficiente para realizar la estadificación tumoral, porque no permite establecer el patrón de infiltración del tejido hematopoyético, deja pasar estadíos incipientes (nodulares o intersticiales) y no puede diferenciar infiltraciones linfoplasmocitarias reactivas de clonales diferenciadas o maduras (30,31,32).
En el grupo 3, conuna concordancia clínico-patológica baja, muy baja o prácticamente inexistente (IK de 0,14 a 0,04) fueron encontradas las mielodisplasias, hiperplasias reactivas y las aplasias medulares, lo que alerta y recuerda al médico tratante la imprescindible indicación de la biopsia de médula ósea para estudios anatomopatológicos complementarios cuando se tienen pacientes con estas presunciones clínicas.
De esta manera se llega a la subclasificación y al diagnóstico definitivo de certeza en estas patologías, requisito para la elección del esquema terapéutico apropiado. Es importante recordar el valor de la práctica de la biopsia de médula ósea en el caso de la aplasia medular, en que solo por estudios histopatológicos se confirma el diagnóstico, descartando otras patologías que pueden presentar clínica semejante (3,10,14). Así también, el valor de la anatomía patológica con técnicas especiales en casos de mielodisplasias, posibilita un estudio más detallado del tejido hematopoyético, evidenciando precisamente la histo-topografía alterada y la presencia de los grupos de células precursoras y blásticas de localización anormal (ALIP) en los cilindros biópsicos (4,14,23). Estos criterios histológicos, junto al recuento de blastos son los actualmente establecidos y utilizados para el diagnóstico, diferenciación y subclasificación en este grupo, incluyéndose la inmunomarcación que puede realizarse ventajosamente al mismo tiempo y en el mismo material (2,24-26).
En el caso de las hiperplasias reactivas, también correspondientes al grupo 3 de baja concordancia, los estudios anatomopatológicos son valiosos para ir descartando los diagnósticos diferenciales. En este punto, en casi todos nuestros casos se han planteado diversos diagnósticos presuntivos clínicos sin tener ninguna certeza diagnóstica. El hecho de que exista una concordancia muy baja en los casos de las mielodisplasias y las hiperplasias reactivas medulares (IK de 0,04 y 0,05), confirma y remarca la importancia en este trabajo, del estudio cito e histopatológico con técnicas especiales en materiales de biopsia y aspirado de médula ósea conjuntos para diagnósticos definitivos.
La aplicación sistemática de las técnicas de citohistoquímica enzimática para el diagnóstico anatomopatológico evalúa al mismo tiempo citologías hematológicas (frotis de sangre periférica y aspirados o improntas medulares) y cortes histológicos de biopsias de médula ósea en parafina(13,14) estando esta metodología muy relacionada a los conceptos y criterios de la actual clasificación internacional de patologías hematológicas de la Organización Mundial de la Salud (OMS),(25) que tiene en cuenta tanto el aspecto morfológico cito-histológico con la aplicación de estas diferentes técnicas como también el aspecto inmunofenotípico, citogenético y molecular. Su valor radica en estandarizar las nomenclaturas y criterios para la definición y clasificación de las patologías, de modo que hematopatólogos, hematólogos, oncólogos y genetistas trabajen conjuntamente en la clínica, diagnóstico, terapéutica y en el estudio comparativo de estas enfermedades en los distintos países.
Teniendo en cuenta estos criterios actuales de la OMS, y siendo la concordancia clínico-patológica en general regular a baja en la mayoría de nuestros casos (89% del total de casos estudiados) necesariamente debe tenerse el apoyo diagnóstico complementario de la anatomía patológica para una conclusión diagnóstica final acertada. En los casos no confirmados por métodos clínico-hematológicos (hallazgos clínicos, laboratorio, frotis de sangre periférica y aspirado medular), la indicación acertada de la biopsia de médula ósea y su estudio anatomopatológico con técnicas especiales en forma conjunta con la citología hematológica en los casos estudiados en nuestro departamento, contribuyeron a proporcionar, esclarecer, confirmar y pronosticar el diagnóstico final de certeza de cada tipo de enfermedad hematológica.
BIBLIOGRAFIA
1.Sans Sabrafen J. Hematología Clínica. Tercera edición. Barcelona. España. Ediciones Doyma. 2001. [ Links ]
2.Knowles DM. Neoplastic Hematopathology. Segunda edición. New York. USA: Williams & Wilkins; 2001. [ Links ]
3.Remmele W, Schaefer HE. Erythropoese, Leukopoese und myeloproliferative Erkrankungen. En: Herausgegeben von W. Remmele. Pathologie 1. Sringer Verlag: Germany. 1984: 5-6: 273-452. [ Links ]
4.Mufti GJ, Flandrin G, Schaefer HE, Sandberg AA and Kanfer E (eds). An Atlas of Malignant Haematology. Cytology, Histology and Cytogenetics. Martin Dunitz Ltd. London; 1996. [ Links ]
5.Bennett JM, Catovsky D, Daniel M, Flandrin G. Proposals for the classification of the acute leukaemias. Br J Haematol 1976; 33: 451-8. [ Links ]
6.Bennett JM, Catovsky D, Daniel MT, Flandrin G, Galton DA, Gralnick HR et al. Proposed revised criteria for the classification of acute myeloid leukemia. A report of the French-American-British Cooperative Group. Ann Med 1989; 103: 6205-12. [ Links ]
7.Catovsky D. The Leukemic Cell. Segunda edition. London UK: Ed Churchill Livingstone. Medical Division of Longman Group UK Limited; 1991. [ Links ]
8.Brunning R. Bone marrow Specimen Processing. En: Knowles DM. Neoplastic Hematopathology. Primera edición. New York. USA: Ediciones Williams & Wilkins. 1991; 35: 1081-1097. [ Links ]
9.Wittels B. Surgical pathology of Bone Marrow-Core Biopsy Diagnosis. Vol 17 in the series Major problems in pathology. Ed. W B Saunders Company. USA; 1985. [ Links ]
10.Nieto L Hernández y Rozman C. Biopsia medular en la clínica hematológica. Salvat Editores, S.A. Barcelona: España; 1980. [ Links ]
11.Schaefer HE. The histotopography of bone marrow involvemeny in low malignant B-Cell lymphoma. En: Hara H (de) Contributions in Celebation of the 65th Published by The First Departament of Pathology, Kochi Medical School, Shinkodo Printing Company, Kochi: Japan; 1995: 115-50. [ Links ]
12.Riede UN, Herbst EW und Schaefer HE. Hämatopoetisches und lymphatisches System. En: Allgemeine und Spezielle Pathologie. Georg Thieme Verlag. Stuttgart: Germany. 1995; 10: 526-86. [ Links ]
13.Figueredo Thiel SJ. Utilización y aplicación de técnicas de citohistoquímica enzimática en biopsias de médula ósea. Anales de la Facultad de Ciencias Médicas. 1997; 30 (1-2): 81-97. [ Links ]
14.Figueredo Thiel SJ. Diagnóstico citohistoquímico sistemático en biopsias de médula ósea y citologías hematológicas en el Paraguay. Trabajo de tesis. Revista Anales de la Facultad de Ciencias Médicas. UNA. 2005; 38.(1-2): 9-21. [ Links ]
15.Schaefer HE. Die histologische Bearbeitungstechnik von Beckenkammbiopsien auf der Basis von Entkalkung und Paraffineinbettung unter Berücksichtigung osteologischer und hämatologischer Fragestellungen. Pathologe 1995; 16: 11-27. [ Links ]
16.Schaefer HE. Methoden zur histologischen, zytologischen und zytochemischen Diagnostik von Blut und Knochenmark. En: Remmele W (Hrsg.) Pathologie. Bd 1. Springer: Verlag. Berlin 1984; 6: 435-52. [ Links ]
17.Schaefer HE. How to fix, decalcify and stain paraffin embedded bone marrow biopsies. Cytology and histology of the normal human bone marrow. En: Lennert K, Hübner eds. Pathologie of the bone marrow. Fischer: Stuttghart 1984; 33-53. [ Links ]
18.Schaefer HE. Zytologische Hämatopathologie unter besonderer Berücksichtigung histochemischer Methoden. Basel: Karger. Beitr Onkol, 1990; 38: 196-260. [ Links ]
19.Jekel JF, Katz DL, Elmore JG. Epidemiology, Biostatistics, and Preventive Medicine. Segunda edición. WB Saunders Company. 2001. [ Links ]
20.Hulley SB and Cummings SR. Diseño de la Investigación Clínica. Reimpresión. Apéndice 13.E.1. 1997; 236. [ Links ]
21.Vives Corrons JL, Aguilar Bascompte JL. Manual de técnicas de laboratorio en hematología. 3° Edición. Masson SA. Barcelona. España. 2006. [ Links ]
22.Bain BJ. Routine und specialised techniques in the diagnosis of haematological neoplasms. J Clin Pathol 1995; 48: 501-8. [ Links ]
23.Thiele J. Introduction to bone marrow pathology. Slide seminar. En: the XIX Brazilian Congress of Pathology of the Brazilian Society of Pathology. Junio, 1993. [ Links ]
24.Brunning RD and McKenna RW. Tumors of the Bone Marrow. Atlas of Tumor Pathology. Juan Rosai Editor. New York; 1994. [ Links ]
25.Jaffee E, Harris N, Stein H and Vardiman J. Pathology and genetics of tumours of haematopoietic and lymphoid tissues. World Health Organization Classification of Tumours. WHO. OMS. Published by IARC Press, International Agency for Research on Cancer. 150 cours Albert Thomas, F-69008 Lyon, France; 2001. [ Links ]
26.Riede UN, Herbst EW und Schaefer HE. Hämatopoetisches und lymphatisches System. En: Allgemeine und Spezielle Pathologie. Georg Thieme Verlag. Stuttgart: Germany. 1995; 10: 526-86. [ Links ]
27.Young NS and Maciejewski J. The pathophysiology of acquired aplastic anemia. The New England Journal of Medicine 1997; 336 (19): 1365-72. [ Links ]
28.Naegeli O. Üeber rothes Knochenmark und Myeloblasten. Dtsch Med Wochenschr 1900; 26: 287-90. [ Links ]
29.Naegeli O. Blutkrankheiten und Blutdiagnostik. Berlin: Springer. 1923. [ Links ]
30.Juneja SK, Wolf MM and Cooper IA. Value of bilateral bone marrow biopsy specimens in non-Hodgkin´s lymphoma. J Clin Pathol 1990; 43: 630-32. [ Links ]
31.Pangalis GA, Roussou PA, Kittas C, Kokkinou S, Fessas P. B-Chronic Lymphocytic Leukaemia. Prognostic Implication of bone marrow histology in 120 Patients. Experience from a Single Hematology Unit.Cáncer 1987; 59:767-71. [ Links ]
32.Figueredo Thiel SJ. Diagnóstico anatomopatológico de las Leucemias a Células Peludas en el Paraguay. 2003. Mem. Inst. Investig. Cienc. Salud, [revista online] 2003. [Accesi 20 setiembre de 2007]; 2(1). Disponible en: http:www.iics.una.py/n/diagnostico anatomopatologico.pdf. [ Links ]
*Autor Correspondiente: Dra.Susy Figueredo Thiel, Sección de Hematopatología
Departamento de Patología, Instituto de Investigaciones en Ciencias de la Salud
Río de la Plata y Lagerenza-Asunción-Paraguay
Teléfono: (595) 21 422-069
Email: patologia@iics.una.py














