INTRODUCCIÓN
El síndrome de Edwards o síndrome de trisomía 18 es un trastorno cromosómico autosómico que se caracteriza por la presencia de un cromosoma 18 extra, completo, parcial o en mosaico. La prevalencia de esta trisomía en recién nacidos se calcula entre 1 en 6.000 a 1 en 8.000, siendo la segunda alteración cromosómica autosómica en frecuencia después de la trisomía 211.
Investigaciones recientes mostraron un aumento de la prevalencia general de trisomía 18 en los últimos 20 años debido al aumento de la edad materna2.
Las características clínicas del síndrome de trisomía 18 son: deficiencia de crecimiento prenatal, características craneofaciales específicas, microcefalia y otras anomalías menores, malformaciones importantes, y marcado retraso psicomotor y cognitivo del desarrollo3.
El retraso del crecimiento comienza en el período prenatal y continúa después del nacimiento, y la mayor parte del tiempo se asocia con problemas de alimentación que pueden requerir nutrición enteral3.
Las características craneofaciales típicas incluyen dolicocefalia, fisuras palpebrales cortas, micrognatia, anomalías externas de las orejas, y piel redundante en la parte posterior del cuello. Otros hallazgos clínicos característicos son el puño apretado con los dedos superiores dedo índice superponiendo el tercero y 5º dedo superponiendo el 4° que es particularmente distintiva, uñas pequeñas, pulgares subdesarrollados, esternón corto y pies de palo. La presencia de malformaciones importantes es común, y cualquier órgano y sistema puede verse afectado. Los defectos cardíacos estructurales ocurren en más del 90% de los bebés3.
En las últimas décadas los avances en medicina fetal y genética fueron exponenciales y actualmente se realiza el diagnóstico prenatal con precisión, lo que nos direcciona a un adecuado asesoramiento genético familiar, orientación de estudios diagnósticos específicos y control de las posibles complicaciones, pues presentan alto riesgo de pérdida fetal o mortinato4.
CASO CLÍNICO
Paciente de 36 años, primípara, con 28 semanas de gestación derivada para realización de ecografía fetal morfológica.
Se realiza la ecografía 2D,3D ,4D y color Doppler utilizando equipo General Electric, Voluson E 10 con transductor convexo y volumétrico.
Describimos los datos patológicos hallados en el feto, único, activo en posición cefálica.
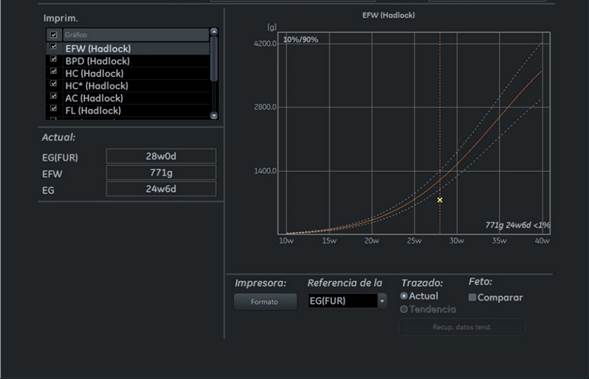
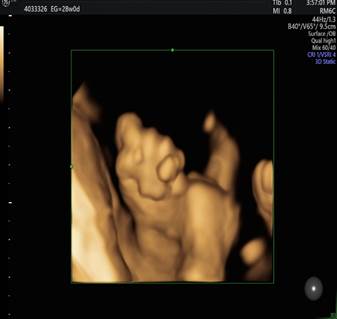
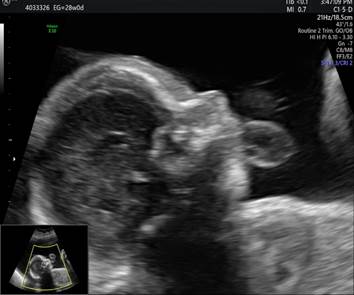
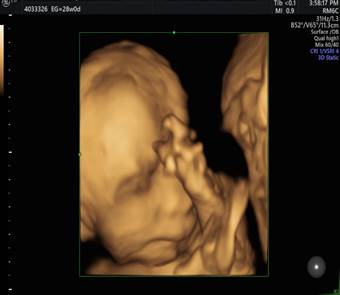
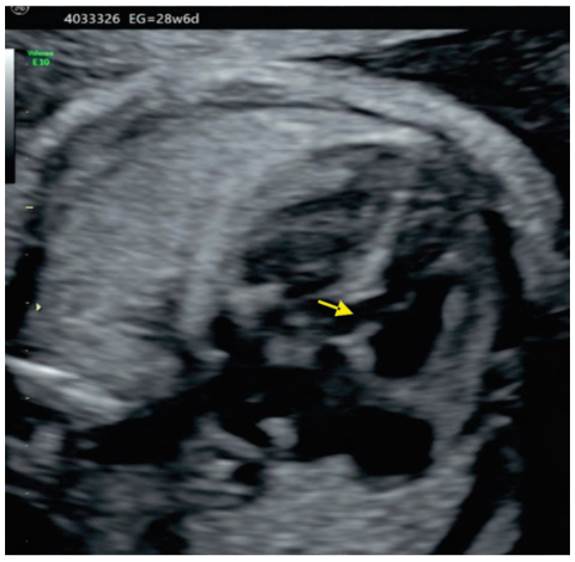
- Crecimiento en percentil inferior a 3 , curva a controlar. Peso 771 gramos. Líquido amniótico aumentado. -Rostro: maxilar inferior disminuido de tamaño. (micrognatia) - Tórax: asimetría en cavidades cardiacas y en corte de tres vasos aumento del diámetro del tronco pulmonar. - Vejiga: irregularidades en la pared vesical. - Cordón: edema de la gelatina de Wharthon - Miembros superiores: mano cerrada con dedos superpuestos. Figura 1, 2, 3, 4 y 5.
La ecocardiografía fetal: Frecuencia 162 latidos por minuto, ritmo regular, conducción1:1. Comunicación interventricular subaortica. Válvula pulmonar displásica engrosada con estenosis e insuficiencia importantes. Tronco pulmonar dilatado. Aumento de cavidades derechas. Figura 6 y 7.
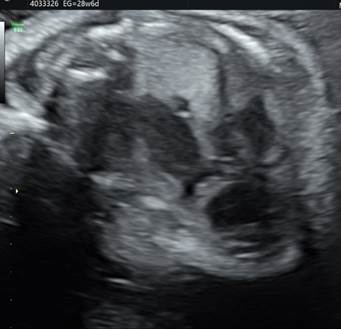
Figura 7 Imagen del tracto de salida del ventrículo derecho. Subaortica válvula pulmonar engrosada, tronco pulmonar dilatado.
Ante estos hallazgos se indica cordocentesis para la realización de estudio cromosómico.
- DATOS DE LA MUESTRA
- Muestra: Sangre de cordón umbilical en Heparina
- Motivo del Análisis: Cardiopatía, restricción del crecimiento,
polihidramnios, micrognatia, dedos superpuestos.
- TÉCNICA:
- Cultivo: Cultivo de la muestra en Karyomax medium
- Coloración: Conven. con Giemsa/Identifi. Bandeo G
- RESULTADO
- Número de células analizadas: 40
- Número de cromosomas: 47
- Fórmula Cromosómica: 47,XX,+18
- DIAGNÓSTICO: En todas las metafases analizadas, a partir de linfocitos
cultivados se ha obtenido una fórmula cromosómica
47,XX,+18, lo que corresponde a un cariotipo femenino
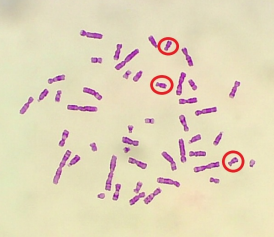
con trisomía del cromosoma 18. Se adjunta imagen de
una metafase señalando a los tres cromosomas 18. Figura 8
DISCUSIÓN
Se destaca la importancia del cribado ecográfico del primer trimestre y la realización de la ecografía obstétrica morfológica como marcador de sospecha de cromosomopatías, apuntar al diagnóstico temprano como conducta ideal, pero en este caso, la paciente recién fue referida a las 28 semanas de gestación, hecho que refleja nuestra realidad país, cuando el seguimiento prenatal se realiza en centros alejados de nuestra capital en detrimento de un diagnóstico precoz. Los hallazgos patológicos en la ecografía morfológica realizada condujeron a la realización de la ecocardiografía fetal y ambos estudios decisivos para aprobar y realizar la cordocentesis. El estudio cromosómico confirmo la sospecha de Trisomía 18.
En otros casos los marcadores séricos maternos motivan los estudios ecográficos especializados en el primer trimestre, se aclara que en este caso no fueron realizados 5,6.
Se suma la importancia de la implementación de servicios de asesoría genética con profesionales especializados para la conformación del equipo multidisciplinario y como herramienta fundamental para los padres7.
Cuando se realiza el diagnóstico prenatal o neonatal de trisomía 18, el asesoramiento de la familia debe ser realista, pero no desolado y no directivo. Los padres tienen que estar preparados tanto para la probabilidad de muerte como para la posibilidad de vivir4. Debido a que los padres tienen que tomar decisiones prácticas de acuerdo con sus valores respecto a la reanimación, cirugía y soporte vital, todas las opciones para el manejo del recién nacido deben explicarse, también debe responderse a la pregunta ineludible de la probabilidad de recurrencia8.
En el aspecto cardiovascular las diversas series muestran que entre el 80% y el 100% de los pacientes con trisomía 18 tienen defectos cardíacos estructurales congénitos9. La ecocardiografía fetal está indicada. Las anomalías cardíacas más comunes son las comunicaciones interventriculares e interauriculares, la persistencia del ductus arterioso5,9. La displasia marcada de la válvula pulmonar con doble lesión estenosis e insuficiencia con marcada dilatación del tronco pulmonar y ambas ramas como se observa en este feto es poco frecuente, debiendo realizarse el diagnóstico diferencial con la agenesia de la válvula pulmonar por lo que se enfatiza en la identificar la válvula pulmonar. La presencia de comunicación interventricular si es característica más frecuente el Síndrome de Edwards10.
La complejidad y la gravedad de la presentación clínica al nacer hacen que el manejo perinatal y neonatal de los bebés con trisomía 18 sea particularmente desafiante, controvertido y único entre múltiples síndromes de anomalía congénita. La comunicación temprana con el equipo de neonatología es fundamental para la conducta terapéutica, al respecto cabe mencionar que el consentimiento adquirido fue únicamente para la presentación de imágenes prenatales, enfatizado por los padres.
La necesidad de medicina fetal de calidad ya se encuentra incrementada, se cuenta con excelente capacidad diagnóstica y terapéutica, pero en nuestra sociedad interconectada con información globalizada el equipo multidisciplinario, obstetra, genetista, neonatólogo y especialistas pediátricos en diversas áreas tiene que conciliar respuestas al creciente nivel de exigencias según cada caso en particular.