INTRODUCCIÓN
Los toxocara canis y catis son helmintos del tipo áscaris, que parasitan el intestino delgado del perro y del gato respectivamente, que son sus huéspedes definitivos. Las hembras eliminan huevos en forma diaria, que en el suelo del ambiente tardan 3-4 semanas en desarrollarse al estado larvario infectante. Éstas, al ser ingeridas por una variedad de especies animales como el ser humano, nunca desarrollarán en su organismo el estadio adulto definitivo, por ser huéspedes intermediarios, también llamados huéspedes paratenicos1. El primer reporte sobre toxocaríasis fue en 1.952 por Beaver, en tres niños que presentaban alta eosinofilia y lesiones granulomatosas crónicas en el hígado e identificaron que las larvas encontradas en el órgano eran de toxocara canis, por lo que designaron a la novel enfermedad como “larva migrans visceral”. El ser humano se infecta al ingerir de forma accidental los huevos infectantes de toxocara, que contaminan frutas y verduras mal lavadas, carne o hígado no bien cocidos; en especial los niños, que tienen el hábito de practicar la onicofagia o la geofagia, y quienes viven en un ambiente contaminado debido a condiciones de pobreza socioeconómica2. Siendo una zoonosis extendida a nivel mundial, constituye una amenaza silenciosa, con gran impacto en la salud pública3. Se estima que millones de personas en Estados Unidos han sido expuestas al parásito toxocara, pero se desconoce cuántos de ellos se enfermaron luego de la infección4. La seroprevalencia de la infección oscila de 19% a 86%, según estudios realizados en diferentes países, siendo más afectados los niños que conviven con cachorros en su hogar y en estrecho contacto con el suelo contaminado; o que viven en condiciones sociales desfavorables5,6. La infección larvaria por toxocara es asintomática en la mayoría de los casos, o puede manifestarse como enfermedad, dando diversos cuadros clínicos como la larva migrans visceral (LMV), la larva migrans ocular (LMO)7 o menos frecuentemente afectando al SNC. La LMV se manifiesta con síntomas y signos diversos que dificultan y atrasan el diagnóstico, siendo el mismo necesario para un tratamiento adecuado. Los signos y síntomas clínicos principales son: afectación del estado general, pérdida de peso, palidez, hepatomegalia, en ocasiones adenomegalias y algunas manifestaciones atópicas como sibilancias, rash cutáneo, alergia alimentaria o artralgia, dolor abdominal recurrente, tos y fiebre; y en el hemograma la presencia de anemia ferropénica, eosinofilia e inmunoglobulinas específicas Ig G4 e Ig E anti-toxocaras8. La fiebre, por ser un síntoma poco destacable de la LMV, está escasamente considerada en la literatura, lo que motiva la presentación del presente caso clínico. Teniendo nuestro país una gran parte de su población viviendo en condiciones de pobreza, sin el saneamiento ambiental adecuado, contando muchos hogares con la presencia de perros mascotas; es necesario sospechar la posibilidad de toxocariasis si el hemograma realizado a un niño revela eosinofilia, aún en ausencia de síntomas, especialmente si ella es elevada, para hacer el estudio que lleve al diagnóstico correspondiente y el tratamiento adecuado.
CASO CLÍNICO
Paciente de 1 año 7 meses de edad, de sexo femenino, procedente de Capiatá, con historia de fiebre intermitente de 2 semanas de evolución. La paciente presentó varios picos febriles al día, graduados, en ocasiones hasta 39ºC; acompañada de tos seca al inicio y luego catarral. Consultó a los 2 días del inicio del cuadro con facultativo, quién al realizarle un hemograma (29/09/18) y constatar leucocitosis: 20.500/mm3, N:45%; L:30%; M:4%; E:20% (eosinófilos absolutos 4.100/mm3); Hg:10.1 gr/dl y datos de ferropenia, indica tratamiento con Ceftriaxona e/v por 3 días, Claritromicina por 10 días y Dipirona. Ante la falta de respuesta a la medicación por persistencia de la fiebre, acude nuevamente al facultativo quién le realiza otro hemograma (09/10/18) con el siguiente resultado: Hg: 9,8 g/dl, GR: 3.790.000/mm3, plaquetas: 556.000/mm3; G.B:59.200/mm3, N:2%; L:4%; M:2%; E:92% (eosinófilos absolutos 54.280), por lo cual lo remite al HCIPS, ingresando a Sala de Lactantes el 10/10/18 con TA: 37º.8 C; peso: 9 kg(P3); talla 82 cm(P50); CC:47 cm(P50). Al examen físico llama la atención palidez cutáneo-mucosa y distención abdominal de difícil palpación, por la escasa colaboración de la paciente. En los antecedentes familiares no se obtuvieron datos de valor y como antecedentes personales dos internaciones previas por gastroenteritis. Condiciones de hábitat: vive en casa de material, con agua potable, no tiene mascotas en la casa, pero refiere contacto con perros de familiares. Ingresa con los diagnósticos de Síndrome febril prolongado, anemia y eosinofilia severa de etiología a determinar. Los análisis realizados el 10/10/18 revelaron: Hg: 8.4 g/dl; GR:3.500.000/mm3; GB:70.510/mm3; NS:12%; L:10%; M:3%; E:75% (eosinófilos absolutos 52.882) y hematimetría con datos de ferropenia; plaquetas: 580.000/mm3; GOT:147 UI/L; GPT:245 UI/L; creatinina, urea, electrolitos, orina, crasis sanguínea, pruebas de STORCH: todas con valores normales, y estudio coproparasitario negativo para vermes y protozoarios. El examen físico del día siguiente reveló hepatomegalia a 8 cm. del reborde costal y punta de bazo. Ante esos datos se reinterroga a los padres, quienes reconocen que la niña tenía el hábito de la geofagia. Con esos antecedentes y la elevada eosinofilia, se sospechó clínicamente la posibilidad de larva migrans visceral (toxocaríasis) por lo cual se inició tratamiento con Albendazol 15 mg/kg/día, al tercer día del ingreso; solicitándose IgE, cuyo valor fue mayor a 2.000 UI/ml, e IgG anti-toxocaras, por la técnica de inmunoabsorciòn de ELISA, que fue positiva. La ecografía abdominal reveló: Hepatomegalia con formaciones micronodulares distribuidas en gran parte del hígado, adenopatías de diverso tamaño en el hilio hepático, esplenomegalia leve con formaciones micronodulares. La paciente continuó con picos de fiebre de 38 a 39ºC, cediendo la misma al cuarto día de internación y al segundo día de iniciada la medicación con Albendazol. Nuevos estudios laboratoriales: GPT: 181 UI/ml; GOT: 120 UI/ml; Proteinograma: proteínas totales 8.1 g/dl; albúmina: 3.8 g/dl; globulinas: 4.3 g/dl, relación A/G 0.9; el proteinograma electroforético reveló hipergammaglobulinemia: proteína total 8.20 g/dl alb. 3.15 g/dl (3.70-4.83); gamaglobulina 2.48 g/dl (0.84-1.36). La Radiografía de tórax demostró discreta infiltración intersticial y el estudio de fondo de ojo fue normal. Fue dada de alta el 18/10/19, al 8º día de internación, con un peso de 9.450 grs. con los diagnósticos de: Larva migrans visceral por toxocaríasis, anemia microcítica hipocrómica moderada y desnutrición calórico-proteica moderada; con indicación de ferroterapia con sulfato ferroso a 3 mg/kg/día, polivitamínico y de repetir el tratamiento con Albendazol 10 días más. El hemograma realizado al alta reveló GR: 3.470.000/mm3; Hg: 8.2 g/dl, hematimetría con datos de ferropenia; G.B: 65.790/mm3; NS: 4%; L: 10%; M: 2%; E: 84% (eosinófilos absolutos 55.263/mm3). En el control del 02/11/18 el hígado se había reducido de tamaño a 5 cm del RCD y el hemograma indicó Hg: 9.3 g/dl; G.R: 3.860.000/mm3; G.B: 36.770/mm3; NS:20%; L:18%; M:4%; E: 58% (eosinófilos absolutos 21.323). En la ecografía abdominal persistía la hepatomegalia con imágenes micronodulares, por lo cual se indicó nuevo plan de tratamiento con Albendazol por 5 días más; y en su último control del 15/11/18 el hemograma reveló: Hg: 9.9 g/dl; G.R: 3.920.000/mm3; G.B: 23.000/ mm3; NS:25%; L:32%; M:4%; E:39% (eosinófilos absolutos 8.970/mm3). Hepatomegalia a 3.5 cm del RCD y a la ecografía reducción del número de imágenes micronodulares. La paciente no acudió a controles posteriores programados.
DISCUSIÓN
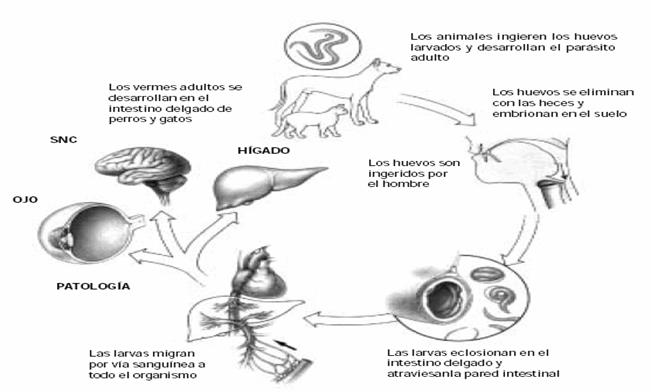
El toxocara canis y el toxocara catis son helmintos áscaris, midiendo los adultos machos de 4 a 10 cms y las hembras 6.5 a 18 cms. de longitud. Parasitan el intestino delgado de perros y gatos respectivamente, que son sus huéspedes definitivos, desde donde las hembras eliminan con las heces más de 200.000 huevos al día, los cuales son esparcidos al suelo del ambiente, sin ser aún infectivos. En este medio tardan 3-6 semanas en llegar al estado embrionado. En este momento adquieren el potencial riesgo de infectar, si son ingeridos accidentalmente por una variedad de huéspedes intermediarios o paratenicos, como aves caseras, ratones, ratas, cerdos, primates y los seres humanos9. El suelo contaminado no es la única fuente de infección; también ocurre por la ingestión de hígado de huéspedes paratenicos parasitados o de verduras contaminadas por aguas de regadío no tratadas. Una vez ingeridos los huevos embrionados eclosionan en el duodeno del huésped paratenico, liberando las larvas que no llegarán al estado adulto al no completar su ciclo de maduración. Estas penetran la mucosa del duodeno e inician el ciclo de la migración larvaria, llegando al hígado a través de la circulación portal y por el sistema venoso de la cava inferior a los pulmones. Los órganos más afectados son el hígado, los pulmones, los ojos, los ganglios, el SNC y el corazón. Al ser detenidas las larvas en esos tejidos se rodean de un granuloma formado por eosinófilos, macrófagos, histiocitos y fibras colágenas. La infección con el parásito produce la activación de la respuesta inmunitaria de tipo mixta, donde el tipo TH1 da una hipersensibilidad retardada, que justifica la formación de granulomas hepáticos; una respuesta polarizada de TH2 CD4+, con la producción de las citosinas L5 y GM-CSF, elevando la producción de eosinófilos y de la L4 que estimula a los linfocitos B, promoviendo el aumento de IgE específica, mediada por moléculas HLA clase II. Las células fagocíticas abundan y las larvas atrapadas en los granulomas eosinofílicos pueden degenerar y calcificarse10, ocurriendo a veces formación de abscesos hepáticos secundarios en los granulomas, más frecuentemente en el lóbulo derecho, generalmente causados por estafilococos áureos11. La larva libera diariamente a la sangre aproximadamente 2ng/día de glicoproteínas antigénicas excretoras-secretoras, que generan anticuerpos específicos de tipo IgG4 e IgE y otras glicoproteínas antigénicas de tipo alergénicas, que son responsables de las reacciones atópicas que presentan muchos pacientes12. La toxocariasis es una zoonosis extendida mundialmente, afectando al ser humano a diferentes edades, principalmente a los niños, en su mayoría pobres, de países del área tropical o subtropical13 y de las áreas rurales de países industrializados14. En una revisión sistemática de 250 estudios de 71 países, desde 1980 hasta 2019, mediante metaanálisis, la tasa global de toxocaríasis fue de 19%, siendo la prevalencia más alta en África con 37.7% y la más baja en el mediterráneo oriental con 8.2%. La seroprevalencia combinada para otras regiones de la OMS fue de 34.1% en el sudeste asiático; 24.2% en el Pacífico Occidental; 22.8% en estadounidenses y 10.5% en regiones europeas15. El ser humano adulto y en particular los niños de 1 a 4 años están más expuestos a contraer la infección al exponerse al suelo de un medio ambiente muy contaminado y en particular si conviven con perros, especialmente cachorros, que se parasitan por vía transplacentaria en el 98% de los casos; siendo capaces a las 3 semanas del nacimiento de albergar en su intestino delgado vermes adultos y por tanto de eliminar huevos infectantes16; también cuando hay pocas normas de higiene personal, constituyendo la toxocaríasis una amenaza silenciosa con un impacto progresivo en la salud pública1. La toxocariasis, en su mayor parte, es una infección silente, asintomática, benigna y autolimitada, y por tanto de no fácil diagnóstico. Deja anticuerpos específicos residuales12, o puede manifestarse como enfermedad, adoptando la forma de larva migrans visceral (LMV), larva migrans ocular (LMO) o afectando al SNC en la forma de neurotoxocarìasis (ver figura 1) y más raramente al corazón como miocarditis, pericarditis o endocarditis de Löeffler17. Canese, et al., en una investigación realizada encontraron la presencia de 53% de huevos de toxocara canis en muestras de arena tomadas de las 51 plazas y parques de Asunción, concluyendo que dichos lugares se constituyen en elevado riesgo para la salud de las personas y en especial para los niños que concurren a las mismas18 y en una investigación posterior demostraron una seroprevalencia de 78% de toxocariasis en niños de un medio rural de Piribebuy y en un área suburbana de Itauguá, siendo más frecuente la forma asintomática en 74%19. La infección por toxocariasis en distintas poblaciones varía muy ampliamente con seroprevalencias del 9.5% al 86.7% 20-23. La sospecha de toxocariasis es orientada por una eosinofilia elevada persistente, que se confirma con el hallazgo de anticuerpos subclase Ig G4 secreción-excreción específico TES (Toxocara excretory-secretory)24; pero en los países subdesarrollados es muy común la existencia de infecciones por otros helmintos, las que pueden dar reacciones cruzadas del TES nativo, teniendo por tanto menor especificidad. Esto motivó el desarrollo de TES con tres antígenos recombinantes TES-26, TES-30USM y TES-120, que tienen sensibilidad y especificidad de 100% en el diagnóstico de toxocariasis25. La eosinofilia puede deberse a diversas otras etiologías y ser de causa primaria o secundaria, que es la más frecuente. Se considera eosinofilia el aumento del recuento absoluto de eosinófilos (RAE) en sangre periférica mayor a 500/mm3 y clasificada como leve con valores de 500-1500/mm3; moderada de 1.500-5.000/mm3 y severa mayor a 5.000/mm3; pudiendo ser transitoria, episódica o persistente26. Los eosinófilos tienen una toxicidad directa a través de la liberación de varias moléculas presentes en sus gránulos citoplasmáticos, como la proteína básica mayor, la peroxidasa eosinofílica, la proteína catiónica eosinofílica27, que activadas juegan un papel importante durante la invasión parasitaria, en especial la proteína catiónica eosinofílica (ECP), con marcada actividad proinflamatoria contra bacterias y parásitos28. Entre las múltiples causas de eosinofilia los parásitos helmintos son una causa importante, pero corresponde a la toxocariasis las cifras más elevadas cuando son comparadas con parásitos intestinales sean helmintos nematodes, cestodes o trematodes29,30. La toxocaríasis se asoció con tos crónica en 32% de los casos31, así también se encontró una asociación significativa entre el asma y toxocariasis32 y con formas graves de asma33, hecho que sin embargo no fue comprobado en otros estudios34,35. En el Hospital Juan P. Garraham, sobre 301 pacientes con diagnóstico de toxocaríasis encontraron 31,5 % con formas oculares, afectando las mismas a un solo ojo, diagnóstico que en los niños pequeños tiende a hacerse en forma tardía debido ya que los mismos difícilmente manifiesten una disminución de la visión, motivando la consulta el estrabismo en 34%36. En la larva migrans ocular no es frecuente el hallazgo de anticuerpos específicos para toxocaras, siendo el diagnóstico por el estudio del fondo de ojo37. Puede también afectar al SNC (neurotoxocarìasis) en forma de meningitis, meningoencefalitis o de mielitis transversa, destacándose eosinofilia tanto en sangre como en el LCR y anticuerpos Ig G para toxocara tanto en el LCR como en sangre periférica 38-40. La eosinofilia persistente puede ser la única manifestación de la toxocariasis41,42. Nuestra paciente tuvo la particularidad de haber iniciado el cuadro de LMV como un síndrome febril, acompañado al inicio de tos catarral persistente, lo que motivó el tratamiento con antibióticos como si fuese una neumonía y sin haberse tenido en cuenta la eosinofilia del 20 % (RAE de 4.100/mm3) que ya presentaba en ese momento. Ante la falta de respuesta a la antibioticoterapia y debido a la persistencia de la fiebre de más de dos semanas de evolución, con empeoramiento del estado general y el descenso de la hemoglobina de 10.1 grs/dl a 9.8 grs/dl, fue internada con los diagnósticos de: síndrome febril prolongado, anemia ferropénica y eosinofilia severa de causa a determinar. El hemograma al ingreso reveló severa eosinofilia de 75% y RAE de 52.882/mm3, hemoglobina de 8.4 grs/dl. El interrogatorio dirigido, donde resaltó el antecedente de la convivencia con perro y el hábito de geofagia, llevó la sospecha de LMV; por lo cual se inició el tratamiento con Albendazol antes de tener estudio confirmatorio, con buena respuesta a la segunda dosis con el cese de la fiebre que había mantenido por más de 20 días. Los estudios posteriores confirmaron el diagnóstico de LMV.
En la literatura revisada la fiebre no es un síntoma destacable de la LMV y cuando ocurre la misma suele ser de corta duración, aunque se ha descrito un caso de un mes de duración en un adulto de 76 años43, mientras en el presente caso la misma fue prolongada con una duración de 20 días. La fiebre cedió en forma rápida con la medicación antiparasitaria, lo que hace presumir a la LMV como causante de la misma. La eosinofilia en general persiste por largo tiempo luego del tratamiento, como lo demuestra el presente caso, lo que es muy común en la LMV44, normalizándose aún en aquellos casos asintomáticos no tratados en un período de 3-5 meses45. Luego del tratamiento la resolución de los granulomas eosinofílicos del hígado ocurre en una mediana de 4 meses46. En este paciente, luego de un mes del alta aún persistían los micronódulos hepáticos al igual que la eosinofilia, pero con una tendencia a la disminución progresiva. En el monitoreo de la toxocariasis, cuando se dispone de la ECP, sus valores elevados en sangre constituyen, con la eosinofilia, un marcador importante de actividad de la infección, mientras los valores de la ECP y la IgE sirven para monitoreo del tratamiento de la infección, ya que ambos disminuyen luego de 6 meses47.
En el tratamiento de la LMV se han usado el Thiabendazol o el Albendazol, siendo más eficaz el Albendazol a 15 mg/kg/día, dividida en dos dosis diarias por 5 días, esquema que puede ser repetido según la evolución48. En las formas oculares LMO al tratamiento con Albendazol se asocia el uso de corticoides orales como la metilpredisona 1 mg/kg/día38,49. Debido al riesgo de la forma ocular que puede desarrollarse en cualquier etapa de la infección, parece justificado implementar tratamiento a todos los niños infectados con toxocara7,50.