GUÍA DE MANEJO DE LA GASTROENTERITIS AGUDA/ENFERMEDAD DIARREICA AGUDA
Definición
Se define generalmente como una disminución de la consistencia de las heces y / o un aumento en la frecuencia de las evacuaciones (típicamente >3 veces en 24 hs.), con o sin fiebre o vómitos. Un cambio en la consistencia de las heces en comparación a las habituales anteriormente, es más indicativo de la diarrea que el número de heces, en particular en los primeros meses de vida. La diarrea aguda suele durar <7 días y no >14 días y los vómitos de 2 a 3 días. (Diarrea prolongada >7 y <14 días; Diarrea crónica >14 días).1,2,3
En los niños con gastroenteritis aguda (GEA), la aparición de diarrea es ya aparente desde el cambio repentino de la consistencia de las deposiciones a evacuaciones sueltas o acuosas. A menudo se asocia a un aumento de la frecuencia, pero esto puede no ser evidente en el momento de la presentación. Presentación, por lo que un cambio repentino de la consistencia (suelta o acuosa) y/o vómitos, ya pueden hacer sospechar un cuadro de gastroenteritis.1,3
Epidemiología
Las enfermedades diarreicas agudas representan una de las primeras causas de morbilidad y mortalidad en niños menores de 5 años de edad. Es un problema de salud pública prioritario en sitios con deficiencia en el saneamiento ambiental. En todo el mundo se producen unos 1 700 millones de casos de enfermedades diarreicas y 760 000 niños menores de cinco años fallecen cada año.1,2,4
Etiología
El 75 -90 % de las diarreas son de causa viral: el rotavirus (agente más frecuente), norovirus4, astrovirus y adenovirus. El 10 a 20% son causadas por agentes bacterianos: Escherichia colienterotoxigénica (ECET), Campylobacterspp., Shigellaspp; E. coli O157:H7, E. coli, enterohemorrágica (ECEH), E. coli productora de la toxina Shiga (ECTS), E. coli productora de verotoxina, Salmonella entérica en sus diferentes serotipos, las intoxicaciones estafilocócicas o por Clostridiumperfringens y un 5% por Giardialamblia o Cryptoporidium.1,2,5
Si la diarrea persiste más allá de cinco a siete días, se deben replantear tres condiciones diferentes: la infección persistente, intolerancia a los alimentos o enfermedades gastrointestinales crónicas, en los que la diarrea puede ser el síntoma de presentación.
Clínica
La GEA puede estar acompañada de inapetencia, dolor abdominal tipo cólico, distensión abdominal, náuseas, tenesmo rectal, entre otros síntomas. Dependiendo de la causa, puede tener fiebre o deposiciones con sangre. Los vómitos y síntomas respiratorios se asociarían con una etiología vírica, sin embargo una fiebre alta (> 40 °C), sangre en las heces, dolor abdominal, y la afectación del sistema nervioso central (estado general) sugeriría un patógeno bacteriano, aunque esta regla no siempre se cumple, por ello la evaluación del paciente en particular es fundamental.1,4,5
El estado de hidratación es muy importante en el niño con diarrea aguda, por lo que se recurre a signos y síntomas clínicos que reflejen de forma indirecta la cantidad de líquidos perdidos. Estas manifestaciones se han utilizado para crear diversas escalas de clasificación de la gravedad de la deshidratación. Otra forma de objetivar la hidratación es mediante la estimación del porcentaje de pérdida de peso, lo cual se obtiene restando el peso en el momento de la valoración inicial del niño del peso antes del inicio de la diarrea. Sin embargo, en la práctica real, en la mayoría de los casos se desconoce el peso del niño, previo a la instalación del cuadro diarreico.1,5
En etapas tempranas de la deshidratación puede que no haya signos clínicos o puede presentarse solamente aumento de la sed. A medida que la deshidratación progresa, la pérdida de líquidos se puede manifestar por incremento de la sed, irritabilidad, disminución en la turgencia de la piel, ojos hundidos, fontanela deprimida (en el lactante < 18 meses) y ausencia de lágrimas. En la deshidratación grave, estos signos y síntomas serán más evidentes o se presentarán con choque hipovolémico, alteración del estado de conciencia, disminución del gasto urinario y del flujo sanguíneo, alterando la perfusión periférica, que pueden conducir a la muerte si no se corrigen adecuadamente.1,3,5,6
Sin embargo no hay un signo clínico único que permita establecer de manera fiable la presencia o la severidad de la deshidratación, y la combinación de varios hallazgos mejora la capacidad diagnóstica.1,3,5
Escalas para evaluar el estado de deshidratación
Para un adecuado diagnóstico del grado de deshidratación se requiere no uno, sino varios hallazgos clínicos, que en combinación ofrecen mayor certeza diagnóstica. Dentro de estos se hará énfasis en el estado de conciencia, ojos hundidos o no, la presencia de lágrimas y la hidratación de las mucosas. También puede considerarse el llenado capilar y el patrón respiratorio, aunque son datos clínicos más tardíos. Estos parámetros ayudan a evaluar el cuadro clínico y autores como Goldman, Friedman y Parkin, las clasifica en: sin deshidratación, deshidratación leve; deshidratación moderada o grave9 (ver Tabla 1). Sin embargo, debe corroborarse su aplicabilidad en centros de atención en Latinoamérica antes de poder generalizar su recomendación.3,5
Tabla 1 Escala Clínica de la deshidratación por gastroenteritis en niños
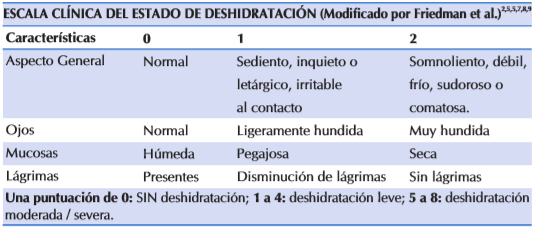
Goldman RD, Friedman JN, Parkin PC. Validation of the clinical dehydration scale for children with acute gastroenteritis. 2008 Sep;122(3):545-9.
Criterios de gravedad y necesidad de hospitalización
No existen criterios estrictos de admisión establecidos para la GEA, según la escala de Gorelick se establece puntajes para clasificar la gravedad en leve, moderada y grave10 (ver Tabla 2). De esta manera las recomendaciones para iniciar tratamiento hospitalario comprenden:3,5
- Choque.
- Deshidratación grave (> 9% del peso corporal).
- Alteraciones neurológicas (letargo, crisis convulsivas, etc.).
- Vómitos persistentes o biliares.
- Problemas sociales que impidan el manejo adecuado en el domicilio.
- Fracaso del tratamiento con SRO.
- Sospecha de proceso quirúrgico
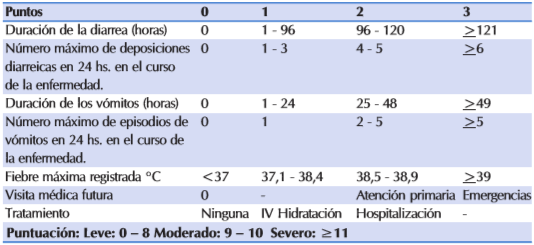
Escala de severidad - Vesikari modificado
Los puntajes de gravedad proporcionan una visión general del cuadro clínico e incluyen el estado de deshidratación y otros parámetros, es que se puede apreciar en la Tabla 3. La evidencia limitada pero sólida apoya su uso. El puntaje se correlaciona significativamente con el grado de deshidratación y la hospitalización del paciente. 3,11,12
Sin embargo, existe aún una falta de consenso sobre cómo definir la gravedad en los estudios basados en la comunidad, sobre la diarrea infantil en los países de bajos y medianos ingresos.13,14
Estudios de Laboratorio
El análisis de sangre o de heces para determinar la etiología viral o bacteriana no está recomendado de forma sistemática.4,8,13
La única medición de laboratorio que parece ser útil para disminuir la probabilidad de >5% de deshidratación es el bicarbonato sérico (bicarbonato sérico normal) (III, C) (recomendaciones débiles, la evidencia de baja calidad).1,3,5,13
Los electrolitos deben ser medidos en los entornos hospitalarios en los niños moderadamente deshidratados, niños con estado grave o shock.(Recomendación fuerte, evidencia de baja calidad)y en todos los niños al inicio y durante la terapiafluídicaendovenosa, porque una hiper o hiponatremia alterarán la velocidad con la cual se administrará los fluidos (fuerte recomendación, evidencia de baja calidad).5,6,7
Manejo de la Gastroenteritis Aguda - Consideraciones especiales
El manejo en esencia, se basa en tres puntos fundamentales: 1) proporcionar rehidratación rápida con solución hipoosmolar por vía oral; 2) asegurar principios de re-alimentación, alentar la alimentación temprana y la lactancia materna según la edad del paciente; 3) evaluar el uso de agentes que son eficaces en la reducción de la intensidad y duración de los síntomas. Los fármacos anti-infecciosos pueden ser considerados en circunstancias específicas (inmunocompromiso u otros) o en los niños en situación de riesgo de infección bacteriana.1,5
Sin embargo, en algunos casos, la diarrea de comienzo aguda puede durar de tres a siete díass. Aunque la diarrea crónica se define como una duración de al menos 14 días, diarrea prolongada de más de siete días es preocupante para los padres y requiere atención médica.
Esquema de rehidratación
La rehidratación oral debería usarse como terapia de primera línea en el manejo de los niños con GEA de leve a moderada:1
No se puede asegurar que la rehidratación enteral sea más efectiva en acortar la duración de la diarrea o en promover el aumento de peso en comparación con la i.v., pero reduce la duración de la estancia hospitalaria.5,15,16
La rehidratación enteral se asocia a un número significativamente menor de efectos adversos en comparación con la terapia i.v. y con una menor estancia hospitalaria, y resulta efectiva en la mayoría de los niños (Grado de evidencia moderada).1,3,5,17,18
Cuando la rehidratación oral no es posible, la rehidratación enteral por vía nasogástrica es efectiva y presenta menos complicaciones que la rehidratación i.v.1,3,7,17
El régimen de hidratación rápida por sonda nasogástrica (40-50 mL/kg durante 3-6 hs.) y el estándar (24 hs) son similares en efectividad.1,3,5,7
Debemos asumir aproximadamente 8 ml / kg para el volumen perdido por un vómito o una diarrea.
La administración de líquidos intravenoso se realizan en los siguientes casos (Recomendación fuerte, evidencia de baja calidad):5,7
- Choque
- La deshidratación con alteración del nivel de conciencia o acidosis grave
- Empeoramiento de la deshidratación o falta de mejoría a pesar de la terapia de rehidratación oral o enteral
- Vómitos persistentes a pesar de la administración de líquidos adecuada por vía oral o a través de una sonda nasogástrica
- Distensión abdominal severa e íleo
El suero de rehidratación oral (SRO) con osmolaridad reducida debe usarse como terapia de primera línea para el tratamiento de niños con GEA. La misma con 60-74 mEq/l de sodio son superiores a los SRO con 75-84 mEq/l de sodio para el tratamiento de los niños con GEA.1,5,19
Incluso en niños con GEA secundaria a infección por V. cholerae, los SRO de osmolaridad reducida son más efectivas al disminuir la necesidad de infusiones i.v. no programadas, el gasto fecal y los episodios de vómito, sin producir o condicionar hiponatremia.1,2,5,7
Se debe considerar una alternativa segura y efectiva la administración de SRO con < 75 mEq/l de sodio adicionadas con zinc para el tratamiento de los menores de 5 años con GEA.1
Las SRO basadas en arroz pueden usarse como terapia alternativa a la SRO basadas en glucosa, especialmente en niños con diarrea por V. cholerae, ya que parecen reducir el gasto fecal y la duración de la diarrea. Se requieren más estudios que comparen SRO-OR con SRO poliméricas.1,5,20
Existen diversos estudios experimentales y en niños con GEA que establecen las SRO adicionadas con polifenolesfitobiológicos como alternativas prometedoras para el tratamiento de la GEA dado su efecto microbiológico adicional.1,5
No existe hasta el momento evidencia suficiente de adecuada calidad que permita recomendar la utilización de SRO adicionadas con otros sustratos como miel o tanato de gelatina para el tratamiento integral de los niños con GEA.5
La alimentación normal para un tratamiento óptimo de los niños con GEA de leve a moderada, debería continuarse sin dejar pasar más de 4-6 h desde el inicio de la rehidratación.(1,5
El protocolo nutricional de los niños con GEA es un aspecto fundamental en el tratamiento y es particularmente relevante en niños con malnutrición.1,5
La alimentación precoz y la continuación con la dieta habitual parecen reportar beneficios dado el efecto trófico que ejerce los nutrientes. (realimentación temprana: antes de las 12 hs y realimentación tardía: después de las 12 hs en niños menores de 5 años).1,5,2,21
La alimentación temprana contribuye a disminuir el riesgo de que aumente la permeabilidad intestinal por la infección, evitando el paso de macromoléculas y sus consecuencias clínicas como la intolerancia a proteínas. También contribuye a mantener la actividad de las disacaridasas y disminuye la hipotrofia intestinal morfológica asociado al reposo intestinal. Todas las guías recientes establecen que la lactancia debería continuarse durante la rehidratación y debería pautarse una dieta apropiada para la edad del niño que debería iniciarse durante o después de la rehidratación inicial (4-6 h).(21,22,23
Las fórmulas sin lactosa pueden disminuir la duración de la diarrea en comparación con las fórmulas con lactosa. Se recomienda una evaluación cuidadosa de coste-beneficio antes de decidir la administración de este tipo de alternativas alimentarias.1,5
Las intervenciones nutricionales, incluyendo las modificaciones de la alimentación - tales como la dilución, libre de lactosa o fórmulas libres de proteína de leche de vaca, no se recomienda en recién nacidos sanos.5
Una recomendación establecida por la OMS y la reciente evidencia y las recomendaciones de las directrices ESPGHAN / ESPID, indican que los pacientes con diarrea que persiste por más de siete días o los hospitalizados por AGE grave pueden beneficiarse de la dieta con formula sin lactosa para reducir la duración de la diarrea.
RACECADROTILO
El racecadrotilo reduce la duración de la diarrea, la tasa de gasto fecal a las 48 h y el número de evacuaciones, con un perfil de seguridad similar al de los pacientes tratados con placebo, y se considera un fármaco costo-efectivo. Evidencia B. Puede ser considerado un coadyuvante eficaz en el tratamiento de la GEA en menores de 5 años, además de ser una alternativa segura y costo-efectiva.5,7,24,25,26,27,28,29,30
ZINC
El zinc puede reducir la duración de la diarrea y la disminuye la diarrea a los 7 días, con relevancia a nivel clínico, (grado de evidencia moderada - alta) por lo que los suplementos de zinc (en dosis bajas) están recomendados por Unicef y la Organización Mundial de la Salud (OMS) como coadyuvantes en el tratamiento para la diarrea aguda en niños > 6 meses en países en desarrollo y se observa un mayor efecto en niños con malnutrición o deficitarios de zinc. Los niños bien nutridos de países con bajo riesgo de déficit de zinc no tienen beneficios y la gravedad de la diarrea tampoco parece estar relacionada con este efecto. En menores de 6 meses, se necesitan más estudios para justificar la suplementación de zinc, considerando el riesgo de vómito y un posible mayor riesgo que beneficio.5,31,32,33,34,35
DIOSMECTITA O ESMECTITA
La Esmectita puede ser considerada en el tratamiento de la GEA en niños, ya que ha demostrado disminuir la duración total de la diarrea y el gasto fecal. Evidencia B. Los resultados muestran que la esmectita disminuyó significativamente la cantidad de heces en niños con diarrea acuosa aguda, especialmente en aquellos que habían dado positivo en rotavirus.3,5,36,37,38,39).
ONDASENTRON
Considerando los múltiples beneficios de la administración de ondansetrón y la potencial reducción de los costos directos e indirectos asociados a la necesidad de hospitalización secundaria a la baja tolerancia de la vía oral en un porcentaje significativo de niños con GEA, se recomienda su utilización en aquellos casos donde los vómitos son la manifestación predominante. El uso de ondansetrón en determinados casos reduce el vómito, la necesidad de rehidratación i.v. y la hospitalización inmediata. El uso debe ser evaluado en paciente con factores de riesgo de arritmia3,5,40,41,42,43).
LOPERAMIDA
Aunque la loperamida parece disminuir la persistencia de la diarrea aguda en niños, no se recomienda su uso debido a que el riesgo de efectos adversos es mayor que los beneficios en este grupo.5,41).
VITAMINA A
No se recomienda el uso de vitamina A de forma sistemática para tratar la GEA en niños, pero podría considerarse para la prevención de determinados cuadros diarreicos con predominio de componente inflamatorio.5,44,45,46
PROBIOTICOS
Los probióticos utilizados conjuntamente con la terapia de rehidratación, parecen ser seguros y tener claros efectos beneficiosos en la reducción de la duración y la frecuencia en la diarrea infecciosa aguda.
Se identifica una equivalencia terapéutica para el uso coadyuvante con SRO. Los Probióticos con buen nivel de evidencia, evidencia B, fuerte recomendación son:
-Lactobacillus reuteri
- Lactobacillus GG, y
- Saccharomyces boulardii.
La evidencia demuestra que los mayores beneficios se obtienen con una sola cepa de microorganismos vivos. No está comprobada la eficacia administrando multicepas simultáneamente.3,5,7,47,48,49,50,51,52).
SIMBIOTICOS
No existe evidencia suficiente hasta el momento que permita recomendar de forma segura.5,53,54
MANEJO CLÍNICO
Escenario A
Manejo Ambulatorio: sin deshidratación con buena tolerancia.
- Paciente sin deshidratación (score de 0), sin criterios de gravedad, ni necesidad de hospitalización.
- Hidratación vía oral: SRO de osmolaridad reducida (60-74 mEq/l de sodio). Las SRO basadas en arroz pueden usarse como terapia alternativa.
- Dieta normal, alimentación habitual.
- Sospecha de etiología bacteriana: evaluar antibioticoterapia vía oral.
- Considerar: racecadrotilo, diosmectita, Zinc y probióticos( Lactobacillusreuteri,Lactobacilluscasei GG, y Saccharomycesboulardii).
Escenario B
Manejo de Urgencias:
B1: Paciente con deshidratación leve (score de 1 -4), sin criterios de gravedad: OBSERVACION EN URGENCIAS.
- SRO de osmolaridad reducida vía oral o SNG si el paciente presenta poca tolerancia a la vía oral.
- Ondasentrónvo/ev/im en pacientes sin tolerancia adecuada con vómitos después de iniciada la rehidratación oral, o pacientes con vómitos incoercibles ≥ 6 veces en 6 horas, vómitos recientes ≥ 1 en 1 hora, en DOSIS ÚNICA. (Evaluar en pacientes con factores de riesgo de arritmia)
- Realimentación rápida (no más de 4 a 6 horas posterior a la rehidratación oral)
- Considerar racecadrotilo, diosmectita, Zinc y probióticos( Lactobacillusreuteri ,Lactobacilluscasei GG, y Saccharomycesboulardii).
- Sospecha de etiología bacteriana: evaluar antibiótico terapia
- Mejoría de los síntomas y el score de hidratación 0: ALTA
B2: Paciente con deshidratación moderada (score de 5 - 8): Internación en Unidad de URGENCIAS no más de 12 hrs.
- SRO de osmolaridad reducida vía oral o SNG si el paciente presenta poca tolerancia a la vía oral o hidratación parenteral según el estado de deshidratación.
- Ondasentrónvo/ev/im en pacientes sin tolerancia adecuada después de iniciada la rehidratación oral o pacientes con vómitos o pacientes con vómitos ≥ 6 veces en 6 horas, vómitos recientes ≥ 1 en 1 hora, en DOSIS ÚNICA.
- Realimentación rápida (no más de 4 a 6 horas posterior a la rehidratación)
- Considerar racecadrotilo, diosmectita, Zinc y probióticos( Lactobacillusreuteri ,Lactobacilluscasei GG, y Saccharomycesboulardii).
- Sospecha de etiología bacteriana: evaluar antibióticoterapia.
- Evaluar métodos de diagnóstico: HMG, electrolitos, glicemia, urea, creatinina, coprocultivo, gasometría etc. según el cuadro del paciente.
- Mejoría de los síntomas y el score de hidratación 0: ALTA
B3: Paciente con criterios de gravedad (Shock): Internación en Unidad de URGENCIAS hasta 24 hrs.
Iniciar algoritmo de manejo de shock: manejo de la vía aérea, instalar accesos venosos o vía intraósea.
- Expansiones con Suero fisiológico a 20cc/kp las veces que sea necesaria para restaurarla presión de perfusión tisular. (El niño con shock hipovolémico que requiera más de 60 ml / kg de reanimación con líquidos debería generar preocupación por las pérdidas continuas o un diagnóstico alternativo como el shock séptico de origen enteral)55,56
- Evaluar inotrópicos una vez restaurada la volemia y si el paciente sigue con mala perfusión periférica.
- Restaurado el estado hemodinámico, descenso del aporte de fluidos y ajustar al estado de deshidratación del paciente.
- Sospecha de etiología bacteriana: evaluar antibióticoterapia.
- Realimentación rápida (no más de 4 a 6 horas posterior a la rehidratación), según el estado del paciente.
- Considerar racecadrotilo, diosmectita, Zinc y probióticos( Lactobacillusreuteri ,Lactobacilluscasei GG, y Saccharomycesboulardii).
- según tolerancia.
- Evaluar métodos de diagnóstico: HMG, electrolitos, glicemia, urea, creatinina, coprocultivo, gasometría etc. según el cuadro del paciente.
- Evaluar UCIP según estado clínico y respuesta al tratamiento.
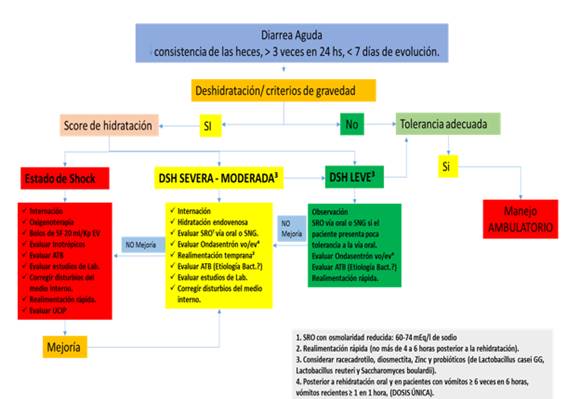
La Figura 1 desarrolla el algoritmo de la actuación en Urgencias de pediatría ante un cuadro de gastroenteritis aguda en niños. Este consenso aporta una sistematización que será fundamental para la atención correcta y óptima que brindará el pediatra en dicha situación.