INTRODUCCIÓN
El Staphylococcus aureus es una bacteria gram-positiva, comensal humana, considerada uno de los principales patógenos humanos. La gran prevalencia de infecciones causadas por esta bacteria, tanto en ambientes comunitarios como hospitalarios, se debe principalmente a la rápida adquisición de resistencia a antibióticos y a su capacidad para formar biofilm 1,2.
Estos biofilms se definen como comunidades o agregados celulares rodeados por una matriz extracelular, que poseen la capacidad de adherirse a numerosas superficies, y constituyen uno de los determinantes de la persistencia de infecciones crónicas por S. aureus, a pesar de una aparente adecuada terapia antibiótica y de la respuesta inmune del huésped 3,4.
La formación del biofilm empieza con la adhesión de una bacteria a una superficie y la posterior secreción de sustancias extracelulares poliméricas, que incluyen polisacáridos, ADN y proteínas, conformando una matriz que propicia la adhesión a otras células bacterianas, constituyendo así una barrera física y electrostática contra los agentes antimicrobianos y contra la respuesta inmune del huésped. Además, dado que el libre flujo se encuentra impedido por esta barrera, existe una carencia de nutrientes en las capas internas del biofilm, por lo que las células que se encuentran en ellas se inactivan metabólicamente, volviéndose menos susceptibles a la acción de los antibióticos; siendo éstas las encargadas de reactivar la infección luego del cese de la situaciones de estrés, como la terapia antibiótica o el ataque del sistema inmune 5,6.
Una de las principales dificultades en el tratamiento de estos biofilms está dada por la heterogeneidad de los mismos. Esto se debe principalmente a diferencias en la capacidad de producción de la adhesina intracelular polisacárida (PIA) por parte de las cepas de S. aureus, siendo el locus icaADBC esencial para su producción y secreción. Éste polisacárido era considerado el principal componente de la matriz extracelular; sin embargo, existen cepas que producen cantidades casi imperceptibles del mismo, por lo que la formación de biofilm ocurre por un mecanismo independiente del locus ica. Comúnmente la formación de biofilm por parte de cepas de S. aureus sensibles a meticilina involucra la producción de PIA, y en contrapartida, en cepas resistentes, la formación involucraría principalmente a ADN extracelular y a la expresión de proteínas de adhesión en la superficie celular 1,4,7,8.
En Paraguay son escasos los datos que hacen referencia a la capacidad de formación de biofilm por parte de cepas de S. aureus resistentes a meticilina causantes de infecciones en niños, por lo que el presente trabajo busca estandarizar un ensayo in vitro que permita la medición de la capacidad de formación de biofilm y su evaluación en cepas representativas de diversos clones circulantes en el país, aislados de población pediátrica.
MATERIALES Y MÉTODOS
El diseño del presente estudio fue de tipo observacional descriptivo de corte transverso, en el que se incluyeron cepas de S. aureus resistentes a meticilina que se encontraban criopreservadas en el biobanco del Instituto de Investigaciones en Ciencias de la Salud y que cumplían los siguientes criterios: ser viables, contar con datos clínicos y microbiológicos (identificación y antibiograma), y con caracterización molecular consistente en perfil de virulencia por detección de genes mecA, pvL, hlA, hlaB, sea, seb, sec, sed, seh, etA, etB y representativas de un grupo clonal específico mediante análisis de polimorfismo de la proteína A (spa typing) y el análisis del polimorfismo de secuencias repetitivas en tándem de número variable (MLVA). Se excluyeron aquellas cepas de S. aureus con una ficha clínica epidemiológica incompleta, o repetidas de un grupo clonal previamente representado, así como aquellas obtenidas a partir de hisopados y puntas de catéter para evitar interferencias debidas a fenómenos de colonización.
Las cepas analizadas en el presente estudio fueron recolectadas dentro de proyectos marco provenientes del área de Bacteriología Molecular del IICS en el año 2012, contando con aprobación del Comité de ética y comité científico del IICS, según código P29/2011, y con la aprobación del Comité de ética en la investigación de la Facultad de Ciencias Químicas de la Universidad Nacional de Asunción según código 372/17.
Cepas bacterianas
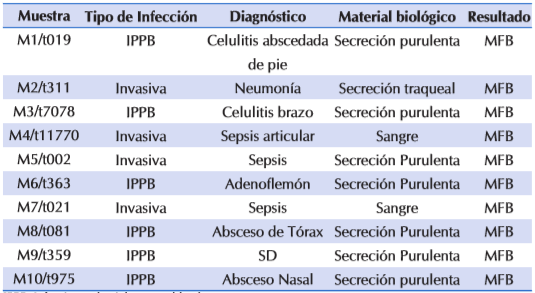
Del total de 347 cepas de SARM colectadas fueron agrupadas según sus perfiles genéticos, en cuanto al polimorfismo de la proteína A y el análisis multilocus de secuencias repetitivas en tándem de número variable (MLVA), en 10 grupos clonales diferentes y para el presente estudio fue escogido un clon representativo de cada perfil y que se identifican como: M1/t019, M2/t311, M3/t7078, M4/t11770, M5/t002, M6/t363, M7/t021, M8/t081, M9/t359, M10/t975.
Estas 10 cepas de SARM fueron obtenidas a partir de fluidos estériles, muestras de piel y tejidos blandos de niños que concurrieron al Hospital de Clínicas de San Lorenzo - FCM UNA, Hospital General Pediátrico Niños de Acosta Ñu, Hospital Nacional e Instituto de Previsión Social en el año 2012. Las mismas fueron consideradas como resistentes a meticilina según criterios del CLSI (Clinical and Laboratory Standars Institute).
La identificación de las cepas en cada centro hospitalario se realizó por métodos fenotípicos y fueron criopreservadas en BHI-Glicerol 15% a -80°C. La confirmación molecular de la identidad de las mismas se realizó por amplificación de los genes ARNr 16S, la cual fue desarrollada empleando oligonucleótidos y condiciones descritas por Manfredi et al 9.
Ensayo en placa para producción de biofilm
Las cepas de S. aureus fueron cultivadas en Agar de Soja Tríptica (TSA, Becton Dickison, USA) durante 24 horas, a 37°C. Se inocularon las colonias en 2 ml de Caldo Triptona Soja (TSB, Becton Dickison, USA) y se incubaron nuevamente por 24 horas, a 37°C. Luego se realizó una dilución 1:50 en medio TSB fresco, al cual se añadió 1% de Glucosa. Se tomaron alícuotas de 200 ul de la suspensión de cada aislado y se inocularon por triplicado en placas de poliestireno (Costar Cornig Incorporated, USA). Se incluyeron 3 pocillos con medio TBS con Glucosa como blanco. Las placas se incubaron a 37°C por 24 horas.
Luego de la incubación, el sobrenadante fue desechado y se realizaron dos lavados a cada pocillo con 200 uL de Buffer Fosfato Salino (PBS, Merck, Alemania). Para fijar las bacterias adheridas, se colocaron 200 uL de etanol al 95% (Cicarelli, Argentina) en cada pocillo, por una hora. Luego de la remoción del etanol, las placas se dejaron secar al aire durante 24 hs. La tinción se realizó con 100 uL de cristal violeta al 1% (Anedra, Argentina). Transcurridos 30 minutos, el colorante fue removido y se realizaron 3 lavados con agua destilada. Se dejó secar la placa por 2 horas y posteriormente fueron añadidos 100 uL de una solución 70:30 de etanol-acetona (Biopack, Argentina). Se realizó la lectura de la densidad óptica a 630 nm mediante un lector de ELISA (Awareness technology Inc, USA).
La formación de biofilm es un fenómeno variable en intensidad pudiendo ser más o menos resistentes o persitentes. El ensayo in vitro permite evaluar la intensidad de persistencia del biolfilm, mediante la aplicación de rangos diversos de absorbancia a partir de un punto de corte. La interpretación de los resultados requiere definir un punto de corte que separe a las bacterias no formadoras de biofilms de aquellas que sí lo son. En este estudio utilizamos la técnica estadística descrita por Stepanovic et al, 2000 para la interpretación de los resultados 10. Para este estudio se calculó la media de la densidad óptica (DO) de los controles y se midió la DO de cada cepa bacteriana individualmente.
El valor de corte por DO (DOc) se definió como el valor de la media del blanco más tres desviaciones estándar por encima de la misma. La intensidad de la formación de biofilm se clasificó en las siguientes categorías:
- No productoras de biofilm (DO ≤ DOc);
- Débiles productoras de biofilm (DOc < DO ≤ 2xDOc);
- Productoras moderadas de biofilm (2xDOc < DO ≤ 4xDOc);
- Fuerte productora de biofilm (4xDOc < DO) 11.
RESULTADOS
El 100% de las cepas testadas resultaron formadoras de biofilm, todas ellas clasificadas como productoras moderadas (Figura 1, Tabla 1).
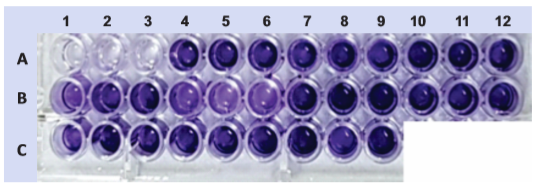
Figura 1 Ensayo in vitro para la detección de biofilm en placa de poliestireno. Todas las muestras se testaron por triplicado. Pocillos del 1A al 3A: Control negativo; 4A al 6A: M1/t019; 7A al 9A: M2/t311; 10A al 12A: M3/t7078; 1B al 3B: M4/t11770; 4B al 6B: M5/t002; 7B al 9B: M6/t363; 10B al 12B: M7/t021; 1C al 3C: M8/t081; 4C al 6C: M9/t359; 7C al 9C: M10/t975.
DISCUSIÓN
El presente trabajo muestra que el potencial de formación de biofilm está ampliamente distribuido entre diversos grupos clonales de cepas de S. aureus que infectaron a niños paraguayos en el año 2012, siendo independiente del tipo de cuadro clínico causado o incluso del perfil de virulencia propio de las cepas, que en muchos casos es muy variable. La capacidad de estas cepas de producir biofilm resulta un hecho alarmante, sobre todo al tratarse de cepas asociadas a infecciones en niños. La relevancia de la producción de biofilm radica sobre todo en la relación de éste a la adquisición de resistencia a antibióticos y a la persistencia de la infección 12.
La adquisición de resistencia a antibióticos asociada a la formación de biofilm puede constituir una de las causas de falla terapéutica. Esto debido a la administración al paciente de antimicrobianos a los cuales, en los ensayos fenotípicos, las bacterias no comprometidas con la formación de biofilm presentan susceptibilidad; desarrollándose la tolerancia a éstos sólo en el sitio de infección debido a la asociación celular para formar la biopelícula. La adquisición de resistencia a antimicrobianos puede darse a través de diversos mecanismos, uno de ellos es la barrera física que constituye la matriz de polisacáridos excretados, que dificulta la penetración de los mismos. Otra de las causas sería la creación de zonas ácidas y anóxicas como consecuencia de la actividad metabólica bacteriana, que pueden contribuir a la degradación de las moléculas de antibiótico 5.
Estos biofilm bacterianos son capaces además de eludir el sistema inmune que, en adición a su capacidad de generar tolerancia al tratamiento antibiótico y al hecho de que el mismo constituye un reservorio a partir del cual se puede dar la dispersión periódica de bacterias hacia otros tejidos, resulta en la persistencia de la infección. La evasión al sistema inmune se da por la incapacidad de las células inmunes fagocíticas y de los anticuerpos de acceder a las células bacterianas, debido a la matriz de polisacáridos, muchas veces empeorando el cuadro debido a la inflamación crónica ocasionada por el daño a los tejidos circundantes al biofilm 13.
En cuanto al tipo de infección asociada a las cepas, no se observaron diferencias en la intensidad de producción de biofilm entre las cepas asociadas a infecciones de piel y partes blandas e infecciones invasivas. Con respecto a este punto, se ha descrito la relevancia de los biofilms bacterianos en ciertos tipos de infección como las asociadas a implantes, osteomielitis, infección pulmonar en fibrosis cística y endocarditis 5.
Es interesante ver que no se han detectado cepas fuertes formadoras de biofilm, las que serían más persistentes en los diversos nichos en los que se desarrollen. Sin embargo, es importante tener en cuenta que, si bien la formación de biofilm de las cepas analizadas es moderada, la misma puede intensificarse en respuesta a distintos estímulos presentes en el medio ambiente. Por lo que es esencial en la práctica clínica mantener de forma estricta medidas de higiene que impidan el establecimiento de biofilms de S. aureus tanto en el ambiente hospitalario como en la comunidad.
Actualmente los esfuerzos están enfocados en mejorar la detección de la formación de biofilm, sobre todo a través de métodos no invasivos, y el desarrollo de estrategias que permitan la prevención y el tratamiento de infecciones asociadas a cepas formadoras de biofilm, así como en el monitoreo de la efectividad de los tratamientos instaurados. Para esto es fundamental tener en cuenta la gran variabilidad genética de las cepas, dado que de ello depende las características del biofilm formado 12,14.
El hecho de contar a nivel nacional con métodos que permitan evaluar la capacidad de formación de biofilm de cepas de S. aureus clínicamente importantes, es un paso inicial para el estudio a profundidad del impacto producido por estas cepas en cuanto a su capacidad de cronificar las infecciones y aumentar su gravedad, ya que de ello dependerá también la correcta elección de la terapia antimicrobiana.
CONCLUSIÓN
La totalidad de las cepas testadas en el estudio resultaron formadoras de biofilm. No se hallaron diferencias en intensidad de formación del biofilm entre cepas en cuanto al tipo de infección o al perfil genético de las mismas. Dada la relevancia del biofilm en las infecciones bacterianas, es importante la necesidad del desarrollo y mejoramiento de técnicas de detección, que permitan la instauración de una terapia efectiva de manera oportuna.