INTRODUCCIÓN
El dilema del oxígeno (O2) en la neonatología es sumamente interesante, pero a la vez frustrante, a pesar de su uso en forma generalizada en los recién nacido (RN) desde hace más de 80 años, aún no se conoce la dosis óptima para cada niño, ni para cada momento de su evolución, debido a que el O2 no sólo es un gas, sino es un fármaco, con sus indicaciones, dosis, efectos adversos y necesidades de monitorización1.
Con relación al descubrimiento del O2 y su uso en la medicina, se remontan a los avances en la física y la química de los siglos XVII y XVIII realizados por Robert Boyle y Robert Hooke quienes estudiaron los principios físicos del aire natural. Antoine Lavoisier acuñó el nombre "oxígeno" en 1777, definiéndolo como un "gas eminentemente respirable". Una publicación de 1891 se refiere al uso de O2 en prematuros que estaban debilitados, publicado por Étienne Tanier. Sin embargo, el empleo del O2 no se volvió sistemático hasta la mitad de 1920, después de que Haldane demostró que el dióxido de carbono (CO2) estimula el centro respiratorio, es así que se empezó a utilizar CO2 y O2 para tratar la depresión narcótica o asfixia pura. Para la mitad del decenio de 1940 se contó con tanques de O2 móviles que ayudaron a suministrar O2 en sala de parto2. A partir de 1950 se inicia la administración de O2, por mascarilla, tubo endotraqueal, oxigeno hiperbárico, cánula nasal, CPAP, ARM, etc.
El suplemento de O2 es un componente importante en las Unidades de Cuidados Intensivos Neonatales (UCIN). Se requiere una vigilancia cuidadosa para minimizar la toxicidad pulmonar o las consecuencias de la hipoxemia o de la hiperoxia. Las dos complicaciones principales de exceso de O2 son la lesión pulmonar y la retinopatía del prematuro3. La saturación de oxígeno (SpO2) óptima para los prematuros atendidos en UCIN aún es un tema que no tiene una respuesta clara. La administración de O2, su monitoreo y los niveles objetivos deseados para los RN, incluyendo los prematuros, serán revisados aquí4.
CONOCIENDO AL OXIGENO
El transporte de O2 a los tejidos, depende de la capacidad de la sangre para llevar O2 y de la velocidad del flujo sanguíneo.
La función celular normal depende de un suministro continuo de O2, el cual una vez inhalado se difunde a través de la membrana alveolocapilar y en la sangre capilar pulmonar. Este gradiente mantiene la tensión arterial de O2 (PaO2) y es en gran parte la fuerza motriz para el suministro de O2 a las células.
Como sabemos el O2 está contenido en la sangre en 2 formas:
Una pequeña cantidad disuelta en el plasma y
Una mayor cantidad unida a la hemoglobina (Hb).
El contenido total de O2 en la sangre es la suma de estas dos cantidades.
A la cantidad de O2 en sangre arterial, se le llama contenido de oxigeno (CaO2).
CaO2= (1,34 x Hb x SaO2) + (0,003 x PaO2).
Donde la Hb es la concentración de la hemoglobina y la SaO2 es la saturación de O2 arterial.
Con relación a la ecuación, la contribución de la Hb al contenido de O2 se describe en el primer segmento donde cada gramo de Hb se une a 1,34ml de O2 cuando está totalmente saturado. El segundo segmento de la ecuación describe la contribución del O2 disuelto en el plasma. La porción disuelta de O2 en la sangre está relacionado en forma lineal con la PO2. El contenido de O2 se incrementa 0,003mL/100ml de sangre por cada 1mm Hg de aumento de la PO2..
El O2 se une en forma reversible a la Hb, cada molécula de Hb puede unirse hasta 4 moléculas de O2, la porción del contenido de O2 unido a la Hb no es lineal con respecto a la PO2.
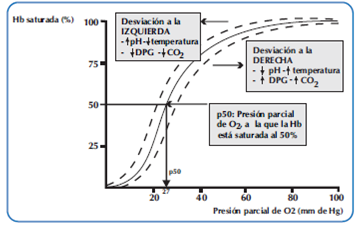
La relación entre la PO2 y la Hb es explicada por la Curva de disociación de la oxihemoglobina (Figura 1). Con una PaO2 por encima de 90 mmHg, la curva es casi plana, la Hb está casi completamente saturada y alcanzando lo máximo que puede unirse (100% de saturación), esto es importante porque una vez que la Hb está saturada los incrementos adicionales en la PO2 no aumentará el contenido de O2 unido, es decir la PaO2 puede seguir subiendo, pero la saturación no (no va pasar de 100%).
A valores más bajos de PO2, la curva cae abruptamente y promueve la liberación de O2 a los tejidos.
La afinidad por el O2, se refiere a la capacidad de la Hb para unirse o liberar O2, es modulada por el pH, CO2 (en parte independiente del pH), 2,3-difosfoglicerato (DPG), la temperatura y la Hb fetal (Figura 1). Es así que el pH bajo, la PCO2alta, el aumento de la temperatura, el aumento de 2,3-difosfoglicerato (DPG) y la proporción disminuida de la Hb fetal reducen la afinidad por el O2 (desplazamiento de la curva de disociación de la oxihemoglobina a la derecha) y en este caso se libera O2 a los tejidos.
Por el contario el pH alto, la PCO2 baja, la disminución de la temperatura, el mayor porcentaje de la Hb fetal y la reducción de 2,3-difosfoglicerato (DPG), incrementan la afinidad de la Hb por el O2 (desplazamiento de la curva de disociación de la oxihemoglobina hacia a la izquierda). Esto significa que puede alcanzar el mismo nivel de saturación con valores de PO2 bajos5.
Se sabe además que la tensión de O2 disminuye a medida que la sangre se aleja de los pulmones y el O2 es liberado de la Hb. Se define como p50 a la presión parcial de O2 necesaria para conseguir una saturación de la Hb del 50%y su valor suele rondar cerca de los 27 mmHg en la curva, punto donde se libera el 50% de oxigeno ligado a la hemoglobina.
Estos cambios en la afinidad promueven el consumo de O2 en los capilares pulmonares y su liberación a los tejidos. Es importante comprender la fisiología para entender los cambios continuos que se produce en los RN sanos y enfermos con el uso continuo del O26.
HIPOXIA E HIPOXEMIA
La hipoxia se produce cuando hay un aporte inadecuado de O2 a los tejidos, mientras que la hipoxemia se observa cuando hay un contenido arterial de O2 bajo, por lo tanto, no son sinónimos, pero frecuentemente ocurre en forma simultánea.
La Hipoxia por definición es un poco más compleja, debido a que la oxigenación tisular es un proceso complicado y multifactorial. Hipoxia significa insuficiente O2 en los tejidos para satisfacer las necesidades metabólicas y el consumo de O2 en un momento determinado, como sabemos puede haber hipoxia con normoxemia, con hipoxemia y aun con hiperoxemia7.
El OXIGENO Y EL ESTRES OXIDATIVO
En condiciones fisiológicas, una pequeña fracción del O2 consumido por las mitocondrias se convierte constantemente en aniones radicales superóxido, peróxido de hidrogeno, radicales de hidróxido y otras sustancias reactivas de O2 (ROS). En condiciones normales la mayor parte de esta molécula es metabolizada por los sistemas antioxidantes6. Sin embargo, el uso de O2 adicional es esencial para la sobrevida de los RN prematuros con falla respiratoria hipóxica y con un uso continuo, el O2 induce al estrés oxidativo, debido a la producción de radicales libres. El daño celular ocurre por superproducción de metabolitos citotóxicos o especies reactivas de O2, que dañan a los ácidos nucleicos, lípidos, proteínas y carbohidratos, llevando a una remodelación estructural como ocurre en el pulmón, alterando así su estructura8,9,10.
Sabemos que dos de las enfermedades producidas por el uso del O2 en los prematuros son la Retinopatía de la Prematurez (ROP) y la Displasia Broncopulmonar (DBP).
La ROP sigue siendo una causa principal de alteración en la visión y ceguera en niños en todo el mundo, la patogenia de la ROP aún no está clara debido a su complejidad; lo mismo es con la DBP que es una enfermedad con un amplio espectro de severidad y una causa importante de morbilidad en los prematuros, afecta a casi la mitad de los RN extremadamente prematuros (<28 semanas) que egresan de las UCIN6,7,8,9,10. Ambas patologías se encuentran relacionadas con los efectos tóxicos del O2.
MEDICIÓN DE LA OXIGENACIÓN
El O2 debe ser monitorizado en los RN que recibenO2 suplementario, para evitar episodios de hipoxemia e hiperoxia, y además evitar el uso de O2 suplementario excesivo e indiscriminado, que puede estar asociado con la mortalidad y los pobres resultados el desarrollo neurológico. El nivel de oxigenación se puede evaluar de varias maneras, por ejemplo la medición de laPaO2 mide la presión parcial de la pequeña cantidad de oxígeno que está disuelto en el plasma, y ha sido considerado como el "patrón oro" para la medición de la oxigenación, sin embargo, el muestreo intermitente de la sangre arterial (gasometría) puede no reflejar las fluctuaciones en la oxigenación que por lo general se presentan en los RN con enfermedad cardiopulmonar.
La otra forma de medir el oxígeno en la sangre es la oximetría de pulso (SpO2), la cual mide la saturación de la hemoglobina unida al O2 y refleja el 98% del contenido de O2 arterial. Esta técnica no invasiva de monitorización proporciona datos que son continuos y por lo la tanto, evita algunas limitaciones del muestreo de sangre arterial intermitente.
La SpO2 mide la saturación en la sangre, pero no mide la PaO2, la presión de dióxido (PCO2) o el pHh. Por lo tanto no sustituye a la gasometría para la valoración integral de los pacientes. Es preciso recalcar que cuando se mide un estado acido base o gas en sangre arterial, el valor de la saturación que se reporta no debe ser tenido en cuenta para el cuidado clínico. Esto se debe a que este valor de saturación es un valor calculado, y dicho cálculo se basa en valores normales de temperatura, concentración de Hb de adulto, pH y PaCO2 de un adulto sano, muy diferente a los de un RN y más aún en el RN enfermo7.
En la mayoría de las Unidades de Cuidados Intensivos Neonatales (UCIN), la oximetría de pulso es el estándar aceptado para la vigilancia habitual y a la SpO2 se le ha llamado el "quinto signo vital"11.Es importante determinar el rango de SpO2 con la oximetría de pulso que satisface adecuadamente las demandas metabólicas del neonato, el valor de oximetría de pulso normal en los RN a término sanos el promedio es de alrededor 97% en el aire ambiente12,13) y alrededor de 95% en los recién nacidos prematuros sanos14.
Los intentos para mantener SpO2 con valores superiores a 95 % con el uso de oxígeno suplementario puede resultar un exceso de exposición al oxígeno y lleva a la hiperoxia.
Actualmente son varios los modelos de saturometros existentes, sin embargo, en los últimos años la tecnología ha mejorado, numerosos trabajos han demostrado la mayor especificidad, sensibilidad y menor margen de error de los monitores fabricados con la llamada tecnología de extracción de señal SET15,16,17) (Masimo(r), Irvine, Ca), la medición de la saturación no se ve afectados por la luz ni por los movimientos que realiza el paciente y además mide el estado de mala perfusión. En nuestro centro lo utilizamos desde hace 5 años y realmente es muy confiable.
OXIGENACIÓN ADECUADA
El O2 es un elemento necesario para la vida, su uso muchas veces termina siendo iatrogénico ya que muchos de los RN son expuestos a la hiperoxia18, cual es la saturación de oxígeno (SpO2) óptima para el tratamiento de RN, ésta aún no ha podido ser determinada. Sin embargo, numerosos y estudios clínicos randomizados, meta-análisis y comentarios publicados recientemente han añadido información valiosa y han permitido el discernimiento19, sobretodo de lo que debería evitarse durante la oxigenoterapia.
Tanto el trabajo publicado por el grupo de Dr. Sola y col3, como el meta-análisis de la Dra. Saugstad OD19,realizaron una revisión bastante exhaustiva sobre el tema, ambos basados en estudios clínicos aleatorizado (ECA) la metodología que mejor evalúa los efectos de la intervención, seleccionados debido a que ellos comparan los resultados de una intención de tratamiento con un rango de SpO2 de 85-89% vs otro con SpO291-95% en niños menores de 28 semanas de gestación. Dichos estudios son US SUPPORT Study Group of the Eunice Kennedy Shriver NICHD Neonatal Research Network (SUPPORT - Estados Unidos), the Benefits of Oxygen Saturation Targeting (BOOST II) trial (llevado a cabo en el Reino Unido, Australia y Nueva Zelanda) y el Canadian Oxygen Trial (COT - Canadá)20,21,22,23,24. En todos los estudios, los oxímetros de pulso utilizados fueron el Masimo con extracción de señal (SET). Para que el estudio sea 'enmascarado' estos monitores fueron modificados para mostrar niveles de SpO2 3% superiores o inferiores a los valores verdaderos de la SpO2 verdadera entre 84-96%, con un 'retorno' gradual o abrupto al valor verdadero que estuviera fuera de este rango. Los clínicos y enfermeros, 'cegados' al monitor asignado al azar y utilizado en el RN a su cargo, 'buscaban' SpO2 de 88-92%, para que luego los investigadores pudieran comparar los RN con intención de tratamiento SpO2 85%-89% (saturación "baja") con los asignados a 91%-95% de SpO2 (saturación "alta").
Las variables de resultado primario fueron similares entre todos los estudios, y consistían en evaluar la tasa de mortalidad o discapacidad a los 18 o 24 meses. El estudio SUPPORT dividió esas variables en resultados a corto plazo (ROP grave, muerte antes del alta del hospital o ambos) y a largo plazo (muerte antes de la evaluación entre 18 a 22 meses o trastornos en el neurodesarrollo a los 18 a 22 meses de edad corregida).
Los dos grupos de infantes, aquéllos expuestos saturación "baja" vs los expuestos a saturación "alta" fueron asignados aleatoriamente y analizados en forma separada.
Tasa de Mortalidad y Baja Saturación de Oxígeno
Tanto el SUPPORT como el BOOST II 'combinado' encontraron una asociación entre un rango de SpO2 "bajo" (85-89%) y una tasa de mortalidad más alta. En el caso de SUPPORT, notaron esto al momento del alta hospitalaria: mayor mortalidad en niños con SpO2 85-89% vs niños con SpO2 91-95% (19.9% vs 16.2%; p=0.045). Por otro lado, BOOST II 'combinado', paró de reclutar bebés cuando un análisis interino del estudio demostró una mayor tasa de mortalidad a las 36 semanas en niños expuestos a saturación "baja": 23.1% de mortalidad en SpO2 85-89% vs 15.9% en SpO2 91-95%, con un riesgo relativo de 1.45 (intervalo de confianza 95%: 1.151.84), p=0.002. En cambio, el estudio COT no ha encontrado diferencias en tasa mortalidad entre los dos grupos, y tampoco lo encontró el BOOST neozelandés.
Tasa de Retinopatía del Prematuro y Alta Saturación de Oxígeno
Tanto SUPPORT como BOOST II encontraron una asociación entre una intención de tratamiento de SpO2 alto (91-95%) y una tasa más alta de ROP severa. Una vez más, el estudio COT difiere con esta asociación.
Las diferencias en los resultados de estos estudios pueden ser atribuidos a diferencias en el diseño, la implementación y el manejo de los datos3,19,25.
Sobre la base de los conocimientos actuales, debemos tratar de evitar tanto la hipoxemia como la hiperoxemia en la práctica clínica diaria. En general, los valores de PaO2 de 50 a 80 mmHg son adecuados para satisfacer las demandas metabólicas y limitar la necesidad de altas concentraciones de oxígeno suplementario que podrían causar daño pulmonar.
¿CUÁL ES SpO2 ADECUADA?
Como sabemos no se conoce SpO2 óptima para cada RN Prematuro. Para la práctica clínica, con el estado actual de los conocimientos, se recomienda una SpO2 entre 86-88% como límite inferior 94% como límite superior. Una práctica que impresiona segura es mantener la alarma siempre operativa y fijadas en 85% en la mínima y 95% en la máxima, cuando se usa el mismo monitor que el utilizado en los ECA3,19,20,21,22,23,24,25,26,27 28).
COMO ADMINISTRAR EL OXIGENO
Los dispositivos para administrar el oxígeno incluyen, cánula nasal, mascara nasal, halo cefálico, Presión Positiva en la Vía Área (CPAP), por tubo endotraqueal, Asistencia Respiratoria Mecánica (ARM).
La cánula nasal de bajo flujo (<2 Litros/min), es uno de las formas más frecuentes de administrarO2 en el periodo neonatal, en baja concentración a través de un dispositivo cuya parte distal se conecta a un fluxómetro y la parte proximal a una cánula nasal con dos "piezas nasales" siliconadas. Es prioritario elegir la cánula de tamaño adecuado, realizar una buena fijación, humidificar, calentar el O2 y medir FiO2.
La concentración de O2 inspirado es una mezcla del aire ambiente (que ingresa por la nariz y la boca) y el O2 suministrado. Cuando se administra O2 por cánula nasal se desconoce la cantidad real de la concentración O2 que recibe el RN, el otro problema que presenta, si uno administra oxigeno frio, está seca las vías aéreas superiores lesionando la mucosa nasal29.
La cánula de alto flujo (> de 2 Litro/min y hasta 6 litros/min) se define como aquella que aporta un flujo de gas por encima del flujo inspiratorio del recién nacido a través de una cánula nasal (son más cortas y binasal), la humidificación y el calentamiento son imprescindible en esta modalidad de terapia. El sistema de alto flujo genera presiones variables en la orofaringe, la presión que se genera depende si la boca está abierta o cerrada y de la cantidad de oxigeno que se fuga por las cánulas nasales. Se puede administrar Fio2 elevadas, la terapia de alto flujo afecta la eliminación de C02, esto depende del flujo y de las fugas, con menor fuga mayor eliminación de CO2, mejora el trabajo respiratorio, disminuye la frecuencia respiratoria. Si bien produce cierto grado de presión positiva en las vías aéreas, no se debe de considerar como un CPAP, ni remplazar al CPAP. Esto se debe a que la relación flujo-presión no es lineal, algunos autores han observado que la presión de distención generada por el sistema de alto flujo de hasta 8 Litros/min no eran superiores a los producidos por 6 cmH2O de CPAP, incluso son menores30).
Se recomienda comenzar con flujo bajo e incrementar lentamente hasta conseguir el efecto deseado, comenzar con 1-1,5 Litros/min y según los requerimientos aumentar el flujo hasta 6 Litros/min.
Los dos sistemas de alto flujo aprobados y de mayor utilización son el de Vapotherm(r) (Stevensville, MD) y el Fischer & Paykel Haelhcare(r) (Irvine, CA. RT329). Ambos sistemas proporcionan flujos variables, calientes (37ºC) y humidificados (100%)31,32.
La revisión del Cochrane33 sobre el uso de la cánula de alto flujo, concluye que tiene tasas similares de eficacia a otras formas de asistencias respiratorias no invasivas en los RN prematuros para la prevención del fracaso del tratamiento, la muerte y la DBP.
Halo Cefálico: Son dispositivo de plástico duro transparente de distinto tamaño que cubren la cabeza del niño. Se debe ubicar la cabeza del RN dentro del halo y mantener libre el espacio entre el cuello y el halo, para permitir la salida de CO2. Cuando uno necesita concentra una mayor cantidad de O2(Fio2) se puede recurrir al halo cefálico hasta el 100%, oxigeno siempre calentado y humidificado, el flujo entre 3-5 litros por minuto suele ser suficiente con halo a abierto y 4 a 8 Litros/min con halo cerrado, recordar que a mayor flujo de oxígeno, mayor es el ruido lo cual puede ser muy molestos para el recién nacido. Se utiliza en aquellos RN que respiran espontáneamente que requieren FiO2≤ 60%, con dificultad respiratoria mínima a moderada con PaCO2 y pH dentro de los valores considerados normales34,35. En nuestra unidad se usa cada vez menos.
Presión Positiva Continua en la Vía Aérea (CPAP): En los RN que requieren asistencia respiratoria adicional, como los RN prematuros con síndrome de dificultad respiratoria (SDR) o apnea, el CPAP es una alternativa a la intubación endotraqueal y la ventilación mecánica36. El RN respira de forma espontánea y se entrega la presión por vía nasal, el CPAP óptimo es la presión positiva que permite mayor entrega de oxígeno a los tejidos.
La administración de la mezcla de gas para producir la Presión Positiva Continua en el sistema se puede realizar mediante un flujo de gas continuo o variable, el CPAP puede ser a burbujas, se puede usar un respirador, pero siempre por vía nasal y el paciente respirando en forma espontánea. Unos de los elementos más importantes utilizados son las interfaces (Prongs), siendo las más usadas y recomendadas las cánulas binasales corta, se utiliza además las mascarillas nasales y con menos frecuencias las cánulas nasofaríngeas binasales37.
En nuestro centro, iniciamos CPAP con un nivel de presión de 5 cm H2O, luego aumentamos progresivamente hasta 8 cmH2O,según sea necesario, flujo de 5 a 8 Litros/min, FiO2 hasta 60% manteniendo un buen intercambio de gases pH> 7,25 y PaCO2 < 60 mmHg y una saturación aceptable entre 88 y 94%.
Debemos de tener en cuenta que los cuidados de enfermerías son fundamentales para el éxito y el mantenimiento del CPAP, creemos que el CPAP ha mejorado la sobrevida de los recién nacidos pretérmino en nuestro centro en los últimos años.
Ventilación con Presión Positiva Intermitente Nasal (VNPPI):
La ventilación nasal con presión positiva intermitente, es una modalidad sencilla, eficaz, de asistencia respiratoria para niños mayores y adultos. Se ha utilizado para tratar la apnea frecuentes o graves en los niños prematuros, los informes de casos de perforaciones gastrointestinales ha limitado su uso generalizado, parece reducir la frecuencia de apneas de manera más eficaz que el CPAP, se necesita más datos acerca de la seguridad y eficacia antes de recomendar la VNPPI como tratamiento estándar en las apneas38.
El USO DE OXIGENO EN LA SALA DE PARTO.
La Academia American de Pediatría (AAP) y la Asociación American del Corazón (AHA) recomienda lo siguiente con relación al uso de O2 en la reanimación39.
La reanimación de los recién nacidos de más de 35 semanas de gestación se comienza con 21% de oxigeno (aire ambiental).
La reanimación de recién nacido de menos de 35 semanas se comienza con 21-30% de oxígeno.
Si el recién nacido está recibiendo oxigeno pero la saturación de oxígeno (SpO2) no está dentro del rango esperado, se puede dar oxígeno, usando un mezclador, ajustar la concentración de oxígeno para conseguir que la saturación de oxigeno (SpO2) este dentro del rango esperado.
Si el recién nacido continua con dificultad respiratoria y no puede mantener SpO2a pesar de dar 100% de oxígeno a flujo libre, se debe considerar el uso del CPAP.
COMENTARIO FINAL
Como vemos el O2 es uno de los tratamientos más empleados en las salas de neonatología como parte del soporte respiratorio, los recién nacidos han recibido más O2 que cualquier otro producto médico en los últimos sesenta años. A pesar de esto seguimos con algunas interrogantes como cuál es la mejor SPO2, 88%-94% o 90%-95% en los prematuros4,40.
Sin embargo está bien establecidas las condiciones que debemos tener aquellos que cuidamos a los recién nacidos para administrar el O2 de manera minimizar la toxicidad del O2 que incluyen:
A. Mezclar con aire (usar blender).
B. Calentar.
C. Humidificar.
D. Medir la FiO2.
E. Usar Saturometro adecuado.
Es imperativo que en nuestro país en aquellos hospitales públicos y privados donde se tratan recién nacidos que requieran O2 como parte de su tratamiento, lo deben de recibir en forma correcta y apropiada. El personal médico y de enfermería debe estar bien entrenado para lograr el uso del O2 en los neonatos, en forma segura y eficaz en la práctica clínica.