Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Pediatría (Asunción)
versão On-line ISSN 1683-9803
Pediatr. (Asunción) v.38 n.2 Asunción ago. 2011
ARTÍCULO ORIGINAL
Valor de Referencia de la Hormona Estimulante de la Tiroides (TSH) por Fluoroinmunoensayo en Neonatos del Paraguay
The Reference Value of Thyroid Stimulating Hormone (TSH) Determined by Fluoroimmunoassay in Paraguayan Newborns
Adriana Valenzuela, Marta Ascurra , Margarita Cabral, Fabiola Blanco, Stella Rodríguez, Idalina Dalles (1)
1. Programa de Prevención de la Fibrosis Quística y del Retardo Mental. Ministerio de Salud Pública y Bienestar Social. Asunción- Paraguay.
Correspondencia: Dra. Marta Ascurra. Centro de Salud Nº 9 Calle: Herminio Giménez c/ Gral. Aguiar. Asunción-Paraguay. E-mail: mascurra@sce.cnc.una.py
Recibido: 11/05/2011, aceptado para publicación: 30/06/2011.
RESUMEN
El término de valores de referencia es un concepto ampliamente aceptado y aplicado internacionalmente y puede ser expresado como el establecimiento y uso de datos relevantes para la interpretación de observaciones médicas. La hormona estimulante de la tiroides (TSH), juega un papel determinante en la detección temprana de una de las pocas causas prevenibles de retardo mental, el hipotiroidismo congénito. Los valores de referencia utilizados en el PPFQRM han sido establecidos según la recomendación del valor dado por la prueba comercial utilizada (<9 Normal, 9-18 borderline, >18µU/ml hipotiroidismo), en muestras de sangre en papel de filtro de recién nacidos entre 2 a 6 días de vida. Se realizó un estudio observacional de corte transverso con 20.168 muestras de sangre seca de recién nacidos de 1 a 7 días de vida a término, para determinar el valor de referencia de la TSH de la población de RN en el Paraguay, utilizándose las medidas de tendencia central y de dispersión: media, mediana, percentiles y la distribución de frecuencias a fin de caracterizar a la variable de interés. El 22% de las muestras presentó valores de TSH entre 0.01-1.0, 25% entre 1.1-2, 19% entre 2.1-3.0, 12% entre 3.1-4, 8% entre 4.1-5 y 14% mayor a 5 µU/ml. Se encontraron los siguientes valores de TSH; media: 2.74, mediana: 2.22, moda: 0.01 y el desvió estándar: 2.14 µU/ml. Para el percentil 75: 3.26, el 95: 6.68 y el percentil 99: 9 µU/ml. En base a estas observaciones se confirma como punto de corte un valor de TSH igual a 10 µU/ml.
Palabras claves: Hipotiroidismo congénito, Valores de Referencia, TSH neonatal.
ABSTRACT
The term “reference values" is widely accepted and applied internationally and can be expressed as the establishment and use of data relevant to the interpretation of medical observations. Thyroid stimulating hormone (TSH) plays a role in early detection of one of the few preventable causes of mental retardation, congenital hypothyroidism. The reference values used in the program for prevention of cystic fibrosis and mental retardation (PPFQRM) were those recommended by the commercial test used (<9 Normal, 9-18 borderline, >18 μU/mL hypothyroidism) using filter paper with blood samples from newborns at 2-6 days of life. We performed a cross-sectional, observational study with 20,168 dried blood samples from full-term newborns at 1-7 days of life to determine the reference value for TSH in the NB population of Paraguay using the measures of central tendency and dispersion: mean, median, percentiles, and frequency distribution in order to describe the variable under study. A TSH of between 0.01--1.0 µU/ml was found in 22% of samples, 1.1—2 µU/ml in 25% of samples, from 2.1--3.0 µU/ml in 19%, between 3.1—4 µU/ml in 12%, from 4.1—5 µU/ml in 8%, and more than 5 µU/ml in 14%. TSH values found were: mean: 2.74, median: 2.22, mode: 0.01, and standard deviation was 2.14 µU/ml. For the 75th percentile: 3.26 µU/ml; 95th: 6.68 µU/ml; and 99th: 9 µU/ml. Based on these observations a cutoff point for TSH was confirmed equivalent to 10 µU/ml.
Keywords: Congenital hypothyroidism, reference values, newborn, thyroid stimulating hormone.
INTRODUCCIÓN
La hormona estimulante de la tiroides (TSH, por sus siglas en inglés) proveniente de la hipófisis, regula la secreción de las hormonas tiroxina (T4) y triyodotironina (T3), las cuales tienen un papel determinante en el proceso del crecimiento inicial y del desarrollo de la mayoría de los órganos, especialmente del cerebro. La ausencia de estas hormonas en el recién nacido (RN), trae como consecuencia la aparición de un cuadro clínico conocido como hipotiroidismo congénito (HC), siendo el déficit del desarrollo intelectual una de las alteraciones más importantes. La detección temprana del HC en el RN puede ser realizada a través del estudio de todas las hormonas tiroideas o solo del análisis de la TSH, siendo por tanto una de las pocas causas de retardo mental prevenible, a través de su diagnostico y tratamiento precoz. El déficit mental es proporcional al tiempo que persiste la falta de hormonas, se ha observado que en el 75% de los individuos afectados, el Coeficiente Intelectual (CI) es de más del 90% cuando el tratamiento es precoz, antes de las 6 semanas de vida, mientras que el CI solo alcanza al 36% cuando este se inicia entre las siete y doce semanas (1).
Debido a que los recién nacidos afectados son asintomáticos y solo un 5% de ellos pueden llegar a presentar algún síntoma clínico de la patología al nacimiento, los programas de detección o screening neonatal se han constituido en el único medio eficaz para alcanzar la detección precoz del HC y su consecuente tratamiento oportuno. Garantizar que se puedan diferenciar los RN sanos de los verdaderamente hipotiroideos depende en gran medida de la utilización de valores de referencia apropiados para cada población (2-3).
El término de valores de referencia es un concepto ampliamente aceptado y aplicado internacionalmente y puede ser expresado como el establecimiento y uso de datos relevantes para la interpretación de observaciones médicas. El punto de corte, constituye el valor de referencia por encima del cual la muestra es considerada positiva y el recién nacido podría estar afectado por un HC, lo cual no seria problema si la distribución de frecuencia de los valores de la TSH para la población normal fuese completamente diferente de la poblacion de hipotiroideos. La realidad es que existen RN normales con valores límites que pueden estar ligeramente elevados y RN hipotiroideos con valores no tan elevados, es decir la distribucion de los valores de la TSH se solapan o traslapan, con la presentación de falsos resultados, que afectan la validez del analisis. A su vez en el caso de la TSH, este valor límite o punto de corte puede verse afectado por factores como la edad al momento de la toma de muestra, la etnia, así como por el consumo de iodo por la madre. Es por ello que para una correcta interpretación de los resultados se recomienda que este sea representativo de la población objeto de estudio (4-6).
En Paraguay la detección neonatal se halla a cargo del Programa de Prevención de la Fibrosis Quística y Prevención del Retardo Mental, producido por el Hipotiroidismo congénito y la Fenilcetonuria (PPFQRM), creado por la Ley No. 2.138/03, que establece la obligatoriedad del estudio a todos los recién nacidos del país, antes de los siete días de vida. Hasta la elaboración de este estudio los valores de referencia utilizados en el PPFQRM han sido establecidos según la recomendación del valor dado por la prueba comercial utilizada (<9 Normal, 9-18 borderline, >18µU/ml hipotiroidismo), de muestras de sangre entera recogida en papel de filtro de RN entre 2 a 6 días de vida. Siendo el objetivo de este trabajo el de determinar los valores de referencia de la TSH de la poblacion de recien nacidos en el Paraguay, utilizando el método de fluoroinmunoensayo a tiempo resuelto, de muestras de sangre entera recogida en papel de filtro provenientes de neonatos a término, entre 1 a 7 días de vida, recolectadas durante el año 2009.
MATERIALES Y MÉTODOS
De las 40.095 muestras que ingresaron al PPFQRM durante el año 2009, fueron seleccionadas 20.168 muestras de sangre seca que cumplieron los criterios de inclusión, de recién nacidos de entre 1 a 7 días de vida, a término, provenientes de las 18 Regiones Sanitarias en las que el Ministerio de Salud divide al país. A fin de llevar a cabo un estudio observacional descriptivo de corte transverso, para determinar en ellas la concentración de la TSH por fluoroinmunoensayo a tiempo resuelto AutoDELPHIA (Perkin Elmer Life Science, Turku, Finland) en fase sólida por una técnica sándwich directa donde dos anticuerpos monoclonales de ratón son contrapuestos a dos determinantes antigénicos de la molécula de TSH, siguiendo la metodología recomendada por el fabricante.
Para los análisis estadísticos, se utilizaron las media, mediana, percentiles y la distribución de frecuencias a fin de caracterizar a la variable de interés.
RESULTADOS
Las edades de los RN estudiados según días de vida se encontró: 1 día: 11%, 2 días: 27%, 3 días: 14%, 4 días: 8%, 5 días: 9%, 6 días: 11% y 7 días: 20%.
El 22% de las muestras presentó valores de TSH entre 0.01-1.0, el 25% entre 1.1-2, el 19% entre 2.1-3.0, el 12% entre 3.1-4, el 8% entre 4.1-5 y el 14% mayor a 5 µU/ml (Figura 1).
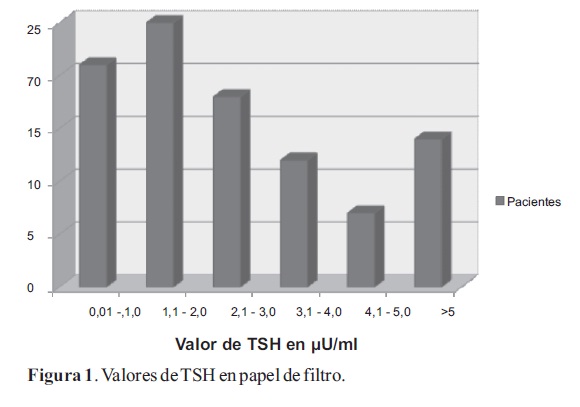
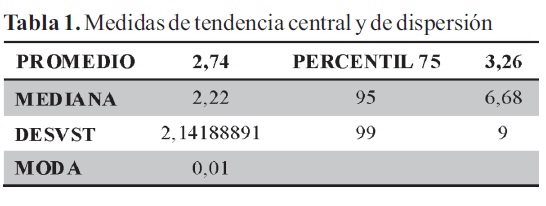
Se encontraron los siguientes valores de TSH; media: 2.74, mediana: 2.22, moda: 0.01 y el desvio estandar: 2.14 µU/ml. Para el percentil 75: 3.26, el 95: 6.68 y el percentil 99: 9 µU/ml (Tabla 1).
En base a estas observaciones se confirma como punto de corte un valor de TSH igual a 10 µU/ml (Figura 2).

DISCUSIÓN
Uno de los principales retos de los programas de detección neonatal del HC, es garantizar la diferenciación de los RN sanos de los hipotiroideos, lo cual depende en gran medida de que el punto de corte establecido corresponda a la población en la cual será aplicada; una vez establecido, éste deberá ser continuamente evaluado a fin de detectar posibles cambios, debido a factores poblacionales tales como un aumento del consumo del iodo, o cambios de la edad de toma de muestra. En Paraguay el consumo de iodo ha ido cada vez más en aumento, lo cual, ha sido implementado a fin de erradicar los desordenes por deficiencia de iodo (DDI).
Si bien, hasta la fecha la permanencia de la madre y el recién nacido en las maternidades publicas es hasta las 24 hs después del parto, estimamos que esto será cambiado, atendiendo a la necesidad de elevar la permanencia de ambos a un mínimo de 48 hs, de no existir complicaciones maternas o del recién nacido. Este aspecto resulta de vital importancia pues la concentración de TSH sufre una tendencia a un aumento fisiológico durante las primeras horas de vida, decreciendo progresivamente dentro de las primeras 48 horas, pudiendo de esta forma, un valor de referencia establecido que no tenga en cuenta estos factores de variabilidad, arrogar un resultado falso positivo (7).
El punto de corte de la TSH debe ser aquel que, en primer lugar permita reducir los falsos positivos, minimizando el número de RN normales a ser re-llamados, por los costos emocionales y económicos que ello genera, a los padres o al Programa, sean estos de ansiedad o de búsqueda y confirmación, mayor aun si el RN proviene de un área rural y de dificil acceso. Y en segundo lugar, debe eliminar por completo los falsos negativos, y así llegar al objetivo principal cual es prevenir el retardo mental en la población neonatal (6,8,9).
CONCLUSIÓN
El valor del punto de corte de la TSH determinado corresponde a 10 uU/ml, el cual ha sido historicamente utilizado por los miembros del laboratorio del PPFQRM. Sin embargo, los controles seguirán realizandose a fin de detectar precozmente los cambios que pudiesen afectar a dicho valor, a fin de ajustarlo si fuese necesario y con ello seguir manteniendo el maximo de sensibilidad.
AGRADECIMIENTOS
Especiales agradecimientos a la Agencia de Cooperación Internacional del Japón-JICA, sin cuyo apoyo este trabajo no hubiera sido posible, al Dr. Gustavo Borrajo por el asesoramiento técnico y científico durante todo el proceso, a la Srta. María Eugenia González por el asesoramiento y ayuda en el trabajo informático y estadístico, así como a los demás miembros del equipo de trabajo del Programa de Prevención del Retardo Mental y la Fibrosis Quística.
REFERENCIAS
1. Wilson J, Foster D, Kronenberg H, Larsen P. Williams Testbook of Endocrynology. Saunders. 9th Edition; 1998. [ Links ]
2. Kapelari K, Kirchlechner C, Högler W, Schweitzer K, Virgolini I, Moncayo R. Pediatric reference intervals for thyroid hormone levels from birth to adulthood: a retrospective study. BMC Endocrine Disorders. 2008;8:15. [ Links ]
3. Comité de Endocrinología. Sociedad Argentina de Programa de pesquisa neonatal de hipotiroidismo congénito de la provincia de Buenos Aires. Recomendaciones para los programas de pesquisa neonatal de hipotiroidismo congénito. Arch Argent Pediatr. 2000;98:244-46. [ Links ]
4. Ritchie R, Palomaki G. Foundation for Blood Research, Scarborough, Selecting clinically relevant populations for reference intervals. Clinical Chemistry and Laboratory Medicine. 2004;42:702-709. [ Links ]
5. Murthy-Korada S, Pearce M, Ward-Platt M. Difficulties in selecting an appropriate Neonatal TSH screening threshold. Arch Dis Child. 2010;95:169-73. [ Links ]
6. Colón C, Alonso-Fernández JR. The TSH threshold in neonatal screening for congenital hypothyroidism: a variable solution. Arch Dis Child. 2010;96:565-66. [ Links ]
7. Marrero-Gonzalez N, Gonzalez-Reyes E. Influencia de la edad en los resultados de cribado neonatal. Rev Mex Patol Clin. 2004;51(4):220-25. [ Links ]
8. Becerra C. Hipotiroidismo congénito y fenilcetonuria en el niño. Rev Chil Pediatr. 2008;79(Supl 1):96-102. [ Links ]
9. Barona-Vilar C, Mas-Pons R, Fullana-Montoro A. La tirotropinemia neonatal como indicador del estado nutricional de yodo en Castellon y Valencia. Rev Esp de Salud Pública. 2008;82(4)405-13. [ Links ]














