Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Pediatría (Asunción)
versão On-line ISSN 1683-9803
Pediatr. (Asunción) v.37 n.2 Asunción ago. 2010
ARTÍCULO ORIGINAL
Daño celular en una población infantil potencialmente expuesta a pesticidas
Cell Damage in a Pediatric Population Potentially Exposed to Pesticides
Benítez-Leite S(1), Macchi ML(1), Fernández V(2), Franco D(2), Ferro EA(3), Mojoli A(2), Cuevas F(2), Alfonso J(2), Sales L(2).
1. Cátedra de Pediatría- Facultad de Ciencias Médicas (FCM), Universidad Nacional de Asunción (UNA). San Lorenzo – Paraguay.
2. Laboratorio de Mutagénesis Ambiental - Facultad Ciencias Exactas y Naturales (FaCEN) UNA.
3. Cátedra de Bioquímica. FCM-UNA.
Correspondencia: Dra. Stela Benitez-Leite, E-mail: stelabenitez@yahoo.com.ar
Articulo recibido en Mayo de 2010, aceptado para publicación Julio de 2010.
Esta investigación se realizó en el marco de la convocatoria 2009 para proyectos de investigación de la Dirección General de Investigaciones Científicas y Tecnológicas de la Universidad Nacional de Asunción.
RESUMEN
Los pesticidas pueden producir efectos agudos o crónicos en la salud humana. Muchos de ellos pueden provocar daño en el material genético. Esta modificación en la información genética se ha relacionado con un alto riesgo de padecer cáncer. El objetivo del presente trabajo es indagar el daño en el material genético de una población infantil expuesta potencialmente a pesticidas en el ambiente. El diseño metodológico fue de tipo observacional y transversal. Participaron en el estudio 48 niños expuestos potencialmente a pesticidas y 46 niños no expuestos. Se obtuvo muestra de la mucosa bucal para determinar daño en el material genético a través de la frecuencia de micronúcleos (MN). Se encontró en el grupo expuesto potencialmente a pesticidas un promedio mayor de micronúcleos (5,1±2,9 vs 1,8±2,0; p<0,0001), un promedio mayor de células binucleadas, (3,5±2,7 vs 1,4±1,4; p<0,0001), mayor frecuencia de cariorrexis (18,2±18,4 vs 5,8±18,4; p<0,004) y picnosis (24,8± 18,0 vs 17,1±8,3; p<0,03). El 40% (19/47) de los niños expuestos potencialmente a pesticidas tuvieron un tiempo de exposición de 6 años. Esta investigación aporta evidencias de daño genético en la población expuesta potencialmente a pesticidas en el ambiente.
Palabras claves: genotoxicidad, pesticidas, niños, medio ambiente
ABSTRACT
Pesticides can cause acute or chronic effects on human health. Many pesticides can cause damage to genetic material. These changes in genetic information have been associated with an increased risk of cancer. The objective of this study is to investigate damage to genetic material in a population of children potentially exposed to pesticides in the environment. The study design was observational and cross sectional. We studied 48 children potentially exposed to pesticides and 46 unexposed children. Samples of the oral mucosa were obtained to determine damage to genetic material using micronucleus frequency (MN).Higher average micronucleus counts were found in the group potentially exposed to pesticides (5.1±2.9 vs. 1.8±2.0, p <0.0001), along with a higher average of binucleate cells (3.5±2.7 vs. 1.4±1.4 p <0.0001), higher frequency of karyorrhexis (18.2±18.4 vs. 5.8± 18.4, p <0.004) and pyknosis (24.8±18.0 vs. 17.1±8.3; p <0.03).Of the children potentially exposed to pesticides, 40% (19/47) had an exposure time of 6 years. This study provides evidence of genetic damage in the population potentially exposed to pesticides in the environment.
Keywords: mutagens, genotoxins, pesticides, children, child, environment
INTRODUCCIÓN
Los pesticidas constituyen una categoría heterogénea de químicos específicamente diseñados para el control de plagas, malezas o enfermedades de las plantas (1).
Su aplicación es todavía el modo más aceptado y efectivo para proteger a las plantas de las plagas, han contribuido significativamente a mejorar la productividad agrícola y el rendimiento de las cosechas y ayudado a limitar la expansión de enfermedades. Sin embargo, los pesticidas también tienen efectos nocivos y pueden dañar la salud humana así como el ambiente. El rango de estos efectos adversos sobre la salud incluye daño agudo e injuria permanente al sistema nervioso, daño pulmonar, daño a órganos reproductivos, disfunción del sistema endocrino y del sistema inmune, defectos del nacimiento y cáncer. Un total de 890 ingredientes activos están registrados como pesticidas en los Estados Unidos de América y actualmente son comercializados en 20.700 productos pesticidas. Muchos de estos componentes permanecerán en el ambiente por muchos años (1-3). Todas las personas están inevitablemente expuestas a los pesticidas a través de la contaminación ambiental o el uso ocupacional. La población general está expuesta a los residuos de los pesticidas incluyendo los productos físicos y biológicos de degradación en el aire, agua, suelo y los alimentos (1). Los casos de intoxicación aguda por pesticidas son una causa de morbilidad y mortalidad en el mundo. Los países en desarrollo son particularmente susceptibles debido a una pobre regulación, a la ausencia de sistemas de vigilancia, a un menor cumplimiento de la ley, a una ausencia de entrenamiento y a un inadecuado acceso a sistemas de información (4).
El grupo de tareas de OMS para la Protección de la Salud Ambiental de los niños ha declarado: “los niños no son adultos pequeños”, la premisa detrás de este principio es que los niños tienen una excepcional vulnerabilidad a los efectos agudos y crónicos de los peligros ambientales y que ellos son desproporcionadamente susceptibles en comparación con los adultos (5,6). Se ha reconocido que los niños son un grupo, dentro de la población, que tiene características particulares de exposición y especial vulnerabilidad a los tóxicos ambientales, y requieren una estrategia, para la evaluación del riesgo, que considere sus características particulares (7). Los niños tienen una exposición desproporcionadamente intensa a muchos agentes ambientales, beben más agua, consumen más alimentos y respiran más aire por peso corporal que los adultos, debido a su conducta “mano a boca”, tienen mayor chance de ingerir compuestos tóxicos presentes en el agua, suelo y polvo de los hogares (8). Los niños por su estatura menor pueden tener mayor exposición al vapor de pesticidas volátiles, particularmente aquellos pesticidas que en su fase gaseosa, tienen una densidad mayor que el aire (6). Finalmente, los niños pueden diferir de los adultos en los niveles de detoxificación, en los procesos de reparación del ADN, y en la proliferación celular. La diferencia más evidente entre niños y adultos es el impacto reducido de tradicionales factores de confusión como el fumar cigarrillos y la exposición ocupacional. Los niños usualmente no fuman activamente y no están expuestos ocupacionalmente a agentes genotóxicos, al menos hasta la adolescencia. Sin embargo, pueden ser fumadores pasivos y tienen mayor chance de ingestión de polvo contaminado. La dieta del niño, que es menos variada que la del adulto, como factor de confusión, puede ejercer un impacto reducido o mayor si alguna parte de la misma se halla contaminada con agentes genotóxicos. Los niños, por razones relacionadas con su edad, son una población vulnerable, y proteger su salud es una prioridad social, científica y emocional (8,9).
La exposición a las toxinas ambientales puede ocurrir por varias rutas: inhalación, ingestión o absorción dérmica, y puede ser durante el período prenatal, y a través de las etapas de desarrollo postnatal. Idealmente la evaluación de la exposición debería estar basada sobre cuestionarios y marcadores caracterizando exposición interna y externa. Los marcadores externos pueden ser medidos en al aire, agua, polvo etc. (8). Los marcadores biológicos han sido definidos como una alteración en los componentes celulares, bioquímicos, procesos, estructura o funciones, que son medibles en una muestra o sistema biológico (10).
Los pesticidas han sido considerados mutágenos químicos potenciales. La mayoría de las exposiciones ambientales y ocupacionales está relacionada con una mezcla de pesticidas y evaluar el potencial genotóxico de componentes simples podría no ser extrapolable a los humanos. El biomonitoreo en poblaciones humanas es una herramienta útil para estimar el riesgo genético frente a la exposición de mezclas complejas de químicos. Aunque un número de biomarcadores está disponible para evaluar respuesta genotóxica transitoria y permanente, los estudios de biomonitoreo se han enfocado esencialmente sobre aberraciones cromosómicas (AC), frecuencia de micronúcleos (MN) e intercambio de cromátidas hermanas (ICH) (1).
El daño al genoma humano es probablemente la causa más importante y fundamental de enfermedades degenerativas y del desarrollo. Está bien establecido que el daño genómico está producido por exposición ambiental a genotoxinas, procedimientos médicos (radiación y químicos), deficiencia de micronutrientes (déficit de folatos), estilos de vida (alcohol, el hábito de fumar, drogas y stress) y factores genéticos tales como defectos hereditarios en el metabolismo y reparación del ADN (11).
La medición de la frecuencia de MN en linfocitos de sangre periférica se utiliza ampliamente en epidemiología molecular y citogenética para evaluar la presencia y extensión de daño cromosómico en poblaciones humanas expuestas a agentes genotóxicos o para determinar la presencia de un perfil genético susceptible. La alta confiabilidad y el bajo costo de la técnica del MN, ha contribuido al éxito y a la adopción de este biomarcador para estudios, in vitro e in vivo, de daños al genoma humano. Los micronúcleos se originan desde fragmentos cromosómicos o de cromosomas completos que no han sido incluidos en el núcleo principal de la célula hija durante la división celular. La formación de micronúcleos en células divididas es el resultado de ruptura cromosómica debida a ausencia o alteración de la reparación de lesiones del ADN, o mala agregación del cromosoma debido a mala función mitótica. El amplio uso actual del ensayo de MN es una oportunidad para aplicarlo en la planificación y validación de programas de vigilancia y prevención de cáncer (12). Estudios conducidos en niños expuestos a contaminantes ambientales revelaron claramente un incremento en la frecuencia de micronúcleos en los expuestos, comparados con los niños referentes (13).
Es esencial tener biomarcadores confiables y relevantes, mínimamente invasores, para mejorar la implementación de biomonitoreo, diagnóstico y tratamiento de enfermedades causadas o asociadas con daño genético. En este aspecto, la frecuencia de MN en células exfoliadas de la mucosa bucal es un método mínimamente invasor, y útil para el monitoreo del daño genético en humanos, el Human Micronucleus Project ha iniciado un proceso internacional de validación para el ensayo de MN en células de la mucosa bucal, similar al realizado previamente utilizando linfocitos humanos (11).
A partir de estas consideraciones se investiga la presencia de marcadores biológicos de genotoxicidad en una población infantil que asiste a una escuela del barrio Los Naranjos de la ciudad de Ñemby que se encuentra ubicada a pocos metros de un establecimiento industrial dedicado a la formulación y síntesis de químicos: insecticidas, fungicidas, herbicidas y coadyuvantes, y otros productos para el agro. Instalado desde junio del año 2003 en el lugar, se definió esta situación como un factor de riesgo potencial para la salud, conforme a las conclusiones del informe final de la inspección técnica de la fábrica realizada por el Ministerio de Salud Pública y Bienestar Social, la Secretaría del Ambiente y OPS/OMS. Luego de la revisión de la capacidad de producción de la planta, las condiciones de manejo de los productos, procesamiento, almacenamiento, así como las deficiencias encontradas para el manejo y tratamiento de los residuos sólidos, líquidos y gaseoso el equipo técnico concluye: “La existencia de emisiones y la eventual exposición a la comunidad, constituyendo un riesgo para la salud de la población y de los trabajadores” (14). Se utiliza como marcador de genotoxicidad la frecuencia de MN en células exfoliadas de la mucosa oral, un método útil y mínimamente invasor para medir daño genético en humanos.
El objetivo general de esta investigación es determinar el efecto de la exposición ambiental a pesticidas sobre el material genético de niños. Los objetivos específicos son: 1) Determinar la frecuencia de micronúcleos en células exfoliadas de la mucosa oral, tanto en niños expuestos potencialmente a pesticidas y no expuestos. 2) Identificar la frecuencia de otros marcadores de daño celular, como: células binucleadas, células con cromatinas condensadas, cariorrexis, células picnóticas y cariolíticas, en niños expuestos potencialmente a pesticidas y en niños no expuestos. 3) Obtener información técnica para apoyar políticas públicas que protejan la vida y la calidad de vida de quienes habitan en la zona potencialmente expuesta.
PACIENTES Y MÉTODOS
Diseño de estudio: el estudio fue de tipo observacional y transversal.
Población potencialmente expuesta: niño/as sanos, en edad escolar matriculados en la escuela de nivel escolar básico Nº 5596 San Pedro y San Pablo de la ciudad de Ñemby en el año 2009.
La mencionada escuela se halla situada a 50 metros de una fábrica que sintetiza y formula pesticidas.
Población no expuesta: niños/as sanos, en edad escolar, que concurren a la escuela Nº 601 Rita Surroca de la ciudad de San Lorenzo y que se encuentra ubicada a 5,5 km de la escuela San Pedro y San Pablo de la ciudad de Ñemby.
La distancia entre ambas escuelas, fue medida a través de un GPS marca GARMIN Etrex. Las coordenadas tomadas con la misma herramienta son:
La escuela Rita Surroca (del grupo no expuesto) tiene la siguiente georreferencia:
Latitud sur: 25º 21' 38.0''
Longitud oeste: 57º 30' 23.1''
La escuela San Pedro y San Pablo (grupo expuesto):
Latitud sur: 25º 24' 03,5''
Longitud oeste: 57º 32' 21,5''
No se registra la presencia de ninguna otra fábrica en las proximidades de ambas escuelas.
Criterios de inclusión:
Asentimiento de los niños y consentimiento informado de los padres para que sus hijos participen del estudio.
Muestreo y reclutamiento:
La investigación fue socializada en el predio de la escuela con la presencia de docentes y padres de alumnos, por parte de 2 pediatras, que además se encargaron de realizar las encuestas y administrar el consentimiento informado. Se incluyeron niños/as que accedieron voluntariamente, junto a sus padres, a formar parte de la investigación.
Las muestras biológicas fueron obtenidas por investigadores del Laboratorio de Mutagénesis Ambiental de la Facultad Ciencias Exactas y Naturales (FaCEN) en junio-julio del 2009 en el grupo expuesto y octubre-noviembre del 2009 en el grupo no expuesto. Se recolectaron 2 muestras de epitelio oral realizando un frotis en la pared interna de ambas mejillas, después de un enjuague bucal con agua.
Bioensayo- Técnica de MN en mucosa bucal
Se raspó cuidadosamente la mucosa bucal de los niños/as con una paleta bajalenguas de madera realizándose un frotis sobre un portaobjeto limpio y dejándolo secar al aire a temperatura ambiente (2 muestras por individuo).
Se fijó el preparado en etanol: ácido acético 3:1 de durante 1 hora y se dejo secar a temperatura ambiente. Se realizó la hidrólisis en HCL 1N de la siguiente manera: 5 minutos a temperatura ambiente, 10 minutos a 60° C y 5 minutos a temperatura ambiente. Posteriormente de acuerdo a la técnica de Tolbert (1.991), las láminas se colorearon en vasos de Coplin con agua fría (5º C) durante 5 minutos con el objetivo de cortar la hidrólisis. Una vez trascurrido el tiempo se dejó secar las láminas.
Luego se colocaron las muestras hidrolizadas, en fuscina básica durante 20 minutos en ausencia de luz.
Se lavaron las láminas con agua corriente, dejándolas secar a temperatura ambiente.
Luego se observaron y analizaron los preparados en microscopios Olympus, Modelo BH2, de procedencia japonesa, a 1000x.
En la primera lámina se contaron 1000 células para búsqueda de MN de ambas poblaciones. Posteriormente, con la segunda lámina se volvieron a contar 1000 células identificando además de micronúcleos otras anormalidades, como células binucleadas, en broken eggs, picnosis, cromatina condensada, y diversos estadios de células en apoptosis.
El mismo procedimiento se realizó en el grupo no expuesto.
Las personas que analizaron las muestras no tenían conocimiento acerca de las características biodemográficas de cada niño estudiado, únicamente las iniciales de los nombres respectivos.
Las microfotografías, fueron obtenidas con aumento 100 X en el laboratorio de microscopía de FaCEN-UNA con una cámara Samsung S860.
Mediciones
Evaluación del efecto citogenético: para la variable resultante micronúcleo la medición se realizó sobre 2000 células por individuo. Para las demás variables resultantes (cel binucleadas, broken eggs, cariolisis, cariorrexis, cromatina condensada, picnosis) el contaje se obtuvo sobre 1000 células por individuo.
Tiempo de exposición: se tomó como tiempo de exposición, la presencia de los niños/as durante 4 horas diarias (turno mañana o tarde), 5 días en la semana y con un mínimo de 1año a 6 años máximo.
Las demás variables secundarias fueron indagadas como variables de confusión o de intoxicación aguda y fueron analizadas como variables cuantitativas o dicotómicas.
Análisis Estadístico
Los datos fueron analizados en el programa Epinfo 2000. Se aplicó la prueba de t de Student para variables que se distribuyen normalmente y el Test de Kruskal-Wallis para variables que se distribuyen asimétricamente para comparar a las dos poblaciones estudiadas. Se asumió un p<0.05 como significativo. Las variables cualitativas se resumieron en proporciones y las variables cuantitativas en media aritmética y desviación estándar.
RESULTADOS
Se analizaron 48 niños expuestos potencialmente a pesticidas en el ambiente y 46 niños no expuestos, provenientes de 2 escuelas diferentes y con una distancia de 5,5km entre ambas.
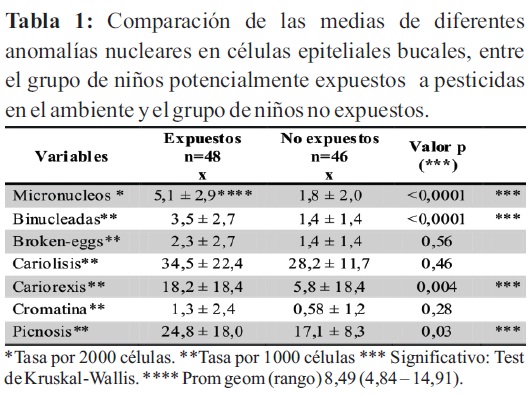
Se encontró que la población potencialmente expuesta a pesticidas en el ambiente, presenta mayor frecuencia de micronúcleos, células binucleadas, cariorrexis, picnosis que la no expuesta y la diferencia es altamente significativa, según la prueba de t, con una p<0,0001 para micronúcleos y células binucleadas y también significativas para cariorrexis y picnosis. Por otro lado, también hubo mayor proporción de células en Broken eggs, cariolisis y cromatina condensada en el grupo expuesto, aunque las cifras no fueron significativas (tabla 1 y 2).
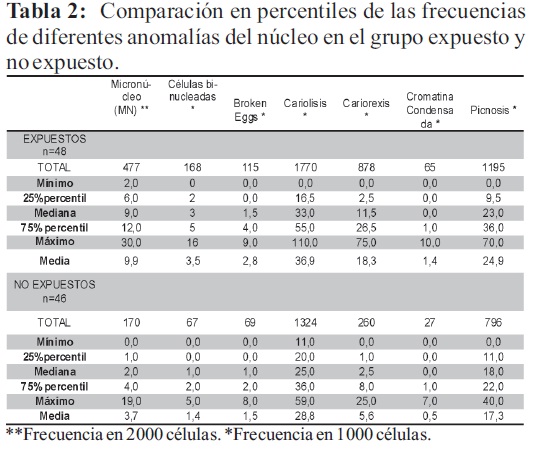
Se tomó como grado de exposición potencial a pesticidas en el ambiente, el tiempo de permanencia en la escuela, de los niños expuestos a partir del funcionamiento de la fábrica de pesticidas. El 83% (39/47) de la muestra estudiada tuvo una exposición potencial entre 1 y 6 años, considerando que la fábrica opera en el lugar desde hace 6 años. Así, el 40% (19/47) de la muestra estudiada tuvo un tiempo de exposición ambiental de 6 años. El 32% (15/47) tuvo un tiempo de exposición entre 4 y 5 años y el 27,7% (13/47) un tiempo de exposición de 1 a 3 años.
No hubo diferencias estadísticamente significativas en la edad, los años de escolarización y el género. La edad promedio fue de 9,6 años (expuestos) y 9,8 años (no expuestos) respectivamente (p<0,3). En los expuestos el promedio de escolarización fue 4,6±2,3 y 4,4 ±2,1 en el grupo de niños no expuestos (p<0,6). La proporción de sexos (F/M) fue del 25/22 (53/47%) en el grupo expuesto y 27/19 (59/41%) en el grupo no expuesto (p<0,3).
En el grupo potencialmente expuesto, la frecuencia de micronúcleos (por cada 2000 células/individuos) fue mayor, no significativa, en el sexo femenino (10,6±5,9) que en el masculino (9,1±5,3) (p<0,3, prueba de Kruskal-Wallis), mientras que en el grupo no expuesto la frecuencia fue mayor en el sexo masculino (4,8±4,7) que en el femenino (2,8±3,6) (p<0,03, prueba de Kruskal-Walis). Las diferencias observadas entre sexos no son suficientes como para considerar a éste como un factor de confusión en la comparación del parámetro entre expuesto y no expuestos.
La exposición a rayos X en los últimos 6 meses, el uso crónico de medicamentos, la utilización de plaguicidas en el hogar fue mayor en el grupo de no expuestos, con diferencias estadísticamente significativas. No hubo diferencias significativas en ambos grupos con las variables de padres fumadores, enfermedad respiratoria, antecedente de abortos, malformación congénita y muerte de un hijo antes de nacer (ver tabla 3).
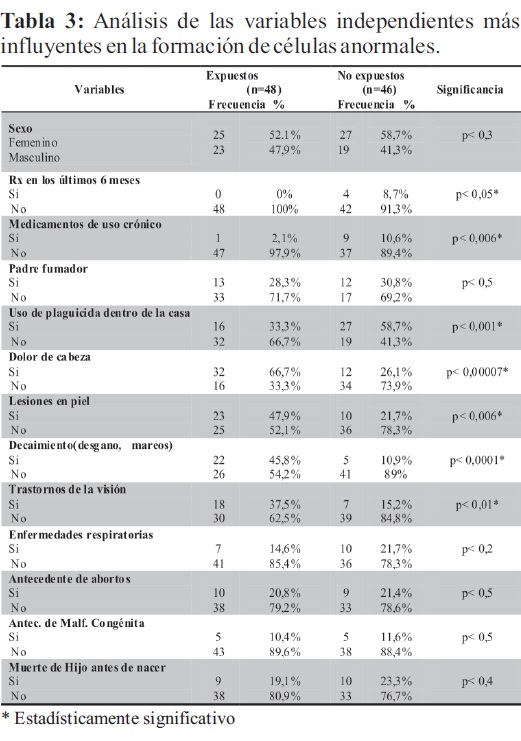
Hubo mayor proporción de cefalea, de lesiones en piel, decaimiento (desgano, falta de fuerza muscular, mareos) y trastornos de la visión en el grupo expuesto a plaguicidas del medio ambiente con diferencias estadísticamente significativas (tabla 3). .
DISCUSIÓN
Los resultados de este estudio muestran una frecuencia significativamente mayor de micronúcleos, células binucleadas, cariorrexis y picnosis en el grupo de niños potencialmente expuestos a pesticidas, que en el grupo no expuesto y la diferencia es altamente significativa para micronúcleos, células binucleadas (p<0,0001) y cariorrexis (p<0,004) y significativa para picnosis (p<0,03). Se halló una mayor proporción de células en broken eggs, cariolisis y con cromatina condensada en el grupo expuesto, aunque las diferencias no fueron significativas. Estos hallazgos demuestran la presencia de biomarcadores que evalúan daño cromosómico como los MN, otros marcadores que indican fallo en la citoquinesis y muerte celular (células binucleadas, células en broken eggs, en cariorrexis, picnosis, cariolisis), en células exfoliadas de la mucosa bucal, de niños que asisten a una escuela ubicada a pocos metros de una fábrica dedicada a la formulación y síntesis de agroquímicos: insecticidas, fungicidas, herbicidas y coadyuvantes, proveen evidencias de genotoxicidad en una población potencialmente expuesta a pesticidas en el ambiente. Los micronúcleos son pequeños núcleos separados del núcleo central de la célula, que se producen durante la telofase de la mitosis (meiosis), pueden formarse por la exclusión de un cromosoma completo (pérdida cromosómica) o de fragmentos cromosómicos (ruptura cromosómica), durante la división celular, su presencia en las células es un reflejo de aberraciones estructurales y o numéricas (efectos clastogénicos y/o aneugénicos). El ensayo de MN en células exfoliadas comprende el análisis microscópico de extendidos epiteliales para determinar la prevalencia de micronucleación. La habilidad del ensayo de MN para detectar tanto efectos clastogénicos como aneugénicos es una ventaja de la técnica (15-19).
En los niños potencialmente expuestos, se halló una frecuencia mayor, estadísticamente significativa, de otras alteraciones nucleares: células binucleadas, células en cariorrexis y células picnóticas, indicando daño cromosómico, alteración en la citoquinesis y muerte celular. Las células con doble núcleo podrían ser un marcador importante de falla en la citoquinesis causada por una frecuencia anormalmente elevada de aneuploidia. La significancia biológica de las células picnóticas y el mecanismo de formación son desconocidos, puede representar un mecanismo alternativo de desintegración nuclear, diferente a la cariorrexis y la cromatina condensada (18). La experiencia con el ensayo de MN, en el bloque citogenético de linfocitos, ha mostrado que el uso de un citoma, en el que no solamente se mide la frecuencia de MN sino también otros marcadores de daño al genoma, células muertas, o degeneradas, así como índice de proliferación, asegura una medición más comprensiva de citoxicidad y efectos genotóxicos (11).
El ensayo de MN ha sido aplicado para evaluar el daño cromosómico en el monitoreo biológico de poblaciones humanas expuestas a una variedad de agentes químicos o físicos mutagénicos y carcinogénicos. Un amplio intervalo de frecuencia basal de MN en células de la mucosa oral ha sido reportado, 0,05 a 11,5 MN/1000 células, con la mayoría de los valores entre 0,5 y 2,5MN/1000 células y no existe un claro patrón de variación entre los laboratorios de diferentes países. Muchos estudios reportan una elevada frecuencia, estadísticamente significativa, en individuos expuestos comparados con un grupo control, aunque los efectos observados son relativamente pequeños, con valores entre 1,1 y 4,0 (11,20,21). Sin embargo, otros estudios no han mostrado cambios estadísticamente significativos (22,23). Una investigación sobre efectos de la exposición acumulativa a formaldehido mostró un incremento de 12 veces la frecuencia de MN en células de la mucosa oral luego de la exposición. Este hallazgo, fue confirmado en una siguiente investigación utilizando una técnica diferente de tinción (11,24).
Se ha hallado incremento significativo de MN células exfoliadas de la mucosa oral en personas expuestas a solventes orgánicos, agentes antineoplásicos, derivados del diesel, hidrocarburos aromáticos policíclicos, pintura que contiene plomo y disolventes y agua contaminada con arsénico, en diversos estudios (11,25). Nery et-al. (13) encontraron que todos los estudios conducidos en niños expuestos a contaminantes ambientales revelaron, claramente, un aumento en la frecuencia de MN, comparados con los niños referentes. Los incrementos de MN fueron estadísticamente significativos, en todos. Los resultados de un estudio realizado en cuatro poblaciones agrícolas ocupacionalmente expuestas a pesticidas no reveló una inducción significativa de daño citogenético, medido por la frecuencia de MN tanto en linfocitos de sangre periférica como en células de la mucosa oral (26).
Otros estudios han fallado en demostrar efectos citogenéticos asociados a los pesticidas, en población ocupacionalmente expuesta, con ensayos para Aberración Cromosómica (AC) y MN en linfocitos de sangre periférica y algunos también para MN en células de mucosa bucal (22,23,27,28). Se ha mostrado aumento de la frecuencia de MN en células de la mucosa oral en un grupo de 30 floricultores mexicanos, siendo la frecuencia de MN con relación a los no expuestos, estadísticamente significativa (29). En un estudio reciente que incluyó una población de 70 floricultores expuestos, en el Norte de Sinaloa, México, se halló frecuencia aumentada de MN en células de la mucosa oral, con relación a la población no expuesta (30). En una investigación realizada en 29 trabajadores agrícolas brasileros, expuestos a pesticidas en campos de soja, se encontró una frecuencia significativamente mayor de MN en células de la mucosa oral, que en el grupo no expuesto (31). Una investigación realizada en la India en 54 trabajadores de una unidad de fabricación de plaguicidas demostró un aumento significativo en la frecuencia de MN en células de la mucosa bucal en comparación con igual número de sujetos no expuestos (32). En el delta de Goksu, Turquía, una región contaminada con una mezcla de pesticidas, se investigó genotoxicidad en 32 personas viviendo en la región, y se halló un aumento significativo de MN en células de la mucosa oral, comparado con igual número de personas no expuestas (33).
La frecuencia de MN en linfocitos de sangre periférica, es extensamente utilizada como biomarcador para señalar la presencia y extensión de daño cromosómico y la estabilidad del genoma, en poblaciones humanas expuestas a agentes genotóxicos, o para determinar la presencia de un perfil genético susceptible. Un total de 6.718 sujetos en quienes se determinó frecuencia de MN, fueron seleccionados de la base de datos del proyecto internacional del MN humano (HUman MicroNucleus (HUMN), los resultados de la investigación proveen evidencias preliminares que la frecuencia de MN en linfocitos de sangre periférica es un marcador biológico predictivo de riesgo de cáncer en una población de sujetos sanos (34).
El estudio de daño al ADN en células exfoliadas de la mucosa oral es un método mínimamente invasor para monitorear poblaciones expuestas a agentes genotóxicos. La presencia de MN y otras anomalías dentro de estas células ha mostrado estar asociada con defectos genéticos en el mantenimiento del genoma, en el envejecimiento temprano, daño genotóxico y algunas enfermedades degenerativas. Sin embargo, es prioritaria la estandarización del método, ya que todavía no se sabe si una frecuencia elevada de MN en la mucosa bucal en población humana es predictiva de riesgo de cáncer, si es específica del sitio o puede extrapolarse a otros sitios (35).
Con relación a la edad y al género, la muestra en ambos grupos ha sido homogénea ya que no mostró diferencias significativas al compararlos. La influencia del sexo ha sido informada para adultos, sin embargo, su influencia no ha sido estadísticamente significativa en individuos menores de 40 años. Llega a ser más pronunciada en sujetos de mayor edad. En una revisión de un conjunto de estudios en adultos se encontró que las mujeres tenían un nivel mayor de frecuencia de MN, equivalente a un 19% más (36).
Datos publicados por Neri et al, en una revisión sobre investigaciones realizadas en niños de 0 a 18 años, expuestos a mutágenos, mostraron que la influencia del sexo sobre la frecuencia de MN era irrelevante (37).
Así mismo, en un metanálisis y un conjunto de estudios de frecuencia basal de MN en niños no se ha encontrado diferencias con relación al sexo (38).
El estudio y la prevención de enfermedades que afectan a los niños debido a exposición no intencional a agentes biológicos, químicos y físicos está emergiendo como un nuevo campo de investigación, de políticas y de prácticas clínicas. Hoy se sabe que el daño a la salud puede producirse con niveles elevados de exposición así como con bajos y prolongados niveles de exposición a tóxicos en el ambiente. Muchas de estas sustancias están ampliamente distribuidas en el ambiente y pueden ser halladas en sangre, fluidos corporales y tejidos de niños y mujeres embarazadas. Aunque las alteraciones son a menudo sutiles a nivel individual, el daño puede ser sustancial a nivel poblacional, en especial cuando una exposición es prevalente (39), en esta investigación el 83% de los niños estudiados tuvo un periodo de exposición potencial entre 1 año y 6 años con un promedio de 4,6 años.
Los plaguicidas, pueden generar contaminación en los ambientes de trabajo donde son manipulados, o en general, en el ambiente que rodea las zonas de manipulación. Las etapas que componen la cadena de los plaguicidas son la fabricación, la formulación, el fraccionamiento y/o envasado, la distribución y la aplicación. En cualquiera de las etapas mencionadas se puede generar contaminación ambiental: del aire, con los polvos de plaguicidas o solventes evaporados; del agua, por derrames y corrientes de lavado; y del suelo, también por derrames y disposición inadecuada de residuos sólidos (40,41). Existen evidencias sobre efectos ambientales de actividades industriales aún después del cese de operaciones por un largo tiempo (42,43).
El aspecto relevante de este estudio es la significativa diferencia de MN en dos grupos de niños escolares, la frecuencia mayor de MN en los que asisten a una escuela próxima a una fábrica de sustancias químicas para el agro, señala que estos se hallan expuestos a genotóxicos. Se debe ampliar la investigación para determinar con mayor aproximación las causas, a través del monitoreo ambiental y otros marcadores biológicos de exposición, de los efectos hallados.
En esta investigación potenciales variables de confusión como la exposición a rayos X en los últimos 6 meses, el uso de medicamentos crónicos, la utilización de plaguicidas en el hogar fue mayor en el grupo de no expuestos a plaguicidas, con diferencias significativas. No hubo diferencias significativas entre ambos grupos con relación a otras variables como padres fumadores, enfermedad respiratoria, antecedente de abortos, malformación congénita y muerte de un hijo antes de nacer.
Hubo mayor proporción de cefalea, de lesiones en piel, decaimiento (desgano, falta de fuerza muscular, mareos) y trastornos de la visión en el grupo expuesto a plaguicidas del medio ambiente, con diferencias significativas que pueden interpretarse como síntomas y signos de exposición aguda. La intoxicación por pesticidas es comúnmente sub-diagnosticada, los hallazgos clínicos de la intoxicación aguda raramente son patognomónicos, puede remedar una enfermedad respiratoria aguda, conjuntivitis, enfermedad gastrointestinal, manifestaciones cutáneas, entre otras (44).
Los problemas que promueven el deterioro genómico en las comunidades y que atañen a la bioética ambiental son: la distribución desigual de tóxicos en relación con la etnicidad o el nivel de ingresos, fallas de protección en el ambiente laboral en regiones de menor desarrollo socioeconómico, ausencia deliberada de información sobre los riesgos de exposición a genotóxicos en el ambiente laboral o en la zona de residencia, deficiente o insuficiente evaluación de genotoxicidad de medicamentos o aditivos alimentarios, deficiente evaluación de genotoxicidad de actividades industriales y de otras no asociadas con la producción de bienes. En la bioética ambiental, el primer principio debe ser el de no maleficencia (primum non nocere). El deber de informar a la sociedad civil se origina en el principio de consentimiento informado. Una comunidad debe elegir si acepta que en su entorno se localicen actividades nocivas. Mientras que los principios de justicia y equidad se encaminan a la distribución de beneficios y riesgos, especialmente al determinar quiénes en la comunidad sufrirán y quiénes se beneficiarán (45). Muchas políticas regulatorias no toman en cuenta la vulnerabilidad única de los niños, cuando establecen los límites (46). El desarrollo de estrategias de evaluación de riesgo, que tengan en cuenta las distintas etapas del desarrollo, a través de la cual todas las generaciones futuras deben pasar es esencial para la salud pública. El objetivo principal es formular políticas que protejan al niño contra agentes potencialmente tóxicos y permita que ellos crezcan, se desarrollen y lleguen a la madurez sin daños. Ningún documento sobre la evaluación del riesgo que no considere las características únicas de exposición y vulnerabilidad de fetos, infantes, niños y adolescentes, puede ser considerado hoy, adecuado para proteger la salud humana. La participación activa de todos los sectores de la sociedad juega un papel importante en la promoción de entornos seguros y saludables para todos (47,48).
La salud de una sociedad puede ser juzgada por la salud de sus niños. Esto supone la identificación precoz de riesgos prevenibles y la traducción inmediata de estos conocimientos en intervenciones eficaces con políticas de protección (49).
Esta investigación permite afirmar que existe una exposición a genotóxicos en un grupo de niños con relación a otro. Se debería establecer un seguimiento a través de marcadores de efecto, como frecuencia de MN, una vez interrumpida la exposición, para determinar la persistencia, o no, de los indicadores biológicos de daño celular.
El principio de precaución puede invocarse cuando es urgente intervenir ante un posible peligro para la salud, o cuando éste se requiere para proteger el medio ambiente en caso de que los datos científicos no permitan una determinación completa del riesgo. En este caso el principio de precaución debe primar e interrumpir la exposición potencial al riesgo, en el menor tiempo posible, mientras tanto se obtengan datos y se definan acciones que protejan la salud de las personas y del medio ambiente en el que ellas viven.
CONCLUSIÓN
Se encontró mayor frecuencia de marcadores biológicos de daño celular, en la población infantil potencialmente expuesta a pesticidas en el ambiente, al compararla con una población similar no expuesta. Las diferencias observadas en los marcadores celulares no pueden ser explicadas por la influencia de otros factores demográficos o ambientales examinados.
REFERENCIAS
1. Bolognesi C. Genotoxicity of pesticides: a review of human biomonitoring studies. Mutat Res. 2003;543:251-72. [ Links ]
2. Palani-Kumar L, Panneerselvam N. Toxic effects of pesticides: a review on cytogenetic biomonitoring studies. Medicine and Biology. 2008;15(2):46-50. [ Links ]
3. Oleskey C, Fleischman A, Goldman L, Hirschhorn K, Landrigan P, Lappé M, et-al. Pesticide testing in humans: ethics and public policy. Environ Health Perspect. 2004;112(8):914-19. [ Links ]
4. Thundiyil JG, Stober J, Besbelli N, Pronczuk J. Acute pesticide poisoning: a proposed classification tool. Bull World Health Organ. 2008;86:205-209. [ Links ]
5. Wild CP, Kleinjans J. Children and increased susceptibility to environmental carcinogens: evidence or empathy? Cancer Epidemiol Biomarkers Prev. 2003;12:1389-394. [ Links ]
6. Garry VF. Pesticides and children. Toxicol Appl Pharmacol. 2004;198:152-63. [ Links ]
7. Landrigan PJ, Kimmel CA, Correa A, Eskenazi B. Children’s health and the environment: public health issues and challenges for risk assessment. Environ Health Perspect. 2004;112(2):257-65. [ Links ]
8. Neri M, Bonassi S, Knudsen LE, Sram RJ, Holland N, Ugolini D, et-al. Children’s exposure to environmental pollutants and biomarkers of genetic damage. I. Overview and critical issues. Mutat Res. 2006; 612 ( 1): 1-13. [ Links ]
9. Merlo DF, Knudesen LE, Matusiewicz K, Niebro´j L, Va-há-kangas KH. Ethics in studies on children and environmental health. Med Ethics. 2007;33:408-13. [ Links ]
10. Manno M, Viau C. Biomonitoring for occupational health risk assessment (BOHRA). Toxicol Lett. 2010;192(1):3-16. [ Links ]
11. Holland N, Bolognesi C, Kirsh-Volders M, Bonassi S, Zeiger E, Knasmueller S, et-al. The micronucleus assay in human buccal cells as a tool for biomonitoring DNA damage: the HUMN project perspective on current status and knowledge gaps. Mutat Res. 2008;656(1-2):93-108. [ Links ]
12. Bonassi S, Znaor A, Ceppi M, Lando C, Chang WP, Holland N, et-al. An increased micronucleus frequency in peripheral blood lymphocytes predicts the risk of cancer in humans. Carcinogenesis. 2007;28(3):625-31. [ Links ]
13. Neri M, Ugolini D, Bonassi S, Fucic A, Holland N, Knudsen LE, et-al. Children’s exposure to environmental pollutants and biomarkers of genetic damage II. Results of a comprehensive literature search and meta-analysis. Mutat Res. 2006;612(1):14-39. [ Links ]
14. Ministerio de Salud Pública y Bienestar Social. Secretaria del Ambiente. Informe de la inspección de la Fábrica Chemtec SAE. Asunción: OPS/OMS; 2009. [ Links ]
15. Tolbert PE, Shy CM, Allen JW. Micronuclei and other nuclear anomalies in buccal smears: methods development. Mutat-Res. 1992;271(1):69-77. [ Links ]
16. Norppa H, Ghita C, Falck M. What do human micronuclei contain? Mutagenesis. 2003;18(3):221-33. [ Links ]
17. Kirsch-Volders M, Fenech M. Inclusion of micronuclei in non-divided mononuclear lymphocytes and necrosis/apoptosis may provide a more comprehensive cytokinesis block micronucleus assay for biomonitoring purposes. Mutagenesis. 2001;16(1):51-58. [ Links ]
18. Thomas P, Holland N, Bolognesi C, Kirsch-Volders M, Bonassi S, Zeiger E, et-al. Buccal micronucleus cytome assay. Nat Protoc. 2009;4(6):825-37. [ Links ]
19. Fenech M, Crott J, Turner J, Brown S. Necrosis, apoptosis, cytostasis and DNA damage in human lymphocytes measured simultaneously within the cytokinesis-block micronucleus assay: description of the method and results for hydrogen peroxide. Mutagenesis. 1999;14(6):605-12. [ Links ]
20. Celik A, Cavas T, S. Ergene-Gozukara S. Cytogenetic biomonitoring in petrol station attendants: micronucleus test in exfoliated buccal cells. Mutagenesis. 2003;18(5):417-21. [ Links ]
21. Gattás GJ, Cardoso-Lde A, Medrado-Faria-Mde A, Saldanha PH. Frequency of oral mucosa micronuclei in gas station operators after introducing methanol. Occup Med (Lond). 2001;51(2):107-13. [ Links ]
22. Pastor S, Creus A, Xamena N, Siffel C, Marcos R. Occupational exposure to pesticides and cytogenetic damage: results of a Hungarian population study using the micronucleus assay in lymphocytes and buccal cells. Environ Mol Mutagen. 2002;40:101-109. [ Links ]
23. Pastor S, Gutierrez S, Creus A, Xamena N, Piperakis S, Marcos R. Cytogenetic analysis of Greek farmers using the micronucleus assay in peripheral lymphocytes and buccal cells. Mutagenesis. 2001;16:539-45. [ Links ]
24. Suruda A, Schulte P, Boeniger M, Hayes RB, Livingston GT, Steenland K, et-al. Cytogenetic effects of formaldehyde exposure in students of mortuary science. Cancer Epidemiol Biomarkers Prev. 1993;2:453-60. [ Links ]
25. Ghosh P, Basu A, Singh KK, Giri AK. Evaluation of cell types for assessment of cytogenetic damage in arsenic exposed population. Mol Cancer. 2008;7:45. [ Links ]
26. Pastor S, Creus A, Parron T, Cebulska-Wasilewska A, Siffel C, Piperakis S, et-al. Biomonitoring of four european populations occupationally exposed to pesticides: use of micronuclei as biomarkers. Mutagenesis. 2003;18:249-58. [ Links ]
27. Hoyos LS, Carvajal S, Solano L, Rodríguez J, Orozco L, López Y, et-al. Cytogenetic monitoring of farmers exposed to pesticides in Colombia. Environ Health Perspect. 1996;104:535-38. [ Links ]
28. Lander BF, Knudsen LE, Gamborg MO, Jarventaus H, Norppa H. Chromosome aberrations in pesticide-exposed greenhouse workers. Scand J Work Environ Health. 2000; 26: 436-42. [ Links ]
29. Gómez-Arroyo S, Díaz-Sánchez Y, Meneses-Perez MA, Villalobos-Pietrini R, De-León-Rodríguez D. Cytogenetic biomonitoring in a Mexican floriculture worker group exposed to pesticidas. Mutat Res. 2000;466:117-24. [ Links ]
30. Martínez-Valenzuela C, Gómez-Arroyo S, Villalobos-Pietrini R, Waliszewski S,Calderón ME. Genotoxic biomonitoring of agricultural workers exposed to pesticides in the north of Sinaloa State, Mexico. Environment International. 2009;35(8):1155-159. [ Links ]
31. Bortoli GM, Azevedo MB, Silva LB. Cytogenetic biomonitoring of Brazilian workers exposed to pesticides: micronucleus analysis in buccal epithelial cells of soybean growers. Mutat Res. 2009;675(1-2):1-4. [ Links ]
32. Sailaja N, Chandrasekhar M, Rekhadevi PV, Mahboob M, Rahman MF, Vuyyuri SB, et-al. Genotoxic evaluation of workers employed in pesticide production. Mutat Res. 2006;609(1):74-80. [ Links ]
33. Ergene S, Celik A, Cavas T, Kaya F. Genotoxic biomonitoring study of population residing in pesticide contaminated regions in Göksu Delta: micronucleus, chromosomal aberrations and sister chromatid exchanges. Environ Int. 2007;33(7):877-85. [ Links ]
34. Mateuca RA, Roelants M, Lamarcovai G, Aka PV, Godderis L, Trem A, et al. Polymorphisms influence micronucleus frequencies in human lymphocytes in vivo. Mutagenesis. 2008;23(1):35-41. [ Links ]
35. Bonassi S, Biasotti B, Kirsch-Volders M, Knasmueller S, Zeiger E, Burgaz S, et-al. State of the art Survey of the buccal micronucleus assay--a first stage in the HUMN(XL) project initiative. Mutagenesis. 2009;24(4):295-302. [ Links ]
36. Bonassi S, Fenech M, Lando C, Lin YP, Ceppi M, Chang WP,et-al. Human MicroNucleus project: international database comparison for results with the cytokinesis-block micronucleus assay in human lymphocytes: I. Effect of laboratory protocol, scoring criteria, and host factors on the frequency of micronuclei. Environ Mol Mutagen. 2001;37(1):31-45. [ Links ]
37. Neri M, Fucic A, Knudsen LE, Lando C, Merlo F, Bonassi S. Micronuclei frequency in children exposed to environmental mutagens: a review. Mutat Res. 2003;544(2-3):243-54. [ Links ]
38. Neri M, Ceppi M, Knudsen LE, Franco Merlo D, Barale R, Puntoni R, et-al. Baseline micronuclei frequency in children: estimates from meta- and pooled analyses. Environ Health Perspect. 2005;113(9):1226-1229. [ Links ]
39. Lamphear BP, Bearer CF. Biomarkers in paediatric research and practice. Arch Dis Child. 2005;90:594-600. [ Links ]
40. Comisión Nacional del Medio Ambiente-Región Metropolitana. Guía para el control y prevención de la contaminación industrial: fabricación de plaguicidas, pesticidas y funguicidas. Santiago: Comisión Nacional del Medio Ambiente; 1998. [ Links ]
41. International Finance Corporation [homepage on the Internet]. Washington. Environmental Health and Safety Guidelines for Pesticide Manufacturing, Formulation, and Packaging. [citado 2010 Junio 20]; 2007. [ Links ]Disponible en: www.ifc.org/ifcext/enviro.nsf/Content/EnvironmentalGuidelines
42. Asmus CI, Alonzo HG, Palácios M, Silva AP, Freitas-Filhote MI, Buosi D, et-al. Assessment of human health risk from organochlorine pesticide residues in Cidade dos Meninos, Duque de Caxias, Rio de Janeiro, Brazil. Cad. Saúde Pública [serie en Internet]. 2008 Abril [citado 2010 Junio 27] ; 24(4): 755-766. [ Links ] Disponible en: http://www.scielo.br/scielo.php?script=sci_arttext&pid=S0102-311X2008000400005&lng=en.doi: 10.1590/S0102-311X2008000400005.
43. Wang G, Lu Y, Wang T, Zhang X, Han J, Luo W, et-al. Factors influencing the spatial distribution of organochlorine pesticides in soils surrounding chemical industrial parks. J Environ Qual. 2009;38:180-187. [ Links ]
44. Alarcon WA, Calvert GM, Blondell JM, Meheler LN, Sievert J, Propeck M et-al. Acute Illnesses Associated With Pesticide Exposure at Schools. JAMA. 2005;294:455-65. [ Links ]
45. Prieto-González EA. Deterioro genómico y manipulación genética: desequilibrio en la prioridad de las agendas públicas. Acta Bioethica. 2007;13(2):223-31. [ Links ]
46. Bearer C. How are children different from adults? Environ Health Perspect. 1995;103(Suppl 6):7-12. [ Links ]
47. World Health Organization. Principles for evaluating health risks in children associated with exposure to chemicals. Ginebra: WHO; 2006. [ Links ]
48. Landrigan PJ, Kimmel CA, Correa A, Eskenazi B. Children’s health and the environment: public health issues and challenges for risk assessment. Environ Health Perspect. 2004;112(2):257-65. [ Links ]
49. Perera FP, Ilman SM, Kinney PL, Whyatt RM, Kelvin EA, Shepard P, E. et-al. The challenge of preventing environmentally related disease in young children: community-based research in New York City. Environ Health Perspect. 2002;110(2):197-204. [ Links ]














