Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Pediatría (Asunción)
versión On-line ISSN 1683-9803
Pediatr. (Asunción) v.37 n.1 Asunción abr. 2010
ARTÍCULO ORIGINAL
Acinetobacter en una Sala de Cuidados Intensivos Pediátricos. Nuestra experiencia
Acinetobacter in a Pediatric Intensive Care Ward. Our Experience
Teme C(1), Franco O(1), Weber E(1), Gurrieri A(1), Samudio-D GC(2)
1. Servicio de Terapia Intensiva Pediátrica. Hospital Central del Instituto de Previsión Social. Asunción-Paraguay.
2. Servicio de Infectología. Hospital Central del Instituto de Previsión Social. Universidad Católica Nuestra Señora de la Asunción-Paraguay.
Solicitud de Sobretiros: Dra. Gloria Samudio. E-mail: gsamudio@click.com.py
Artículo recibido en diciembre de 2009, aceptado para su publicación en febrero de 2010.
RESUMEN
Introducción: El Acinetobacter es un cocobacilo Gram negativo, cuya importancia radica en su capacidad para adquirir rápidamente resistencia frente a los antibióticos de amplio espectro y causar brotes de infecciones nosocomiales. Según reporte del WHONET, Servicio de Microbiología del Hospital Central del Instituto de Previsión Social, la incidencia del Acinetobacter en nuestra unidad ha ido en aumento con el correr de los años. La dificultad para el control de este germen radica en su gran capacidad para fijarse y sobrevivir durante largos períodos de tiempo en superficies secas, pero el mecanismo de transmisión más importante son las manos del personal sanitario.
Objetivo: Describir las características clínicas y epidemiológicas de los pacientes con infecciones por Acinetobacter en Unidad de Terapia Intensiva Pediátrica.
Material y Método: Estudio descriptivo y retrospectivo, en el periodo de enero de 2005 a agosto de 2007. Se incluyó a todos los pacientes cuyos cultivos fueron positivos para Acinetobacter.
Resultados: De 18 pacientes, 7 de sexo femenino (39%) y 11 del masculino (61%), la edad promedio fue de 4,7 meses con rango entre 4 días a 15 años. La estancia hospitalaria promedio fue de 44 días (10 a 104 días); todos los pacientes utilizaron catéteres venosos centrales, 4 en promedio (1 a 9 catéteres). Previo al aislamiento del germen, en 16/18 pacientes se utilizó antibióticos de amplio espectro por 8,6 días y ARM (89%) con 12 días en promedio. El germen fue aislado en secreción traqueal 10/18 (55%), hemocultivo 5/18 (28%), punta de catéter 2/18 (11%) y secreción ótica 1/18 (6%). Fueron considerados en 16/18 (89%) gérmenes intrahospitalarios y en 2/18 (11%) provenientes de la comunidad. Fue utilizado como tratamiento Colistina en 7/18 (39%), otros antibióticos-ATB en 9/18 (50%) y sin tratamiento 2/18 (11%). La mortalidad relacionada con la infección fue 17% (3/18) y la no relacionada 6% (1/18).
Conclusión: Los pacientes con ingreso de urgencia a UTI, con tratamiento antibiótico previo, altamente invadidos y aquellos con sepsis previa estarían más predispuestos a sufrir infecciones por Acinetobacter. La presencia de este germen en la UTI debe ser considerado motivo de preocupación por la capacidad de permanecer e infectar por largos períodos de tiempo. Se debe realizar esfuerzos para la identificación de gérmenes nosocomiales, de manera a establecer medidas rápidas de control. Son necesarios más estudios para establecer factores de riesgo en nuestra población.
Palabras claves: Acinetobacter, sensibilidad, pediatría.
ABSTRACT
Introduction: Acinetobacter is a Gram-negative coccobacillus whose importance lies in its ability to rapidly acquire resistance to broad spectrum antibiotics and cause nosocomial outbreaks. According to the WHONET analysis done by the microbiology department of the central hospital of the Institute of Social Security, the incidence of Acinetobacter in our unit has increased over the years. Acinetobacter is difficult to control because it is capable of surviving for extended periods on dry surfaces, although the most important means of transmission is on the hands of medical personnel.
Objective: To describe the clinical and epidemiological characteristics of patients with Acinetobacter infections in the pediatric intensive care unit. Material and Methods: A descriptive and retrospective study done from January 2005 to August 2007. All patients with positive cultures for Acinetobacter were included.
Results: Of 18 patients, 7 (39%) were female and 11 (61%) were male, while the average age was 4.7 months, with a range of from 4 days to 15 years. Average hospital stay was 44 days (10 to 104 days). Patients were catheterized with an average of 4 central venous catheters (1 to 9 catheters). Prior to isolation of the germ, 16 of 18 patients received broad-spectrum antibiotics for 8.6 days and 89% received mechanically assisted ventilation for an average of 12 days. From 10 of 18 patients the bacteria was isolated from tracheal secretions, from 5/18 (28%) from blood cultures, from 2/18 (11%) from catheters and 1/18 (6%) from ear discharge. Bacteria were considered to be hospital-acquired in 16/18 cases (89%) and community-acquired in 2/18 (11%). Treatment was with colistin in 7/18 (39%), other antibiotics in 9/18 (50%) and no treatment was received by 2/18 (11%). Infection-related mortality was 17% (3/18) and unrelated mortality 6% (1/18).
Conclusion: Patients entering the ICU on an emergency basis with widespread infection and prior antibiotic treatment and those with prior sepsis are more prone to infection by Acinetobacter. The presence of Acinetobacter in the ICU should be considered a reason for concern due to its ability to survive and cause infections over long periods of time. Efforts should be made to identify infectious agents found in hospitals to quickly establish means of limiting them. Further study is needed to determine the risk factors for our population.
Keywords: Acinetobacter, susceptibility, pediatrics, hospital infections.
INTRODUCCIÓN
El Acinetobacter es un cocobacilo Gram negativo, no fermentador, aerobio, oxidasa negativo, que sobrevive con gran facilidad en superficies inanimadas colonizando con frecuencia la piel humana (1-4).
Las bacterias que componen el género Acinetobacter fueron identificadas por primera vez en la primera década del siglo XX, pero el papel etiológico que estos microorganismos de distribución universal tienen en la producción de infecciones sólo se descubrió después del advenimiento de los métodos modernos para el control de las infecciones. Antes de la década de 1970 el género Acinetobacter a menudo era de difícil identificación debido a la ausencia de rasgos distintivos. En el curso de los años, el redescubrimiento de estos microorganismos que se encuentran diseminados en todo el mundo, condujo a la creación de numerosos géneros con la correspondiente confusión taxonómica resultante. Hasta 1986 se admitía una especie (Acinetobacter calcoaceticus) con dos subespecies (anitratus e lwoffi ) (1,5).
Posteriormente la diferenciación de las distintas especies se ha realizado a través de métodos fenotípicos, y la clasificación taxonómica actual del género Acinetobacter está basada en técnicas de hibridación ADN – ADN (1,6-8).
Su verdadera importancia radica en la capacidad que posee para adquirir rápidamente resistencia a los antibióticos de amplio espectro y ser responsables de brotes de infecciones nosocomiales incluyendo bacteriemias, neumonías, meningitis, infecciones urinarias, infecciones relacionadas con catéteres intravasculares, abscesos abdominales e infecciones de heridas quirúrgicas (9-10). La dificultad para el control de este germen se halla en dicha capacidad para fijarse y sobrevivir durante largos períodos de tiempo en superficies secas inanimadas (cabeceras de cama, almohadas, mesas, aparatos de ECG, tomas de O2, laringoscopios, grifos de agua corriente, catéteres para angiografía, paños de lavado, respiradores, guantes contaminados, fracción proteica del plasma), pero el mecanismo de transmisión más importante lo constituyen las manos del personal sanitario (9).
Clasificación de las especies de Acinetobacter.
- Acinetobacter calcoaceticus: Especie genómica 1
- Acinetobacter baumannii: Especie genómica 2
- Acinetobacter haemolyticus: Especie genómica 4
- Acinetobacter junii: Especie genómica 5
- Acinetobacter johnsonii: Especie genómica 7
- Acinetobacter lwoffi: Especie genómica 8
- Acinetobacter radioresistens: Especie genómica 12
- Especies Acinetobacter innominadas: >14 otras especies genómicas
Ha sido aislado de numerosas secreciones humanas, como el esputo, la orina, la materia fecal y las secreciones vaginales. Hasta el 25% de los adultos normales presenta una colonización cutánea por Acinetobacter y el 7% de los adultos y los niños de corta edad presentan colonización faríngea transitoria (11).
Estas bacterias constituyen los microorganismos gram negativos persistentes más frecuentemente presentes en la piel del personal hospitalario y se comunicó colonización por éste germen en el 45% de los sitios de traqueostomía en pacientes internados (11,12). Los factores de riesgo específicos para la adquisición de una infección nosocomial consisten en la prolongada estancia hospitalaria, la cirugía, las heridas, la infección previa, el tratamiento previo con antibióticos de amplio espectro, la nutrición parenteral, la presencia de un catéter intravenoso o ureteral permanente, la admisión en una unidad de quemados o UTI y la asistencia mecánica respiratoria (5,13).
Dado que es un germen habitual de la piel, muchos de sus aislamientos en pacientes hospitalizados han sido interpretados como simples colonizaciones. Sin embargo, estudios posteriores sugerían que infecciones tales como las bacteriemias o las neumonías asociadas a ventilación mecánica causadas por Acinetobacter tenían mortalidad atribuible significativa que oscilaba entre el 20 y el 35%. Esta mortalidad podría estar causada por la virulencia intrínseca de esta bacteria o por su elevada resistencia a los antibióticos (6,14).
Las especies de Acinetobacter pueden provocar infecciones purulentas casi en cualquier órgano del cuerpo. Si bien estas bacterias se consideran oportunistas en el ámbito hospitalario, también se comunicaron casos de infección adquirida en la comunidad. El tracto respiratorio es la localización más frecuente de la infección por Acinetobacter debido a la colonización orofaríngea transitoria de personas sanas y el elevado índice de colonización de los sitios de traqueostomía. La neumonía adquirida en la comunidad por lo general afecta a pacientes con un compromiso de los mecanismos de defensa(11,15). La máxima repercusión deriva del papel desempeñado por estas bacterias en la etiología de la neumonía nosocomial, sobre todo los casos asociados con el respirador. La incidencia de bacteriemia es de hasta 8,4% de todos los casos de bacteriemia y se relaciona cada vez con mayor frecuencia a infecciones del tracto respiratorio y el uso de catéteres intravenosos; otros focos menos frecuentes consisten en infecciones urinarias, heridas, la piel y el abdomen. Hasta el 30% de los pacientes con bacteriemias padece shock séptico y el índice de mortalidad oscila entre el 17 y el 46 %(9,16). La bacteriemia por otras especies de Acinetobacter no A. baumannii por lo general es menos severa que la producida por A. baumannii. La meningitis por Acinetobacter es una infección infrecuente, por lo general se observa después de intervenciones neuroquirúrgicas. Las heridas traumáticas, quemaduras y las incisiones quirúrgicas pueden ser colonizadas debido a la facultad de estos microorganismos para desarrollarse en presencia de tejidos inviables y cuerpos extraños. Durante la guerra de Vietnam, fueron los bacilos Gram negativos aislados con mayor frecuencia de las heridas traumáticas contaminadas de las extremidades inferiores (1,2).
La interpretación de los resultados del cultivo requiere considerar la colonización y la contaminación potenciales. El aislamiento del Acinetobacter de pacientes colonizados no es una indicación estricta para la instauración de un tratamiento específico o preventivo. En celulitis o flebitis localizadas asociadas con cuerpo extraño (por ejemplo: un catéter intravenoso o puntos de sutura) por lo general son suficientes la extracción del cuerpo extraño y las medidas locales. Pero en el caso de un síndrome séptico, endocarditis, meningitis, osteomielitis o bacteriemia es necesario administrar un tratamiento antibiótico intensivo sistémico(17).
Los carbapenemes (imipenem y meropenem) continúan siendo el tratamiento de elección para las infecciones en que se sospeche Acinetobacter. Si bien el imipenem sigue siendo un fármaco confiable, los brotes epidémicos provocados por cepas resistentes son motivo de gran preocupación (14,18).
Las polimixinas (metansulfonato de colistina) constituyen un grupo de antimicrobianos antiguos disponibles para su uso desde hace más de 50 años. Trabajos recientes, en su mayoría con pacientes en situación crítica indican que, si bien un cierto grado de toxicidad renal es relativamente frecuente con su uso, la elevación de la creatinina no suele ser excesiva y prácticamente siempre revierte al final del tratamiento; y la neurotoxicidad es infrecuente siempre que se respeten las dosificaciones y se controlen adecuadamente sus concentraciones. La falta de efectos colaterales graves aunado a una falta de otras opciones terapéuticas convierten a este antibiótico en el tratamiento de elección para enfrentar a este germen (6,10,14,19,20).
La prevalencia de gram negativos multirresistentes va en aumento, y no es descartable que se incremente en el futuro a partir de las mismas o de otras especies; la colistina puede desempeñar un papel importante en el tratamiento de las infecciones por estos gérmenes multirresistentes en un futuro próximo (10).
Según reporte del WHONET del Servicio de Microbiología del Hospital Central del Instituto de Previsión Social, la incidencia de Acinetobacter en nuestra Unidad de Cuidados Intensivos ha ido en aumento a través de los años llegando a convertirse en uno de los microorganismos aislados frecuentemente en pacientes internados (21).
OBJETIVO
Describir las características clínicas y epidemiológicas de los pacientes con cultivos positivos a Acinetobacter en la UTIP.
MATERIAL Y MÉTODO
Estudio descriptivo, retrospectivo, en el periodo comprendido de enero de 2005 a agosto de 2007. Se incluyeron todos los pacientes cuyos cultivos fueron positivos para Acinetobacter.
RESULTADOS
Fueron incluidos 18 pacientes con cultivos positivos para Acinetobacter. De ellos: 7 fueron de sexo femenino que correspondió al 39% y 11 del masculino que correspondió al 61%. La edad promedio fue de 4,7 meses con un rango de 4 días a 15 años.
La estancia hospitalaria total de los mismos fue en promedio de 44 días, con un mínimo de días de internación de 10 y un máximo de 104 días.
Todos los pacientes utilizaron catéteres venosos centrales, en promedio de 4 catéteres, con un mínimo de uno y un máximo de nueve catéteres. La permanencia total del catéter fue en promedio de 18 días.
Del total de 18 pacientes, 16 (89%) fueron sometidos a Asistencia Mecánica Respiratoria (ARM). El tiempo promedio de ARM en los pacientes, previo al aislamiento del germen, fue de 12 días con un rango de 1 a 37 días.
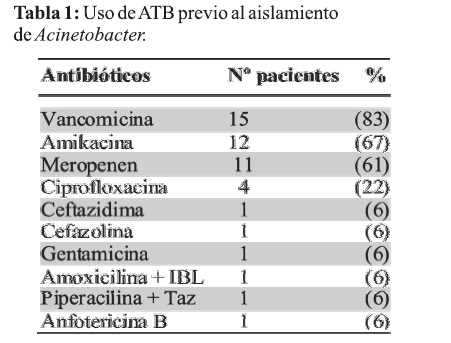
Al investigar sobre el uso de antibióticos de amplio espectro previo al aislamiento del Acinetobacter, se encontró que 16 pacientes (89%) habían utilizado cobertura antibiótica previamente, siendo el promedio de tratamiento de 8,6 días con un mínimo de uno y un máximo de 37 días de tratamiento. El antibiótico más utilizado previamente fue Vancomicina (83%) seguido de Amikacina (67%), Meropenen (61%) y en cuarto lugar Ciprofloxacina (22%) (Tabla 1).
De los gérmenes aislados 2 de ellos fueron tipificados como Acinetobacter Baumannii (11%) y 16 como Acinetobacter sp (89%).
Al investigar el origen del Acinetobacter se asumió ; que dos de ellos eran extrahospitalarios o de la comunidad debido a su alta sensibilidad a los antibióticos comunes y a que fueron aislados el primer día de ingreso de los pacientes. Fueron considerados intrahospitalarios 16 (89%) teniendo en cuenta el patrón de multirresistencia de los mismos y el tiempo de hospitalización del paciente al momento de adquirir la infección, que fue en todos los casos mayor de tres días.
Al determinar el sitio de aislamiento del Acinetobacter en pacientes de UTI (N=18), 10 fueron en secreción traqueal que correspondió a un 55%, 5 en hemocultivo correspondiendo al 28%, colonización de punta de catéter (con hemocultivo negativo) en 2 pacientes (11%), y en secreción ótica en 1 paciente (6%).
Los factores relacionados con el aislamiento del germen, en todos los pacientes fueron, los ingresos de urgencia a la unidad de terapia intensiva, el tratamiento previo con antibióticos, la alta invasividad (catéteres intravenosos, intubación endotraqueal, sondas vesicales.) y la presencia de sepsis previa que se presentó en 16 de los 18 pacientes.
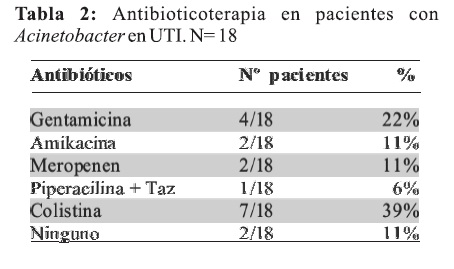
El tratamiento antibiótico (Tabla 2) utilizado fue colistina en 7 pacientes (39%), con otros antibióticos fueron tratados 9 pacientes (50%) entre los cuales figuran Gentamicina en 4 pacientes (22%), Meropenen y Amikacina en 2 pacientes respectivamente (11%) y Piperacilina+Tazobactan uno (6%). Dos pacientes no recibieron tratamiento antibiótico alguno por encontrarse en ellos colonización de punta de catéter ambos casos. Los pacientes a los cuales debió indicarse colistina, por sensibilidad en el antibiograma tuvieron una respuesta adecuada, sin constatarse efectos adversos relacionados a la droga durante su estancia en la UCI.
La mortalidad global fue del 22% (4 pacientes). La mortalidad relacionada con la infección fue del 17% (3 pacientes) y la no relacionada fue del 6% tratándose de un paciente con diagnóstico de Craneofaringioma.
DISCUSIÓN
La Infections Diseases Society of América ha publicado una “lista de choque”, una especie de lista negra orientada para llamar la atención sobre los siete microorganismos considerados más peligrosos existentes en la actualidad: Staphylococcus aureus resistente a la meticilina, Escherichia coli, Klepsiella spp., Aspergillus spp., Enterococcus faecium, Pseudomonas aeruginosa y el Acinetobacter, no sólo por su virulencia sino por ser resistentes a la gran mayoría de los antibióticos disponibles hoy en día (10).
El control y el manejo de las infecciones intrahospitalarias se han constituido desde hace un tiempo, en un problema fundamental para la atención de la salud. Las infecciones adquiridas en los hospitales incrementan la morbi-mortalidad y la estancia hospitalaria; asimismo causan un enorme impacto en relación a los costos. El hallazgo de Acinetobacter en las Unidades de Terapia Intensiva se constituye en un hecho preocupante, pues es sabido que este germen puede persistir por mucho tiempo en los muebles y aparatos médicos, (5) y si bien en esta serie no fueron cultivadas muestras de los implementos mencionados, su persistencia a través del tiempo obliga a sospechar que esta situación no sea ajena a nuestra Unidad.
Pocos de nuestros pacientes presentaron infección de origen comunitario en nuestra serie y fueron los que respondieron rápidamente a antibioticoterapia de espectro reducido, con una importante diferencia de aquellos que lo adquirieron en el ámbito hospitalario (6,14).
La colistina fue empleada en los casos en que el germen fue sensible sólo a este antibiótico, sin reportarse efectos adversos, ubicando nuevamente a esta droga en el campo de los antibióticos seleccionables para tratar infecciones de este tipo. En coincidencia con otros autores, (2,6) tampoco hemos encontrado efectos adversos, aunque el número de pacientes es muy reducido para establecer la seguridad absoluta en el uso de esta droga en pediatría. Nuevos trabajos dirigidos específicamente a la eficacia y seguridad de este fármaco son necesarios para establecer datos certeros acerca de su uso los niños.
Se sabe por otra parte que las cifras de mortalidad dependen del tipo de pacientes afectados por este germen y que por tratarse de pacientes graves internados en terapia intensiva, sometidos a múltiples procedimientos, es llamativa una mortalidad atribuida a la infección de tan sólo 17%, por debajo de lo reportado en otras series (10).
Sólo aquellas medidas que influyan sobre el lavado correcto de manos, uso de guantes individuales por paciente, limpieza exhaustiva de materiales inertes, aislamiento temporal de pacientes afectos y concientización de todo el personal, han mostrado ser eficaces en el control de este microorganismo, así como la necesidad de establecer políticas en el uso racional de antibióticos asumidas por el personal facultativo (12,22).
Tal vez el agente terapéutico más activo en las actuales circunstancias pudiera ser la Colistina, un antibiótico considerado de la “vieja guardia” que fuera abandonado prematuramente debido a su toxicidad renal; hoy recuperado para su utilización en base a las nuevas evidencias científicas a su favor (4,10).
CONCLUSIÓN
Los pacientes con ingresos de urgencia a la UTI, con tratamiento antibiótico de amplio espectro previo, altamente invadidos y aquellos con diagnóstico previo de sepsis estarían más predispuestos a sufrir infecciones por Acinetobacter. La presencia de este germen en la UTI debe ser considerado motivo de preocupación por la capacidad de permanecer e infectar por largos períodos de tiempo.
Se deben realizar esfuerzos tendientes a la identificación de los gérmenes nosocomiales, de manera a instituír medidas rápidas de control.
Son necesarios más estudios para establecer factores de riesgo en nuestra población.
REFERENCIAS
1. Allen D, Hartman B. Especies de acinetobacter. En: Mandell D. Enfermedades infecciosas: principios y práctica. 5ta ed. Buenos Aires: Médica Panamericana; 2002.p. 2840-845.
2. Diomedi A. Infecciones por acinetobacter baumanii resistente: consideraciones epidemiológicas y de manejo antimicrobiano actualizado. Revista Chilena de Infectología. 2005;22(4):298- 320.
3. López-Brea M, Alarcón T, López S. Consideraciones microbiológicas y terapéuticas de la infección por acinetobacter spp. Revista Española de Quimioterapia. 1998;11(2):21-25.
4. Villers D, Espaze E, Coste-Burel M. Nosocomial acinetobacter baumanii infections. Microbiological and Clinical Epidemiology. 1998;129(3):182-89.
5. Suresb J, Geetanjali L, Meenakshi S. Clinical and demografic features of infection caused by acinetobacter species. Indian Journal of Medical Sciences. 2006;60(9):351-60.
6. Garnacha J. Tratamiento antibiótico de las infecciones graves por acinetobacter spp. Revista Electrónica de Medicina Interna. 2004;4(6):9-14.
7. Álvarez-Lerma F, Palomar M, Olaechea P. Estudio nacional de vigilancia de infección nosocomial en Unidades de Cuidados Intensivos: informe evolutivo. Med Intensiva. 2007; 31 (1): 6-17. [ Links ]
8. Álvarez-Lerma F, Palomar M, Insausti J. Enfermedades infecciosas y microbiología clínica. Med Intensiva. 2005;23(9):533 -539.
9. Salas J, Cabezas T, Álvarez R. Infección/colonización nosocomial de las vías respiratorias por acinetobacter baumannii en una planta de Medicina Interna. Anales de Medicina Interna. 2002;19(10):511-14.
10. Trujillo G. Acinetobacter baumannii problemático y además multirresistente. Colombia: Editorial Asociación Colombiana de Infectología; 2006.
11. Cisneros J, Garnacho-Montero J. Neumonía nosocomial por acinetobacter Baumanii. Enfermedades Infecciosas y Microbiología clínica. 2005;23(3):46-51.
12. Cisneros J, Pachón J. Acinetobacter baumannii: un patógeno nosocomial de difícil control. Enfermedades Infecciosas y Microbiología clínica. 2003;21(5):221-23.
13. Prashanth K, Bradrinath S. Nosocomial infections to acinetobacter species: clinical findings, risk and prognostic factors. Indian J Med Microbiol. 2006;24(1):39-44.
14. Oliver A. Resistencia a carbapenems y acinetobacter baumanii. Enfermedades Infecciosas y Microbiología Clínica. 2004;22(5):259-61. [ Links ]
15. Medina J, Formento C,Pontet J. Factores de riesgo para desarrollar neumonía asociada a ventilación por acinetobacter spp. Revista Médica del Uruguay. 2002;18(3):256-64. [ Links ]
16. Domínguez M, Sepúlveda M, Bello H. Aislamiento de acinetobacter spp desde muestras clínicas en el Hospital Clínico Regional Guillermo Grant Benavente. Revista Chilena de Infectología. 2007;17(4):321- 25.
17. Ireghu K, Ogunsola F. Infections caused by acinetobacter species and their susceptibility to 14 antibioties in Lagos University Teaching Hospital. West African Journal of Medicine.2002;21(3):226-29.
18. Oliveira-de-Pontes U, Menezes E, Cunha F.Perfil de resistencia de acinetobacter baumannii a antimicrobianos nas Unidades de Terapia Intensiva a Semi - Intensiva do Hospital General de Fortaleza. RBAC. 2006;38(2):123-26.
19. Chang P, Hsueh R, Sheng P. Multidrug-resistant acinetobacter baumanii isolates in pediatric patiens of a University Hospital of Taiwán. J Microbiol Inmunol Infect. 2007;40:406-10.
20. Muñoz JL, García JA. Colistimetato: un viejo antimicrobiano recuperado por nuevas evidencias científicas. Revista Española Quimioterapia. 2005;18(1):11-13.
21. WHONET. Revista Electrónica. Servicio de Microbiología del H.C. I.P.S; 2006. [ Links ]
22. Tapia R, Sepúlveda G. Brote de neumonía nosocomial por acinetobacter baumannii asociado a procedimientos de apoyo respiratorio en un Servicio de Medicina Interna. Clínica y Ciencia, Chile. 2002;1(4):40-42. [ Links ]














