INTRODUCCIÓN
En diciembre de 2019, varios servicios de salud de China continental, informaron la presencia de pacientes con neumonía de etiología desconocida y que estaban vinculados epidemiológicamente con un mercado de mariscos y otros animales en Wuhan, provincia de Hubei. El brote se extendió rápidamente por todo el mundo. En marzo del 2020, la Organización Mundial de la Salud (OMS) declaró el nacimiento de una nueva pandemia por coronavirus al que se denominó COVID-19, que hasta el 6 de diciembre de 2021 se habían reportado 266.041.035 casos y 5.259.026 fallecidos alrededor del mundo1,2.
En Paraguay, el primer caso confirmado fue reportado el 7 de marzo de 2019 y para diciembre del 2021, se confirmaron 463.260 casos y 16.476 óbitos. Al inicio de la pandemia, las medidas de prevención estaban basadas exclusivamente en las llamadas medidas no farmacológicas, como el lavado de manos y el distanciamiento social. En el ámbito de los servicios de salud, considerados de mayor riesgo, las medidas de protección se basaban en el abastecimiento y uso adecuado de los equipos de protección personal, además de las ya citadas medidas no farmacológicas. En este escenario, el país se encontraba saliendo de una epidemia de dengue que había golpeado fuertemente los servicios, apenas se estaban recuperando y había que hacer frente a la nueva situación mundial, sin prácticamente recursos económicos, que, si los hubiera, no se podía obtener debido al desabastecimiento a nivel mundial3-5.
La principal función de las vacunas es la de otorgar protección contra el patógeno hacia el cual está dirigido, y es una de las estrategias de salud pública más eficaces. Cambia los escenarios de cualquier evento en donde esté relacionado alguna enfermedad prevenible por vacunas y deberían ser siempre accesibles y asequibles. Prácticamente, desde el inicio de la pandemia de la COVID-19, los países con la estructura y los medios han iniciado la carrera para la producción de vacunas y a casi dos años se han desarrollado más de 200 vacunas, las que se encuentran en diferentes etapas de aprobación para su uso6,7.
El 30 de diciembre del 2020 se lanzó el Plan Nacional de Vacunación contra la COVID-19 con el propósito de desarrollar el componente de vacunación como parte de las intervenciones farmacológicas para el control y la prevención de la COVID-19. En febrero del 2021, había 41 vacunas en fase I, 22 en fase I/II, 20 en fase III y ocho estaban aprobadas para uso de emergencia, que eran la Pfizer/BioNTech, Moderna, AstraZeneca, Sinovac, Sinopharm, Sputnik V, Cansino y vacuna a virus inactivado del Instituto de Wuhan, China. Ante este escenario, el Plan de Vacunación del Paraguay prioriza a la población meta en tres grupos, inicialmente; el primero constituido por personal de salud y adultos mayores de 60 años; en el segundo grupo, personas de 18 a 59 años con enfermedad de base, docentes de nivel inicial y primaria, trabajadores de servicios esenciales y población indígena; como tercer grupo prioritario los trabajadores de aeropuertos y puntos de entrada del país y personas privadas de libertad, teniendo una meta de vacunación del 80% de la población prioritaria8,9.
El Plan Nacional también contempla la vigilancia de eventos supuestamente atribuibles a la Vacunación o inmunización (ESAVI), que tiene como objetivo vigilar la seguridad de la vacuna contra la COVID-19 a través de la notificación, investigación y clasificación de dichos eventos. Todo medicamento, incluidas las vacunas, pueden causar efectos adversos leves, moderados o graves y desde el Programa de inmunizaciones conjuntamente con la Dirección Nacional de Vigilancia Sanitaria (DINAVISA) realizan el seguimiento y monitoreo de las notificaciones de los ESAVI. Estos eventos se clasifican según su severidad en no grave y grave. Todos los casos deben ser notificados o reportados, para lo cual se ha dispuesto un apartado en la página del Ministerio de Salud Pública y Bienestar Social (MSPyBS) que está enlazado con el Sistema Nacional de Farmacovigilancia que conduce a una ficha de notificación, donde se colecta información sobre el evento8,10,11.
El objetivo del presente trabajo fue determinar los efectos adversos más comunes en las vacunas contra el COVID-19 aplicadas en el Paraguay en el año 2021.
MATERIAL Y MÉTODO
Se realizó un estudio descriptivo, analítico de corte transversal; para la colecta de información se efectuó una encuesta online mediante la aplicación de “Google Forms” difundida por las plataformas WhatsApp, Facebook, Instagram y Twitter, durante la semana comprendida entre el 29 de septiembre al 07 de octubre del 2021, en cuyo encabezado se explicaba el propósito del trabajo.
La encuesta recogía datos socio-demográficos como: edad (años cumplidos), sexo, departamento de residencia (Concepción, San Pedro, Cordillera, Guairá, Caaguazú, Caazapá, Itapúa, Misiones, Paraguarí, Alto Paraná, Central, Ñeembucú, Amambay, Canindeyú, Presidente Hayes, Boquerón, Alto Paraguay, Capital, precargados en el cuestionario.
Los datos relacionados con las vacunas fueron, tipo de vacuna/plataforma recibida (Sputnik V, AstraZeneca, Covaxin, Sinopharm, Sinovac (CoronaVac), Pfizer, Moderna, Jansen), dosis recibidas, signos y síntomas presentados con la primera y segunda dosis aplicadas.
Los datos recolectados fueron extraídos del formulario Google a una planilla Excel; fueron analizados por estadística descriptiva en Epi Info 7.2.5.0; según el tipo de variable; para contrastar las variables categóricas se utilizó la prueba de chi cuadrado o la prueba exacta de Fisher en caso necesario. El nivel de significación estadística adoptado para todas las pruebas de contraste fue p < 0,05 y la asociación entre variables fue medida por la Odd Ratio (OR). Los resultados se presentaron en tablas que fueron elaboradas en Excel 2007-2013.
RESULTADOS
Respondieron la encuesta 641 personas con un promedio de edad de 27 años ± 13 años, 69% del sexo femenino, 54% del departamento Central. El 75% recibió las dos dosis, 56,3% de las personas tuvieron alguna reacción adversa con la primera dosis y el 45,7% con la segunda.
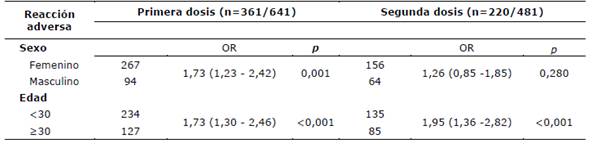
Hubo significativamente mayor reacción adversa en las mujeres y en los menores de 30 años de edad con la primera dosis (p< 0,001). Con la segunda dosis mayor proporción de participantes menores de 30 años tuvieron reacción adversa (p< 0,001). La frecuencia de efectos adversos con la primera dosis fue de 56,3% (361/641) y 31,8% (220/484) en la segunda dosis. Tabla 1
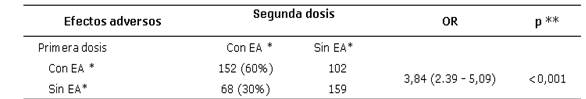
En cuanto a los efectos adversos y dosis aplicadas, aquellos que presentaron EA en la primera dosis tuvieron casi cuatro veces más chance de presentar efectos adversos también en la segunda dosis. Tabla 2.
Se analizaron los EA por plataforma aplicada, tanto en la primera como en la segunda dosis; en primeras dosis, la chance de presentar EA se asoció a la plataforma Sputnik V (OR=1,69; IC95% 1,14 - 2,51; p=0,01); mientras que, en segundas dosis, la chance de presentar EA se asoció a la plataforma Pfizer (OR = 1,88; IC95% 1,31 - 2,71; p=0,0008). Tabla 3.
Tabla 3. Reacciones adversas según plataforma aplicada
| Plataforma | Primera dosis (n=641) | Segunda dosis (n=481) | ||||
|---|---|---|---|---|---|---|
| Si | OR | p | Si | OR | p | |
| Pfizer | 168/361 (47%) | 0,78 (0,5-1,07) | 0,156 | 134/252 (53%) | 1,88 (1,31-2,71) | 0,0008 |
| Sputnik | 92/139 (66%) | 1,69 (1,14-2,51) | 0,010 | 28/60 (47%) | 1,03 (0,60-1,78) | 1,000 |
| AstraZeneca | 59/99 (60%) | 1,17 (0,75 -1,81) | 0,545 | 24/91 (26%) | 0,35 (0,21-0,58) | 0,000 |
| Moderna | 18/34 (53%) | 0,86 (0,43-1,73) | 0,817 | 17/27 (63%) | 2,10 (0,94 -4,69) | 0,098 |
| Covaxin | 13/26 (50%) | 0,76 (0,34 -1,68) | 0,644 | 11/26 (42%) | 0,86 (0,38 -1,92) | 0,873 |
| Hayat vax (SINOPHARM) | 4/11 (36%) | 0,43 (0.12 -1,50) | 0,149 | 3/11(27%) | 0,86 (0,38 -1,92) | 0,439 |
| Jassen | 2/3 (67%) | 1,55 (0,14 - 17,22) | 0,594 | - | ||
| Sinovac (CORONAVAC) | 5/14 (36%) | 0,42 (0,14 -1,27) | 0,097 | 3/11 (27%) | 0,31 (0,08 -1,14) | 0, 054 |
Observando los efectos adversos por dosis recibidas de las vacunas, la Pfizer, la Sputnik V y la AstraZeneca presentaron una variedad de sintomatologías; sin embargo, se distinguieron algunos eventos adversos que se presentaron con mayor frecuencia en todas las vacunas como fiebre, fatiga, dolor muscular/articular, dolor e hinchazón en el lugar de la inyección y dolor de cabeza, también se encontró EA menos frecuentes como diarrea, tos y disminución de apetito que solamente se presentaron en las vacunas mencionadas anteriormente. Tablas 4 y 5
Tabla 4. Signos y síntomas referidos por los encuestados en la primera dosis por plataforma
| Signos/síntomas | Pfizer | Sputnik | AstraZeneca | Moderna | Covaxin | Hayat Vax | Sinovac | Janssen |
|---|---|---|---|---|---|---|---|---|
| n= 315 | n= 139 | n=99 | n=34 | n=26 | n=11 | n=14 | n=3 | |
| n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | |
| Dolor e hinchazón en el sitio de aplicación | 112(36) | 39 (28) | 15(15) | 13(38) | 5(19) | 1(9) | 9(64) | 1(33) |
| Fatiga | 57(18) | 40(29) | 21(21) | 3(9) | 2(8) | 1(9) | 2(14) | 1(33) |
| Dolor de cabeza | 51(16) | 49(29) | 22(22) | 5(15) | 4(15) | 1(9) | 3(21) | 1(33) |
| Dolor muscular/articular | 47(15) | 47(34) | 26(26) | 6(18) | 3(12) | 1(9) | 3(21) | 1(33) |
| Fiebre | 36(11) | 38(27) | 28(28) | 5(15) | 2(8) | 1(9) | 0 | 1(33) |
| Somnolencia | 21(7) | 11(8) | 10(10) | 2(6) | 2(8) | 0 | 0 | 0 |
| Escalofríos | 15(5) | 32(23) | 18(18) | 1(3) | 2(8) | 0 | 0 | 1(33) |
| Otros* | 74(23) | 72(52) | 23(23) | 5(15) | 15(58) | 2(18) | 0 | 1(33) |
* alergia, arritmia, disminución del apetito, inflamación, enrojecimiento, náuseas, mareos, sudoración y tos.
Tabla 5. Signos y síntomas referidos por los encuestados en la segunda dosis por plataforma
| Signos/Síntomas | Pfizer | Sputnik | AstraZeneca | Moderna | Covaxin | HayatVax | Sinovac |
|---|---|---|---|---|---|---|---|
| n=250 | n=60 | n=91 | n=26 | n= 13 | n= 11 | n= 14 | |
| n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | n° (%) | |
| Dolor e hinchazón en el sitio de aplicación | 68 (27) | 13(22) | 4 (4) | 7 (27) | 5 (38) | 2 (18) | 1 (7) |
| Fatiga | 54 (22) | 13(22) | 6 (7) | 7 (27) | 6 (46) | 1 (9) | 3 (21) |
| Dolor de cabeza | 41 (16) | 10(17) | 11 (12) | 6 (23) | 4 (31) | 1 (9) | 0 |
| Dolor muscular/Articular | 37 (15) | 10(17) | 10 (11) | 9 (35) | 5 (38) | 0 | 0 |
| Fiebre | 34 (14) | 8 (13) | 5 (5) | 6 (23) | 1 (8) | 1 (9) | 0 |
| Somnolencia | 17 (7) | 6(10) | 2 (2) | 5 (19) | 2 (15) | 1 (9) | 1 (7) |
| Escalofríos | 22 (9) | 4 (7) | 3 (3) | 3 (12) | 0 | 0 | 0 |
| Otros * | 55 (22) | 17 (28) | 6 (7) | 15 (58) | 5 (38) | 0 | 0 |
*alergia, arritmia, disminución del apetito, inflamación, enrojecimiento, náuseas, mareos, sudoración y tos.
DISCUSIÓN
Las medidas preventivas para limitar la transmisión del SARS-CoV-2 se han implementado a nivel global desde el inicio de la pandemia del COVID-19. La vacunación fue implementada a fines del 2020. La Administración de Drogas y Alimentos de los EEUU autorizó dos vacunas de ARN para usos de emergencia y en febrero de 2021, vacunas con vector viral 12. Paraguay inició la vacunación el 22 de febrero con el personal de salud de primera línea, es decir, que están involucrados en la atención directa a los pacientes con COVID 1913.
Una prueba de que las vacunas activan al sistema inmunitario es la aparición de los efectos secundarios que siguen a la aplicación de las mismas. Estos efectos van desde efectos leves hasta graves, por lo que la aplicación de los biológicos puede causar temor entre la población. Sin dudas, cualquier vacunación inducirá efectos secundarios transitorios debido a la respuesta inmunitaria activada y al traumatismo del tejido en el lugar de la inyección. Los efectos adversos se clasificaron como locales, sistémicos y alérgicos dependiendo de la de la severidad de la respuesta (14.
En el estudio se ha identificado diferencias significativas en la presentación de efectos secundarios a la vacunación en relación con los sexos y las dosis. Los varones y las mujeres responden de manera diferente a la vacunación. Las diferencias biológicas, como las hormonas endocrinas y sexuales, juegan un papel importante en la alta respuesta de las mujeres a las vacunas bacterianas y virales. También se han observado variaciones de acuerdo al sexo en la farmacocinética y la farmacodinámica, siendo las mujeres más susceptibles a los efectos adversos. Estos efectos se han atribuido a que las mujeres tienen un porcentaje de grasa corporal más significativo que los hombres, lo que afecta el volumen de distribución y eliminación de los medicamentos (15-17.
Se encontraron diferencias significativas en la presentación de efectos adversos entre la primera y segunda dosis, que difieren de otros trabajos. Según una revisión sistemática, después de la segunda dosis hubo mayores efectos adversos que la primera. Los efectos secundarios promedio después de la primera dosis fueron del 79 % y del 84 % después de la segunda dosis. Al comparar la segunda y la primera dosis de la vacuna, un estudio publicado por la Administración de Drogas y Alimentos de los EE. UU. indicó que la incidencia de efectos adversos locales fue algo mayor después de la segunda dosis. Abu Hammad et al. demostraron que los efectos adversos eran más frecuentes después de la segunda dosis. Según Elnaem et al., alrededor del 40 % de los efectos adversos ocurrieron con mayor frecuencia con la segunda dosis, especialmente en quienes recibieron la vacuna Pfizer-BioNTech frente a quienes recibieron la vacuna Sinovac o AstraZeneca18-20.
A principios de enero del 2021, la Agencia Europea del Medicamento habían aprobado el uso de tres vacunas Pfizer/BioNtech, AstraZeneca y Moderna con niveles de seguridad y eficacia adecuados, confirmando que no se presentaron efectos adversos graves en las personas vacunadas (6,21-23. En un estudio transversal realizado en Arabia Saudita en el 2021, donde un poco más del 80% había recibido Pfizer y reportaron dolor local en 79,3%, dolor articular 23,1, dolor de cabeza 21,8 %, fiebre 21,0 %, escalofríos 15,5 %, enrojecimiento en el sitio de la inyección 14,8%. Además, ninguno refirió una reacción grave, concordando con los hallazgos en este trabajo.
Una revisión sistemática mostró que el 50% de los encuestados, refirieron haber recibido Pfizer, 27,1% SINOVAC y el 19,3 % AstraZeneca; el 76,8% experimento efectos adversos, 40% en la segunda dosis, 61,1% en el lugar de la inyección, y 48,8 % cansancio, resultado que concuerda, en cierta medida con los hallazgos de este trabajo. Entre los efectos adversos sistémicos se cita el dolor muscular en el 39,67% de los encuestados, 33,27 presentaron dolor de cabeza, 25,75% dolor articular, 18% fiebre, entre otras manifestaciones18.
La vacuna AstraZeneca, fue la que presentó fiebre y dolores musculares entre sus efectos adversos, todos clasificados como leves. Se ha informado, en un primer momento, la aparición de un efecto secundario real, aunque raro, que consistía en un trastorno inusual de la coagulación, principalmente en personas jóvenes, por lo que varios países desaconsejaron su utilización. Hasta el 30 de mayo del 2021, España ha reportado 21 casos de síndrome de trombosis con trombocitopenia, con cinco óbitos y una tasa de 4 por cada millón7,24.
En cuanto a la vacuna Sputnik, más de la mitad presentó dolor de cabeza y dolor corporal, ninguno refirió síntomas respiratorios, como encontró Logunov en un ensayo aleatorizado de fase 3, realizado en Rusia y en otro estudio realizado en Buenos Aires que incluyo a 660.000 personas mayores de 60 años, donde más del 60% habían sido inmunizados con dicha vacuna, se evidencian que la fiebre acompañada de cefalea y o mialgias son las manifestaciones más frecuentes en 38,46% de los vacunados23-26.
Cuando las ventajas de la vacunación se comparan con los riesgos de contraer una infección grave por COVID-19 o desarrollar lo que parecen ser efectos secundarios a corto plazo, en gran medida leves o moderados, los beneficios superan significativamente los riesgos. Los resultados deberían tranquilizar al público de que los beneficios de la vacunación superan con creces los riesgos y ayudarán a reducir la vacilación de la vacuna entre las personas preocupadas por la seguridad de la vacuna y los posibles efectos adversos.
En conclusión, los hallazgos este estudio indican que las reacciones adversas a la vacuna Pfizer-BioNTech COVID-19 son comunes, generalmente leves y autolimitadas. Nadie reportó shock anafiláctico o respuestas alérgicas graves. Los efectos adversos locales ocurren más que los sistémicos. El efecto adverso local que ocurre con mayor frecuencia es el dolor en el lugar de la inyección y la hinchazón local.