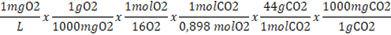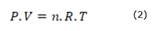INTRODUCCIÓN
La producción de biocombustibles, se basa principalmente en productos de uso alimenticio, generando esto un conflicto a la hora de utilizar los mismos y la utilización de combustibles fósiles, la principal causante de CO2 en el ambiente, dos razones por las cuales es importante explorar fuentes alternativas que contrarresten está problemática. El Boletín de la OMS sobre los Gases de Efecto Invernadero (WMO, 2019) ha mostrado que la concentración media anual mundial de dióxido de carbono (CO2) alcanzó las 407,8 partes por millón (ppm) en 2018, tras haber sido de 405,5 ppm en 2017; Por eso la importancia de realizar estudios de fuentes alternativas, tales como los biocombustibles, que tienen procesos de obtención, sobre todo, sustentables y sostenibles. Sin embargo, en la mayoría de los casos, la producción de biocombustibles utiliza como insumo principal, productos que forman parte del mercado alimenticio, compitiendo directamente con este último (Zarini, 2011). Los diferentes insumos para la producción de biocombustibles, entre los que se destacan la caña de azúcar, el trigo, girasol y soja, representan una de las causas del incremento de los precios de los alimentos a nivel mundial. De ahí surge la producción de biodiesel a partir de otras alternativas, como es el caso del cultivo y procesamiento de microalgas, pudiendo tener así mayor cantidad del mismo, por menos espacio, en comparación a cultivos, siendo las microalgas de fácil adaptación a las condiciones ambientales expuestas. insistir en su capacidad de absorber CO2.
El uso de los reactores raceway ya ha sido estudiado para la producción de biomasa de varias microalgas, especialmente las variables de temperatura, medios nutritivos y el pH, a distintos tiempos. Utilizando un reactor raceway de 4,55m x 1,30m x 0,50m (3 m3) de largo, ancho y alto respectivamente, se observó en promedio un 308,4 mg/L de crecimiento de biomasa de Chlorella vulgaris en un rango de temperatura entre 24°C y 34°C, con un pH entre 7 y 9, con iluminación proveniente de la luz natural, además de utilizar como medio de cultivo una solución que contenía NPK en proporción 16-20-0 (Matanguihan, y otros, 2020).
En China se ha utilizado el reactor raceway para analizar la capacidad de Chlorella vulgaris para remover fósforo y amonio en orina de cerdo pretratada, donde se utilizó un reactor raceway de 0,80m x 0,20m x 0,15m (0.024 m3) de largo, ancho y alto, respectivamente, Se observó una producción de biomasa de 1,287 mg/L, con medio de cultivo BG11 adaptado con orina de cerdo, con pH ajustado a 6, con rango de temperatura de entre 27 °C a 33 °C y un rango de luz de entre 700 Lux a 5000 Lux (Zou, y otros, 2020). En otro estudio hecho en Argelia, utilizando Chlorella pyrenoidosa con un reactor raceway 1,5m x 0,6m x 0,4m (0,36 m3) de largo, ancho y profundidad respectivamente de dónde las condiciones de temperatura iban de 18-31 °C durante el día, y de 6-15 °C durante la noche. Como medio se utilizó agua residual, con pH inicial de 7,8. Bajo estas condiciones se obtuvo una biomasa de 1,71 g/L (Siham, Djamal, Luveshan, Ismail, & Faizal, 2016). Estudio realizado en Tailandia con Chlorella JPR-1, se obtuvo un máximo de 5,8 g/L de biomasa, con una administración de flujo de aire de 0,5 vvm con 10 % de CO2. Esto se realizó en un reactor de 0,4m3, con medio de cultivo M4N, a temperatura constante de 30°C, con pH inicial de 5,5 realizado durante 7 días (Kumoro, Hadiyanto, & Susanto, 2013).
Solo existen antecedentes de la producción de Chlorella a nivel de laboratorio en Paraguay en condiciones controladas y a pequeña escala. Es por eso que se realiza un estudio de campo para observar el comportamiento de Chlorella vulgaris en la producción de biomasa bajo condiciones ambientales naturales del Paraguay, es importante considerar las condiciones ambientales de la bibliografía citada anteriormente.
MATERIALES Y MÉTODOS
Diseño del biorreactor I
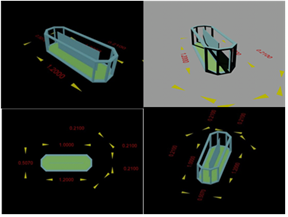
El biorreactor I consistió en una pecera de vidrio con espesor de un (1) cm, de 54cm x 20cm x 30cm de largo, ancho y alto respectivamente (Figura 1), a la cual se le colocó una lámina de vidrio de 20 cm altura y 34 cm de largo en la parte central, además de 4 láminas en las esquinas de 10 cm de ancho y 20 cm de altura, para que el medio pueda circular, y no quede estancado.
Diseño y construcción del biorreactor II
Las dimensiones del reactor fueron tomadas del trabajo de (Sanchez, González, Maceiras, Cancela, & Urrejola, 2011), con ligeras modificaciones. El modelo original poseía un ancho de 40 cm, un largo de 140 cm y una altura de 40 cm. Las dimensiones utilizadas para el ancho, largo y alto son de 50 cm, 150 cm y 40 cm respectivamente. Se decidió aumentar las dimensiones para que las algas tengan mayor superficie de contacto con la luz. El modelo inicial poseía una capacidad de aproximadamente unos 210 L, mientras que este modelo posee una capacidad de unos 280 L, es decir, un aumento aproximado de un 33%.
Obtención de la cepa de Chlorella vulgaris
La cepa fue donada por la encargada del laboratorio de Hidrobiología de la Facultad de Ciencias Exactas y Naturales (FACEN) de la Universidad Nacional de Asunción (UNA), Lic. Melissa Dos Santos. Las cepas se encontraban en dos (2) frascos de 100ml.
Cultivo y conservación del inóculo en el laboratorio.
Al inicio, se utilizaron dos (2) frascos de 100 ml que contenían las microalgas, que luego fueron vertidos en dos (2) erlenmeyer de 500 ml, donde se mantuvieron con aireación constante con una bomba de aire para acuarios, y la iluminación se realizaba con luz artificial mediante un foco de 15 watts, durante tres (3) semanas.
De cada erlenmeyer utilizado para conservar los cultivos, se tomó 250 mL para distribuirlos en cuatro (4) kitasato de un (1) L, donde permanecieron con aireación constante y luz artificial durante un mes. Las microalgas fueron alimentadas con fertilizante NPK (Nitrógeno, fósforo y potasio) 20 20 20 (Aminoleaf 600), con una concentración de 1,5 g/L en agua destilada.
Se seleccionó uno de los kitasato y se colocó los 1 (un) litro en el biorreactor I, una vez realizada la inoculación, se duplicó el volumen de inoculación y cada siete (7) días, se le agregaba 600 ml de medio NPK 20 20 20 al biorreactor I, hasta alcanzar los 10 litros.
Los 10 litros se pasaron a un bidón de 20 litros, siendo aireado por burbujeadores. Cada semana se le suministraba un (1) litro de medio fresco preparado con el mismo fertilizante en agua destilada. Una vez que se llegó a los 20 litros, cada semana se extraían dos (2) litros del medio y se colocaban en otro bidón de 20 litros, reponiendose con otros dos (2) litros de medio fresco al bidón del cual se extrajo inicialmente. Se realizó este proceso hasta conseguir cuatro (4) bidones del mismo volumen, teniendo en total 80 litros, los cuales se trasladaron al biorreactor II. El mismo era suministrado con dos (2) L de medio fresco por día, preparado de la misma manera, con 1,5 g de fertilizante NPK 20 20 20, en un (1) litro de agua mineral para este caso.
Sistema de agitación
Para la agitación en el biorreactor I, se utilizó un agitador axial doble, que trabajaba a 140 rpm, con una inclinación aproximada de 40° sobre la pecera. La agitación en el reactor II se realizaba con una bomba de 4500 L/h de caudal y de 55W, reforzado con otra bomba con caudal de 750 L/h de 12 W, colocado del lado contrario a la primera bomba, para reforzar la circulación, durante 24 horas.
Sistema de iluminación
Para los cultivos en escala laboratorio, se utilizó un foco led de 15 W con 1530 lm colocado a un costado de los erlenmeyer. El biorreactor I utilizado fue puesto dentro del laboratorio de investigación, a un costado de la mesada, de manera a que se encuentre cerca de la ventana para poder recibir así la luz solar. En el caso del biorreactor II, se colocó en un lugar abierto, pero con techo, para recibir mucha fuente de luz y a la vez estar cubierto de posibles problemas con el clima.
Diseño para la recolección de datos
La recolección de datos de los distintos parámetros, en ambos reactores, fueron realizados con componentes de Arduino; los parámetros monitoreados fueron los siguientes: temperatura del ambiente, humedad del ambiente, pH, oxígeno disuelto, turbidez e intensidad lumínica. Los componentes utilizados fueron los siguientes:
Módulo RTC DS3231 (registro de tiempo)
Módulo sensor fotoresistivo OPAMP LM393 (sensor de intensidad lumínica)
Kit analógico de pH (sensor de pH)
Módulo DHT11 (sensor de temperatura y humedad ambiental)
Sensor de turbidez analógico SN0189 (sensor de turbidez)
Kit de Medidor/Sensor Analógico de Oxígeno Disuelto RB-Dfr-781 (sensor de oxígeno disuelto)
Todos los parámetros eran registrados cada 30 min en el software de Arduino, y al término de cada día los valores eran copiados a planillas de Excel.
TRATAMIENTO DE LOS DATOS
Para el tratamiento estadístico se consideraron como principales enfoques al análisis de resultados por coeficiente de correlación, luego se procedió a la interpretación de resultados estadísticos descriptivos como las medidas de tendencia central que son la media, la moda y la mediana, y las medidas de dispersión, la varianza, el máximo, el mínimo, rango y desviación estándar. Los tratamientos se realizaron con el software Excel, añadiendo el complemento de “Análisis de datos”. Para el caso de la correlación de coeficientes, se tomaron en cuenta aquellas correlaciones que tuvieron un valor por encima 0,50 y aquellas por debajo de -0,50, considerándose como correlaciones significativas. Estas consideraciones según Cohen, 1988.
RESULTADOS
ANÁLISIS DE LOS FACTORES Y CONDICIONES DE LA CHLORELLA VULGARIS EN EL BIORREACTOR TIPO RACEWAY.
Análisis de correlación entre variables.
En las siguientes tablas se muestra el grado de relación que se obtiene comparando cada variable entre sí. Los valores van desde el -1 hasta 1. Primeramente, se tienen los gráficos realizados en el biorreactor I, realizadas en los meses de octubre, noviembre y diciembre del año 2019, siendo en total 12 semanas de mediciones. Posterior a eso se tienen los gráficos del biorreactor II de escala mayor realizados en los meses de febrero, marzo y abril del año 2021, en total se tienen ocho (8) semanas.
Biorreactor I
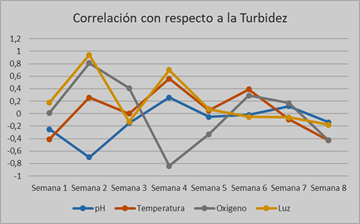
Durante las primeras tres (3) semanas se observa una correlación fuerte entre la turbidez y el oxígeno, a partir de la cuarta semana existe poca correlación. De igual manera, se observa una correlación entre la turbidez y la temperatura, siendo esta bastante considerable durante varias semanas. Existe poca correlación entre la turbidez y la luz durante las primeras semanas, pero esta cobra una correlación considerable a partir de la semana seis (6) en adelante, a excepción de las últimas 2 semanas. Con respecto al pH, la correlación es bastante significativa y tiende a ser negativa en la mayor parte del ensayo. Con respecto a la humedad, se observa una correlación negativa considerable durante las primeras semanas.
Tabla 1. Variables con respecto a turbidez en el biorreactor I.
| Turbidez vs | pH | Temperatura | Oxígeno | Luz | Humedad |
| Semana 1 | -0,12 | 0,62 | 0,56 | -0,39 | -0,58 |
| Semana 2 | -0,36 | 0,25 | 0,57 | 0,28 | -0,30 |
| Semana 3 | -0,95 | 0,44 | 0,56 | 0,08 | -0,41 |
| Semana 4 | -0,71 | 0,41 | -0,12 | -0,24 | -0,21 |
| Semana 5 | -0,73 | 0,10 | 0,05 | 0,04 | -0,17 |
| Semana 6 | -0,81 | 0,01 | 0,14 | 0,69 | -0,39 |
| Semana 7 | -0,60 | 0,49 | 0,17 | 0,35 | 0,07 |
| Semana 8 | 0,34 | 0,33 | 0,26 | 0,74 | -0,15 |
| Semana 9 | -0,15 | 0,72 | 0,35 | 0,46 | 0,04 |
| Semana 10 | -0,51 | 0,35 | 0,19 | 0,38 | -0,09 |
| Semana 11 | -0,46 | 0,60 | 0,34 | 0,12 | -0,09 |
| Semana 12 | -0,03 | 0,17 | 0,48 | -0,26 | -0,13 |
Fuente: Elaboración propia (2021)
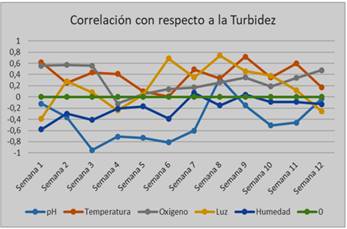
Figura 3. Gráfica de correlación de variables con respecto a turbidez en el biorreactor I. (Las correlaciones positivas significativas estan marcadas de color verde y, las correlaciones postivas debiles, de color verde claro. Mientras que las correlaciones negativas significativas estan marcadas de color amarillo, y las correlaciones negativas debiles de amarillo claro. Las correlaciones no significativas, se encuentran sin color).
Biorreactor II
Se observa una correlación no tan fuerte entre la turbidez y el oxígeno, a excepción de las semanas cuatro (4), cinco (5) y ocho (8), donde se observa una correlación negativa. Durante la primera semana se observa una correlación negativa entre la turbidez y la temperatura, luego se consigue una correlación positiva durante mes y medio, hasta la semana siete (7) donde empieza a influir negativamente.
No se observa mucha correlación entre la turbidez y la luz, a excepción de las semanas dos (2) y cuatro (4). La turbidez en correlación con el pH presenta una tendencia negativa
Tabla 2. Correlaciones más resaltantes en el biorreactor II
| Turbidez vs | pH | Temperatura | Oxígeno | Luz |
| Semana 1 | -0,25 | -0,41 | 0,01 | 0,18 |
| Semana 2 | -0,70 | 0,26 | 0,81 | 0,94 |
| Semana 3 | -0,15 | 0,00 | 0,41 | -0,13 |
| Semana 4 | 0,26 | 0,56 | -0,84 | 0,70 |
| Semana 5 | -0,05 | 0,05 | -0,33 | 0,07 |
| Semana 6 | -0,02 | 0,39 | 0,29 | -0,05 |
| Semana 7 | 0,12 | -0,09 | 0,17 | -0,06 |
| Semana 8 | -0,14 | -0,43 | -0,43 | -0,18 |
Fuente: Elaboración propia (2021)
CALCULO DE LA PRODUCCION DE BIOMQASA ALGAL Y LA CANTIDAD DE CO2 EXTRAIDO DEL MEDIO AMBIENTE.
En la Tabla 3 y 4 se pueden observar la cantidad de biomasa generada en promedio semanal para ambos biorreactores, así como el consumo de CO2, en promedio diario. Los valores obtenidos de biomasa, son promedios de cada semana provenientes de la recopilación realizada por el Arduino. Para el cálculo de CO2, se hizo estequiometría, de la obtención de biomasa, utilizada de la siguiente manera:
Para conocer el volumen de CO2 que se extrae del medio ambiente, se hace una conversión utilizando la fórmula de los gases ideales, como se muestra en la siguiente ecuación:
Donde la presión y la temperatura se consideran constantes, por lo que la expresión se compone de la siguiente manera:
Donde:
Para el caso del biorreactor I, se extrajo 58,99 mL de CO2 por cada L de medio; mientras que para el biorreactor II, serían unos 53,93 mL de CO2 por cada L de medio.
Tabla 3. Valores promedio de CO2 consumidos y la biomasa generada en el bioreactor I.
| Semanas | Promedio de CO2 (mg/L.día) | Biomasa (mg/L.día) |
|---|---|---|
| 1 | 19,94 | 669 |
| 2 | 19,17 | 602 |
| 3 | 16,35 | 532 |
| 4 | 16,11 | 485 |
| 5 | 19,35 | 558 |
| 6 | 17,19 | 781 |
| 7 | 14,55 | 696 |
| 8 | 15,34 | 631 |
| 9 | 15,12 | 676 |
| 10 | 13,80 | 611 |
| 11 | 14,88 | 711 |
| 12 | 14,42 | 797 |
| General | 16,35 | 646 |
Fuente: Elaboración propia (2021)
DISCUSIÓN
Se obtuvo en promedio 521,2 mg/L de biomasa por día, durante el tiempo de funcionamiento del biorreactor II. Cabe resaltar que estas estimaciones son teóricas, ya que no hubo manera de demostrar estos valores de forma empírica. Diariamente se extrajo alrededor de 14,95 mg/L de CO2 del ambiente (o equivalente 53.93 mL de CO2/L por día). Esto puede beneficiar a agroindustrias, ganadería o actividades urbanas, para disminuir la huella de carbono, ya que aparte del CO2, las microalgas absorben nutrientes que se encuentran en los residuos producidos en las mismas. Contrastando con los estudios bibliográficos citados en la introducción, el valor de biomasa que resulta más similar a lo obtenido en este trabajo, fue el obtenido en el estudio de Matanguihan y otros, 2020. Mucha de la similitud se debe al rango de temperatura de entre 24°C y 34°C, rango de pH de entre siete (7) y nueve (9), el medio utilizado (es bastante similar, a diferencia de la proporción de potasio), iluminación totalmente natural y el funcionamiento del reactor durante un largo periodo de tiempo, en relación a los demás estudios. Para mejorar la producción de biomasa se podría optar por cambiar el medio de cultivo a BG11. Si bien el periodo de funcionamiento resulta un factor fundamental, lo ideal es que se trabaje cuatro (4) semanas, porque luego de este periodo, la productividad empieza a decaer al aumentar la turbidez. A nivel industrial se debe de considerar este punto para realizar la cosecha y la renovación del medio. En cuanto a temperatura y luz, es primordial mantenerlos estables, esto a escala industrial resultaría difícil sin recurrir a medios mecánicos de agitación y control de temperatura. En un sistema bien controlado, como en el caso del biorreactor I, se comprueba que se obtiene una buena productividad de biomasa al ser un sistema de poco volumen, en el cual es fácil controlar la temperatura, la iluminación y la agitación. La agitación, en ambos casos, es influyente en la absorción del CO2 y la disipación del O2 al ambiente.
Se recomienda a escala piloto e industrial, en condiciones ambientales, trabajar con un sistema con mayor área de trabajo, para lograr captar más luz, lograr mejor captación de CO2 y disipación de O2, dado que disminuiría el uso de agitadores (costo energético). El control de la temperatura, sería, por tanto, un parámetro a investigar de acuerdo a la estación climática, régimen de lluvia, mapa de radiación solar, ubicación geográfica para ver la incidencia de estos en la producción de biomasa.
Se debería de analizar el perfil lipídico del microorganismo cultivado a escala industrial y determinar así, si resulta rentable la utilización de la biomasa para la producción de biodiesel, o si por otra parte, resulta rentable su utilización para la obtención de aceites esenciales para el consumo humano y/o animal.