INTRODUCCIÓN
La leishmaniasis es una enfermedad causada por un parásito protozoario intracelular transmitido por la picadura de una flebotomina hembra. Las manifestaciones clínicas van desde úlceras cutáneas hasta enfermedad multiorgánica sistémica. La leishmaniasis visceral es causada principalmente por las dos especies relacionadas Leishmania donovani y Leishmania infantum1.
Se observa en regiones tropicales y templadas, India, Nepal Bangladesh, Sudán, Etiopía y Brasil, constituyendo los cuatro focos más grandes de leishmaniasis visceral, al implicar 90% de los casos en el mundo2.
Las dos etapas de desarrollo son el amastigote y el promastigote, con el primero infectando las vacuolas lisosomales en las células fagocíticas. El promastigote es una forma extracelular que se adhiere a las microvellosidades de los insectos3.
La temperatura es un factor importante que ayuda a determinar la localización de las lesiones leishmaniales. Las especies que causan leishmaniasis visceral son capaces de crecer a temperaturas centrales, mientras que las responsables de la leishmaniasis cutánea crecen mejor a temperaturas más bajas. La patogénesis aparece relacionada con la citotoxicidad de las células T4.
La enfermedad visceral, la forma más devastadora y fatal, se conoce clásicamente como kala-azar o el nombre indio para "fiebre negra / enfermedad", que es una referencia al oscurecimiento característico de la piel que se observa en pacientes con esta afección, que probablemente sea producto de la mayor producción de hormona adenocorticotropina inducida por citosinas4.
Históricamente, los aspirados de médula ósea, hígado o esplénicos fueron la clave para el diagnóstico de laboratorio de la enfermedad visceral, pero en la práctica actual la alta sensibilidad y especificidad del ensayo K39 recombinante generalmente ha hecho que este tipo de estudio sea innecesario4.
El diagnóstico definitivo de la enfermedad visceral se realiza mediante la observación del parásito (más específicamente, amastigotes en el tejido) en frotis de Giemsa teñidos o mediante la observación del cultivo de aspirados de médula ósea, esplénicos, hepáticos o ganglios linfáticos4.
Las complicaciones ocurren como consecuencia de anemia, leucopenia y trombocitopenia. Pueden incluir infección bacteriana secundaria, sangrado incontrolado, ruptura esplénica, edema, caquexia e hiperpigmentación. En ausencia de tratamiento, la tasa de letalidad de la leishmaniasis visceral es mayor a 90 por ciento5. Según datos obtenidos de la OPS la tasa de letalidad mantiene una tendencia creciente y en el 2020 se reportó la tasa más alta desde el 2012, que fue tres veces mayor que la tasa de letalidad global por leishmaniasis visceral de 2,7%6. En un estudio realizado en Paraguay entre el 2008 y 2014 se encontró una letalidad de 9,13%7.
CASO CLÍNICO
Paciente masculino de 38 años de edad, constructor, originario de Encarnación, zona urbana, acude al Hospital Regional de Encarnación, Paraguay, por fatiga y debilidad generalizada.
Al interrogatorio refiere cuadro de tres meses de evolución que inicia con aumento de la circunferencia abdominal. Dos meses antes presenta fatiga a grandes esfuerzos, más pérdida de apetito al que posteriormente se agrega pérdida de peso de aproximadamente 16 kilogramos. Un mes antes refiere tos seca de predominio nocturno. Se agrega además sensación febril de predominio nocturno que se acompaña de sudoración profusa y escalofríos diariamente. Tres días antes presenta exacerbación de la fatiga, presentándose incluso durante el reposo
Al ingreso se encuentra hemodinámicamente estable, buena mecánica respiratoria, afebril, caquéctico, con hiperpigmentación generalizada de piel y palidez de mucosas. Presenta además abdomen distendido, tenso, hígado palpable a cuatro centímetros por debajo del reborde costal, bazo a ocho centímetros del reborde costal, a la percusión impresiona hígado de 18 centímetros de longitud.
Al ingreso se realiza analítica laboratorial donde se observa pancitopenia (tabla 1). Se realiza además una tomografía simple de tórax donde no se observan datos de valor. Se solicita RK39 el cual retorna positivo por lo que se decide iniciar anfotericina B desoxicolato por cuadro clínico y epidemiológico sugerente de leishmaniasis visceral a dosis de 50 mg/día.
En su día dos de internación presenta edema de miembros y testículos, agregándose además hematomas en zonas de presión. Se solicita frotis de sangre periférica donde se observa disminución significativa de recuento de plaquetas por lo que se decide suspensión de anfotericina B ante sospecha de reacción secundaria a medicación.
Tabla 1 Datos laboratoriales diarios del paciente donde se observan disminución progresiva de la hemoglobina y las plaquetas
| Día 1 | Día 2 | Día 3 | |
| Hemoglobina (g/dL) | 7,7 | 7,5 | 6,1 |
| Hematocrito (%) | 24 | 23 | 18 |
| Leucocitos (mm3) | 1.100 | 900 | 1.500 |
| Neutrófilos (%) | 49 | 51 | |
| Linfocitos (%) | 45 | 43 | |
| Plaquetas (mm3) | 81.000 | 45.000 | 25.000 |
| VIH: negativo | pH: 7,30 | ||
| RK39: positivo | pCO2: 45 | ||
| pO2: 67 | |||
| EB: -4 | |||
| HCO3: 25 | |||
| FiO2: 21% |
En su día tres de internación paciente presenta dificultad respiratoria rápidamente progresiva, por lo que se realiza gasometría arterial donde se observa hipoxemia y acidosis respiratoria por lo que se procede a la colocación de oxígeno suplementario. Dos horas más tarde se agrega tos expectorante de características sanguinolentas. Se solicita crasis sanguínea donde se observa leve disminución del tiempo de protrombina, sin observarse anomalías del fibrinógeno. Se realiza tomografía simple de tórax donde se observa imagen en vidrio deslustrado y engrosamiento de septos interlobares, sugerente de hemorragia alveolar masiva (figura 1).
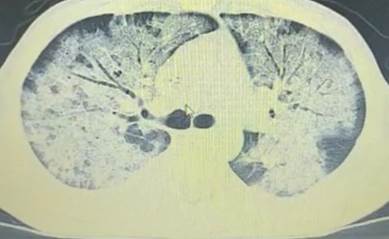
Figura 1 Tomografía de tórax donde se observa imagen en vidrio deslustrado, bilateral, sugerente de hemorragia alveolar masiva.
Se decide transfusión de plaquetas por presentar trombocitopenia grave y sangrado activo. Además, recibe transfusión de glóbulos rojos concentrados por presentar anemia grave y hemorragia activa.
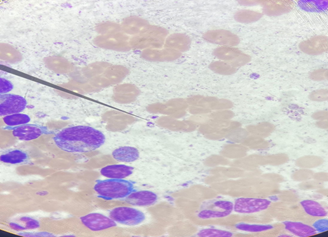
Se realiza punción de médula ósea donde se observan amastigotes y se descarta histiocitosis-hemofagocítica secundaria a leishmaniasis visceral y otros diagnósticos (figura 2).
Ante sospecha de exacerbación de la trombocitopenia por medicación se decide suspender esquema de tratamiento, iniciando así anfotericina B liposomal a 3 mg/kp/día durante 7 días; la hemorragia cesa a las 48 horas del inicio del nuevo esquema de tratamiento; produciéndose además aumento de plaquetas y estabilización de los valores de hemoglobina. El paciente es dado de alta afebril, con buena tolerancia oral, mejoría clínica y laboratorial, en planes de seguimiento por consultorio externo.
DISCUSIÓN
Dado que los parásitos se replican en el sistema retículo endotelial, se acumulan cargas muy altas de los mismos en el bazo, el hígado y la médula ósea, pudiendo provocar complicaciones hemorrágicas principalmente por trombocitopenia y disfunción hepática. La hemorragia masiva en la Leishmaniasis visceral se encuentra descrita como una complicación sumamente rara que se puede presentar dentro del síndrome hemofagocitario o fuera de él.
Actualmente, la anfotericina liposomal es un fármaco antileishmanial de primera línea, recomendado según datos de eficacia y mayor seguridad, disponible en diferentes regiones endémicas del mundo. El régimen de dosificación aprobado por la FDA es de 3 mg/kg/día por vía intravenosa los días 1 a 5, 14 y 21 (dosis total 21 mg/kg)8.
Por la poca disponibilidad de anfotericina B liposomal y su gran costo, en el Paraguay se utiliza como droga alternativa de elección a la anfotericina B desoxicolato, reservándose la presentación liposomal, bien conocida como droga de primera línea, para casos de leishmaniasis visceral que no haya respondido a la forma grave, presente contraindicaciones para la forma desoxicolato o hayan presentado reacciones adversas a la medicación.
Como bien es sabido la anfotericina B presenta acción sobre la médula ósea, pudiendo provocar alteraciones hematológicas, más frecuentemente anemia; pero también hubo casos reportados de trombocitopenia9.
Las complicaciones potencialmente letales por anfotericina B desoxicolato han sido descritas en menos del 1% de los casos, entre dichas complicaciones se nombra a la trombocitopenia como una de ellas10.
El paciente en cuestión presentó una complicación de la patología que fue intensificada con el primer esquema de medicación, el cual puede causar alteraciones hematológicas por toxicidad medular, lo cual desencadena intensificación de la trombocitopenia y esta una hemorragia alveolar masiva que fue mejorando en el transcurso de los días con el nuevo esquema de tratamiento.