INTRODUCCIÓN
La leche es un alimento que contiene nutrientes esenciales para el crecimiento y desarrollo, forma parte de la canasta básica del hogar, su costo es accesible y su consumo es recomendado a lo largo del ciclo vital (1,2. A pesar de su valor nutritivo, pertenece al grupo de alimentos de mayor riesgo en salud pública, debido a su amplio consumo y la alta susceptibilidad para transmitir enfermedades por presencia de microorganismos y contaminantes como medicamentos veterinarios, hormonas, plaguicidas y antibióticos (3.
Los antibióticos y antimicrobianos como los β-lactámicos (penicilinas sintéticas y cefalosporinas), tetraciclinas (oxitetraciclina), macrólidos (espiramicina y tilosina), entre otros, son utilizados en la ganadería lechera, habitualmente con fines terapéuticos o en el tratamiento profiláctico de las vacas no lactantes (4. Los residuos de los mismos pueden ser excretados durante largos periodos después del parto, constituyéndose en uno de los principales contaminantes de la leche (5.
La presencia de residuos de antibióticos en la leche, es una preocupación latente para la salud pública mundial, pues, a pesar de que los niveles detectados sean mínimos, en los humanos, la ingestión regular de pequeñas cantidades de una misma sustancia podría inducir a manifestaciones tóxicas a largo plazo, debido a los efectos acumulativos (6. Así, algunas personas pueden desarrollar hipersensibilidad, resistencia, reacciones alérgicas y efectos tóxicos, mutagénicos, teratogénicos y/o carcinogénicos por la ingestión regular de leche con pequeñas cantidades de antibióticos (4. Adicionalmente, los antibióticos presentes en la leche pueden inducir alteración de la flora intestinal, desarrollo de microorganismos patógenos y reducción de la síntesis de vitaminas (7.
Se han establecido límites máximos de residuos (LMR) para los antibióticos, o límites permisibles en los productos derivados de la leche, que no deben ser superados en ningún caso; por lo tanto, lo más indicado es hacer uso racional de estos medicamentos (8.
Otro microrganismo contaminante de la leche vacuna es la Aflatoxina M1, la cual se produce como derivado metabólico de la aflatoxina B1. Tiene una gran actividad hepatotóxica, cancerígena, teratogénica y mutagénica y por ende representa un riesgo para la salud de las poblaciones. Adicionalmente, el control de los niveles de Aflatoxina M1 constituye un desafío para los productores lácteos que desean acceder a mercados más competitivos como la Unión Europea (UE), donde los límites máximos tolerables son más estrecho que los establecidos por el Mercado Común del Sur MERCOSUR, o la Administración de Alimentos y Medicamentos de los Estados Unidos, FDA (Food and Drug Administration)9-11.
El comercio internacional de leche y sus derivados es cada vez más exigente y en la actualidad, las restricciones de tipo sanitaria, conjuntamente con aquellas relacionadas al uso de insumos químicos en los sistemas de producción (antibióticos, medicamentos veterinarios o sustancias anabolizantes) constituyen las principales limitantes del comercio entre los países (8.
La situación ha exigido que los países desarrollen programas de control de residuos biológicos, con el objetivo de otorgar mayor seguridad respecto a la inocuidad y calidad de los productos para los consumidores, tratando de dar cumplimiento a normativas internacionales que buscan proteger al consumidor y al mismo tiempo favorecer la comercialización de los productos pecuarios12.
En Paraguay, la producción, distribución, utilización y control de los productos de uso veterinario como los antibióticos están regulados por la Ley 667/95; que establece el régimen de registro y fiscalización integral de los productos de uso veterinario y fija condiciones para desarrollar actividades de elaboración, fraccionamiento, distribución, tenencia, importación, exportación, expendio y uso de dichos productos (13. De acuerdo a esta ley todo producto a ser utilizado en medicina veterinaria, así como las empresas que desarrollen actividades de elaboración, fraccionamiento, distribución, importación, tenencia y expendio deberán estar aprobadas y registradas por el Ministerio de Agricultura y Ganadería.
El estatus sanitario en términos de inocuidad para los alimentos de origen pecuario (leche y productos de origen animal) es poco conocido en el país, debido a la falta de políticas que valoren los riesgos asociados a la presencia de residuos de medicamentos veterinarios, plaguicidas, hormonas, toxinas, aditivos y metales pesados en los alimentos a los cuales accede la población.
En virtud de lo anterior, este estudio tuvo como objetivo determinar la presencia de antibióticos y de micotoxinas en una muestra representativa de leche fluida pasteurizada elaborada, envasada y registrada en el Paraguay según los estándares del MERCOSUR y la FDA, debido a que podría tener un efecto adverso en la salud pública, representando la propagación de bacterias resistentes a diversos antibióticos uno de los principales problemas emergentes en salud pública.
MATERIALES Y MÉTODOS
Se realizó un estudio transversal entre los meses de Agosto del 2015 a Julio del 2016, en el cual se calculó el tamaño de la muestra utilizando el método recomendado por el Codex CAC/GL 50-200414. Se utilizó un muestreo de dos clases simples para lotes individuales. Se definió el tipo de preocupación como: peligro directo para la salud y el nivel de peligro como: peligro moderado derivado de la posible propagación amplia en el alimento.
Recolección de muestras de leche
Dos nutricionistas y un veterinario y un tecnólogo de alimentos debidamente entrenados fueron los responsables de recolectar las muestras en distintos puntos de venta de la zona metropolitana del país, verificando que el producto se encontrara dentro de su vida útil, respondiendo al mes estacional establecido para la toma de muestra y teniendo en cuenta la temperatura de conservación de la leche pasteurizada en envase de cartón (temperatura ambiente) y de plástico (menor a 6°C). A partir de un mismo lote de producción se extrajeron 6 muestras de manera a tener representatividad del lote del que provenía. Las muestras fueron recolectadas considerando la estacionalidad (invierno y verano) y enviadas al Laboratorio del Instituto Nacional de Alimentación y Nutrición (INAN). Este laboratorio cuenta con certificación para el análisis de alimentos.
Para el análisis se utilizó el promedio de los valores de 5 muestras de leche. La sexta muestra fue conservada a 4°C en condiciones de refrigeración, con el fin de utilizarla para la validación de los resultados, en el caso de obtener muestras con valores positivos para antibiótico o micotoxina.
Se incluyeron en el estudio, los valores promedios de 450 muestras (90 valores finales) de leches fluidas pasteurizadas de producción nacional en envases de 1 litro (plástico y cartón), con Registro Sanitario de Producto Alimentario (RSPA) vigente al momento de la recolección de los datos. Se excluyeron las muestras cuyos envases presentaron roturas, orificios o cualquier indicio de alteración.
En las muestras se determinó la presencia de antibióticos β-lactámicos, estreptomicina, cloranfenicol, tetraciclina y gentamicina, así como también se estudió la presencia de Aflatoxina M1.
Análisis de las muestras
Tamizaje de antibióticos en leche: Se utilizaron los test cualitativos 4Sensor y Gentasensor, enfatizando que en el país no se registraban antecedentes del uso de los test rápidos para la detección de antibióticos en leche pasteurizada.
4Sensor: 4Sensor ©2016 Unisensor, es una prueba competitiva que involucra receptores específicos y anticuerpos monoclonales genéricos en una sola operación. Se utiliza para la detección de antibióticos β-lactámicos, estreptomicina, cloranfenicol y tetraciclinas en la leche.
El kit consta de un micropocillo que contiene cantidades predeterminadas de receptores y anticuerpos unidos a partículas de oro y una tira reactiva compuesta de un conjunto de membranas con líneas de captura específicas. Durante el análisis se incubó la muestra en baño término a 40ºC por 10 minutos, luego de retirar la tira reactiva, se procedió a leer directamente las intensidades de color como presencia/ausencia (resultado cualitativo). La aparición de líneas con mayor intensidad de color que el control se interpretó como ausencia de los analitos específicos en la muestra de leche y cuando la intensidad del color fue menor que el control, se asumió que la muestra estaba contaminada.
Gentasensor: Es un método cualitativo rápido. Para el cual se incubó la muestra en baño térmico a 40°C durante 6 minutos, sin preparación alguna. La interpretación de los resultados también se realizó mediante la lectura de las intensidades de color. Líneas con el color más claro que la línea de control o sin formación de coloración rosada/rojiza indicó un resultado positivo para gentamicina.
Tamizaje de micotoxinas en leche: Para la detección de Aflatoxinas M1 (micotoxinas) en las muestras de leche se utilizó el test AflaSensor Quanti Milk. Éste es un test cuantitativo, rápido y sensible [límite de detección: 0,02 ppb (20 ppt)];, que permite la detección y cuantificación de AFM1 en la leche (rango de trabajo: 20 a 150 ppt). Se colocó una muestra de 200 μl de leche en los pocillos de ensayo y se mezcló con el reactivo. Se incubó la muestra por 3 minutos a 40°C, luego se introdujeron las tiras reactivas en los pocillos y se incubaron nuevamente las muestras durante 7 minutos (40°C). Finalmente, se retiraron las tiras reactivas e interpretaron directamente los resultados usando un instrumento para la lectura (Readsensor).
Validación del test rápido versus Cromatografía Líquida de Alta Eficacia con Espectrómetro de Masas en Tándem (LC/MS/MS): Teniendo en cuenta que no se registraban precedentes en el uso del kit Aflasensor, los resultados fueron validados en una submuestra de leches (n= 51), utilizando como método de referencia la Cromatografía Líquida de Alta Eficacia con Espectrómetro de Masas en Tándem (LC/MS/MS).
El procedimiento se realizó en un laboratorio de control de control de alimentos y medio ambiente, el cual cuenta con la acreditación NP-ISO/IEC 17025:2006 otorgado por el Organismo Nacional de Acreditación (ONA), que garantiza la confianza en los resultados de los análisis de este tipo15.
Según el protocolo se realizó la extracción en medio hexano y mezcla con metanol cloruro de sodio. Posteriormente se procedió a la partición y eliminación de la fase hexánica, partición con cloroformo, eliminación de la fase acuosa etanólica. Para la concentración, se eliminó la fase clorofórmica, con evaporadores rotatorios y nitrógeno (en los casos de necesidad). El cleanup se realizó por extracción en fase sólida en minicolumnas de silicagel. Se acondicionó el medio con hexano, seguidamente se redisolvió la muestra en cloroformo-hexano. A continuación, se sembró en la columna. Se realizó el lavado con mezcla benceno-ácido acético, seguidamente se volvió a lavar con mezcla éter-hexano y se eluyó con mezcla dicloro-metano-acetona. Se secó la muestra en ambiente de nitrógeno (pureza 99,99%) y al ser éste un punto crítico, se procedió inmediatamente a la derivatización, la cual se realizó con ácido trifluoroacético y la resuspensión en mezcla acetona-agua.
La separación isocrática se logró utilizando una columna Hypersil BDS C18 (5 mm, 250 × 4 mm) suministrada por HP (Alemania). La fase móvil que consiste en agua destilada (pH = 5.8 con H2SO4): acetonitrilo, 85:15 (v/v), se bombeó a un caudal de 1,5 ml/min. Los analitos se detectaron a 450 nm usando un ajuste de 0,01 A.U.F.S. El volumen inyectado fue de 20 μl y la cromatografía se realizó a 24°C.
RESULTADOS
En la Tabla 1 se observa que las muestras tomadas en verano provenían de 15 marcas procesadas, envasadas y registradas en Paraguay, mientras que las recolectadas en invierno provenían de 17 marcas. De las muestras que se recolectaron en verano 13 (28,9%) eran leches descremadas, 4 (8,9%) leches semidescremadas y 28 (62,2%) leches enteras. En inverno 14 (31,1%) muestras eran de leches descremadas, 4 (8,9%) semidescremadas y 27 (60,0%) leches enteras. Tanto en verano como en inverno 24 (53,3%) muestras se encontraban en envase plástico y 21 (46,7%) en cartón.
Tabla 1: Características generales de 45 muestras de leche fluida pasteurizada procesada, envasada y registrada en Paraguay, según estacionalidad
| Características | Verano (n=45) | Invierno (n=45) |
|---|---|---|
| n (%) | n (%) | |
| Marcas muestreadas | 15 (100) | 17 (100) |
| Tipo de leche | ||
| Descremada | 13 (28,9) | 14 (31,1) |
| Semidescremada | 4 (8,9) | 4 (8,9) |
| Entera | 28 (62,2) | 27 (60,0) |
| Tipo de envase contenedor | ||
| Plástico (sachet) | 24 (53,3) | 24 (53,3) |
| Cartón | 21 (46,7) | 21 (46,7) |
En la Tabla 2 se aprecia que todas las muestras de leche pasteurizada recolectadas durante el verano dieron resultado negativo al análisis de presencia de residuos antibióticos y el mismo resultado se obtuvo al analizar las muestras recolectadas durante el inverno.
Tabla 2: Detección de antibióticos en muestras de leche fluida pasteurizada procesada, envasada y registrada en Paraguay, por estacionalidad
| Antibióticos | Verano (n=45) | Invierno (n=45) | ||
|---|---|---|---|---|
| Positivo | Negativo | Positivo | Negativo | |
| n (%) | n (%) | |||
| β-lactámicos | 45 (100) | 0 | 45 (100) | |
| Estreptomicina | 45 (100) | 0 | 45 (100) | |
| Cloranfenicol | 45 (100) | 0 | 45 (100) | |
| Tetraciclina | 45 (100) | 0 | 45 (100) | |
| Gentamicina | 45 (100) | 0 | 45 (100) | |
En el Gráfico 1 se observa que los niveles de Aflatoxina M1 determinados por Aflasensor (test rápido), se distribuyeron asimétricamente, siendo la mediana 0,052 ppb, con valores límites entre 0,019 - 0,160 ppb.

Gráfico 1 Distribución de valores de Aflatoxina M1 en leche fluida pasteurizada, según la estacionalidad.
En la Tabla 3 se presentan los niveles de Aflatoxina M1 determinados por Aflasensor. Según la estacionalidad, la mediana en verano fue significativamente menor que en invierno (0,042 ppb vs 0,066 ppb; Man Whitney, p<0,001).
Tabla 3: Niveles de micotoxina M1 determinados por Aflasensor, según estacionalidad.
| Verano (n=45) | Invierno (n=45) | ||
|---|---|---|---|
| Me (RIC) | Me (RIC) | valor p a | |
| Aflatoxinas (ppb) b | 0,042 (0,028) | 0,066 (0,040) | < 0,001 |
Me: mediana. RIC: rango intercuartílico [Me (p75-p25)].
Diferencias evaluadas utilizando el test Mann-Whitney.
Al categorizar los valores de Aflatoxinas M1 utilizando los límites establecidos por el MERCOSUR y la FDA, en las 90 muestras analizadas, los niveles de micotoxinas en ambas estaciones (verano e invierno) se encontraban dentro de los límites establecidos. Sin embargo, cuando fueron evaluadas según la normativa de la Unión Europea (UE), el 56,6% (51/90) del total de las muestras presentaban niveles elevados independientes de la estacionalidad. Al tener en cuenta la estacionalidad se pudo observar una proporción significativamente mayor en invierno ya que el 77,8% (n 35/45) de las muestras fueron positivas para micotoxinas versus el 35,6% (n 16/45) de las muestras recogidas en el verano; X 2, p<0,0001 (valores mostrados en la Tabla 4).
Tabla 4: Presencia de aflatoxinas en muestras de leche fluida pasteurizada procesada, envasada y registrada en Paraguay, según temporalidad.
| Verano (n=45) | Invierno (n=45) | ||
|---|---|---|---|
| n (%) | n (%) | valor pa | |
| Según MERCOSUR | |||
| Aflatoxinas M1 ≤ 0,5 ppb b | 45 (100) | 45 (100) | |
| Aflatoxinas M1 > 0,5 ppb b | - | - | |
| Según UE | |||
| Aflatoxinas M1 ≤ 0,05 ppb c | 29 (64,4) | 10 (22,2) | < 0,001 |
| Aflatoxinas M1 > 0,05 ppb c | 16 (35,6) | 35 (77,8) |
a Diferencias halladas utilizando el test Chi cuadrado.
b Puntos de corte: límites permitidos por el Mercado Común del Sur (MERCOSUR)
c Puntos de corte: límites permitidos por la Unión Europea (UE).
Análisis comparativo entre métodos
En la Tabla 5 se presentan los valores obtenidos a través de las dos metodologías utilizadas en la investigación. En las 51 muestras analizadas por HPLC, los niveles de micotoxina M1 determinados se distribuyeron asimétricamente, siendo la mediana 0,009 ppb (valores límites 0,009-0,19 ppb). Los valores de micotoxinas se hallaban dentro de los límites según lo establecido según la normativa del Mercosur y también por la de la FDA, tanto en invierno como en verano. Sin embargo, al ser evaluadas según la norma de la UE, se pudo observar mayor proporción durante el invierno correspondiente al 43,5% (10/23) ya que en verano fue del 7,1% (2/28) lo cual fue significativo (X2, p<0,0001).
Tabla 5: Valores obtenidos a través del kit Aflasensor versus HPLC.
| Aflasensor | HPLC | |
|---|---|---|
| n=51 | n=51 | |
| Mínimo | 0,019 | 0,009 |
| Máximo | 0,16 | 0,19 |
| Mediana | 0,052 | 0,009 |
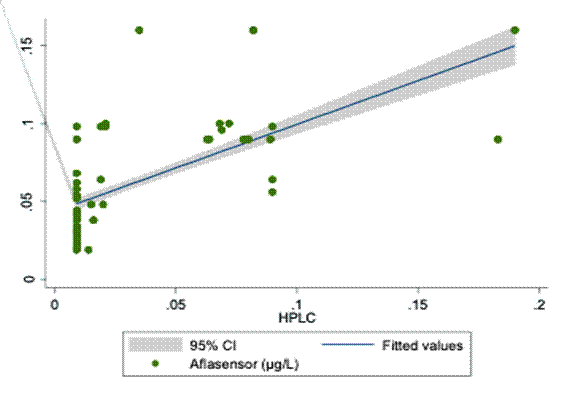
El análisis comparativo de Aflatoxinas M1 presentes en las muestras de leche fluida pasteurizada obtenidas por el Aflasensor y por HPLC arrojó una correlación positiva igual a 0,6387 y estadísticamente significativa (p<0,001), ver Gráfico 2.
DISCUSIÓN
La leche es un alimento altamente nutritivo y de consumo frecuente en todos los grupos poblaciones. Sin embargo, debido a sus características podría considerarse un alimento crítico pues es una fuente propicia para el crecimiento de microorganismos y podría actuar como causante de intoxicaciones alimentarias, por lo tanto la detección y el control de los potenciales contaminantes de la leche es fundamental (16.
En la presente investigación la totalidad de las muestras de leche analizadas no presentaron residuos de antibióticos y los niveles de micotoxinas se encontraron dentro de los límites establecidos por el MERCOSUR y la FDA (<0,5 ppb).
Los resultados reportados por Sandoval A. en el año 2017, muestran una tendencia similar a la hallada en el presente estudio, pues en 100 muestras de leche adquiridas en cuatro ciudades de Paraguay (San Lorenzo, Ñemby, Luque y Limpio), no se detectaron residuos de antibióticos en el 97% de los casos17, aclarando que las muestras de este último estudio correspondían a leches crudas y que el análisis fue realizado utilizando un método de detección distinto.
A nivel internacional, estudios llevados a cabo en Colombia, Guatemala y Brasil, dan cuenta que los residuos de antibióticos se encuentran presentes en menos del 5% de las muestras analizadas (18-20. Sin embargo, las normativas internacionales establecen que no es aceptable la presencia de residuos de antibióticos u otros productos veterinarios en leches, debido al potencial efecto nocivo sobre la salud de los consumidores, principalmente de los niños.
En los últimos 20 años, el número de publicaciones relacionadas a la detección de residuos de antibióticos en la leche ha aumentado en un 20%, indicando claramente que existe un marcado interés y preocupación en el tema y en consecuencia en el desarrollo de métodos de detección oportuna de los mismos (21.
Los desafíos actuales en términos de salud pública se encuentran en desarrollar herramientas de detección altamente sensibles que eviten falsos negativos en el proceso de clasificación instantánea de las muestras y en contar con procedimientos de confirmación y cuantificación de residuos de antibióticos que sean rápidos, sensibles, económicos y de uso sencillo que permitan la prohibición de los alimentos que contienen niveles por encima de los límites máximos (4,22.
Por otra parte, en la presente investigación se demostró que los niveles de micotoxinas se encontraron dentro de los límites establecidos en el MERCOSUR. Sin embargo, no ocurrió lo mismo al utilizar los estándares de la UE. También se comprobó que la estacionalidad tiene influencia en los niveles de micotoxinas, siendo mayor su presencia en invierno que en verano.
La UE limita los niveles de Aflatoxina M1 ≤0,05 mg/kg en la leche. Prácticamente, el límite reglamentario se define como la concentración de Aflatoxina M1 en la leche equivalente al 1,7% (rango de 0,8 a 2,0%) de la concentración Aflatoxinas totales en materia seca9.
En la revisión realizada por Iqbal et al. se aprecia que la presencia de AFM1 en la leche y los productos lácteos en el continente europeo fue relativamente baja debido a las estrictas regulaciones para estas toxinas23.
Las buenas prácticas pecuarias por parte de los productores primarios de los hatos lecheros del país y los controles frecuentes por parte de los industriales podrían ser algunas de las estrategias que sumadas a las estrictas reglamentaciones permitan que el consumidor final acceda a un producto de alta calidad.
Es imperioso que el país cuente con un sistema de vigilancia de manera coordinada entre los entes sanitarios reguladores para la realización del Monitoreo de antibióticos y micotoxinas en productos lácteos, de forma sistemática y regular, estas medidas permitirán ofrecer a la población un alimento inocuo, principalmente para los niños ya que los mismos, son más susceptibles a las micotoxinas. Al mismo tiempo, se podrá competir en mercados más exigentes como el europeo.
CONCLUSIÓN
Finalmente se concluye que en ninguna de las muestras analizadas se detectó presencia de los antibióticos estudiados y en todas ellas los niveles de micotoxinas se encontraban por debajo de la concentración máxima permitida por las normativas del MERCOSUR y FDA, pero si queremos acceder a mercados más exigentes como los de la Unión Europea (UE), con valores límites más exigentes (0,05 ppb), deberemos trabajar con mayor énfasis en la implementación de Buenas prácticas pecuarias.