Introducción
Existen dos parámetros importantes a tener en cuenta durante el proceso de fermentación industrial para la producción de vino, cerveza y bioetanol (Dasari et al., 2011; Morales et al., 2015) Estos proveen información sobre la del proceso de fermentación, los cuales son importantes para la optimización para mejorar el rendimiento y la calidad de los productos (Zhang et al., 2019).
Es importante determinar el incremento de etanol a lo largo de la fermentación. Para este fin han sido desarrollados varios métodos, entre los que se encuentran: las diferentes técnicas cromatográfica, incluyendo cromatografías de gases, cromatografía de gases-espectrometría de masas, cromatografía líquida cuya principal desventaja es la utilización de equipos de costo elevado, consumen mucho tiempo y no pueden ser utilizadas para monitorear el progreso de la fermentación (García-Martínez et al., 2011; Li et al., 2009; Zhang et al., 2015) También se encuentran los métodos gravimétricos, que requieren la destilación como paso previo a la cuantificación, siendo el volumen mínimo de destilación 100 ml del cultivo fermentativo, asimismo, consume mucho tiempo impidiendo que la cuantificación de etanol sea de alto rendimiento. Junto con los métodos mencionados anteriormente, se han desarrollado métodos químicos, los cuales están basados en los cambios colorimétricos, que son causados por la reacción de reactivos específicos con el etanol. Entre estos métodos se encuentran el método de dicromato de potasio. A pesar de la ventaja que presenta este método de cuantificación, presenta algunos problemas que están haciendo que su uso sea dejado de lado (Nascimento et al., 2008; Neves et al., 2015; Zhang et al. 2013).
El primer problema consiste en que el dicromato es altamente carcinógeno debido al Cr (VI). El segundo, la presencia de los azúcares reductores y otros subproductos en el caldo de fermentación, interfieren en la determinación de la concentración de etanol con dicromato de potasio. Zhang et al, 2019, desarrolló un método de cuantificación de etanol en el caldo de fermentación utilizando el reactivo permanganato de potasio, con la ventaja de que este reactivo evita el problema de interferencia debido a la presencia de los azúcares reductores y otros compuestos orgánicos (Cabañero et al. 2010; Li et al., 2013).
En este trabajo se realizó una validación del método de cuantificación de etanol propuesta por Zhang et al., 2019, con modificaciones, realizando los ensayos de linealidad, precisión y veracidad (Latimer, 2012; Duffau et al., 2010; Morillas, 2016), para utilizarlo en métodos de cuantificación de etanol en laboratorio.
Materiales y métodos
Preparación de soluciones y reactivos
Reactivo de DNS: En 26,2 ml de NaOH 2M se disolvió lentamente 18,5 g de tartrato de sodio y potasio en agitación constante. Asimismo, se disolvieron 0,5 g de fenol cristalino y 0,5 g de sulfito de sodio. Se agregó agua destilada hasta completar 60 ml. Se agregaron lentamente 0,63 g de ácido 3,5 dinitrosalicílico y se dejó en agitación overnight a 70 rpm. Luego de conseguir la disolución total, se llevó a 100 ml de volumen en un matraz aforado. Se filtró con papel de filtro cualitativo y se refrigeró hasta su uso.
Permanganato de potasio: La preparación del reactivo de permanganato de potasio se realizó de la siguiente manera: se pesaron 0,395 g de permanganato de potasio y 10 g de tetraborato de sodio y se disolvieron en 250 ml de ácido sulfúrico concentrado, se enfrió a temperatura ambiente y se llevó a volumen de 1000 ml.
Soluciones estàndares
Para el ensayo con el reactivo de DNS se prepararon por duplicado soluciones estándar de glucosa a partir de una solución madre de dextrosa anhidra (Anedra lote 28910-1) de 1 g/L, obteniendo las siguientes concentraciones de trabajo: 0,0625 g/L, 0,125 g/L, 0,25 g/L, 0,5 g/L y 1 g/L. También se preparó una solución testigo de glucosa de 0,4 g/L, utilizando Dextrosa anhidra, PANREAC Química S. A. Como blanco se empleó una mezcla de agua destilada con el reactivo de DNS para los están- dares, para las muestras en medio YPD se utilizó como blanco una matriz YP (Extracto de levadura 10 g/L, Peptona de carne 20 g/L).
Asimismo para el ensayo con permanganato de potasio se prepararon soluciones estándar de etanol y glucosa. Para realizar una curva de calibración se prepararon por duplicado soluciones estándar de glucosa a partir de una solución stock de 0,125 g/L de dextrosa anhidra (Anedra lote 28910-1), realizando diluciones seriadas para obtener las siguientes concentraciones de trabajo: 0,0625 g/L, 0,0312 g/L, 0,0156g/L, 0,0078 g/L, 0,0039 g/L, 0,00195 g/L. Asimismo se preparó por duplicado un testigo de 0,04 g/L de glucosa utilizando dextrosa anhidra (PANREAC Química S. A). Además, para realizar una curva de calibración se prepararon por duplicado soluciones de etanol estándar a partir de una solución stock de 0,0625 ml/L de etanol absoluto (Merck, lote 1.00983.1000) realizando diluciones seriadas para obtener las siguientes concentraciones de trabajo: 0,0625 ml/L, 0,0312 ml/L, 0,0156 ml/L, 0,0078 ml/L, 0,0039 ml/L, 0,0019 ml/L. Además, se pre- paró por duplicado una solución testigo de 0,025 ml/L de etanol utilizando etanol absoluto (Cicarelli Laboratorios, Lote 64714). Como blanco de las soluciones estándares se utilizó agua destilada y para las muestras en YPD se utilizó como blanco una matriz YP (Extracto de levadura 10 g/L, Peptona de carne 20 g/L).
Pretratamiento de las muestras
Para el ensayo de veracidad, se preparó por duplicado, medio YPD con una concentración conocida de etanol (4,76 ml etanol/L). Se tomó una alícuota de cada medio y se centrifugaron a 13800 rpm y 4ºC, durante 5 min. Luego se recuperaron los sobrenadantes y se mezclaron con ácido tricloroacético (TCA) en una relación 1:1, manteniendo la mezcla a temperatura ambiente por 5 min. Luego, las mezclas se centrifugaron a 13800 rpm y 4ºC, durante 5 min, se recuperaron los sobrenadantes y se mezclaron con 1/5 volumen de Bromuro de hexadeciltrimetilamonio (CTAB, por sus siglas en inglés). Las mezclas se incuba- ron en un termobloque a 65ºC durante 10 min, se centrifugaron a 13800 rpm y 4ºC por 10 min y se recuperaron los sobrenadantes, denominándolos muestras pretratadas. A partir de estas muestras pretratadas se procedió a realizar las reacciones con DNS y con permanganato de potasio para la cuantificación de etanol.
Ensayo con el reactivo de DNS
La reacción de determinación de la concentración de azúcares reductores se realizó de la siguiente manera: en sendos tubos de ensayo de vidrio se adicionó 300 µl de las soluciones preparadas (estándares, testigos, blancos y muestras) y 900 µl del reactivo de DNS. Luego los tubos se incubaron a 100ºC durante 10 min y se enfriaron en hielo. Se realizó la medición de la absorbancia por espectrofotometría a 550 nm. Se construyó la curva de calibración a partir de los valores obtenidos con las soluciones estándar para la posterior determinación de la concentración de azúcares reductores en las muestras.
Ensayo con el reactivo permanganato de potasio
La reacción de cuantificación de etanol se realizó de la siguiente manera: En tubos de ensayo de vidrio se adicionaron 0,6 ml de las soluciones preparadas (estándares, testigos, blancos, muestras) y 0,6 ml del reactivo de permanganato de potasio. Se determinó la absorbancia inicial a 526 nm (absorbancia antes de la reacción) de las soluciones preparadas (estándares, testigos, blancos y muestras) por espectrofotometría. Seguidamente, las mezclas se incubaron a 40ºC por 90 min en un baño termostatizado. Luego se enfriaron hasta alcanzar tempera- tura ambiente y se determinó la absorbancia final a 526 nm (absorbancia después de la reacción). Se construyó la curva de calibración a partir de los valores obtenidos con las soluciones estándar para la posterior determinación de la concentración de etanol en las muestras.
Cálculo de la concentración de etanol
A continuación, se describen los pasos para realizar el cálculo de la concentración de etanol:
1: Se realizó la sustracción de los valores de absorbancia de las muestras medidas a 526 nm antes y después de la re- acción de oxidación con el reactivo de permanganato de potasio. Los valores finales de absorbancia a 526 nm de las muestras se denominan “A”.
2: la concentración de azúcares reductores presentes en las muestras se calcula re- emplazando el valor de absorbancia a 550 nm de las muestras en la ecuación de la recta de la curva de calibración obtenida a partir de la reacción del reactivo de DNS con las soluciones estándares de glucosa.
3: Una vez cuantificada la concentración de azúcares reductores en la muestra, se extrapola el valor de concentración de azúcares reductores de las muestras en la curva de calibración obtenida a partir de la reacción del permanganato de potasio con las soluciones estándares de glucosa, con el fin de obtener el valor de absorbancia de los azúcares reductores a 526 nm. A este valor se lo denominamos “B”.4: La absorbancia a 526 nm correspondiente al etanol presente en la muestra se calcula realizando la sustracción A - B.
5: La concentración de etanol en las muestras se calcula introduciendo el valor resultante de absorbancia a 526 nm correspondiente al etanol (A - B), en la ecuación de la recta de la curva de calibración obtenida a partir de la reacción del permanganato de potasio con las soluciones estándares de etanol.
Resultados
Ensayo con el reactivo DNS
Aplicando el ensayo de Linealidad al método de cuantificación de azúcares reductores se obtuvo la curva de calibración a partir de 5 concentraciones diferentes de la solución stock, evaluadas por duplicado. La ecuación de la recta obtenida mediante un ajuste lineal fue y = 3,3709x - 0,082 con un valor de R2 igual a 0,9957 (Figura 1 A), por lo que se infiere que el ensayo se ajusta correctamente al modelo lineal (R2 mayor o igual a 0,995) en el rango de los valores de absorbancia de trabajo. Asimismo, se calculó para las réplicas de cada nivel analizado el valor residual construyendo el gráfico de distribución de residuos (Figura 1 B), en el cual no se observa tendencia de los residuos a través del cambio de concentración del analito.
Asimismo, por medio del ensayo de Precisión se analizaron 20 réplicas de un testigo de glucosa (0,4 g/L), obteniendo como promedio de las mediciones un valor de 0,41 g/L de glucosa con un desvío estándar de 0,01 y un RSD% de 3,07%. Con estos resultados se construyó el gráfico de control de valor medio para otorgar validez a cada ensayo realizado (Figura 2). Como se observa en dicho gráfico todos los valores obtenidos a lo largo del trabajo se ubicaron dentro de la región normal esperada, es decir entre el límite de alarma inferior (LAI) y el límite de alarma superior (LAS), lo cual indica que los resultados de los ensayos realizados fueron confiables.
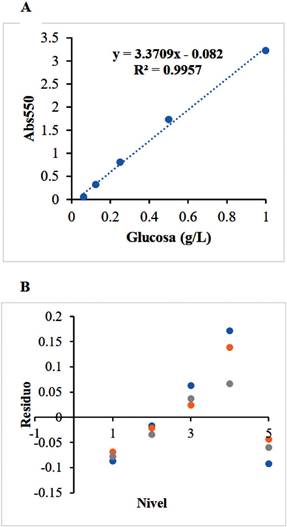
Figura 1 Ensayo de Linealidad aplicado a la reacción con el reactivo de DNS del método de cuantificación de etanol. A) Curva de calibración obtenida a partir del ensayo de Linealidad aplicado al método de cuantificación de azúcares reductores del método de cuantificación de etanol. A la curva se le aplicó un ajuste lineal obteniendo la ecuación de la recta y = 3,37095x - 0,082 con un R2 = 0,9961. B) Gráfico de distribución de los residuos para las réplicas de cada nivel.
Reacción de oxidación total de los estándares glucosa con el reactivo permanganato de potasio
Aplicando el ensayo de Linealidad a la reacción de oxidación de las soluciones estándares de glucosa con el reactivo de permanganato de potasio, se obtuvo la curva de calibración a partir de 5 concentraciones diferentes de la solución stock evaluadas por duplicado. La ecuación de la recta obtenida mediante un ajuste lineal fue y = 19,301x + 0,025 con un valor de R2 igual a 0,9996 (Figura 3 A), por lo que se infiere que el ensayo se ajusta correctamente al modelo lineal (R2 mayor o igual a 0,995) en el rango de los valores de absorbancia de trabajo. Asimismo, se calculó para las réplicas de cada nivel analizado el valor residual construyendo el gráfico de distribución de residuos (Figura 3 B), en el cual no se observa tendencia de los residuos a través del cambio de concentración del analito. Asimismo, por medio del ensayo de Precisión se analizaron 20 réplicas de un testigo de glucosa (0,04 g/L), obteniendo como promedio de las mediciones un valor de 0,042 g/L de glucosa con un desvío estándar de 0,001 y un RSD% de 2.56%. Con estos resultados se construyó el gráfico de control de valor medio para otorgar validez a cada ensayo realizado (Figura 4). Como se observa en dicho gráfico todos los valores obtenidos a lo largo del trabajo se ubicaron dentro de la región normal esperada, es decir entre el límite de alarma inferior (LAI) y el límite de alarma superior (LAS), lo cual indica que los resultados de los ensayos realizados fueron confiables.

Figura 2 Gráfico de control de valor medio correspondiente al ensayo de la reacción de los estándares glucosa con el reactivo de permanganato de potasio del método de cuantificación de etanol. En el gráfico se indican los resultados a partir del aná lisis de la muestra control (solución testigo de glucosa de 0,04 g/L) para cada semana en que se realizó el ensayo de la reacción de los estándares glucosa con el reactivo de permanganato de potasio del método de cuantificación de etanol.
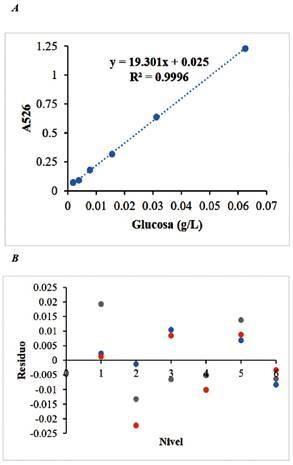
Figura 3 Ensayo de Linealidad aplicado a la reacción de oxidación de las soluciones estándar de glucosa con el reactivo de permanganato de potasio del método de cuantificación de etanol. A) Curva de calibración obtenida a partir del ensayo de Linealidad aplicado a la reacción de glucosa con el reactivo de permanganato de potasio del método de cuantificación de etanol. A la curva se le aplicó un ajuste lineal obteniendo la ecuación de la recta y = 19,301x + 0,025 con un de R² = 0,9996. B) Gráfico de distribución de los residuos para las réplicas de cada nivel.
Reacción de oxidación total de los estándares etanol con el reactivo permanganato de potasio
Aplicando el ensayo de Linealidad a la reacción de oxidación de las soluciones estándares de etanol con el reactivo de permanganato de potasio se obtuvo la curva de calibración a partir de 5 concentraciones diferentes de la solución stock, evaluadas por duplicado. La ecuación de la recta obtenida mediante un ajuste lineal fue y = 14,89x+ 0,1563 con un valor de R2 igual a 0,9907 (Figura 5 A), por lo que se infiere que el ensayo se ajusta correctamente al modelo lineal (R2 mayor o igual a 0,995) en el rango de los valores de absorbancia de trabajo. Asimismo, se calculó para las réplicas de cada nivel analizado el valor residual construyendo el gráfico de distribución de residuos (Figura 5 B), en el cual no se observa tendencia de los residuos a través del cambio de concentración del analito.
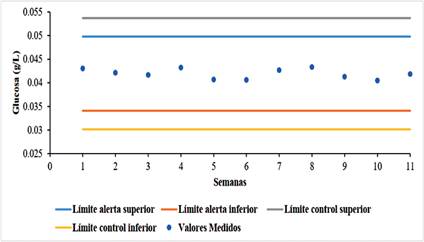
Figura 4 Gráfico de control de valor medio correspondiente al ensayo de la reacción de los estándares glucosa con el reactivo de permanganato de potasio del método de cuantificación de etanol. En el gráfico se indican los resultados a partir del aná lisis de la muestra control (solución testigo de glucosa de 0,04 g/L) para cada semana en que se realizó el ensayo de la reacción de los estándares glucosa con el reactivo de permanganato de potasio del método de cuantificación de etanol
Asimismo, por medio del ensayo de Precisión se analizaron 20 réplicas de un testigo de etanol (0,025 ml/L), obteniendo como promedio de las mediciones un valor de 0,023 ml/L de etanol con un desvío estándar de 0,001 y un RSD% de 5.04%. Con estos resultados se construyó el gráfico de control de valor medio para otorgar validez a cada ensayo realizado (Figura 6). Como se observa en dicho gráfico todos los valores obtenidos a lo largo del trabajo se ubicaron dentro de la región normal esperada, es decir entre el límite de alarma inferior (LAI) y el límite de alarma superior (LAS), lo cual indica que los resultados de los ensayos realizados fueron confiables.
Para el ensayo de veracidad del método de cuantificación de etanol se realizó por duplicado un análisis de la técnica en medio complejo YPD con un valor teórico de etanol en las muestras de 4,76 ml etanol/L. Se logró determinar que el porcentaje de recuperación del testigo de etanol preparado en medio complejo YPD fue 99,76%. Así, se obtuvo un valor de recuperación del analito en la matriz dentro del rango esperado, lo que sugiere que el método de cuantificación de etanol no presenta sesgo significativo.
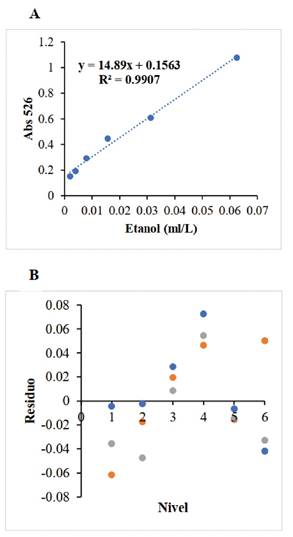
Figura 5 Ensayo de Linealidad aplicado a la reacción de oxidación de las soluciones estándar de etanol con el reactivo de permanganato de potasio. A) Curva de calibración obtenida a partir del ensayo de Linealidad aplicado a la reacción de etanol con el reactivo de permanganato de potasio del método de cuantificación de etanol. A la curva se le aplicó un ajuste lineal obteniendo la ecuación de la recta y = 14,89x + 0,1563 con un de R² = 0,9907. B) Gráfico de distribución de los residuos para las réplicas de cada nivel.
En la Tabla 1 se presenta un resumen de los resultados obtenidos en la validación del método de cuantificación de etanol utilizando el reactivo de permanganato de potasio, como también los rangos de aceptación para cada ensayo
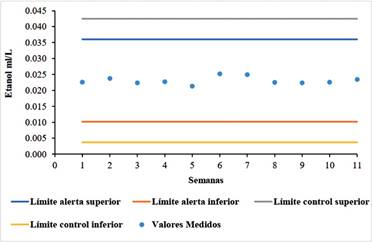
Figura 6 Gráfico de control de valor medio correspondiente al ensayo de la reacción de los estándares etanol con el reactivo de permanganato de potasio del método de cuantificación de etanol. En el gráfico se indican los resultados a partir del análisis de la muestra control (solución testigo de etanol de 0,025 ml/L) para cada semana en que se realizó el ensayo de la reacción de los estándares etanol con el reactivo de permanganato de potasio del método de cuantificación de etanol.
Discusión
Se ha realizado el ensayo de validación del método de cuantificación de etanol propuesto por Zhang et al., 2019, con modificaciones, aplicando los ensayos de Linealidad, Precisión y Veracidad. Para el ensayo de Linealidad se analizó por triplicado cinco concentraciones diferentes de cada solución estándar, y se estableció un valor de rango de aceptación un coeficiente de correlación (R2) superior o igual a 0,995. Como se observa en la Tabla 1, tanto el ensayo de reacción con DNS, como el de la reacción de los estándares glucosa con permanganato de potasio (Figuras 1 y 3), se encuentran dentro del rango de aceptación, presentando un R2 de 0,9957 y 0,9996 respectivamente, asimismo, en sus respectivos gráficos de distribución se observa que los ensayos presentan distribución aleatoria en sus residuos, lo que indica que no hay tendencia en los resultados obtenidos por los mismos.
En el ensayo de Linealidad de la reacción de los estándares etanol con el reactivo permanganato de potasio se observa que el valor de R2 es de 0,9907 (Figura 1 A), inferior al rango de aceptación, esta diferencia puede deberse a que el reactivo de per- manganato de potasio se oxida rápidamente con el etanol, por lo que no se obtuvo un valor similar o superior al 0,995. No obstante en los demás ensayos de validación, este método se encontró dentro de los rangos de aceptación, lo que indica que el resultado obtenido es certero y confiable. Asimismo, se observa que los residuos presentan distribución aleatoria (Figura 1 B), lo que indica que los resul tados obtenidos no presentan tendencia.
En los ensayos de precisión, se observa que las tres reacciones del método de cuantificación se encuentran en el rango de aceptación, así como también, puede observarse en las respectivas gráficas de control que los valores obtenidos en este ensayo se encuentran dentro de los límites de alarma superior e inferior (Figuras 2, 4, y 6). Finalmente en el ensayo de veracidad, se obtuvo que el valor de concentración de etanol fue de 99,76%, encontrándose dentro del rango de aceptación para este ensayo. El ensayo de veracidad se realizó aplicando los tres ensayos en simultáneo, tal y como se haría en un proceso de fermentación.
Con los datos obtenidos, se infiere que el método de cuantificación de etanol con el reactivo de permanganato de potasio brinda resultados certeros y confiables para la determinación de la concentra ción de etanol durante el proceso de fermentación, siendo una de sus ventajas que al utilizar pequeños volúmenes de muestra, y no requerir procedimientos demandantes en costo y tiempo, permite evaluar la evolución del proceso de fermentación.
Conclusión
Se ha realizado la validación del método de cuantificación de etanol propuesto por Zhang et al., 2019, con modificaciones, aplicando los ensayos de Linealidad, Precisión y Veracidad. Los valores obtenidos indican que los resultados obtenidos por el mismo son certeros y confiables, lo que permitiría su utilización en la determinación de la concentración de etanol durante el proceso de fermentación alcohólica, ya sea en la producción de bebidas alcohólicas, como en la producción de biocombustibles como el bioetanol y/o el biobutanol, así como también en cultivos de microorganismos fermentadores como bacterias, hongos y levaduras.
Agradecimientos
Agradezcemos principalmente al CONACyT por la financiación del proyecto de tesis de José Escurra, llevado a cabo en el Departamento de Biotecnología de la FACEN-UNA.
El autor principal también agradece a su madre por guiarle al amor a la ciencia desde pequeño y de manera muy especial agradece, con amor incondicional por siempre, a Esmilce Apuril por su apoyo en todos sus proyectos y metas científicas.
Contribución de los autores
El presente trabajo es resultado parcial del proyecto de tesis de Maestría en Biotecnología Industrial, realizado por José Escurra. Diego Noseda dio tutoría y orientación al autor principal durante la elaboración de la tesis. Francisco Ferreira dio orientación y apoyo en procedimientos químicos y experimentales.












 uBio
uBio 


