INTRODUCCION
La fibrosis quística es una afección de herencia autosómica recesiva, caracterizada por disfunción de las glándulas de secreción exocrina. Está causada por mutaciones en el gen que codifica la proteína reguladora de la conductancia transmembrana (CFTR), y se expresa en órganos como pulmones, páncreas, tracto biliar, y glándulas sudoríparas 1. Es la causa más frecuente de insuficiencia pancreática exocrina (IPE) en la infancia. La IPE está presente en el 85-90 % de casos, observándose fuerte correlación genotipo/fenotipo. De las más de 2 mil variantes del gen FQ, la más común es la deleción del alelo F508 del gen CFTR ((F508 o F508del), que se halla en aproximadamente 70% de los alelos CFTR defectuosos, variando según el grupo étnico. La mayoría de los homocigotos F508del tienen IPE, mientras los heterocigotos tienen función pancreática residual, pudiendo evolucionar hacia la IPE 2-4.
La disfunción de la proteína CFTR, reguladora del transporte de cloro en la superficie epitelial, condiciona secreciones viscosas que obstruyen los conductos pancreáticos 4,5. La IPE es el resultado de la destrucción del tejido exocrino, con pérdida de función de acinos y conductos, que inicia entre las 28 y 32 semanas de vida fetal. Al año ya hay destrucción acinar avanzada. Se reduce la secreción de agua, bicarbonato y enzimas (lipasa, proteasa y amilasa), dando lugar a maldigestión de grasas, proteínas y vitaminas liposolubles. Por la escasez de bicarbonato, un pH ácido intestinal favorece la inactivación de la lipasa y la precipitación de sales biliares, dificultando la formación de micelas y la absorción de grasas. La malabsorción se expresa como dolor abdominal, flatulencias, diarrea crónica, esteatorrea, creatorrea y escasa ganancia ponderal 1,4,6.
La IPE puede manifestarse desde las primeras semanas en las variantes severas, o instalarse a lo largo de los primeros meses o años de vida. Dada la capacidad de reserva del páncreas, los síntomas pueden no apreciarse hasta que la función esté muy alterada y la destrucción sea mayor del 90 %. La esteatorrea se evalúa cuantificando la grasa en materia fecal a través de la técnica de Van de Kamer y el Coeficiente de Absorción de Grasas que relaciona la grasa excretada respecto de la ingerida siendo normales valores mayores a 85% y 93% en niños menores de 6 meses y mayores respectivamente 5.
La elastasa 1 fecal (EF-1) examen sencillo y no invasivo, es altamente predictivo de IPE en niños con síntomas gastrointestinales o escasa ganancia de peso, pues niños sanos, aún prematuros, muestran niveles de EF en rangos normales desde las dos semanas de vida. Una concentración <200 μg/g en las heces se considera anormal. La sensibilidad de EF-1 para IPE leve, moderada y grave es del 63%, 100% y 100%, respectivamente. La EF tiene una especificidad del 93% en pacientes con IPE 1,7,8.
Por la malabsorción de macro y micronutrientes y desajustes entre requerimientos e ingesta, la IPE aboca a la desnutrición sin terapia adecuada. Tratar la malabsorción para optimizar el crecimiento y el estado nutricional es clave 9. La terapia de reposición con enzimas pancreáticas (TREP), ha mostrado eficacia para compensar la malabsorción, logrando crecimiento y estado nutricional óptimos, con síntomas mínimos 2,3,9,10.
En la FQ es esencial una TREP con una dieta alta en calorías, grasas y suplementos de vitaminas liposolubles, pues el estado nutricional se correlaciona directamente con el pronóstico, la calidad de vida y la supervivencia 3,9,10.
Para optimizar la absorción sería deseable en el duodeno una concentración de lipasa, amilasa y proteasa similar a una secreción pancreática fisiológica. Las enzimas con cubierta entérica (CE) de origen porcino, utilizadas desde la década de los 80, constituyen el tratamiento estándar para la IPE, pues permiten una dieta variada, normal o alta en lípidos, con una absorción entre 85-95% de la grasa ingerida 2.
Actualmente, se investigan enzimas alternativas a las de origen porcino 7. Ante la sospecha clínica de IPE se debe iniciar la TREP ajustando la dosis según la respuesta. Se requieren más ensayos controlados aleatorizados bien diseñados para optimizar la TREP 2,11.
PRESENTACIONES ENZIMATICAS PARA LA TREP
La TREP es la terapéutica actual para la IPE en la FQ. Las formulaciones contienen una combinación de enzimas pancreáticas: lipasa, amilasa, proteasa y otros componentes, derivados de páncreas porcino 2,9.
La FDA, incluye a las enzimas pancreáticas en la categoría de productos biológicos 12.
Los preparados buscan normalizar la absorción de los nutrientes, de manera fisiológica, apuntando a que en el duodeno haya concentración de lipasa, amilasa y proteasa similar a la secreción pancreática normal, con “provisión de cantidad correcta” de enzimas, en el “lugar adecuado”, en el “momento oportuno”, con un ritmo de liberación paralelo al vaciado gástrico de los alimentos 13.
Se ha evolucionado desde los “extractos pancreáticos liofilizados” en los que gran parte de las enzimas se inactivaban con la acidez gástrica, requiriendo agregado de bicarbonato o supresores de ácido, a las formulaciones de enzimas con cubierta entérica (CE) que, aunque resisten a la acidez gástrica, no obtienen un vaciado gastro-duodeno paralelo a las partículas alimentarias de menor tamaño. Surgen entonces las microesferas con CE, que logran disminuir la excreción residual de grasa 3,13.
Existen una variedad de concentraciones y presentaciones aprobadas por la FDA, para todos los rangos etarios 4. Entre ellas se encuentran las formulaciones de microesferas con CE; Creón y Pertyze y las micro tabletas; Pancreaze y Zenpep. Completa la lista Viokace que carece de CE 3.
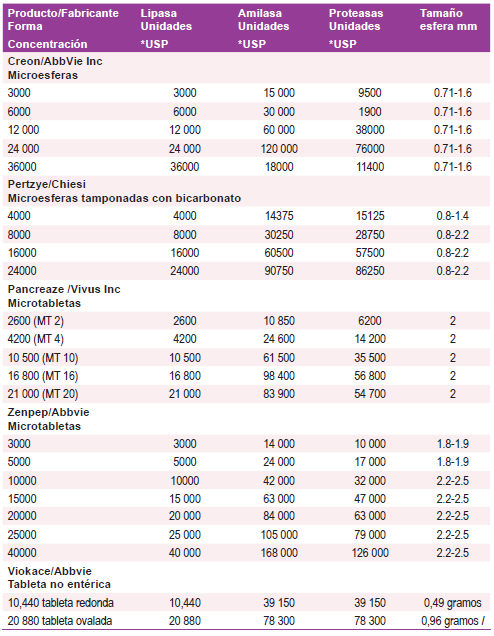
Las características de los diferentes preparados se detallan en la Tabla 1.
Las unidades de lipasa, amilasa y proteasas difieren entre un producto y otro. Igual variabilidad ocurre con el tamaño de las microesferas y micro tabletas. El tamaño óptimo para las microesferas sería de 1,4 + 0,3 mm, que lograría un vaciamiento gástrico en paralelo al de los alimentos 3.
Por convención el número agregado a la marca comercial, especifica la concentración de unidades de lipasa por capsula 4,14. El propósito de diferentes concentraciones, es optimizar las dosis reduciendo la cantidad de capsulas. Se recomienda optar por un solo tipo de preparado para evitar confusiones, ofreciendo orientaciones individualizadas y precisas sobre su uso apropiado 4. No se recomiendan las “enzimas genéricas” que han demostrado menor actividad de lipasa en relación con el informe del etiquetado 3.
En dosis equivalentes de lipasa, las enzimas con CE tamponada logran aumento significativo en la absorción grasa comparado con las de CE sin tampón. Pertzye® / Pancrecarb®: es una fórmula de CE tamponada con bicarbonato, para optimizar el pH en el microambiente que rodea las microesferas. La capacidad enzimática es preservada por la CE hasta su liberación en el duodeno 15.
NUEVAS ENZIMAS
Aunque las enzimas posean CE para evitar la inactivación por el ácido gástrico, los trastornos gastrointestinales aún son relevantes, pudiendo haber respuestas sub óptimas por factores como activación inadecuada en un duodeno con pH bajo, entre otros 15,16.
Nuevas formulaciones surgen con el interés de optimizar su acción:
Relizorb; es un “cartucho de enzimas pancreáticas” para hidrolisis de lípidos de las fórmulas enterales, de uso único, diseñado para el suministro durante la alimentación por sonda, lográndose la hidrólisis en más del 90 % de los triglicéridos en la mayoría de las fórmulas testeadas in vitro. Los reportes apuntan a su seguridad y efectividad, demostrando aumento al doble en los índices omega-3, importante en la absorción lipídica en pacientes con alimentación enteral. Aprobado en el año 2015 para adultos y en el 2017 para niños a partir de 5 años. Entre 10 a 15 % de niños y adolescentes con FQ, no logran el objetivo nutricional con la ingesta y requieren alimentación enteral. Ante la ausencia de estudios aleatorizados controlados con las enzimas convencionales, Relizorb constituye una opción 3,17,18.
Se encuentran en estudio otras enzimas como Liprotamasa: derivada de la biotecnología, que combina lipasa cristalina, proteasa cristalina y amilasa amorfa, sin CE y Lipasa microbiana NM-BL, aún no disponibles para su uso clínico” 3,4,10,19.
REQUERIMIENTOS Y DOSIFICACIÓN DE LATREP
En el tratamiento de la IPE en la FQ son de suma importancia: la educación de pacientes, el aporte nutricional adecuado y una TREP efectiva 4. La IPE está presente al nacimiento en el 60% de los diagnosticados a través del tamiz neonatal; evoluciona durante el primer año de vida y cerca de 90% de niños tendrán IPE al año de edad 1,8.
Los niños con FQ y evidencia de IPE deben iniciar TREP, aún en ausencia de signos de malabsorción, tanto aquellos con lactancia materna exclusiva, lactancia mixta o con fórmulas infantiles, incluidas fórmulas elementales con triglicéridos de cadena media (TCM); o los que reciben alimentación complementaria 1,8.
En niños, los requerimientos enzimáticos pueden ser calculados a partir del peso corporal o por el contenido de grasa de cada alimento. Es importante un manejo multidisciplinario, para el cálculo de la cantidad y tipo de grasa en cada alimento 4.
En lactantes, se recomienda iniciar a una dosis de 2000 a 5000 UI de lipasa por comida (usualmente 120 ml o 4 oz, aunque consuma menos). Se realizará seguimiento de peso y talla, así como de síntomas de malabsorción para guiar el ajuste de dosis. No hay estudios que determinen la dosis óptima 1,8.
En niños mayores de 2 años, la dosis recomendada es de 500 - 2500 UI de lipasa/kg por comida, y la mitad de esta dosis en cada colación 4. En base a los gramos de grasa ingeridos, se recomiendan 500 a 4000 UI de lipasa por gramo de grasa, ya que esta sería la respuesta pancreática de lipasa 4.
En niños de 2 a 5 años, de acuerdo con la Cystic Fibrosis Foundation (CFF) la dosis máxima es de 10,000 UI de lipasa/kg/día 20.
MODO DE ADMINISTRACIÓN
Han demostrado mayor eficacia. las enzimas en microesferas con CE. Las microesferas vienen incluidas en una cápsula de gelatina que se disuelve en el estómago. Esta CE se disuelve a un pH de 5-5.5, que se obtiene en el intestino delgado distal en la FQ 21.
Si bien no existe evidencia de estudios controlados, se sugiere administrarlas al inicio de cada alimentación con leche materna, fórmula láctea, colación o comida. Si el tiempo de alimentación es prolongado, es necesario fraccionar la dosis de las enzimas: 50% al comienzo y 50% a la mitad de la comida, mientras se corrige el hábito o se plantean vías complementarias o alternativas de alimentación. Si no hay respuesta satisfactoria, podrán ser administradas durante o justo al finalizar cada comida, y no deben ser expuestas al calor, pues pueden perder efectividad 4.
Las cápsulas deben ser deglutidas intactas. En los lactantes, que no pueden deglutirlas, abrirlas inmediatamente antes de la alimentación y administrar los gránulos, sin molerlos, con un poco de líquido o fórmula, directamente en la boca, o si ya inició otros alimentos, mezclarlas con papillas o purés, de preferencia ácidas (por ej. de manzana) para evitar la activación de las microesferas, debiendo consumirse inmediatamente. No deben agregarse los gránulos de enzimas en el volumen total de la comida o leche, ni masticarse o triturarse, ya que pierden efectividad. Tampoco deben permanecer en la boca pues pueden causar irritación 4.
La secreción disminuida de bicarbonato en la FQ condiciona un ambiente intestinal ácido, que ocasiona disolución ineficaz de la CE de las enzimas, precipitación de los ácidos biliares esenciales para la formación de micelas y absorción de grasas, ocasionando mala digestión y malabsorción 22.
Los inhibidores de bomba de protones (IBP), pudieran mejorar la disponibilidad de ácidos biliares y la activación de las microesferas de enzimas optimizando la absorción. No hay evidencia clara sobre su uso rutinario. Se puede considerar un curso corto si no hay ganancia de peso y/o persisten síntomas 4,23.
En la alimentación enteral: Si bien no hay guías precisas, se recomienda administrar la enzima al inicio, al término o en medio de la misma; ya sea que se administre en bolo o en infusión continua; pudiendo combinar métodos. No aplastar o disolver las microesferas, ya que pierden efectividad 4,23. Pueden suministrarse por tubos de alimentación enteral Pertzye(, Creon( y Relizorb(.
Pertzye 4000(: puede administrarse 4000 UI de lipasa, mezclado con 10 ml de puré de manzana, a través de tubos de gastrostomía de 14 Fr o mayor, las veces necesarias hasta alcanzar la dosis deseada. No dar más de 2 cápsulas a través de un tubo de gastrostomía a la vez 24. Creon(: Los gránulos se pueden mezclar con alimentos blandos para bebés de pH <4.5 y administrarse, sin obstrucción, adherencia o daño visible de estos, y sin pérdida de actividad de lipasa, a través de los tubos enterales Kimberly-Clark( MIC Bolus de 14 Fr, Botón Mic-Key de Kimberly-Clark( de 14 Fr o mayores, Bard( Tri-Funnel 18 Fr y Botón Bard( 18 Fr.25 Relizorb(: es un cartucho de lipasa específicamente diseñado para alimentación enteral 25-26.
EFICACIA Y CONTROL DE LA TREP
Si bien existe una dosis de enzimas establecida para el inicio, esta se ajustará según la respuesta clínica y analítica. Al evaluar la eficacia deben valorarse aspectos como: síntomas abdominales (malestar y distensión), características de las deposiciones (número, volumen, grasa fecal) y progresión pondo-estatural. El control bioquímico de la efectividad del tratamiento se basa en la cuantificación de grasas en heces y el coeficiente de absorción de grasas 13,27.
Se recomienda monitorear el estado nutricional a intervalos regulares: mensualmente en lactantes, cada 3 meses en niños mayores y adolescentes, y cada 6 meses en adultos 11.
No todos los productos son igualmente eficaces, variando en su potencia y propiedades.
La eficacia depende asimismo del recubrimiento y tamaño de las partículas de enzima.
Idealmente debieran dosificarse según el contenido de grasa de cada comida (2.000 UI lipasa/g de grasa), ajustando las dosis hasta los límites permitidos, según respuesta clínica y analítica 13,27. Un proyecto europeo, el Proyecto MyCyFAPP, ha desarrollado un método para ajustar la dosis de enzimas necesarias en cada comida. Se trata de una aplicación instalada en el celular, que, introduciendo los alimentos a ingerir, indica a cada paciente la dosis de enzimas necesarias 11.
Respuesta inadecuada a TREP
Ante una respuesta clínica inadecuada a TREP con dosis máximas, revisar posibles factores que puedan influir en la eficacia.
a) Factores de adherencia al tratamiento, voluntaria o por desconocimiento
-Olvidar las tomas o no ingerirlas en los momentos indicados de las comidas.
-Triturar o masticar las perlas de enzimas.
-Tiempo de alimentación prolongado.
-Exposición prolongada a alimentos alcalinos.
-Ingesta excesiva de jugos / zumos / gaseosas.
-Rechazo: adolescentes y pacientes que no quieran ganar peso.
b) Factores propios de la TREP
-Caducidad o almacenamiento inadecuado de enzimas.
-Concentración incorrecta.
c) Factores que influyen sobre la adecuada actividad enzimática (4,13)
-Inactivación por pH inadecuado, relacionada a secreción disminuida de bicarbonato.
-Retraso en la liberación / variaciones en el vaciamiento gástrico y el tránsito intestinal.
-Deficiencia de ácidos biliares: Emulsión inadecuada y escasa formación micelar.
-Moco intestinal espeso.
-Sobrecrecimiento bacteriano intestinal.
-Liberación de mediadores neurohormonales inhibitorios
d) Enfermedad gastrointestinal intercurrente
Enteroparasitosis. RGE mal controlado. Síndrome de intestino corto. Enteritis pseudomembranosa. Enfermedad hepatobiliar. Enfermedad celiaca. Enfermedad inflamatoria intestinal.
Se precisan investigaciones para definir la eficacia, seguridad y efectos a largo plazo de la TREP 13. La dosificación óptima, requiere discernimiento e individualización. Se recomiendan las preparaciones patentadas 3,28.
EFECTOS ADVERSOS Y COMPLICACIONES ASOCIADOS A TREP
La TREP de origen porcino se utiliza con seguridad desde hace décadas sin efectos adversos graves. En forma infrecuente se observaron efectos leves relacionados a algunos preparados, la mayoría dosis dependiente, por administración inapropiada, o por exposición a altas temperaturas debido a conocimiento insuficiente 29,30. En raros casos pudieran relacionarse a hipersensibilidad a algún componente 19.
Efectos locales
Los efectos locales son en su mayoría dosis dependientes. La pancreatina puede producir inflamación en boca y región perianal. Los gránulos no deben ser masticados ya que su activación precoz puede causar irritación de la mucosa oral 4. Si permanecen en la boca pueden producir irritación, estomatitis y úlceras mucosas. En lactantes si no pueden ser deglutidas rápidamente, se recomienda mezclarlas con un poco de alimento al inicio de la comida. Es importante el lavado bucal tras su administración 30-32.
Efectos generales
Los síntomas y signos generales atribuidos frecuentemente son dosis dependiente y raramente relacionados a reacciones de sensibilización 32.
Efectos adversos dosis dependiente:
-Síntomas digestivos: náuseas, vómitos, meteorismo, retortijones, diarrea, estreñimiento.
-Hiperuricemia e hiperuricosuria relacionados con dosis muy elevadas.
-Carencia de hierro: la TREP prolongada pudiera disminuir la absorción de hierro.
-Colopatía fibrosante: Se reportó estenosis de colon con fibrosis en pacientes que recibían dosis de TREP superiores a 10.000 U de lipasa/kilo/peso/día. Es el principal efecto adverso y debe sospecharse ante dolor abdominal y obstrucción intestinal. Únicamente fue descrita con altas dosis de TREP y aunque la asociación es clara, su fisiopatología no es bien comprendida 4,5,13,29,30.
Efectos adversos relacionadas a hipersensibilidad: muy infrecuentes y leves 32
-Digestivos: diarrea, náuseas, calambres, dolor abdominal.
-Respiratorios: congestión nasal, estornudos, lagrimeo, rash cutáneo y urticaria, opresión torácica, dificultad respiratoria, crisis de broncoespasmo y asma.
-Cefalea y mareos, hematuria, artralgias, edema de pies o piernas.
Erróneamente son atribuidos a las TREP, las diarreas, cólicos, constipación o fallas de crecimiento relacionadas a ajustes inadecuados y dosis subóptimas de la TREP o los desajustes en las calorías para edad y peso 4,13,30.
La causa más común de efectos adversos se relaciona con el mal manejo o mal ajuste de las dosis de enzimas. Si son administradas en forma y dosis correcta, se debe adjudicar el efecto a otra causa ajena a la TREP 4,29.
CONTRAINDICACIONES
Los preparados enzimáticos estarán contraindicados en los casos excepcionales de hipersensibilidad a proteínas porcinas 32.
TREP EN PACIENTES TRATADOS CON MODULADORES CFTR
En la actualidad existen reportes sobre la recuperación de la función pancreática con la asociación de los nuevos moduladores, sin embargo, la evidencia requiere mayor solidez para apoyar la interrupción de las enzimas pancreáticas en estos pacientes 33.
CONCLUSION
La dosificación óptima de TRE, requiere discernimiento e individualización. Se precisan investigaciones que aporten mayor evidencia para definir las diferentes formas de TREP, su eficacia, seguridad y función en la mejora del estado nutricional, la calidad de vida, los efectos a largo plazo, así como precisar las dosificaciones según los rangos de IPE 13. Se recomiendan las preparaciones patentadas de enzimas pancreáticas, pues no hay evidencias sobre la eficacia de las preparaciones genéricas.
Agradecimientos a los Profesores del WG de LASPGHAN: Lucrecia Suarez Cortina (España) y Juan Rivera Medina (Perú) como revisores de los manuscritos.
Contribución de los autores:
- Dra. Josefina Monserrat Cázares: selección de artículos científicos y redacción de secciones asignadas
- Dra. Lourdes Ortiz Paranza: selección de artículos científicos y redacción de secciones asignadas
- Dra. Lorena Rodríguez González: selección de artículos científicos redacción de secciones asignadas
- Dra. Lidia Garcete Mañotti: selección de artículos científicos, organización y redacción del artículo.
- Dra. Marta Wagener: concepción del estudio, tutoría de investigación, revisión del artículo.
- Dra. Lucrecia Suarez Cortina: revisión del artículo.
- Dr. Juan Rivera Medina: revisión del artículo.
Conflicto de intereses: Los autores declaran no tener conflicto de intereses, en relación a este artículo.
Financiación: No existe fuente de financiación externa.