INTRODUCCION
El adenocarcinoma pancreático ductal (APD) es la cuarta causa de muerte por cáncer con una incidencia en aumento en ambos sexos en los países occidentales, proyectándose que se convertirá en la segunda causa para el 2030 1. El pronóstico es sombrío con una sobrevida global de menos de 9% a 5 años 2.
El diagnóstico precoz es fundamental, si bien la ictericia de tipo obstructiva orienta el diagnóstico, está presente en solo 55% de los casos, otros signos menos específicos son más frecuentes como la astenia, anorexia y pérdida de peso, así como el dolor abdominal estando presentes en más del 80 % de casos en el momento del diagnóstico. El examen por imágenes de primera línea para el diagnóstico de ADP es la Tomografía Axial Computarizada (TAC) con contraste endovenoso, teniendo una precisión diagnóstica por encima de 90% 6.
Presentamos una paciente de sexo femenino de 60 años de edad con diagnóstico de APD con infiltración venosa tratada con cirugía. En caso de tumores cosiderados “Borderlines” con infiltración venosa el riesgo de márgenes positivos es muy elevado razón por la cual un tratamiento de inducción con quimioterapia está indicado.
CASO CLÍNICO
Paciente de sexo femenino de 60 años de edad que presenta una pérdida de peso de 5 kilos en 6 meses, se realiza una ecografía donde se visualiza una formación de aspecto nodular, hipoecogénica en cabeza de páncreas de 3 cm de diámetro.
En la Tomografía Axial Computarizada con contraste endovenoso, confirma en la porción anterior de cabeza del páncreas una formación nodular sólida hipodensa de 3.4 x 2.2 cm, sin adenopatías ni lesiones a distancia, con infiltración de más de 180° y deformación de la VMS (Figura 1).
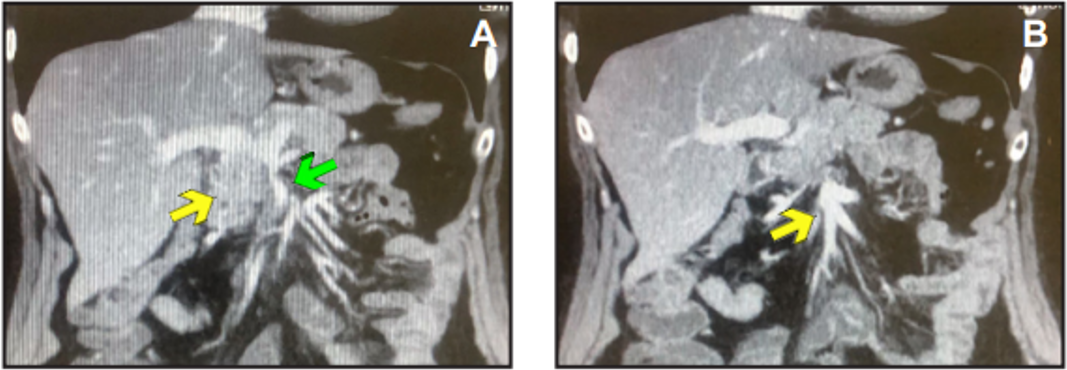
Figura 1. TAC abdominal con contraste endovenoso en fase portal A: masa pancreática sugestiva de neoplasia (flecha blanca) asociada a deformación con afinamiento de la VMS (flecha negra), B: Dilatación proximal de afluentes de la VMS (flecha blanca)
En la Ecoendoscopía, la lesión a nivel del páncreas mide 32 mm de diámetro, con contacto circunferencial de la VMS y estenosis de la misma, que al examen histológico corresponde a un Adenocarcinoma Ductal infiltrante, moderada a pobremente diferenciado. Se decide en reunión de concertación pluridisciplinaria realizar tratamiento de inducción considerando a la lesión como un APD “Borderline” de tipo venoso, resecable.
Se realizan 4 ciclos de quimioterapia de FOLFIRINOX modificado (Irinotecan, oxaplatino, leucoxetina, 5-fluorouracilo). La TAC post quimioterapia muestra una reducción del volumen del nódulo pancreático a 2,7 x 2,5 cm.
En la Resonancia Magnética Nuclear la lesión mide 27 mm de diámetro y deforma el extremo superior de la vena mesentérica superior en 360° de su circunferencia con estrechamiento de hasta un calibre de 2 mm y una longitud de 1cm, sin observarse lesiones sospechosas de metástasis hepáticas.
Durante la laparotomía, el estudio intraoperatorio de los ganglios interaórticocavos fue negativo para metástasis, sin lesiones de carcinomatosis peritoneal ni metástasis hepáticas. Luego del control de la arteria mesentérica superior que no se encuentra infiltrada, la disección confirma una infiltración de aspecto circunferencial de dos (2) cm de la vena mesentérica superior y, se procede a realizar una DPC con resección de la vena mesentérica superior de tres cm (Figura 2) asociada a una reconstrucción venosa termino-terminal, con anastomosis de la VMS a la confluencia esplenomesaráica (Figura 3) y montaje tipo CHILD.
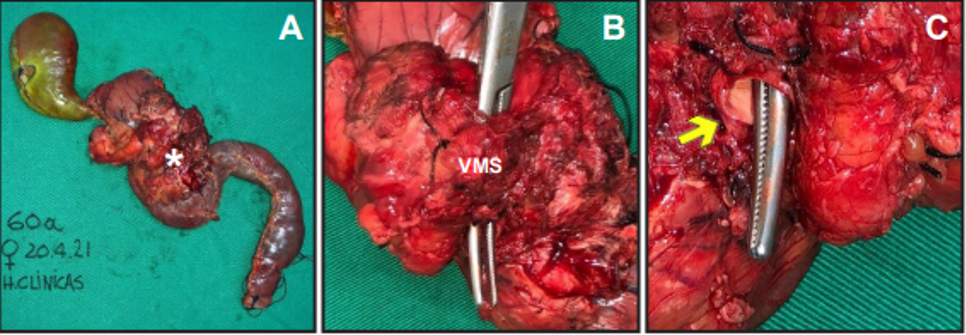
Figura 2. Imágenes de la pieza de DPC, A: Neoplasia pancreática cefálica (*), B: Tronco de la Vena Mesentérica Superior resecada, C: Intima del extremo proximal de VMS (flecha blanca)
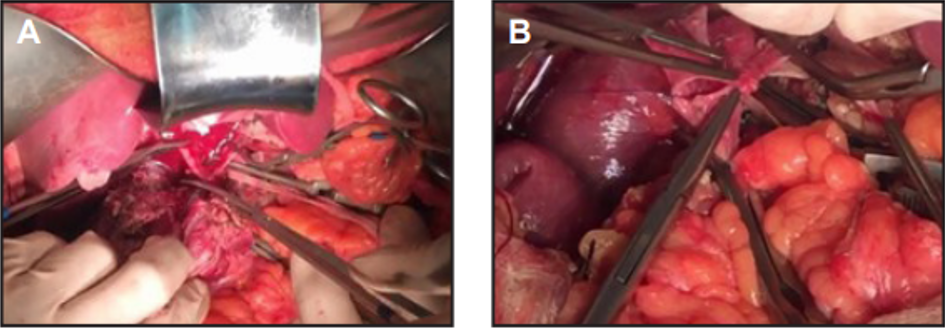
Figura 3. Cirugíavascular A: Sección de la VMS a nivel de la confluencia esplenomesentérica, B: Reconstrucción venosa por anastomosis termino-terminal de la VMS a la confluencia
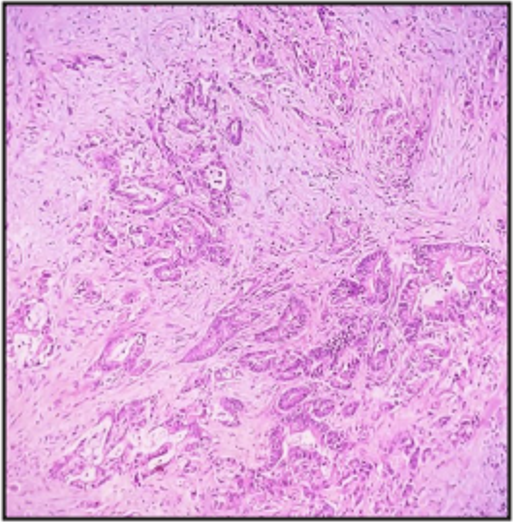
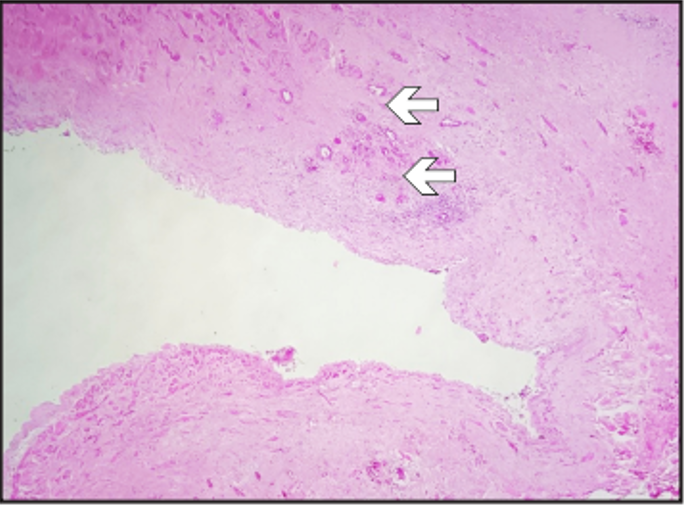
En el estudio histológico, se observó un Adenocarcinoma Ductal infiltrante, moderadamente diferenciado (Figura 4), en cuerpo del páncreas de 4,2 cm, con numerosos focos de invasión perineural e infiltración circunferencial a la pared de la vena mesentérica superior (Figura 5), con márgenes próximos a 1 mm perivascular, el más cercano. Se constató metástasis a 2 de 7 ganglios pancreático-duodenales inferiores y, fueron negativos para neoplasia: 14 ganglios peripancreático duodenales superior, anterior y posterior, así como ganglios interaortocavo 4, ganglio de la hoz de la arteria hepática común 1 y a 1 ganglio del tronco celiaco. Por lo que el TNM es ypT3, ypN1, ypM0 y, corresponde a un estadio IIB.
La paciente presenta al quinto día de post operatorio una fistula pancreática Tipo B, cicatrizada con derivados de la somatostatina y nutrición parenteral. Alta a los 17 días con evolución favorable.
DISCUSION
El adenocarcinoma pancreático ductal (APD) es la cuarta causa de muerte por cáncer con una incidencia en aumento en ambos sexos en los países occidentales, proyectándose que se convertirá en la segunda causa para el año 2030 1. El pronóstico es sombrío, con una sobrevida global de menos de 9% a 5 años 2.
En la actualidad el único tratamiento considerado curativo es la cirugía asociada a una quimioterapia ayudante. Sin embargo, solo el 15 a 20 % de estos pacientes pueden beneficiarse de una resección, lo que explica el mal pronóstico de los mismos 3.
El diagnóstico precoz es por ello fundamental para el tratamiento y el pronóstico del APD. El tiempo promedio entre la aparición del primer síntoma y el diagnóstico es de aproximadamente entre 6 a 9 semanas, dependiendo de los síntomas y del tipo del primer especialista consultado, así mismo el tiempo transcurrido entre la aparición del primer síntoma y el inicio del tratamiento tiene un impacto directo en la sobrevida 4,5.
La ictericia, si bien orienta el diagnóstico, está presente en solo 55% de los casos, otros signos menos específicos, son más frecuentes como la astenia, anorexia y pérdida de peso, así como el dolor abdominal estando presentes en más del 80 % de casos en el momento del diagnóstico. Nuestra paciente presentó pérdida de peso y astenia lo que condicionó la realización de una ecografía abdominal, sin embargo, el examen de primera línea para el diagnóstico de ADP es la Tomografía axial Computarizada (TAC) con contraste endovenoso, teniendo una precisión diagnóstica por encima de 90% 6.
El informe de la TAC debe idealmente estar estructurado según protocolos estandarizados, que analicen la resecabilidad de la lesión, así como eventuales contactos, deformaciones y/o estenosis vasculares cuantificando dichos contactos en mayores o menores de 180° 7.
La evaluación de la extensión a distancia se basa en la TAC toraco-abdomino-pélvica, no debiendo el tiempo entre la TAC y la cirugía superar las cuatro semanas por el riesgo de aparición de lesiones hepáticas y/o peritoneales descubiertas durante la cirugía 5.
El valor de los marcadores tumorales es muy limitado para el diagnóstico de APD, el único que debe ser solicitado es el CA 19-9, el alto número de falsos positivos se presenta en pacientes diabéticos y sobre todo con colestasis y una parte de los falsos negativos en pacientes con grupo sanguíneo Lewis negativo. La elevación por encima de 100 a 160, seria predictiva de una enfermedad metastásica 8. En este caso, la paciente presentó valores normales de CA 19-9.
El diagnóstico de APD puede ser fuertemente sugerido por la asociación de elementos clínicos: edad, ictericia de tipo obstructivo, vesícula palpable indolora, alteración del estado general y de imágenes: lesión hipodensa que toma el contraste en la fase tardía con dilatación proximal del conducto pancreática, atrofia parenquimatosa y dilatación de las vías biliares, además entre los diagnósticos diferenciales existen lesiones que son igualmente de tratamiento quirúrgico, calculándose el riesgo de cirugía por lesiones benignas pancreáticas no quirúrgicas de aproximadamente 7% 9.
Existen varias clasificaciones de los tumores considerados resecables, sin embargo, la más utilizada es la del National Comprehensive Cancer Network (NCCN), que se basa en la relación del tumor con estructuras vasculares, dividiéndolos de esta forma en resecables, de resección limite “Borderline” y localmente avanzados 10.
Son tumores considerados “resecables”, los que no presentan contacto con estructuras vasculares, o cuando existe un contacto aislado venoso < 180° de la circunferencia, sin irregularidades ni deformación con la Vena Mesentérica Superior (VMS) y/o la Vena Porta (VP), que permitan potencialmente una reconstrucción 10.
Son tumores “Borderlines”, cuando presentan al menos uno de los siguientes criterios: contacto < 180° de la circunferencia de la Arteria Mesentérica Superior (AMS) o del Tronco Celiaco (TC), un contacto < a 180° de la circunferencia VMS y/o VP con deformación y/o irregularidades de sus contorno o contacto> a 180° de la circunferencia de la VMS o VP 10.
“Localmente avanzados” son aquellos que presentan al menos un criterio de los siguientes: contacto> a 180° con la AMS o TC y a nivel venoso oclusión extensa de la VMS o VP o una reconstrucción imposible 10.
Dentro del plan pre quirúrgico, el drenaje de una posible ictericia debe ser selectivo, ya que puede aumentar la morbilidad de la cirugía pudiendo presentar complicaciones graves como pancreatitis necrotizantes. La necesidad de los drenajes debería ser reservado para los casos con ictericia severa, colangitis, insuficiencia renal relacionada a la hiperbilirrubinemia 11.
El objetivo de la cirugía es obtener la exéresis completa con márgenes de resección R0, asociándose a un mejor pronóstico, con una sobrevida entre 30 a 40 meses 11,12, a menudo la resección es macroscópicamente completa, sin embargo, la distancia entre los márgenes y el tumor es <1 mm, permitiendo sin embargo una sobrevida prolongada con una sobrevida actual de 5 años de 10 a 15% 13.
En caso de tumores de tipo “Borderlines” el riesgo de márgenes positivos es muy elevado razón por la cual un tratamiento de neoadyuvancia está indicado. Para los tumores de tipo “borderline” venoso, donde una resección vascular está indicada, un tratamiento de inducción con quimioterapia pre operatoria está recomendado. En estos pacientes la sobrevida luego de la cirugía es mejor cuando es asociada a un tratamiento de inducción que con la cirugía sola. 14,15. Actualmente la quimioterapia con mejores resultados es el Folfirinox, que permite obtener tasas de resecabilidad para los tumores “borderlines” secundarias de 60-65% 16,17.
En estos pacientes con resecabilidad “limite” y luego de la confirmación intraoperatoria de la ausencia de contraindicaciones, se realiza la DPC asociada a la resección venosa. Según el consenso del Grupo Internacional de Estudio de Cirugía Pancreática (ISGPS) las resecciones venosas se clasifican en: Tipo 1: escisión venosa parcial con sutura directa (venorrafia) Tipo 2: escisión venosa parcial con un reconstruida con parche; Tipo 3: resección segmentaria con anastomosis veno-venosa primaria, como es el caso de nuestra paciente donde se realizó la resección de la VMS; y Tipo 4: resección segmentaria con injerto venoso interpuesto 18.
En la bibliografía consultada, no se encontraron publicaciones de casos en Paraguay, constituyéndose éste, como el primer caso reportado.
En los ADP considerados “Borderlines” de tipo venoso, la asociación de quimioterapia de inducción a la resección pancreática y venosa permite mejorar la sobrevida, siendo recomendada actualmente como tratamiento de tipo curativo en esta patología de pronóstico sombrío.
Contribución de los autores:
Los participantes del trabajo han aportado a la redacción del borrador del artículo y la revisión crítica de su contenido, así como la revisión y aprobación del trabajo final. Dra Oertell realizó la descripción de Patología, las fotografías histológicas, así como la revisión del trabajo final.
Conflicto de intereses: no existen conflictos de interés comercial.
Fuente de Financiación: Autofinanciado por los autores.