INTRODUCCION
La fosfomicina es un antibiótico natural, que actúa sobre la síntesis de la pared celular, con actividad bactericida y de amplio espectro, que comprende cocos grampositivos y negativos, y bacilos gramnegativos aerobios y facultativos, que incluyen Serratia spp y Pseudomonas aeruginosa 1.
Es un derivado del ácido fosfónico que se identificó y notificó por primera vez en 1969, a partir de varias cepas de Streptomyces spp 2. Se ha utilizado en la mayoría de los países europeos y fue aprobado por la Administración de Alimentos y Medicamentos (FDA) en los Estados Unidos en 1996, para usarse en forma oral como fosfomicina trometamina en el tratamiento de la cistitis no complicada 3.
Además de su empleo en infección urinaria, la fosfomicina ha sido utilizado para el tratamiento de diversas infecciones como septicemia, endocarditis, peritonitis, infecciones respiratorias, osteomielitis, meningitis o encefalitis, infecciones de oído, nariz y garganta, infecciones obstétricas y ginecológicas e infecciones del pie diabético; tanto en su formulación intravenosa (sal disódica) como oral (sal cálcica o trometamol) 4. El posicionamiento de la fosfomicina aún se está por definir, cuanto más se la conoce, más beneficios potenciales se encuentran, particularmente en combinación con otros antibióticos en infecciones por gérmenes multirresistentes 5.
La fosfomicina es utilizada para el tratamiento de las infecciones urinarias, en particular la cistitis, así como también para prevención de las mismas 6. Es considerado como un antibiotico de primera línea en la cistitis aguda no complicada en publicaciones internacionales 7 y nacionales 8.
Por otra parte, algunos autores también mencionan a la fosfomicina como antibiótico de uso en infecciones urinarias complicadas de pacientes hospitalizados 9,10.
El efecto adverso más común consiste en malestar gastrointestinal leve, motivo por el que se asume que la fosfomicina tiene un perfil de seguridad elevado. La tasa de efectos adversos reportados en la literatura médica relacionada con el uso de fosfomicina oral varía entre 2 - 6%, aumentando con tasas más elevadas en enfermos que recibieron más de una dosis 3) (11,12. En pocas palabras, tiene un bajo poder tóxico que afecta solo el tracto digestivo, como ser diarreas leves 1. Puede encontrase también una hipopotasemia leve (26%), lo que sugiere que la monitorización del potasio puede ser prudente, especialmente cuando se utilizan ciclos prolongados de fosfomicina intravenosa 12. Los efectos adversos sobre la microbiota normal y la aparición de gérmenes resistentes en el organismo son mínimos 13. Después de la ingesta de una dosis única de 3 gramos el impacto sobre los microorganismos intestinales no está bien establecido. Sin embargo, un tratamiento intravenoso más prolongado con dosis elevadas (5 gramos dos veces al día durante 5 días) altera de manera importante la microbiota intestinal, produciendo principalmente una disminución de las Enterobacteriaceae 14.
Recurrir a antibióticos en uso desde hace muchos años en la asistencia clínica, obedece a la falta de nuevos antibióticos para varios tipos de infecciones 15. Así, en los últimos años, el interés por el uso de fosfomicina ha aumentado notablemente en la comunidad médica y científica, debido a la alta incidencia de microorganismos multirresistentes para los que la fosfomicina constituye, sola o en combinación, una alternativa de tratamiento 4,5,16,17.
A tener presente que también se dispone de fosfomicina de uso intravenoso, que puede resultar de mucha utilidad en infecciones urinarias complicadas como lo han demostrado recientes publicaciones 18-20.
Actividad antibacteriana.
La fosfomicina posee un mecanismo de acción único, bloqueando el primer paso de la síntesis del peptidoglucano. Este compuesto no presenta resistencias cruzadas con otros antibióticos por lo que se ha empleado para el tratamiento de patógenos multirresistentes como Staphylococcus aureus resistente a meticilina (SARM), enterobacterias productoras de BLEE y carbapenemasas, y en Pseudomonas aeruginosa multirresistentes 15. Además, la fosfomicina actúa reduciendo la adherencia de las bacterias a los epitelios, como por ejemplo al epitelio urinario 21.
En cuanto a sus propiedades físico-químicas, fosfomicina es una molécula de bajo peso molecular, soluble en agua, con baja unión a proteínas plasmáticas que difunde fácilmente a la mayoría de tejidos corporales y al líquido intersticial 22. La vida media (símbolo t1⁄2) es el tiempo necesario para que la cantidad de un fármaco se reduzca a la mitad de su valor inicial, siendo para la fosfomicina de 5 - 8 h 23,24.
Sensibilidad in vitro y efectividad in vivo.
Sir Alexander Fleming, microbiólogo británico, fue uno de los primeros en realizar una prueba de sensibilidad in vitro 25. Dentro de la primera década del inicio de la terapia antimicrobiana, las correlaciones de los resultados clínicos con las pruebas de sensibilidad empezaron a ser cuestionadas 26.
La extrapolación de los resultados microbiológicos del laboratorio a la asistencia clínica del paciente presenta muchas dificultades que puede llevar a un sobretratamiento innecesario del paciente, hecho que tiene su razón de ser en la necesidad de dar protección al doliente infectado 27. El problema central es que los agentes antibacterianos deben actuar en un ambiente complejo, en el que las propiedades antibacterianas puras, reveladas en el estudio de sensibilidad in vitro pueden ser muy influenciadas por consideraciones farmacológicas, por la enfermedad de base del paciente y por las condiciones inmunológicas del paciente 28-34.
En el país se ha encontrado en un quinquenio, a E. coli como germen causal de la mayoría de las infecciones urinarias 35, así como también se ha identificado en esta bacteria la producción de BLEE como un importante factor de resistencia a los antibióticos 36.
Dado que la cistitis aguda es la más común de las manifestaciones de la infección urinaria, y la más prevalente en las mujeres, la fosfomicina es uno de los antibióticos de primera elección para el tratamiento de esta afección, en dosis única de 3 g por vía oral. 37. Como ya hemos mencionado se ha extendido su uso en infecciones urinarias complicadas de pacientes hospitalizados y otras infecciones 4,5,9,10,16,17.
En base a estas consideraciones que apuntan a la importancia de la fosfomicina para el tratamiento de las infecciones urinarias, pretendemos con este trabajo evaluar la sensibilidad in vitro de E. coli a dicho antibiótico, a partir de urocultivos tomados en dos lapsos de colección de datos, en personas de ambos sexos incluidos cultivos de orina con gérmenes que producen BLEE.
Límites del trabajo. Este estudio in vitro, podría ser considerado como una referencia para un mejor conocimiento de la fosfomicina por el cuerpo médico del país. Naturalmente que deberán seguir estudios clínicos de infecciones urinarias tratadas con este fármaco.
MATERIALES Y MÉTODOS
Este es un estudio observacional, descriptivo, retrospectivo, con muestreo transversal no probabilístico de casos consecutivos, en el que se evaluaron muestras de orina y aislados de E. coli. Las muestras de orina se colectaron en dos periodos, noviembre de 2019 y febrero-marzo del 2021, provenientes de pacientes que concurrieron voluntariamente al laboratorio San Roque para la toma del material, con un pedido por escrito de sus médicos tratantes en el marco de una atención clínica. Los médicos tratantes solo tenían relación asistencial con los pacientes, y no forman parte del grupo de investigación.
Fueron incluidos los urocultivos con desarrollo de E. coli en cultivo monomicrobiano y recuento mayor a 10.000 UFC/mL. En el primer periodo, durante el mes de noviembre de 2019 se incluyeron 100 muestras con aislados de E. coli (Submuestra A) y en el segundo periodo, durante los meses de febrero y marzo de 2021, se obtuvieron 160 aislados de E. coli (Submuestra B).
En el proceso de estudio de las muestras de orina se cumplieron las siguientes etapas:
1. Examen físico-químico, microscópico y cultivo. Las muestras de orina fueron procesadas en la sección de Microbiología del Laboratorio San Roque. El cultivo se realizó inoculando 5 uL de orina en medios de agar sangre y agar eosina azul de metileno, las cuales se incubaron por 24 horas a 35°C 38. Por otra parte, se realizó el examen microscópico del sedimento urinario y la determinación de densidad urinaria, pH, proteínas y nitritos mediante tiras reactivas siguiendo las instrucciones del fabricante.
2. Identificación del microorganismo. Se realizó la identificación bacteriana por métodos convencionales utilizando pruebas bioquímicas de TSI (Triple Sugar Iron), citrato, lisina, SIM (Sulfuro-Indol-Motilidad), urea y RMVP (Rojo de metilo-Voges Proskauer) 38.
3. Antibiograma. La susceptibilidad frente a los antibióticos se realizó por el método de difusión de discos en agar Mueller Hinton (Oxoid®), según recomendaciones del Clinical Laboratory Standards Institute (CLSI) 39. Cada suspensión bacteriana fue preparada con solución fisiológica estéril, ajustando la turbidez a la escala 0,5 de Mc Farland, y verificada con turbidimetro. Se determinó la susceptibilidad in vitro frente a fosfomicina 200 μg, nitrofurantoina 300 μg, trimetoprima 5 μg, trimetoprima/sulfametoxazol 1.25/ 23.75 μg y ciprofloxacina 5 μg (Oxoid®). Los discos de fosfomicina utilizados contenían 200 μg con agregado de 50 μg de glucosa 6-fosfato, y en la medición de los halos de inhibición no fueron consideradas las colonias intrahalo, según lo recomendado por el CLSI 39. Se consideraron sensibles halos mayores de 16 mm, intermedios 12-15 mm y resistentes menores de 12 mm 38.
4. Detección de betalactamasa de espectro extendido. La detección de BLEE se realizó mediante el método fenotípico basado en la demostración de sinergia con discos de cefalosporinas de tercera generación: ceftazidima 30 μg y cefotaxima 30 μg colocando equidistantes a un disco de amoxicilina+ ácido clavulánico 20/10 μg. Una zona de inhibición agrandada o distorsionada alrededor de uno o ambos discos de cefalosporinas fue interpretada como sinergia entre la cefalosporina respectiva y amoxicilina + ácido clavulánico y la cepa considerada productora de BLEE 38.
5. Cepas de referencia. Se utilizaron cepas de referencia de la American Type Culture Collection (ATCC): E. coli ATCC 25922 para control de las pruebas de identificación y sensibilidad y E. coli ATCC 35218 para controlar la detección de la betalactamasa de espectro extendido.
6. Análisis estadístico. Los datos se asentaron en una planilla Excel (MS Office, Microsoft), y se analizaron con Microsoft Excel previa suscripción a Microsoft 365 y Epi Info™ 7.2.1 | CDC (CDC: Centers for Disease Control and Prevention Atlanta, Estados Unidos de América), cuyo uso no necesita suscripción ni pago.
7. Aspectos éticos. Los datos se obtuvieron de una fuente secundaria, respetando la confidencialidad de los datos personales, sin que su uso originara costos adicionales a los pacientes, quienes concurrieron libremente y por indicación médica a realizarse las pruebas analíticas. El urocultivo forma parte de un examen asistencial, por lo tanto, no necesita un consentimiento informado. Los datos resultantes de esta investigación podrían beneficiar a los pacientes para el tratamiento de la infección urinaria que padecen, y a los médicos de asistencia dotándoles de un fármaco reconocido como útil para el tratamiento farmacológico de dicha afección. Fue aprobado por el Comité de Etica en la Investigación de la Facultad de Ciencias de la Salud de la Universidad Católica de Asunción, según Acta Nº 02/2021.
RESULTADOS
En total fueron analizados 260 urocultivos, 100 (38%) en el primer periodo de observación (Submuestra A) y 160 (62%) del segundo periodo (Submuestra B) provenientes de 233 pacientes de sexo femenino (90%) y 27 de sexo masculino (10%). Esta distribución no mostró diferencia significativa entre las submuestras (p= 0,272, chi cuadrado).
Las edades del conjunto de pacientes se distribuyeron de la siguiente manera: 40 pacientes (15%) de 18 a 39 años, 60 pacientes (23%) de 40 a 59 años, y 160 (62%) con edad igual o mayor a 60 años. Las medias de edad de los pacientes no mostraron diferencia en los dos periodos de colecta, con 62,3 y 63,8 años, respectivamente (p= 0,566, t de Student).
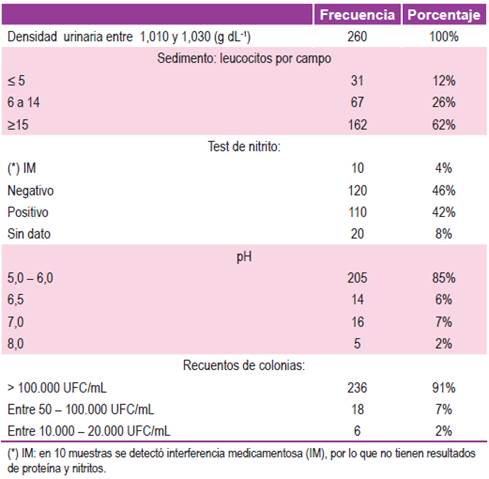
Los datos fisicoquímicos y el recuento de microorganismos se resumen en la Tabla 1.
(*) IM: en 10 muestras se detectó interferencia medicamentosa (IM), por lo que no tienen resultados de proteína y nitritos.
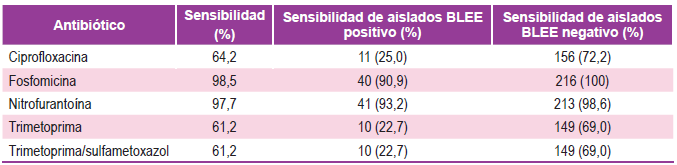
Con relación a la sensiblidad de los aislados de E. coli frente a los antibióticos evaluados se observó la mayor sensibilidad para fosfomicina (98,5%) y nitrofurantoina (97,7%). Ciprofloxacina, trimetoprima y la combinación sulfametoxazol/trimetoprima exhibieron sensibilidad menor y muy similar, con cifras de 64,2%, 61,2% y 61,2% respectivamente.
En 44 (16,9%) de los aislados de E. coli se detectó la presencia de BLEE y es destacable la alta sensibilidad que mostraron a fosfomicina y nitrofurantoína, aún frente a los aislados positivos para BLEE, con frecuencias de 90,9% y 93,2%, respectivamente. La sensibilidad del total de aislados frente a los antibióticos ensayados, y cotejada con la presencia de BLEE se resume en la Tabla 2.
Tabla 2. Sensibilidad frente a antibióticos de E. coli BLEE positivos y negativos en la muestra completa. (n=260)
A pesar que la muestra no fue diseñada para hacer comparaciones, las submuestras son muy similares en edad (medias 62,3 y 63,8 años, p= 0,566, t de Student) y distribución de sexo (87,0% y 91,3% de pacientes de sexo femenino en los grupos A y B, respectivamente (p= 0,272, chi cuadrado). En ambos periodos la mayoría de los pacientes mostró recuento bacteriano superior a 100.000 UFC/mL (A 88,0%, B 92,5%) y tampoco la frecuencia de BLEE mostró variación significativa, detectándose en 21 muestras (21%) del primer grupo y en 23 (14,4%) del segundo (p= 0,166, chi cuadrado).
Cuando se compara la proporción de aislados sensibles a los diferentes antibióticos obtenidos en las dos oportunidades, no se observan diferencias significativas, excepto para ciprofloxacina para el que se observó un aumento de la sensibilidad en el segundo grupo (Tabla 3).
DISCUSION
Si bien E. coli y la fosfomicina no se encuentran afectados directamente por la osmolaridad y el pH urinario datos que figuran en la Tabla Nº 1, estos parámetros pueden afectar la eficacia antibacteriana, por ejemplo, con el uso de los aminoglucósidos 40.
Orientan hacia el diagnóstico de infecciones la presencia de leucocituria, que en el presente estudio fue > 5 leucocitos por campo en el 88% de los urocultivos, aunque no es específica de esta afección ya que puede encontrarse en la nefritis intersticial, la poliquistosis renal o la necrosis papilar. Las tiras reactivas revelan la presencia de bacteriuria mediante la detección de la presencia de nitritos en la orina, que resultó positiva en el 42% de las muestras examinadas. Como sabemos esta prueba es poco sensible, pero específica. El control del pH urinario se situó en el 85 % de los casos entre 5,0 - 6,0. El urocultivo permite identificar el microorganismo causal de la infección urinaria y la realización del antibiograma. En nuestro estudio el 91% de las muestras presentaron recuentos de colonias > 100.000 UFC/mL 41.
En 44 (16,9%) de los aislados de E. coli se detectó la presencia de BLEE. Resulta muy importante resaltar la alta sensibilidad que mostraron estos aislados BLEE positivos a la fosfomicina así como también a la nitrofurantoína. La alta sensibilidad frente a estos antibióticos se observó con los gérmenes no productores y también con los productores de BLEE, con frecuencias de sensibilidad mayor al 90% en ambos casos, hechos que nos permiten considerar a la fosfomicina para el tratamiento empírico de la cistitis aguda en nuestra población. El mismo razonamiento rige para la nitrofurantoína. Ambos son considerados como antibióticos de primera elección para cistitis aguda no complicada de la mujer 13.
La terapia empírica con antibióticos se encuentra basada en la clínica y en la epidemiología local. Por lo tanto, justifican su indicación si el antibiótico que se pretende utilizar en un determinado caso, tiene una prevalencia de resistencia < 20% para los casos de cistitis y
< 10% en los casos de infecciones urinarias altas 42. La fosfomicina en nuestro estudio se encuentra dentro de estos rangos.
En la cistitis no complicada E. coli constituye el agente etiológico más frecuente y en el presente trabajo la menor frecuencia de resistencia se observó frente a fosfomicina y nitrofurantoína, hecho que los convierte en agentes de primera línea para tratar esta afección 43. Este hecho fue corroborado en el presente estudio, constatándose alta sensibilidad de los aislados de E. coli frente a estos dos agentes antimicrobianos, incluyendo aquellos que expresan BLEE y sin variación significativa de la eficacia in vitro entre los dos periodos de colecta analizados (Tablas Nº 2 y 3).
Una dosis de única de fosfomicina trometamol es una alternativa segura y eficaz en el tratamiento de infecciones urinarias del embarazo 44.
Las tasas de infección del tracto urinario por E. coli multirresistente (MDR) han aumentado drásticamente y el tratamiento de estas infecciones con combinaciones de antibióticos simples y dobles se ha vuelto limitado o ineficaz. Esta situación ha hecho aumentar el interés en la fosfomicina, dado que representa una opción de tratamiento 22,45.
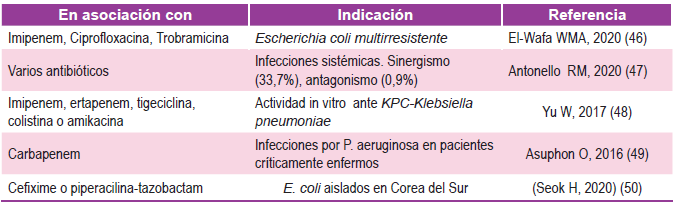
Es mencionado también en la literatura la utilización de la fosfomicina en combinación con otros antibióticos para diversas situaciones clínicas 46-50.
CONCLUSION
La alta sensibilidad demostrada en el presente estudio por E. coli a la fosfomicina, abre la posibilidad de considerar a este antibiótico como de primera elección en las infecciones urinarias bajas, aún en los casos con presencia de gérmenes productores de BLEE. Nuevas posibilidades emergentes consideran utilizarlo en asociación con otros antibióticos, ante la presencia de multirresistencia.
CONTRIBUCION DE LOS AUTORES
Francisco Vicente Santa Cruz Segovia: concepción del estudio y redacción del artículo. Norma Fariña González, María del Carmen Rolón Fernández, Alicia Pereira Fariña: contribuciones microbiológicas, realizacion de urocultivos y pruebas de sensibilidad, Alejandra Leticia Walder Encina: supervisión del proyecto, lectura crítica, conclusiones. Esteban Antonio Ferro Bertolotto: análisis de los datos, extracción de resultados, preparación de las tablas y conclusiones.
AGRADECIMIENTO
Al personal administrativo y profesional del Laboratorio del Sanatorio San Roque.
CONFLICTOS DE INTERES
Los autores declaran no tener conflictos de interés en la realización del presente estudio.