INTRODUCCION
La enfermedad de Chagas, causada por el parásito Trypanosoma cruzi, afecta aproximadamente a 6 millones de personas, distribuida en casi toda América Central y Sur. Las manifestaciones clínicas y características epidemiológicas son altamente variables entre una y otra zona endémica (1-2. En Paraguay se estima que aproximadamente 150.000 personas estarían infectadas (3. Existen áreas históricamente endémicas, como Paraguarí y Cordillera de la Región Oriental, donde la seroprevalencia en la década pasada era del 10 al 12% en el grupo etáreo de 15 a 45 años (3 y en la Región Occidental o Chaco en las comunidades indígenas las prevalencias estaban por encima del 50%4. El principal vector transmisor de la enfermedad de Chagas en la Región del Cono Sur de América ha sido el Triatoma infestans4, sin embargo, el parásito puede tener como vectores a más de 140 especies de triatominos, y los reservorios incluyen a 150 especies de 24 familias de animales domésticos y silvestres5-6. El fenómeno básico de la transmisión vectorial del T. cruzi al hombre y la adaptación de los triatominos al ecotopo doméstico, más precisamente su domiciliación, dependen de factores tales como su grado de antropofilia, disponibilidad de alimento y condiciones de la vivienda. La transmisión vectorial se lleva a cabo principalmente a través de vectores estrictamente domiciliados. En Paraguay, se ha logrado la eliminación de la transmisión vectorial intradomiciliar por T. infestans en la Región Oriental en el año 2008 y se encuentran desde esa fecha bajo vigilancia entomológica, esta situación crea un nicho disponible para T. sordida (vector secundario abundante en peridomicilio en áreas rurales)7. En reportes previos de nuestro grupo de trabajo, sobre la capacidad vectorial de la especie T. sordida provenientes de áreas endémicas de la Región Oriental (año 2005 al 2007) y Occidental (años 2013 al 2015) del Paraguay, ya se describió una elevada colonización e infección natural. En el departamento de Concepción (R. Oriental) la colonización intradomiciliar fue del 44% con una infección natural del 11%8; mientras que en el Chaco Paraguayo (R. Occidental) se ha estimado un 87% de riesgo de transmisión de T. cruzi intradomiciliar por T. sordida9. Estos resultados evidencian la capacidad adaptativa de esta especie al domicilio, y un incremento de su potencial vectorial para transmitir la enfermedad de Chagas en áreas del país. Con el fin de ampliar el estudio sobre este vector en otros departamentos, el presente estudio tuvo como objetivo emplear biomarcadores moleculares para evaluar el impacto de la infestación intra y peridomicilar de T. sordida en viviendas bajo vigilancia entomológica de departamentos de la Región Oriental del Paraguay en el período 2007 al 2015.
MATERIALES Y MÉTODOS
Área de estudio y población: Se analizaron un total de 559 ejemplares de T. sordida con datos epidemiológicos como sitio de captura y estadío, distribuidos de la siguiente manera: 335 ejemplares de 253 viviendas de Paraguarí, 144 ejemplares de 91 viviendas de San Pedro y 80 ejemplares de 52 viviendas de Cordillera, capturados en el período 2007 al 2015 por funcionarios del SENEPA (MSP y BS) y conservados a -20°C. Los triatominos fueron clasificados taxonómicamente según Lent y Wygodzinsky10 y analizados por microscopía óptica por funcionarios del departamento de Entomología del SENEPA. La captura de los ejemplares en cada vivienda corresponde a una actividad realizada dentro de la vigilancia entomológica del Programa Nacional de Chagas, en localidades previamente fumigadas por la presencia de T. infestans (vector primario).
Disección de triatominos: Se disectó el contenido abdominal de los 559 ejemplares de T. sordida colocados en tubo individuales con buffer de lisis compuesto por solución Tris pH 7,4, EDTA, NaCl y SDS8-9.
Extracción de ADN: Para la extracción de ADN se realizó la incubación de cada tubo con 5 ul de proteinasa K (20 g/mL) a 60ºC por 1 hora. La enzima fue inactivada por calentamiento a 95ºC por 10 minutos. El ADN fue purificado por el método de extracción: fenol-cloroformo descrito por Sambrook et al.11) y precipitación con etanol puro, previa adición de 20 μg de glucógeno y acetato de sodio 3M, pH 5,4 en un 10% del volumen recuperado. El pellet de ADN se resuspendió en 100 μL de agua destilada estéril8-9.
Infección natural con T. cruzi : La identificación especie específica de T. cruzi se realizó por el método PCR empleando como blanco las secuencias repetitivas de ADN nuclear (microsatélites) de T. cruzi, con los cebadores TCZ1 y TCZ2 descrito por Moser et al. y ADN kinetoplastídico con cebadores 121 y 12212. Los productos amplificados fueron analizados en geles de agarosa al 2%, teñidos con bromuro de etidio y visualizados bajo un transiluminador UV.
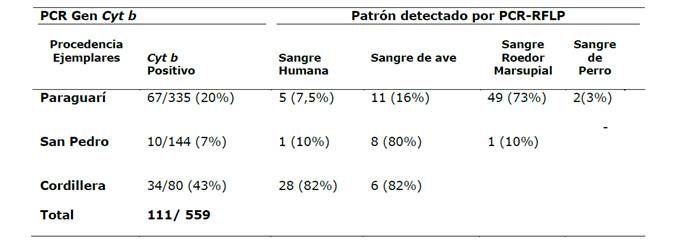
Detección de fuente de alimentación: Para la identificación de la fuente de alimentación se empleó como marcador molecular el gen del citocromo b (Cyt b), por medio de la técnica Reacción en Cadena de la Polimerasa seguida de Polimorfismo de Longitud de Fragmentos de Restricción (PCR-RFLP). Para la PCR que amplifica el gen mitocondrial Cyt b se utilizaron los cebadores Cyt b1 y Cyt b2 y para la RFLP de los productos amplificados se emplearon las enzimas de restricción: Hae III y Mwo I; descrito por Osnaghi et al. y Mota et al.13-14, que permite la determinación de los patrones de alimentación. El ADN de 4 especies se empleó como controles positivos: humano, ave (gallina), roedor y perro según protocolo descrito por Chena et al.15. Los productos amplificados fueron analizados por electroforesis en geles de agarosa al 2%, teñidos con bromuro de etidio y visualizados bajo un transiluminador UV.
RESULTADOS
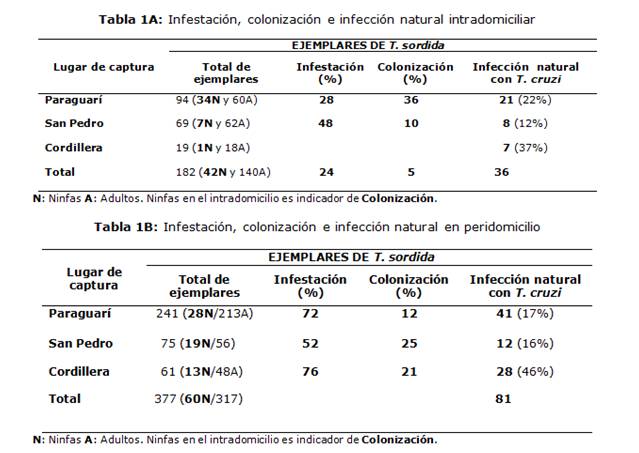
Se analizaron un total de 559 ejemplares de T. sordida, provenientes de los departamentos Paraguarí, Cordillera y San Pedro de la Región Oriental capturados en los años 2007 al 2015. En cuanto al lugar de captura y estadío, se observó una infestación intradomiciliar del 28%, 48% y 24% y un índice de colonización (ninfas en el intradomicilio) de 36%, 10% y 5%, en Paraguarí, San Pedro y Cordillera respectivamente. El número de ejemplares capturados en el peridomicilio en los tres departamentos fue mayor que en el domicilio: 241/335 (72%) triatominos en Paraguarí, 75/144 (52%) triatominos en San Pedro y 61/80 (76%) triatominos en Cordillera (Tablas 1A y B).
Tablas 1Ay B: Sitio de captura (Intra/ Peridomiciliar), colonización e infección natural de los 559 ejemplares de T. sordida por departamento- Estadíos (ninfas: N, adultos: A)
Identificación de infección natural con T. cruzi por PCR: Se detectó infección natural con T. cruzi en 117 de 559 (21%) ejemplares capturados, con un mayor índice de infección en ejemplares de Cordillera 44% (35/80), seguido por Paraguarí 19% (62/335) y San Pedro 14% (20/144). Tablas 1A y B. En la Figura 1 se puede observar los productos de PCR obtenidos con los cebadores 121-122.

Figura 1: Amplificación de ADN de T. cruzi en T. sordida. Productos amplificados de ADN de T. cruzi en T. sordida con los cebadores 121, 122 que arrojan un tamaño de 330 pares de bases (pb). Carril 1: Marcador de peso molecular de 100pb. Carril 2: control positivo de reacción de PCR equivalente a 100 parásitos. Carriles 3 y 5: muestras de T. sordida con T. cruzi positivo equivalentes a 100 parásitos. Carril 4: control positivo de reacción equivalente a 10 parásitos.
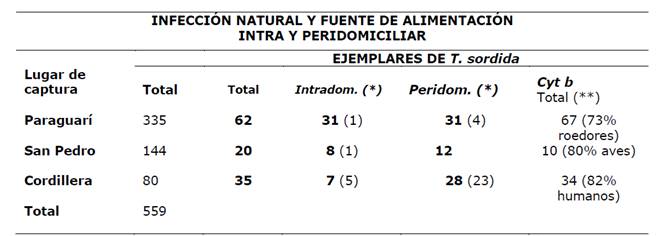
Fuente de alimentación: Del total de 559 ejemplares analizados, 111 (20%) dieron positivos para el cyt b, ver en la Tabla 2. Sangre de roedores/marsupiales fue mayoritaria como fuente de alimentación en Paraguarí 49/67 (73%), mientras que el 80% de los 10 ejemplares positivos de San Pedro contenían en el abdomen sangre de aves. Un elevado porcentaje de triatominos con sangre humana como fuente de alimentación, se detectó en Cordillera en 28 (82%) ejemplares de T. sordida de los 34 cytb positivos capturados en ese departamento; y 5 de los 7 triatominos infectados con T. cruzi y capturados en el intradomicilio se habían alimentado con sangre humana (Tabla 3). En la Figura 2 se pueden observar los amplificados del gen cyt b en las muestras de T. sordida y en la Figura 3 se observan los patrones de alimentación obtenidos con la enzima Hae III.

Figura 2: Amplificación del gen cyt b en las muestras de T. sordida. Carril 1: control positivo ADN de la especie ave (gallina). Carriles 2, 3 y 4: muestras de T. sordida cyt b positivas. Carril 5: control positivo de ADN humano. Carril 6: Marcador de peso molecular de 100 pares de bases.
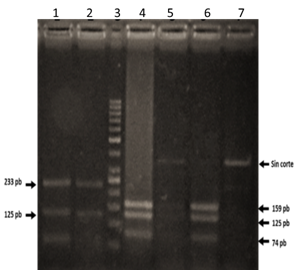
Figura 3: Patrones de alimentación en T. sordida con Hae III. Carril 1: Control positivo de especie humana con productos de 125 y 233 pb. Carril 2: muestra de T. sordida con patrón de sangre humana. Carril 3: Marcador de peso molecular de 50pb. Carril 4: Control positivo de la especie ave (gallina) con productos de 74, 125 y 159 pb. Carriles 5 y 6: muestras de T. sordida con patrón de sangre de gallina. Carril 7: producto de T. sordida cyt b positivo sin corte con Hae III con un tamaño de 358 bp.
Tabla 3: Sitio de captura (Intra/ Peridomiciliar) e infección natural asociados a la fuente de alimentación de los 559 ejemplares de T. sordida por departamento.
(*) sangre humana. (**) preferencia alimenticia mayoritaria detectada por la técnica PCR-RFLP aplicada al gen Cytb ( ) ejemplares que dieron sangre humana como fuente de alimentación e infección con T. cruzi en intra y peridomicilio.
DISCUSIÓN
En este estudio se detectaron una elevada infestación y colonización intradomiciliar de ejemplares de T. sordida en las viviendas de tres departamentos de la Región Oriental, además de una frecuencia importante de infección natural con T. cruzi y sangre humana como fuente de alimentación. La especie T. sordida representa un problema epidemiológico en numerosos países del Cono Sur debido a su amplia valencia ecológica, que se manifiesta en su hallazgo en biotopos silvestres, peridomésticos, así como dentro de la vivienda16. Se destaca la elevada frecuencia de infección natural con T. cruzi en T. sordida de los dptos. Paraguarí, San Pedro y Cordillera (19%, 14% y 44%) respectivamente, en estudios anteriores de nuestro grupo de trabajo sobre la capacidad vectorial de la especie T. sordida provenientes de áreas endémicas, se reportó en el departamento de Concepción 44% de colonización intradomiciliar y 10,6% de infección natural8 y en la Región Occidental en un estudio publicado en el año 2016, realizado con T. sordida de los tres departamentos de la región, capturados en los años 2010-2013 se había detectado en 147 viviendas, infestación y colonización en el intradomicilio y peridomiciliar del 8.2% y 53.7% respectivamente, además se estimó un elevado riesgo de transmisión de T. cruzi intradomiciliar que fue del 87%9. Otro estudio del año 2018 realizado con 220 ejemplares de T. sordida capturados en 67 viviendas de 24 localidades del Chaco Paraguayo en los años 2014-2016, se detectó infestación y colonización en el intradomicilio del 19% y 38% y en el peridomicilio 81% y 80%, respectivamente e infección con T. cruzi en un 17,3% de los ejemplares analizados17. En países de la Región del Cono Sur, como en Argentina, existen estudios que reportan desde el 2% hasta el 12% de infección natural en ejemplares de T. sordida capturados en el peridomicilio18,19.
La densidad de ejemplares de T. sordida en el peridomicilio detectada en este estudio fue mayor que en el domicilio, hecho que concuerda con lo reportado en la Región18,19 lo que evidencia una adaptación aún fuerte de T. sordida al peridomicilio.
En cuanto a la fuente de alimentación detectados en los ejemplares analizados, se destaca la sangre humana como fuente mayoritaria de alimentación en los ejemplares de los tres departamentos en un 7,5%, 10% y 82% respectivamente. En Paraguay ya en 1997 se realizaron estudios sobre las preferencias alimentarias de triatominos con antisueros, uno de ellos realizado con poblaciones domiciliarias y peridomiciliarias de triatominos procedentes de Paraguarí reportó tres fuentes de alimentación más frecuentes: sangre de aves de corral (50,2%), sangre humana (14,7%) y de perro (5,3%), con menor frecuencia se encontró sangre de gato y roedores20. En Brasil ya se habían reportado datos similares en cuanto a hábitos alimenticios de ésta especie de triatomino en regiones de ese país21.
Nuestro grupo de trabajo ha realizado estudios con T. sordida en lo referente a fuente de alimentación por el método PCR-RFLP del gen cyt b en ejemplares de áreas de las Regiónes Oriental y Occidental, en un estudio publicado en el año 2012, sobre un total de 216 ejemplares capturados en el departamento de Concepción, 11 dieron cyt b positivos, de los cuales 8 dieron patrón de sangre humana y 1 ejemplar dio sangre de gallina como patrón alimenticio8 Un estudio en T. sordida de la Región Occidental publicado recientemente detectó la fuente de alimentación en 13 de 220 ejemplares de T. sordida analizados (6%), todos resultaron positivos para sangre de gallina y correspondían a captura en el peridomicilio17.
Se destaca en éste estudio el elevado porcentaje de triatominos con sangre humana detectada como fuente de alimentación, en los que también se detectó una frecuencia elevada de infección natural con T. cruzi así como infestación y colonización intradomiciliar. Estos resultados evidencian la capacidad adaptativa de esta especie al domicilio, y un incremento de su potencial vectorial para transmitir la enfermedad de Chagas en áreas del país.