INTRODUCCIÓN
El género Flavivirusstá conformado por 53 especies virales, entre ellos, los de mayor importancia en la salud pública son el virus del dengue (DENV), el virus Zika (ZIKV), el virus de la encefalitis de San Luis (SLEV), el virus de la fiebre amarilla (YFV), el virus del Nilo Occidental (WNV) y el virus de la encefalitis japonesa (JEV). Los mismos son trasmitidos por artrópodos, principalmente mosquitos y poseen un genoma compuesto de ácido ribonucleico (ARN) de simple hebra, lineal y de polaridad positiva1. Son responsables de una considerable morbi-mortalidad que puede causar en humanos desde cuadros febriles hasta afecciones graves como encefalitis, fiebres hemorrágicas y hepatitis2,3.
Los flavivirus que han sido detectados en el Paraguay son el DENV, el YFV y el ZIKV. El DENV puede provocar desde un cuadro febril leve hasta casos graves y es el causante de epidemias año tras año desde su primera introducción al país en 1999. El YFV puede producir una enfermedad febril con hemorragias e ictericia, este virus fue detectado en nuestro país por última vez en el 2008. El ZIKV se encuentra asociado a cuadros febriles y a malformaciones congénitas, el mismo fue introducido al territorio nacional en el 2015 detectándose 6 casos, y luego en 2016 se reportaron 8 casos confirmados4. El dengue es endémico en Paraguay y se han observado grandes epidemias causadas por este virus, ocurriendo algunas de las mayores epidemias entre 2011-2013. Así, en 2011 fueron registrados 42.264 casos, 97 de dengue grave y 62 muertes5. En 2012, se detectó por primera vez el DENV-4, y se observó un total de 14.873 casos, con 42 muertes6. Mientras que en 2013, fueron notificados al sistema de vigilancia 154.287 casos de síndrome febril agudo, de los cuales 31.314 fueron casos confirmados de dengue por laboratorio y/o nexo epidemiológico7.
Existen varias técnicas para el diagnóstico de los flavivirus, entre ellas las técnicas moleculares poseen la ventaja de ser sensibles y específicas, son capaces de identificar los tipos como en el caso del DENV y además es posible diferenciar los flavivirus evitando las reacciones cruzadas, las cuales representan una de las grandes dificultades de las técnicas serológicas en el diagnóstico de estos virus8.
Por ello, el objetivo de este estudio fue detectar infecciones por flavivirus mediante una reacción de RT-nested PCR genérica descripta por Sánchez Seco et al. en 195 muestras de individuos con sospecha de dengue y negativos para el antígeno NS1 (método inmunocromatográfico), procedentes del área metropolitana de Asunción en el periodo 2011-2013.
MATERIALES Y MÉTODOS
Diseño y muestreo
Se llevó a cabo un estudio observacional descriptivo de corte transverso, con muestreo no probabilístico por conveniencia. Las muestras fueron colectadas en el Servicio del “Laboratorio de urgencias, hormonas y marcadores tumorales” del Hospital Central - Instituto de Previsión Social (HC-IPS) en épocas correspondientes a epidemias de dengue de 2011 (febrero a mayo), 2012 (febrero a mayo) y 2013 (enero a mayo).
En el presente estudio fueron incluidas 195 muestras de pacientes febriles (hasta 5 días del inicio de fiebre) con sospecha clínica de infección aguda por DENV y con resultado negativo para el antígeno NS1 de DENV por el método inmunocromatográfico para DENV (Standard Diagnostics, Inc., Corea). De las muestras incluidas en el estudio 56/195 (28,7%) correspondieron al 2011, 61/195 (31,3%) al 2012 y 78/195 (40,0%) al 2013.
Cada muestra estuvo acompañada de una ficha que incluía las características clínicas (fiebre, cefalea, dolor retro-ocular, entre otros), epidemiológicas y demográficas.
Todos los pacientes incluidos en el estudio presentaron como máximo 5 días desde el inicio de las manifestaciones clínicas.
El presente estudio fue aprobado por los Comités Científico y Ético del IICS - UNA, con código de aprobación P34/2012. Las muestras de los pacientes fueron codificadas, para asegurar la confidencialidad de los datos y proteger la identidad de los pacientes.
Controles positivos utilizados
Como controles positivos para la detección del genoma de flavivirus y tipos de DENV se utilizaron cepas virales de DENV cedidas por el Dr. Víctor Aquino del Laboratorio de Virología de la Facultad de Ciencias Farmacéuticas de Ribeirão Preto - Universidad de São Paulo, (FCFRP-USP), Brasil. Se incluyeron las siguientes cepas: DENV-1 cepa Mochizuki con título de 1x108 unidades formadoras de placas/mililitro (UFP/mL), DENV-2 cepa NGC con título de 5,75x106 UFP/mL y DENV-3 cepa BR/D3 SL3/2002 con título de 1x107 UFP/mL, provenientes de sobrenadante de cultivo celular de células C6/36 con 20% de suero fetal bovino (SFB). La cepa control para el DENV-4 fue la H241 con título 6,3x108 PFU/mL obtenida de cerebro de ratón lactante (tipo BALB/c). Los controles positivos fueron conservados a -70°C hasta su utilización.
Extracción de ARN viral
La extracción de ARN viral se llevó a cabo a partir de 200 µL de suero de pacientes con el kit comercial AxyPrep™ Body Fluid Viral DNA/RNA Miniprep Kit (Axygen Biosciences, EEUU) siguiendo las instrucciones del fabricante. El ARN extraído fue almacenado a -70°C hasta su procesamiento.
Búsqueda del genoma de flavivirus mediante RT-nested PCR genérica
La búsqueda del genoma de flavivirus se realizó a través de la reacción de RT-nested-PCR descripta por Sánchez Seco et al. 2005, con algunas modificaciones (SS1)(9). La retrotranscripción (RT) para la obtención del ácido desoxirribonucleico complementario (cADN) a partir del ARN previamente extraído se realizó utilizando una transcriptasa reversa Moloney Murine Leukemia Virus (M-MLV) (Promega, EEUU) y random primers (Byodinamics, AR). Posteriormente se realizó la reacción de nested PCR descripta por Sánchez Seco et al., 2005. Se realizó la corrida electroforética del producto de amplificación obtenido (143 pares de bases, pb) en gel de poliacrilamida al 7% (con relación de acrilamida-bisacrilamida de 29/1) con marcador de peso molecular de 100 pares de bases (pb). Para visualizar el producto de amplificación se utilizó tinción con nitrato de plata(10).
Determinación del límite de detección de la reacción de RT-nested-PCR genérica para flavivirus
Para la determinación del límite de detección de la reacción de RT-nested-PCR para el genoma de flavivirus se utilizó la cepa Mochizuki de DENV-1 con un título de 1x108 UFP/mL, realizando diluciones seriadas hasta la dilución 10-10 que fueron analizadas a través de la reacción de RT-nested-PCR. Este ensayo se realizó por triplicado.
El límite de detección de la reacción corresponde a la concentración de virus presente en la dilución más baja del control utilizado que resultó positivo.
Posteriormente, se realizó la detección del genoma de flavivirus por la RT-nested PCR genérica en las 195 muestras de suero incluidas en el estudio.
Búsqueda del genoma de DENV
La búsqueda del genoma del DENV fue realizada en todas las muestras positivas para el flavivirus, a través de dos reacciones de multiplex RT-nested PCRs que amplifican fragmentos de la región NS5 del genoma descriptas por: 1) Sánchez Seco et al., 2006 (SS2, utilizando el producto de la primera reacción de la RT-nested PCR genérica para flavivirus previamente descripta)11 y 2) Bronzoni et al., 2005 (empleando cDNA obtenido por la técnica previamente descripta)12.
En ambas reacciones, se realizó la corrida electroforética en gel de poliacrilamida al 5% con marcador de peso molecular de 100 pb. Para visualizar el producto de amplificación obtenido en la nested PCR se tiñó el gel con nitrato de plata, detectándose la presencia de genoma de DENV-1-4 por la diferencia de tamaños de los productos de amplificación10.
Determinación del límite de detección de las multiplex RT-nested-PCR específicas para DENV
Para determinar el límite de detección de ambas reacciones de detección y tipificación de DENV se utilizó la cepa Mochizuki de DENV-1 con un título de 1x108 UFP/mL y la cepa NGC de DENV-2 con un título de 5,75x106 UFP/mL, realizando diluciones seriadas de los mismos (de 10-2 a 10-11) y posteriormente se llevó a cabo la multiplex RT-nested-PCR según las indicaciones mencionadas previamente. El ensayo fue realizado por triplicado.
Se consideró a la concentración de virus presente en la dilución más baja de los controles utilizados que resultaron positivos como el límite de detección de las reacciones.
Posteriormente a lo mencionado se realizó la detección del genoma de DENV en todas las muestras positivas para flavivirus, por ambas multiplex-RT-nested PCRs.
Todas las muestras positivas para el genoma de DENV con resultados discordantes entre los multiplex RT-nested PCRs se confirmaron por la repetición del ensayo a partir de una alícuota del ARN previamente extraído
Secuenciación de productos de amplificación de muestras con resultados discordantes entre reacciones para detección de DENV
Se sometieron a secuenciación las muestras positivas para flavivirus con resultados discordantes entre las reacciones de multiplex RT-nested PCRs para tipificación de DENV. En estos casos fue secuenciado el fragmento de 143 pb obtenido a partir de la reacción de PCR genérica para la detección de flavivirus (primers Flavi 2+ y Flavi 2- ). Además, se intentó secuenciar los productos de amplificación procedentes de la primera reacción de ambas metodologías a fin de analizar posibles variaciones en las regiones donde hibridan los primers.
Los fragmentos amplificados fueron purificados mediante el kit comercial AxyPrep DNA Gel Extraction (Axygen Biosciences, EEUU) siguiendo las instrucciones del fabricante y posteriormente fueron sometidos a secuenciación a través del servicio de la empresa Macrogen (Seúl, Corea del Sur).
Las secuencias de nucleótidos fueron analizadas y editadas con el software BioEdit v7.0.7.0. Las secuencias obtenidas se compararon mediante el algoritmoBasic Local Alignment Search Tool(BLAST) con las secuencias de nucleótidos del gen NS5 de los flavivirus existentes en la base de datos del GenBank del NCBI (http://blast.ncbi.nlm.nih.gov/Blast.cgi)13.
RESULTADOS
Características clínicas y demográficas de los pacientes
De las 195 muestras de individuos con sospecha de dengue y con resultado de antígeno NS1 de DENV negativo por método inmunocromatográfico, el 40% (78/195) correspondió a varones y el 60% (117/195) a mujeres. La mediana de edad de los mismos fue de 27 ±19 años, con un rango de 1 a 86 años. El 53,9% del total de pacientes tenía menos de 30 años.
Con respecto a las manifestaciones clínicas referidas por los pacientes se registró una amplia variedad de signos y síntomas. Los síntomas más frecuentes fueron cefalea y mialgias con 66,7% (130/195) y 61,5% (120/195), respectivamente. No se refirieron manifestaciones clínicas graves.
En cuanto a la distribución geográfica de los pacientes según su procedencia, se consideró la división política del Paraguay en 17 departamentos distribuidos en dos grandes regiones: Oriental y Occidental. Los casos provenían de 20 ciudades correspondientes a 3 departamentos del país. La mayoría de los casos eran del área de Gran Asunción (Departamento Central - Región Oriental), que incluye área metropolitana de Asunción, Mariano Roque Alonso, San Lorenzo, Luque, Ñemby, Capiatá, Limpio, Fernando de la Mora, Lambaré, San Antonio y Villa Elisa; y otras ciudades como Areguá, Villeta e Ypané, pertenecientes al mencionado Departamento. La mayoría de los casos, 37,4% (73/195), refirieron proceder de distintos barrios de Asunción, dos pacientes eran de la ciudad de Emboscada (Departamento de Cordillera), y otro de Villa Hayes (Departamento de Presidente Hayes -Región Occidental), ciudades que limitan con el Departamento. Un paciente procedía de Ciudad del Este (Departamento de Alto Paraná), ciudad que limita con el Brasil.
Determinación del límite de detección de la reacción de RT-nested-PCR genérica para flavivirus
En la Figura 1 se muestra la presencia de un fragmento de amplificación hasta la dilución 10-7 del control (DENV-1 cepa Mochizuki con título de 1x108 UFP/mL), por lo cual el límite de detección obtenido fue de 0,2 UFP (10 UFP/mL).
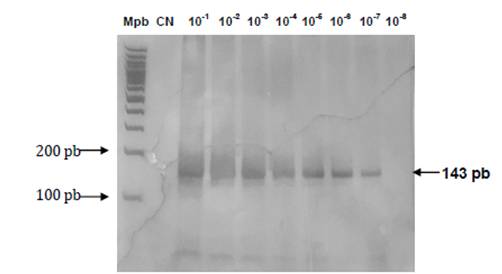
Figura 1 Límite de detección de la RT-nested PCR genérica de flavivirus utilizando los primers Flavi2+ y Flavi2-. Electroforesis en gel de poliacrilamida al 7% de los productos amplificados para el fragmento del gen NS5 de flavivirus. Carril 1: marcador de 100 pb (Mpb). Carril 2: Control Negativo (CN). Carriles 3 al 10: diluciones del control positivo de 10-1 a 10-8 (DENV-1 cepa Mochizuki con título de 1x108 UFP/mL)
Determinación del límite de detección de la multiplex RT-nested-PCR para DENV según SS2
En relación al control para DENV-1 (DENV-1 cepa Mochizuki con título de 1x108 UFP/mL) utilizado se observó la presencia de amplificación hasta la dilución 10-8, por lo tanto se detectó hasta una concentración del control de: 1 UFP/mL, lo cual equivale a 0,02 UFP por reacción, mientras que para DENV-2 se observó fragmento de amplificación hasta la dilución 10-5 del control (DENV-2 cepa NGC con título de 5,75x106 UFP/mL) lo cual corresponde un límite de detección de 0,9 UFP (57,5 UFP/mL).
Determinación del límite de detección de la multiplex RT-nested-PCR para DENV según Bronzoni et al., 2005
El control para DENV-1 (DENV-1 cepa Mochizuki con título de 1x108 UFP/mL) resultó positivo hasta la dilución 10-9. Por lo tanto, el límite de detección fue de 0,002 UFP (10-1 UFP/mL), mientras que para DENV-2 se observó fragmento de amplificación hasta la dilución 10-10 del control (DENV-2 cepa NGC con título de 5,75x106 UFP/mL), lo cual corresponde a un límite de detección de 1x10-5 UFP (5,75x10-4 UFP/mL).
Detección del genoma viral de flavivirus por RT-nested-PCR genérica en el suero de pacientes con sospecha de infección aguda por DENV
De las 195 muestras incluidas en este estudio, 43 resultaron positivas para el genoma de flavivirus, lo cual equivale al 22% de las muestras estudiadas.
Detección del genoma de DENV en sueros de pacientes positivos para flavivirus por multiplex RT-nested PCR adaptada de SS2
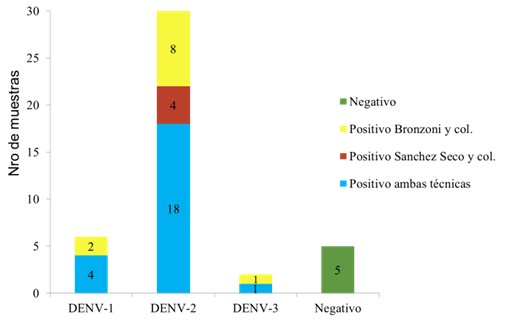
Del total de 195 muestras, 43 fueron positivas para flavivirus, de las cuales 27 (62,3%) fueron positivas para DENV, y de ellas 4 (9,3%) fueron positivas para DENV-1, 22 (51,1%) para DENV-2 y 1 (2,3%) para DENV-3.
Detección del genoma de DENV en el suero de pacientes positivos flavivirus por multiplex RT-nested PCR adaptada de Bronzoni et al., 2005(12)
Del total de 43/195 muestras positivas para flavivirus, 34 (79%) fueron positivas para DENV mediante esta reacción, de las cuales 6 (13,9%) correspondían a DENV-1, 26 (60,4%) a DENV-2 y 2 (4,6%) a DENV-3.
Como se puede observar en la Figura 2, al comparar los resultados obtenidos por ambas metodologías, se vieron resultados concordantes en 28/43 (65,1%) muestras, de las cuales 23 fueron positivas y 5 negativas. De las 23 muestras positivas para DENV, se identificaron 4 casos de DENV-1, 18 de DENV-2 y 1 de DENV-3.
Por otro lado, 4 muestras fueron detectadas solamente por la reacción de SS2, las mismas correspondieron a DENV-2. Además, 11 muestras fueron identificadas únicamente por la reacción de Bronzoni (2 DENV-1, 8 DENV-2 y 1 DENV-3). No se observaron discrepancias entre los tipos de DENV identificados por ambas metodologías.
Finalmente resultaron positivas para el genoma de DENV por una o ambas PCRs 38/43 muestras de suero, equivalente al 88,4% de las mismas y 5 muestras resultaron indeterminadas (positivas para Flavivirus y negativas para DENV).
Confirmación de los resultados obtenidos por secuenciación:
Secuenciación del amplicón de la reacción de RT- nested PCR para detección de flavivirus (143 pb) de los casos que presentaron resultados discrepantes por las reacciones de multiplex RT-nested PCR para DENV
De las 15 muestras que presentaron resultados discrepantes entre ambas metodologías utilizadas para detectar los tipos de DENV 1-4, en 10 de las mismas fue posible obtener un fragmento que cumplió con los requerimientos para la secuenciación (concentración mínima de 10 ng/uL). Luego de analizar por BLAST las secuencias obtenidas, se observaron porcentajes de identidad del 97 al 100% con cepas de DENV-2 depositadas en el GenBank.
A fin de descartar que la discordancia entre los resultados obtenidos entre ambas técnicas (multiplex RT-nested PCR) utilizadas para la detección de tipos de DENV, se deba a la presencia de mismatch en la región de hibridación de primers. Se procedió a secuenciar la primera reacción. Solo pudo ser secuenciado el producto de la primera reacción de una muestra, para la cual se obtuvo un resultado positivo para DENV-2 por la reacción de Bronzoni et al., 2005(12) pero resultado negativo por la reacción de Sánchez Seco et al., 2006. En la Figura 3 se muestra el alineamiento parcial de la secuencia obtenida con el primer ND2 (Sánchez Seco et al., 2006) y se puede observar que existe un alineamiento perfecto entre la secuencia obtenida y el primer, por lo tanto no existe mismatch en la región de hibridación en este caso.
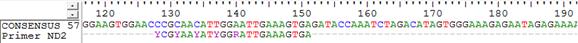
Figura 3 Alineamiento para verificar mismatch en la región de hibridación del primer . Secuencia obtenida de la región parcial del gen NS5 de una muestra positiva para DENV-2 (por reacción de Bronzoni et al., 2005) utilizando primers FG1 y FG2 alineada con el primer ND2 (Sánchez Seco et al., 2006). (R= A o G, Y= C o T)
DISCUSIÓN
Los flavivirus son una preocupación real para la salud pública9. En este estudio se implementaron técnicas de biología molecular que permitieron el estudio de infecciones por flavivirus en individuos con sospecha clínica de dengue y resultado negativo para antígeno NS1 de DENV, provenientes del área metropolitana de Asunción, en el periodo 2011 a 2013.
Las técnicas utilizadas para diagnóstico y vigilancia deben ser rápidas, simples y deben detectar un amplio número de patógenos con elevada sensibilidad. El uso de primers universales especialmente los género-específico permiten la detección de varios virus que se encuentran dentro de un mismo grupo, posibilitando el diagnóstico de un número mayor de infecciones.
En el presente trabajo se estandarizaron técnicas, obteniéndose buenas sensibilidades: reacción de RT-nested PCR Flavivirus con una sensibilidad de 0,2 UFP por reacción, y multiplex RT-nestedPCR para tipos de DENV según SS2 de 0,02 UFP por reacción y 0,9 UFP por reacción para DENV-1 y DENV-2 respectivamente; y para RT-nested PCR para tipos de DENV según Bronzoni et al., 2005 de 0,002 UFP por reacción e inferior a 0,001 a UFP por reacción para DENV-1 y DENV-2 respectivamente. Las mismas fueron comparables a las obtenidas por otros autores9,11,12.
La nestedPCR para detección de DENV (SS2) fue seleccionada ya que permite identificar los tipos de DENV a partir del producto de amplificación de la primera reacción de la RT-nested PCR genérica ahorrando así tiempo y reactivos.
A fin de comparar dos multiplex RT-nestedPCR para tipificación de DENV se implementó la reacción descripta por Bronzoni et al., 200512.
La reacción descripta por Bronzoni et al., 2005 posee mayor sensibilidad para la detección de DENV-1 y DENV-2 comparada a la reacción de SS2. Por lo cual esta técnica sería de gran utilidad en la detección DENV en pacientes febriles.
Fue detectado el genoma viral de flavivirus en el 22,1% (43/195) de las muestras estudiadas (negativas para antígeno NS1 de DENV). La frecuencia de infección por flavivirus detectada en 2011, 2012 y 2013 fue similar.
El 20,5% (40/195) de las muestras estudiadas fueron reportadas como falsos negativos para DENV mediante el test inmunocromatográfico de detección de antígeno NS1. Los tests inmunocromatográficos son ampliamente utilizados en nuestro país para el diagnóstico de la infección por DENV, tanto en centros asistenciales del sector público como en laboratorios privados. Si bien el fabricante reporta una elevada sensibilidad (92,8%) y especificidad del 98.4%), estudios como el de Tricou et al. (2010) reportan una sensibilidad del 80,3% para una infección primaria por DENV, mientras que la sensibilidad decae a un 56,3% en los casos de infecciones secundarias para el test inmunocromatográfico empleado en este estudio14, mientras que Blacksell et al. (2012) reportan sensibilidades variadas de acuerdo a diversas marcas de tests inmunocromatográficos que van del 99 al 10% 15.
Los resultados sugieren que existe una discrepancia entre la sensibilidad declarada por los fabricantes y las reportadas en publicaciones científicas. Esto puede deberse a que las pruebas de diagnóstico no están sujetas a estrictas regulaciones en muchos países en desarrollo, como el nuestro. Como resultado, estas pruebas a menudo son comercializadas sin evidencia de efectividad8.
Los principales factores asociados con un resultado falso negativo de los tests inmunocromatográficos para DENV son una viremia relativamente baja y una infección secundaria (debido a la presencia de inmunocomplejos virus-IgG pre-existentes) 14. Teniendo en cuenta el gran número de epidemias de dengue ocurridas en nuestro país, existe alto riesgo de que gran parte de la población curse con infecciones secundarias ante una nueva exposición al virus. Por ello, se destaca la importancia de implementar nuevas metodologías más sensibles para el diagnóstico de la infección por DENV. Esto es de gran relevancia ya que los resultados obtenidos a través de dichas metodologías son utilizadas en la gestión clínica, la vigilancia, las investigaciones de brotes y permiten la intervención temprana para el tratamiento de los pacientes y prevenir o controlar las epidemias8.
Se observaron discrepancias en los resultados de detección del genoma de DENV al comparar las reacciones de RT-nested PCRs utilizadas 11 de las muestras fueron positivas para alguno de los tipos de DENV por la RT-nested PCR de Bronzoni et al., 2005(12) pero negativas por la reacción de SS2. Al analizar el alineamiento de la secuencia obtenida del fragmento de la primera reacción de Bronzoni con el primer para DENV-2 de SS2, se puede observar que el primer alinea con la secuencia obtenida. Por lo cual el resultado negativo para esta muestra no se debe a variaciones en la secuencia (mismatch con el primer), y pudo deberse a que la reacción de SS2 es menos sensible que la descripta por Bronzoni et al., 200512.
Por otro lado, 4 muestras resultaron positivas para DENV-2 por la reacción de SS2 pero negativas por la reacción de Bronzoni et al., 2005. Según mencionan Bronzoni et al., en algunas ocasiones la reacción puede arrojar resultados falsos negativos debido a variaciones en las secuencias nucleotídicas entre cepas virales, las cuales, pueden afectar a la hibridación de los primers. Según lo señalado por SS2, el uso de primers degenerados constituye una de las estrategias, junto al estudio de un gran número de secuencias, para evitar los problemas de hibridación debido a dichas variaciones. El análisis para verificar posibles variaciones en las secuencias donde hibrida el primer no pudo realizarse ya que no se logró amplificar el producto de la primera reacción descripta por SS2. Además, la obtención de resultados negativos pudo deberse a la degradación del material.
Con respecto a la distribución de las muestras positivas para el genoma de DENV por año (2011-2013) concuerdan con los reportes del Ministerio de Salud Pública (MSP), exceptuando la detección en este estudio de 2 casos de DENV-3 en 2011 mientras que el MSP no reportó casos de DENV-3 en este año. Esto puede deberse a que durante las epidemias de dengue, solo un bajo porcentaje de muestras positivas son tipificadas. Por lo tanto, es probable que durante el 2011 haya circulado DENV-3 en baja frecuencia, además debe considerarse que en 2010 el DENV-3 fue reportado como uno de los tipos circulantes en el país.
Por tanto, según los resultados obtenidos en este estudio, estas técnicas moleculares podrían ser utilizadas en los casos de resultado de antígeno NS1 para DENV negativo, a fin de identificar los resultados falsos negativos para infección por DENV y además, proporcionar la posibilidad de detectar otras virosis.
Los hallazgos del presente estudio remarcan la necesidad de un mejor estudio de los casos febriles con resultado negativo por el método inmunocromatográfico durante epidemias de DENV.
Cabe destacar, que en 5 muestras no pudo determinarse la especie de flavivirus, lo que puede deberse a infecciones causadas por otros flavivirus. Para identificar la especie de viral, se podría realizar la secuenciación de los productos de amplificación obtenidos.
A través de este estudio se realizó la estandarización de técnicas moleculares para detección genérica de flavivirus y también los tipos de DENV con una buena sensibilidad. Lo cual es de suma importancia ya que uno de los pilares más importantes para el control de las enfermedades transmitidas por arbovirus es la disponibilidad de buenos sistemas de detección que permitan determinar el nivel de actividad vírica, y de este modo, aplicar sistemas de vigilancia eficaces. Cabe destacar que a través de la reacción de RT-nested genérica para flavivirus se podría detectar por secuenciación otros flavivirus como el virus del ZIKA, el virus de la Fiebre Amarilla ya reportados en nuestro país y también otras virosis aún no reportadas.