Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Memorias del Instituto de Investigaciones en Ciencias de la Salud
On-line version ISSN 1812-9528
Mem. Inst. Investig. Cienc. Salud vol.7 no.1 Asunción June 2009
REPORTE DE CASO
Secuestro pulmonar infradiafragmático asociado a malformación adenomatoidea quística congénita
Infradiaphragmatic pulmonary sequestration combined with cystic adenomatoid malformation
*Ruoti Cosp MI, Galeano Monti JI, de Agustín Sacristán JLII, González de Agüero L RII, Fabre González EII
ICátedra de Ginecología y Obstetricia, Facultad de Ciencias Médicas, Universidad Nacional de Asunción (UNA). Paraguay
IIDepartamento de Ginecología y Obstetricia Hospital Clínico Universitario Lozano Blesa, Zaragoza, España
RESUMEN
El secuestro pulmonar (SP) es raro, es la presencia de tejido pulmonar no unido al resto del pulmón pudiendo ser intralobar o extralobar (más común). El diagnóstico definitivo de una masa abdominal superior fetal sólo puede hacerse después del nacimiento, tras una serie de revisiones ultrasonográficas o de imágenes. Presentamos caso clínico de primigesta, 34 años. Ecografía en la 17ª semana: imagen multiquística de 15 mm de diámetro en polo superior del riñón izquierdo fetal. Cariotipo fetal tras amniocentesis: 46 XX. Ecografía en la 20ª semana: ausencia de otras alteraciones estructurales. Ecografía en la 33ª semana: imagen multiquística de 20 mm de diámetro, independiente del riñón. Se sugiere diagnóstico de neuroblastoma suprarrenal izquierdo. En la 39ª semana: nacido de 3160 gramos, Apgar de 9/10, sin complicaciones. Ecografía neonatal: tumoración mixta de predominio líquido de 3 cm de diámetro sobre el riñón izquierdo pero independiente. Resonancia magnética: masa adrenal izquierda compatible con neuroblastoma. Al 36º día de vida: laparotomía subcostal izquierda, riñón y glándulas suprarrenales izquierdas normales, comprimidos por tumor quístico de 3 x 2,5 cm, semisólido, adherido al diafragma. Extirpación completa. Diagnóstico anatomopatológico: secuestro pulmonar infradiafragmático con cambios de malformación adenomatoidea congénita de tipo II. Los tumores abdominales constituyen el 5 % de las anormalidades detectadas en ecografía prenatal. El diagnóstico diferencial incluye neuroblastoma, hemorragia adrenal, tumores renales, teratomas y secuestro pulmonar extralobar intraabdominal (SPEI). El SPEI constituye el 2 a 5 % de los secuestros pulmonares y tiene una alta incidencia de coexistencia con MAQC tipo II.
Palabras claves: Secuestro pulmonar infradiafragmático, Malformación Adenomatosa Quística Congénita, Masa abdominal fetal.
ABSTRACT
The pulmonary sequestration (SP) is rare and characterized by the presence of pulmonary tissue not joined to the rest of the normal lung. It could be intralobar or more commonly extralobar. The definite diagnosis of a fetal upper abdominal mass can be made only after birth and following a series of ultrasonographic or image exams. We present the clinical case of a primipara of 34 years old. A 17th week ultrasound showed a multicystic image of 15 mm diameter in the upper pole of the fetal left kidney. The fetal cariotype after amniocentesis was 46 XX. The 20th week ultrasound showed the absence of other structure alterations. The 33th week ultrasound showed a multicystic image of 20mm diameter separated from the kidney. A diagnosis of left adrenal neuroblastoma is suggested. The labor occurred at 39th week with a newborn of 3,160 grams, Apgar of 9/10 without complications. The neonatal ultrasound revealed a mixed tumor of liquid predominance of 3 cm diameter above but independent from the left kidney. A magnetic resonance imaging showed a left adrenal mass compatible with a neuroblastoma. At the 36th day of life, a left subcostal laparotomy showed a normal left kidney and left suprarenal glandules compressed by a semisolid cystic tumor of 3 x 2.5 cm adhered to diaphragm. A complete extirpation was carried out and the anatomopathological diagnosis showed an infradiaphragmatic pulmonary sequestration combined with a type II cystic adenomatoid malformation. Abdominal tumors represent 5 % of the abnormalities detected in prenatal ultrasound. The differential diagnosis includes neuroblastoma, adrenal hemorrhage, kidney tumors, teratomas and intraabdominal pulmonary sequestration (IPS). The IPS constitutes 2 to 5 % of the pulmonary sequestration and has a high frequency of coexistence with type II cystic adenomatoid malformation.
Keywords: Infradiaphragmatic pulmonary sequestration, Congenital cystic adenomatoid malformation, Fetal abdominal mass.
INTRODUCCIÓN
Las anomalías congénitas del pulmón comprenden un extenso número de patologías. Algunas se presentan como síndromes clínicos característicos, otras solo se consideran variaciones anatómicas que no requieren tratamiento.
Las malformaciones pulmonares congénitas tienen una incidencia estimada del 2,2% del total de malformaciones congénitas (1).
Existe un grupo de anomalías que se han denominado malformaciones broncopulmonares del intestino anterior que comprenden a los quistes broncógenos, secuestro pulmonar, quistes de duplicación y malformación adenomatoidea quística (2). El secuestro pulmonar (SP) es una rara anomalía que consiste en la presencia de tejido pulmonar que no se encuentra unido al resto del pulmón y no se comunica con el árbol bronquial o con las arterias pulmonares (3,4).
El SP puede ser intralobar o extralobar, este último es más común en el diagnóstico prenatal y está asociado con un incremento en el riesgo de hernia diafragmática, anormalidades cardíacas y duplicación gástrica. El 90% por ciento de los extralobares están en el lado izquierdo, en la región posterobasal, en el surco costofrénico. Se describe además una relación de 4:1 entre masculino y femenino (5). La malformación adenomatosa quística congénita (MAQC) ocurre en aproximadamente 1 en 4000 embarazos. Es un desarrollo hamartomatoso anormal de el pulmón con proliferación de estructuras quísticas semejantes a bronquios y bronquiolos (excluyen alveolos) que pueden contener tejido elástico, cartílago y músculo. Representa aproximadamente el 25% de todas las lesiones congénitas del pulmón y en su presentación prenatal, la lesión es usualmente unilateral (6).
Un diagnóstico definitivo no siempre aparece cuando una masa abdominal superior fetal está presente. El aspecto ultrasonográfico de una variedad de condiciones patológicas tiene características similares y pueden ser difíciles de diferenciar hasta para el más experimentado personal. Un diagnóstico final sólo puede hacerse después del nacimiento, tras haber realizado una serie de revisiones ultrasonográficas o de imágenes (7). Presentamos el caso de una paciente con una gestación en la que se observa una masa a nivel del abdomen superior fetal en la ecografía obstétrica.
CASO CLINICO
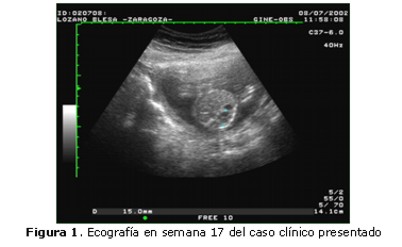
Primigesta de 34 años, sin antecedentes personales o familiares de interés, que cursa con gestación sin alteraciones. En la exploración ecográfica básica (Figura 1) realizada en la 17ª semana de embarazo se observa una imagen multiquística de 15 mm de diámetro a nivel del polo superior del riñón izquierdo fetal, no pudiendo establecerse con precisión su dependencia.
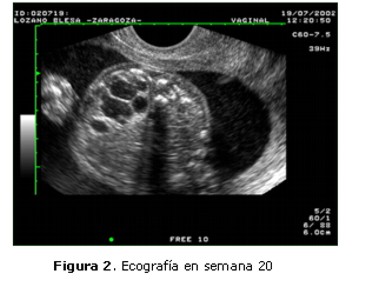
Se realizó cariotipo fetal tras amniocentesis con resultado 46 XX. En la ecografía de diagnóstico prenatal realizada en la 20ª semana (Figura 2) no se objetivan otras alteraciones estructurales ni cambios en la imagen multiquística.
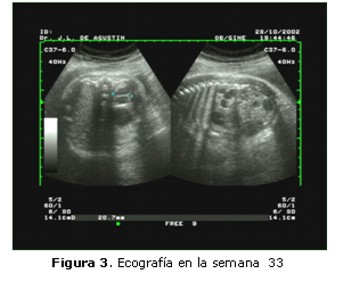
En la exploración ecográfica realizada en la 33ª semana (Figura 3) de gestación se observa como persiste la imagen multiquística de 20 mm de diámetro y se comprueba que es una estructura independiente del riñón. Su localización y características morfológicas sugieren el diagnostico de neuroblastoma suprarrenal izquierdo.
La gestación evoluciona sin alteraciones, finalizando en la 39ª semana mediante la aplicación de un fórceps por riesgo de pérdida del bienestar fetal. Nacido de sexo femenino y 3.160 gr de peso con una puntuación de Apgar de 9/10 al primer y quinto minuto respectivamente. La adaptación neonatal trascurre sin complicaciones.
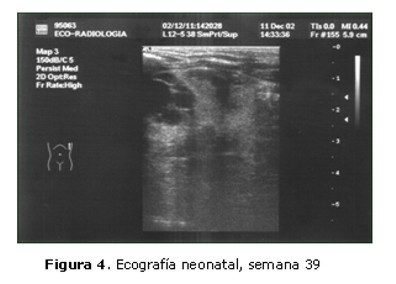
Se realiza ecografía neonatal (Figura 4) que objetiva una tumoración mixta de predominio líquido de 3 cm de diámetro situada sobre el riñón izquierdo pero independiente.
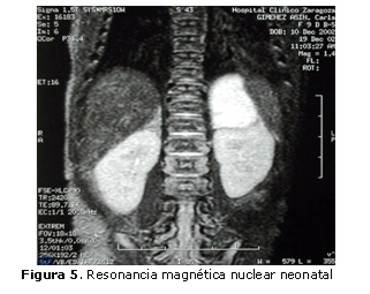
La resonancia magnética neonatal (Figura 5) informa de masa adrenal izquierda con criterios compatibles con neuroblastoma.
Con tal diagnóstico se realiza al 36º día de vida laparotomía subcostal izquierda, se identifican riñón y glándulas suprarrenales izquierdas normales, comprimidos ambos por una tumoración quística de 3 x 2,5 cm, semisólida al corte y adherida al diafragma. Se realiza la extirpación completa del tumor. La intervención cursa sin complicaciones al igual que la evolución posterior.
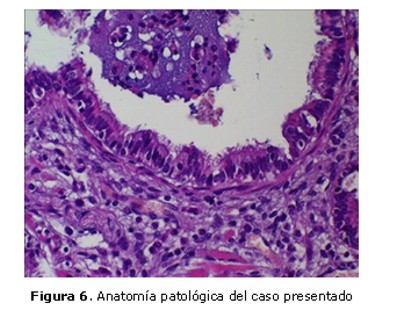
El diagnóstico anatomopatológico fue secuestro pulmonar infradiafragmático con cambios de malformación adenomatoidea congénita de tipo II (Figura 6).
DISCUSION
El caso presentado ilustra la dificultad diagnóstica en este tipo de lesiones por lo que se debe conocer cuales son los posibles diagnósticos diferenciales.
Los tumores abdominales fetales constituyen aproximadamente el 5% de las anormalidades detectadas en la ecografía prenatal. El diagnóstico diferencial de masas intraabdominales y/o retroperitoneales dependen de la adecuada evaluación del tamaño, posición y del aspecto sonográfico característico (7).
En el diagnóstico diferencial de masas intraabdominales se incluyen principalmente el neuroblastoma (el tumor maligno más frecuente en el neonato, caracterizado por bordes pobremente definidos, ecogenicidad baja o mixta, usualmente con focos de calcificación) y la hemorragia adrenal, menos frecuentemente, tumores renales y teratomas y aún más raramente secuestro pulmonar extralobar intraabdominal (SPEI) (5). Pryce usó por primera vez el término secuestro pulmonar en 1946 y luego clasificó la lesión como intralobar y extralobar basado en el patrón morfológico de la secuestración (8).
Diversas teorías etiológicas han intentado explicar el origen embriológico de los SP. La teoría más frecuentemente aceptada es la insuficiente velocidad en el desarrollo de la arteria pulmonar para suplementar crecimiento al pulmón, por este motivo, un segmento adquiere vascularización desde la aorta. El SP consiste en la exclusión de un segmento del parénquima pulmonar de su continuidad con el árbol bronquial que es irrigado desde circulación sistémica (2).
El secuestro pulmonar intralobar representa el 75% de todos los SP. Consiste en un segmento anormal de tejido pulmonar que comparte la pleura visceral de un lóbulo pulmonar normal y que carece de comunicación normal con el árbol traqueobronquial, aunque puede conseguirse cantidad variable de aire dentro del tejido anómalo. Casi siempre ocurre dentro del lóbulo inferior, más frecuente en el pulmón izquierdo que en el derecho (8). Las principales características patológicas son inflamación crónica, cambios quísticos y fibrosis. Las ramas aórticas anómalas que irrigan la lesión son característicamente localizadas dentro del ligamento pulmonar inferior. La gran mayoría de los secuestros intralobares son drenados por venas pulmonares normales dentro de la aurícula izquierda (9).
El secuestro pulmonar extralobar es una entidad completamente distinta y representa el 25% de todos los SP. La malformación es diagnosticada durante los primeros días o semanas de vida del paciente y, menos frecuentemente, en la infancia tardía o niñez temprana. Consiste en un lóbulo separado, accesorio, de tejido pulmonar que es envuelto en su propia pleura.
El secuestro pulmonar extralobar infradiafragmático es una malformación congénita extremadamente rara, que es más frecuentemente diagnosticada en el período prenatal durante el examen ecográfico de rutina del feto o en los primeros 6 meses de vida, en raras ocasionas es descubierta incidentalmente en adultos. Se ha sugerido que se produce por el atrapamiento de tejido dentro del espacio infradiafragmático, justo antes del cierre de la membrana pleuroperitoneal que ocurre entre las 5 y 8 semanas de gestación (10).
El SP constituye el 23% de las lesiones pulmonares detectadas prenatalmente, mientras que el SPEI constituye el 8 a 10% de los secuestros pulmonares y tiene una alta incidencia (aproximadamente 58%) de coexistencia con MAQC tipo II. Según otras fuentes, el secuestro pulmonar retroperitoneal ocurre en el 2-5% de los secuestros (5,7,10).
El SPEI típicamente aparece como una masa ecogénica sólida, bien definida en la ecografía prenatal o como una masa hiperintensa en la Resonancia Magnética. En la Tomografía Computada (TC) posnatal, el SPEI usualmente se manifiesta como una masa de baja densidad en la región suprarrenal izquierda con un mínimo acrecentamiento con el contraste o ningún acrecentamiento del mismo. El uso de aguja fina biópsica para establecer el diagnóstico fue sugerido pero no siempre realizado con suceso en los casos de SPEI (5,10).
Características inusuales de la TC fueron reportadas en un caso de SPEI combinado con MAQC. La TC posnatal inmediata y el seguimiento con TC, demostraron un reemplazo de áreas quísticas intralesionales por contenido sólido, progresivamente en las diferentes TC (10). Chin y Tang describieron por primera vez la MAQC en 1949. Esta representa un desarrollo hamartomatoso anormal de el pulmón con proliferación de estructuras quísticas semejantes a bronquios y bronquiolos (excluyen alveolos) que pueden contener tejido elástico, cartílago y músculo. Representa aproximadamente el 25% de todas las lesiones congénitas del pulmón (6). En 1976, Stocker y colaboradores (11) clasificaron dicha anomalía en tres tipos para su análisis patológico. El Tipo I consiste en quistes de 2-10cm de diámetro y es la variedad más común. El Tipo II, quistes numerosos más pequeños y uniformes de 0.5-2 cm de diámetro, y tipo III son lesiones de apariencia sólida que microscópicamente se demuestran quistes diminutos (6). Las MAQC, normalmente comunican con el árbol pulmonar normal y son irrigados por la arteria pulmonar. La presencia de una MAQC incluida en un segmento pulmonar secuestrado es una entidad muy poco frecuente (11,12). La anomalía ha sido descrita dentro de un SP por Zangwill y col. refieren que en sus 30 casos de secuestro pulmonar extralobar aproximadamente 25% contiene una MAQC tipo II (13). Conran y Stocker refieren una coexistencia de SP extralobar y MAQC tipo II superior al 50% de los casos (14), en tanto que Hellmuth D (15), describe un ejemplo de malformación adenomatoidea quística como manifestaciones quísticas unilobular.
Existen en la literatura, muy pocas descripciones de casos aislados de masas ecográficas abdominales prenatales que luego resultaron ser SPEI con características de MAQC, por lo que consideramos que la descripción de este caso es de mucho valor.
BIBLIOGRAFÍA
1. Evrard V, Ceulemans J. Congenital parenchymatous malformations of the lung. World J Surg 1999; 23:1123-32. [ Links ]
2. Sánchez A, Somoza I, Liras J, Méndez R, Tellado M, Rìos J et al.. Malformación adenomatoidea quística congénita asociada a secuestro pulmonar. Presentación de dos casos clínicos. Cir Pediatr 2005; 18:39-41. [ Links ]
3. Berrocal T, Madrid C, Novo S, Gutiérrez J, Arjonilla A, Gómez-León N. Congenital anomalies of the tracheobronchial tree, lung, and mediastinum: embryology, radiology, and pathology. Radiographics 2003;24:e17. [ Links ]
4. Shanmugam G, MacArthur K, Pollock J. Congenital lung malformations-antenatal and postnatal evaluation and management. Eur J Cardiothorac Surg 2005; 27:45-52. [ Links ]
5. Hernanz-Schulman M, Johnson JE, Holcomb GW, Neblett WW, Heller RM, Ambrosino MM. Retroperitoneal pulmonary sequestration: Imaging findings, histopathologic correlation, and relationship to cystic adenomatoid malformation. AJR 1997;168:1277-81. [ Links ]
6. Plit ML, Blott JA, Lakis N, Murray J, Plit M. Clinical, radiographic and lung function features of diffuse congenital cystic adenomatoid malformation of the lung in an adult. Eur Respir J 1997; 10:1680-2. [ Links ]
7. Watson S, Benzei R. Fetal upper abdominal masses: a prenatal diagnostic dilemma. ASUM Ultrasound Bulletin 2005;8:19-21. [ Links ]
8. Frazier A, Rosado de Christensen M, Stocker J, Tompleton P. Intralobar sequestration: radiologic-pathologic correlation. Radiographics 1997; 17:725-45. [ Links ]
9. Ayala D, Dinamarca O, García B. Caso clínico-radiológico para diagnóstico secuestro pulmonar. Rev Chil Pediatr 1999;70-.6. [ Links ]
10. Kim HK, Choi YH, Ryu SM, Kim HK, Chae YS, Sohn YS, et al. Infected Infradiaphragmatic Retroperitoneal Extralobar Pulmonary Sequestration: A Case Report. J Korean Med Sci 2005; 20:1070-2. [ Links ]
11. Stocker J, Maxwell J. Congenital cystic adenomatoid malformation of the lung. Classification and morphologic spectrum. Hum Pathol 1977;8:155-71. [ Links ]
12. Zangwill BC, Stocker JT. Congenital cystic adenomatoid malformation within an extralobar pulmonary sequestration. Pediatr Pathol 1993;13:309-15. [ Links ]
13. Fraggetta F, Cacciaguerra S, Nash R, Davenport M. Intra-abdominal pulmonary sequestration associated with congenital cystic adenomatoid malformation of the lung: just an unusual combination of rare pathologies?. Pathol Res Pract 1998;194:209-11. [ Links ]
14.Conran RM, Stocker JT. Extralobar sequestration with frequently associated congenital cystic adenomatoid malformation, type 2: report of 50 cases. Pediatr Dev Pathol 1999;2:454-63. [ Links ]
15. Hellmuth D, Glerant JC, Sevestre H. Pulmonary adenomatoid malformation presenting as unilobar cysts in an adult. Res Med 1998; 92:1364-76. [ Links ]
*Autor Correspondiente: Dr. Miguel Ruoti Cosp, Cátedra de Ginecología y Obstetricia,
Facultad de Ciencias Médicas, Universidad Nacional de Asunción, Paraguay
Email: mruoticosp@hotmail.com